文章信息
- 赵嘉咏, 申晓靖, 张白帆, 王泽乾, 夏胜利, 黄学勇, 许汴利 .
- Zhao Jiayong, Shen Xiaojing, Zhang Baifan, Wang Zeqian, Xia Shengli, Huang Xueyong, Xu Bianli .
- 河南省2013-2015年病毒性腹泻哨点医院监测结果与分析
- Surveillance for viral diarrhea in sentinel hospitals in Henan province, 2013-2015
- 中华流行病学杂志, 2016, 37(10): 1392-1396
- CHINESE JOURNAL OF EPIDEMIOLOGY, 2016, 37(10): 1392-1396
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2016.10.015
-
文章历史
收稿日期: 2016-04-16
2. 456750 淇县疾病预防控制中心
2. Qixian County Center for Disease Control and Prevention, Qixian 456750, China
病毒性腹泻为腹泻病毒感染肠道后,引起以呕吐和腹泻为主要临床特征,伴有发热、厌食、腹痛及全身不适症等中毒症状的自限性急性感染性腹泻[1],临床上又称为病毒性胃肠炎,粪-口途径传播,在我国传染病防治法中列为丙类传染病[2]。引起病毒性腹泻的主要病原体包括人感染轮状病毒(Human Rotavirus,HRV),分为A、B、C三组;人感染杯状病毒(Human Calicivirus,HuCV),包括诺如病毒与札如病毒;人感染星状病毒(Human Astrovirus,HAtV)及肠道腺病毒(Enteric Adenovirus,EAdV)[1]。本研究对河南省2013-2015年采集自4个县(市)5岁以下婴幼儿住院病例腹泻粪便中的HRV、HuCV、HAtV、EAdV 4类7种病原体进行检测与基因型别分析,为其疾病监测、防控策略制定、暴发疫情调查及疫苗研发提供基线数据与科学依据。
对象与方法1. 研究对象:依据“十二五”科技重大专项腹泻症候群研究方案制定的病毒性腹泻病例定义(每日排便3次或3次以上,且粪便性状有改变,呈稀便、水样便等;粪便常规镜检WBC<15,未见RBC)对郑州市、周口市、登封市、商丘市睢县4家监测哨点医院(郑州市、周口市、登封市为城市监测哨点,睢县为农村监测哨点)5岁以下(1~59月龄)住院腹泻患儿,进行粪便样本采集。
2. 样本采集与保存:粪便标本在患者发病3 d内或入院24 h内采集,每病程(3~7 d)采集1次。固体便每份取5~10 g,水样便或稀便每份取5~10 ml,置-20 ℃冻存,在检测前避免反复冻融。
3. 临床信息:按照研究方案设计的个案调查表收集腹泻病例的姓名、性别、年龄、家庭住址、临床症状(体征)等信息。
4. 试剂与仪器:A组HRV ELISA检测试剂盒购自英国OXOID公司;病毒核酸提取试剂盒(磁珠法)购自西安天隆科技有限公司;SuperScript Ⅲ反转录酶购自美国Invitrogen公司;dNTP MIX、GoTaq DNA聚合酶购自美国Promega公司;检测及分型引物(HPLC纯化)由上海英骏生物有限公司合成;100 bp Marker购自宝生物工程(大连)有限公司;电泳琼脂糖购自西班牙Biowest公司;50×TAE电泳缓冲液购自北京索莱宝有限公司。NP968型自动核酸提取仪购自西安天隆科技有限公司;去离子水系统购自美国Millipore公司;Minispin台式离心机、PCR仪购自德国Eppendorf公司;核酸电泳及凝胶成像系统购自美国Bio-Rad公司。
5. 标本检测:①A组HRV抗原检测:参照腹泻症候群技术方案进行预处理和双抗体夹心法ELISA检测A组HRV[3]。②病毒总核酸提取及A组HRV基因分型:取样本稀释液200 μl,使用自动核酸提取仪进行病毒总核酸(DNA&RNA)的提取。提取产物参照腹泻症候群研究方案提供的A组HRV G(病毒外壳蛋白VP7)/P(病毒外壳蛋白VP4)基因分型方法进行[3]。③B/C组HRV、HuCV(诺如Ⅰ型/Ⅱ型、札如病毒)、HAtV及EAdV检测:参照腹泻症候群技术方案进行检测,其中B/C组HRV、HuCV(诺如Ⅰ型/Ⅱ型、札如病毒)和HAtV采用二步多重RT-PCR法,EAdV采用单重PCR法[4]。④电泳、测序与结果判断:取10 μl PCR扩增产物行1.5%琼脂糖凝胶电泳(140 V,30 min)。根据产物片段大小及数目组合判断A组HRV基因型别及其他腹泻病毒种类。对于疑似A组HRV混合感染的PCR产物由上海生工生物工程公司纯化测序,序列使用DNAstar软件进行拼接校正后通过美国国家生物技术信息中心(NCBI,http://www.ncbi.nlm.nih.gov/)GenBank数据库进行比对分析以确定对应型别。
6. 统计学分析:采用Excel 2007软件进行数据录入与整理,检测结果及临床症状等资料,采用例数或百分比描述;比率组间比较采用 χ2检验,以P<0.05判定差异有统计学意义。
结 果1. 病毒性腹泻病原谱:880份腹泻样本(2013年323份,2014年274份,2015年283份,共计880份,其中男性476份,女性404份)中共检出阳性样本594份(包括混合感染样本24份),总阳性率为67.5%,混合感染率为2.7%:检出HRV(A、B、C三组)370份,其中A组343份,B组8份,C组19份,总阳性率为42.0%;检出HuCV 162份,阳性率为18.4%;检出HAtV 69份,阳性率为7.8%;检出EAdV 17份,阳性率为1.9%。以HRV和HuCV感染为主。
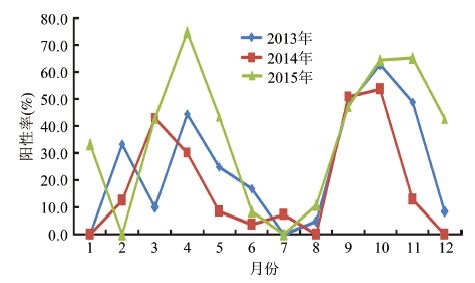
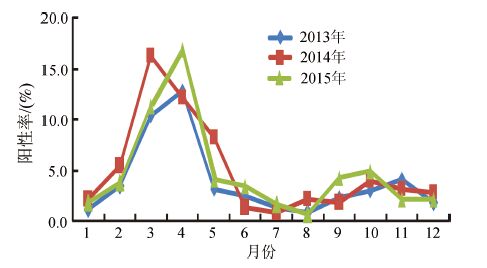
2. A组HRV检测:880份腹泻样本共检出A组HRV 343份,总阳性率为39.0%。其中2013-2015年阳性率分别为40.6%(131/323)、30.7%(84/274)和45.2%(128/283)。农村监测点的阳性率(57.4%,195/340)显著高于城市(27.4%,148/540)监测点( χ2=23.19,P<0.001)。分月份看,每年的10月阳性率最高,3年的平均阳性率为60.4 %;阳性率最低的是每年的7月,3年的平均阳性率为2.4%。检出率的季节性变化显著,存在秋季(9-11月)和春季(3-5月)两个较为显著的高峰(表 1,图 1)。
|
| 图 1 2013-2015年河南省4个县(市)腹泻样本A组HRV阳性率逐月变化 |
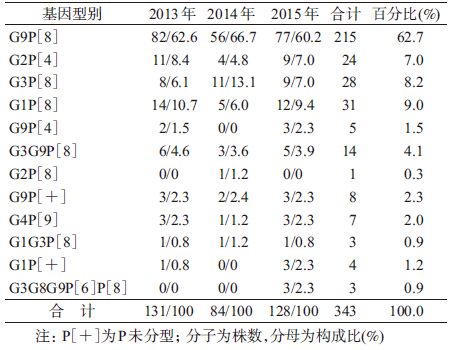
3. A组HRV G/P分型:343株A组HRV G分型以G1、G2、G3、G9为主;P分型以P[4]、P[8]为主。A组HRV型别有G1P[8]、G2P[4]、G2P[8]、G3P[8]、G4P[9]、G9P[4]、G9P[8],以G9P[8]、G2 P[4]、G3P[8]、G1P[8]为主。另外经测序证实还存在混合感染的型别,有G1G3P[8]、G3G9P[8]、G3G8G9P[6]P[8](表 2)。
4. HuCV检出情况:880份腹泻样本共检出HuCV 162份,检出率为18.4%,其中诺如Ⅰ型32份(19.8%),诺如Ⅱ型117份(72.2%),札如病毒13份(8.0%)。城市阳性率为23.5%(127/540),农村阳性率为10.3%(35/340),城市显著高于农村( χ2=23.19,P<0.001)。以诺如Ⅱ型病毒为主的HuCV检出率呈现较为显著的季节性特点:每年的3-5月检出率最高,3年的平均阳性率为12.7 %;每年的7-8月检出率最低,3年的平均阳性率为1.3%,存在春季(3-5月)感染高峰(图 2)。
|
| 图 2 2013-2015年河南省4个县(市)腹泻样本HuCV阳性率逐月变化 |
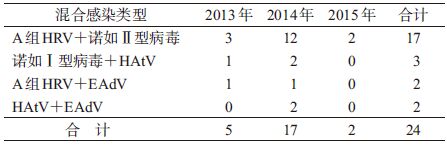
5. 病毒检出情况:880份腹泻样本共检出B组HRV 8份,检出率为0.9%;检出C组HRV 19份,检出率为2.2%;检出HAtV 69份,检出率为7.8%;检出EAdV 17份,检出率为1.9%。混合感染病例检出情况见表 3。
6. 病毒性腹泻感染病例流行病学资料分析:
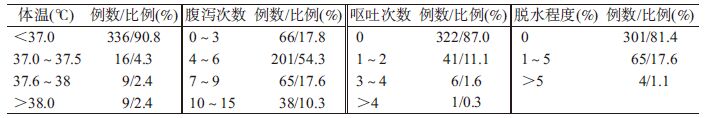
(1)370例HRV感染病例中,224例为男性,阳性率为47.1%(224/476);146例为女性,阳性率为36.1%(146/404),男女性别比1.5 ∶ 1,男性感染率高于女性( χ2=10.695,P=0.001 1);年龄分布为:0~6月龄162例,阳性率为48.1%(162/337),7~12月龄88例,阳性率为46.8%(88/188),1~2岁41例,阳性率为40.2%(41/102),2~3岁40例,阳性率为43.5%(40/92),3~4岁28例,阳性率为29.8%(28/94),4~5岁11例,阳性率为16.4%(11/67)。其中0~6月龄组的阳性率高于3~4岁( χ2=9.968,P=0.002)与4~5岁,差异有统计学意义( χ2=22.870,P<0.001);7~12月龄组阳性率高于4~5岁,差异有统计学意义( χ2=19.208,P<0.001);1~2岁年龄组阳性率高于4~5岁,差异有统计学意义( χ2=10.733,P=0.001);2~3岁年龄组阳性率高于4~5岁,差异有统计学意义( χ2=13.030,P<0.001),阳性病例主要为0~12月龄的婴幼儿患者,且低年龄组阳性率高于高年龄组,差异有统计学意义( χ2=30.848,P<0.001);城市病例156例,阳性率为28.9%(156/540),农村病例195例,阳性率为57.4%(195/340),农村高于城市,差异有统计学意义( χ2=70.499,P<0.001);从临床体征看,大部分的阳性病例不发热或轻度发热;轻度与中度腹泻为主;未出现呕吐、脱水等症状(表 4)。
(2)248例HuCV、HAtV及EAdV感染病例中,131例为男性,阳性率为27.5%(131/476);117例为女性,阳性率为28.9%(117/404),男女性别比1.1 ∶ 1( χ2=0.224,P>0.001),阳性率差异无统计学意义。病例主要为3~5岁的低龄儿童(65.7%,163/248);城市病例174例,阳性率为32.2%(174/540),农村病例74例,阳性率为21.8%(74/340),城市高于农村,差异有统计学意义( χ2=11.273,P=0.000 7);从临床体征看,大部分病例不发热或轻度发热;以轻度和中度腹泻为主;呕吐及中重度脱水现象则高于HRV感染(表 5)。
病毒性腹泻可由多种病原引起,主要为HRV、HuCV、HAtV和EAdV 4大类别。据WHO一项统计数据显示,腹泻病毒在发展中国家腹泻病原谱构成比重超过50%,其中HRV的比重超过30%;即使在发达国家,病毒感染的比例也超过30%[5]。本研究的病原学数据充分验证了这一点:河南省5岁以下儿童的腹泻病毒感染率高达67.5%,HRV感染率超过40%,其他类病毒感染率将近30%。病毒性腹泻虽然其临床症状相近,但各自的病原学特点与致病机制不尽相同,因此在低龄儿童中深入和持续开展病毒性腹泻监测及病原学研究对该病的防控具有重要意义。
HRV为双链RNA病毒,1973年由澳大利亚的Ruth Bishop首次发现,A、B、C组均可感染人[2]。A组HRV是5岁以下儿童感染性重症胃肠炎的主要病原,占腹泻住院儿童的比例为20%~60%,其导致的腹泻症状重,造成的疾病负担巨大,成为全球最为关注的腹泻病原。根据WHO估算,每年约61.1万婴幼儿死亡,特别是在非洲、亚洲及南美洲地区的发展中国家[5]。由于A组HRV抗原型别的复杂性、多样性及变异性,持续开展其病原学监测,掌握其感染状况及基因型别的分布和变异趋势对于开展疾病负担调查,制定防控策略提供重要的基线数据,同时为疫苗研发和改进也提供了关键的参考依据。Gl/G2/G3/G4/G9,P[4]/P[6]/P[8]是世界范围内最常见的优势株型,20世纪90年代中叶,最常见的4种组合依然为G1P[8]、G2P[4]、G3P[8]和G4P[6][6]。近年来,A组HRV又呈现新的分子流行病学特点,G9型呈快速上升趋势,G9P[8]型已成为第5种新的流行型别[7]。从本研究看,河南省A组HRV的基因型别以G9P[8]、G1P[8]、G2P[4]、G3P[8]为主,与目前世界范围的A组HRV的病原学特征和流行趋势是一致的。从河南省的历史监测数据看,G9P[8]型别占比上升最为迅速,已成为河南省5岁以下儿童A组HRV感染的主要型别。另外河南省A组HRV病原学的另一个特点就是存在混合感染型别,由于A组HRV的易感性、抗原多样性及机体感染后免疫力难以持久和交叉免疫保护力弱等特点,5岁以下儿童感染率可接近100%,且易形成不同型别的反复感染,因此在同一患者体内可检测出多种型别[8],本研究结果同样证实了这一点,且混合感染的型别与单重感染的流行型别基本上是一致的。B、C组HRV虽然检出率不高,但也是引起成年人和婴幼儿散发或暴发感染的病原,在河南省处理的一起腹泻暴发疫情中,就曾检测出多份C组HRV。从临床症状看,大部分病例以轻、中度腹泻为主,没有出现发热、呕吐、脱水等症状,体现了HRV感染以轻症为主和自限性的特点;河南省HRV感染病例年龄分布相对集中(0~12月龄)、男性高于女性、低年龄组高于高年龄组、农村感染率显著高于城市是其主要的流行病学特点。
HuCV是仅次于HRV的重要腹泻病原,具有发病急、传播速度快、感染性强、波及范围广等特点[9],同时也和食品安全关系日益紧密,近年来世界范围内发生过多起由诺如病毒感染引起的大规模食物中毒事件和暴发疫情,故其日益受到重视[10]。从河南省的监测数据看,诺如Ⅱ型病毒是5岁以下儿童感染的主要型别,但与HRV感染不同的是其临床症状更为严重,春夏季高发,病例易感年龄段后移(3~5岁),且城市儿童的感染率高于农村。HAtV与EAdV分别为单正链RNA和双链DNA病毒,相比HRV和HuCV,其检出率低,季节性弱[11],但其作为病毒性腹泻病原谱的重要组成部分,同样存在暴发流行的可能性,需要持续给予关注。
由于腹泻病毒在传播途径和模式上的相似性,类型间病原和亚型间的病例混合感染也是病毒性腹泻监测中的常见情况,欧洲地区的混合感染率在4.4%~29.0%,且存在3~4重感染[12];中国河南省5岁以下儿童型别间混合感染率(2.7%)低于欧洲地区,仅存在2重感染模式,A组HRV+诺如Ⅱ型的组合占比最高,这两种病原的检出率也是最高的。对混合感染型腹泻病毒致病机制、临床体征、传播模式的研究将有助于加深对疾病本身的了解和把握,推动学科发展和科学防控。
| [1] | 中国疾病预防控制中心. 全国病毒性腹泻监测方案[Z]. 中国疾病预防控制中心,2007. Chinese Center for Disease Control and Prevention(China CDC). National surveillance project for viral diarrhea[Z]. Beijing:China CDC,2007. |
| [2] | 李奇凤, 杨学磊. 轮状病毒的研究进展[J]. 国际病毒学杂志 , 2009, 16 (5) : 150–154 DOI:10.3706/cma.j.issn.1673-4092.2009.05.006 Li QF, Yang XL. Progress in rotavirus studies[J]. Int J Virol , 2009, 16 (5) : 150–154 DOI:10.3706/cma.j.issn.1673-4092.2009.05.006 |
| [3] | 董慧瑾, 钱渊. 婴幼儿腹泻相关的轮状病毒分子流行病学最新研究进展[J]. 国际病毒学杂志 , 2009, 16 (2) : 48–52 DOI:10.3760/cam.j.issn.1673-4092.2009.02.004 Dong HJ, Qian Y. Recent advances in molecular epidemiology of rotavirus in infants and young children[J]. Int J Virol , 2009, 16 (2) : 48–52 DOI:10.3760/cam.j.issn.1673-4092.2009.02.004 |
| [4] | 张现娥, 李丹地, 李响, 等. 长春地区2010年度婴幼儿腹泻的病原学研究及流行病学特点[J]. 中华实验和临床病毒学杂志 , 2012, 26 (1) : 5–7 DOI:10.3760/cma.j.issn.1003-9279.2012.01.003 Zhang XE, Li DD, Li X, et al. Etiological and epidemiological study on viral diarrhea among children in Changchun[J]. Chin J Exp Clin Virol , 2012, 26 (1) : 5–7 DOI:10.3760/cma.j.issn.1003-9279.2012.01.003 |
| [5] | Hungerford D, Vivancos R, EuroRotaNet Network Members, et al. In-season and out-of-season variation of rotavirus genotype distribution and age of infection across 12 European countries before the introduction of routine vaccination,2007/08 to 2012/13[J]. Euro Surveill , 2016, 21 (2) : 106–128 DOI:10.2807/1560-7917.ES.2016.21.2.30106 |
| [6] | Leino T, Ollgren J, Strömberg N, et al. Evaluation of the intussusception risk after pentavalent rotavirus vaccination in finnish infants[J]. PLoS One , 2016, 11 (3) : e0144812 DOI:10.1371/journal.pone.0144812 |
| [7] | Fumian TM, Leite JPG, Rocha MS, et al. Performance of a one-step quantitative duplex RT-PCR for detection of rotavirus A and noroviruses GⅡ during two periods of high viral circulation[J]. J Virol Methods , 2016, 228 : 123–129 DOI:10.1016/j.jviromet.2015.11.008 |
| [8] | YeHC, LiuYH. Epidemiological study of rotavirus diarrhea in Beijing area from 2010 to 2012[J]. Chin J Exp Clin Virol , 2012, 26 (6) : 432–434 DOI:10.3760/cma.j.issn.1003-9279.2012.06.010 |
| [9] | Torner N, Martinez A, Broner S, et al. Epidemiology of acute gastroenteritis outbreaks caused by human calicivirus (Norovirus and Sapovirus) in Catalonia:a two year prospective study,2010-2011[J]. PLoS One , 2016, 11 (4) : e0152503 DOI:10.1371/journal.pone.0152503 |
| [10] | Hou J, Sánchez-Vizcaíno F, McGahie D, et al. European molecular epidemiology and strain diversity of feline calicivirus[J]. Vet Rec , 2016, 178 (5) : 114–115 DOI:10.1136/vr.103446 |
| [11] | Yoneda M, Nakano M, Sugimoto D, et al. Epidemiological characteristics of sapovirus and human astrovirus detected among children in the nara prefecture,Japan,during 2009/2010-2014/2015 seasons[J]. Jpn J Infect Dis , 2016 DOI:10.7883/yoken.JJID.2015.529 |
| [12] | Rodrigues MT, Henzel A, Staggemeier R, et al. Human adenovirus spread,rainfalls,and the occurrence of gastroenteritis cases in a Brazilian basin[J]. Environ Monit Assess , 2015, 187 (11) : 720 DOI:10.1007/s10661-015-4917-4 |
 2016, Vol. 37
2016, Vol. 37