文章信息
- 赵嘉咏, 穆玉姣, 张白帆, 夏胜利, 苏佳, 黄学勇, 许汴利 .
- Zhao Jiayong, Mu Yujiao, Zhang Baifan, Xia Shengli, Su Jia, Huang Xueyong, Xu Bianli .
- 河南省2011-2015年非伤寒沙门菌病原学与耐药监测
- Etiology and drug resistance of non-typhi Salmonella in Henan province, 2011-2015
- 中华流行病学杂志, 2016, 37(9): 1253-1256
- CHINESE JOURNAL OF EPIDEMIOLOGY, 2016, 37(9): 1253-1256
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2016.09.014
-
文章历史
收稿日期: 2016-03-31
沙门菌属是寄居在人类和动物肠道内生化反应和抗原构造相似的一类革兰阴性杆菌,是重要的人兽共患病原菌,也是造成人类食物中毒和引发食源性传染病暴发疫情的常见病原,其临床症状可表现为急性胃肠炎、肠热症(即伤寒与副伤寒)及败血症3种类型。沙门菌无荚膜,有动力,兼性厌氧,根据Kauffman-White(K-W)血清分型表,沙门属菌可分为肠炎沙门菌和邦戈尔沙门菌2个群2 700余种血清型,其在动物、食品和≤5岁低龄儿童中的检出率高,致病力强[1]。本研究对分离自河南省2011-2015年腹泻病例粪便样本中的非伤寒沙门菌进行形态学、生化鉴定,血清学分型,药物敏感性测试,深入了解和掌握其病原学特点,为相关疾病的监测、暴发预警与溯源提供基线数据。
材料与方法1. 菌株来源:参照“十二五”科技重大专项“腹泻病症候群监测技术方案”制定的腹泻病例定义[每日排便3次或以上、且大便性状有改变(呈稀便、水样便、黏脓便或脓血便等)]对河南省2011-2015年腹泻病多病原监测系统5个哨点医院全年肠道门诊及住院(郑州市、登封市、周口市、中牟县、睢县)病例进行样本采集和分离培养。5年共采集粪便样本37 528份,分离到非伤寒沙门菌1 351株,总分离率为3.6%。其中,2011年5 731份194株,2012年6 857份204株,2013年7 122份292株,2014年9 538份333株,2015年8 280份328株;按监测哨点分郑州市5 764份329株,登封市8 115份274株,周口市8 750份261株,睢县10 324份423株,中牟县4 575株64株。
2. 主要试剂:亚硒酸盐煌绿增菌液(SBG),沙门菌科玛嘉鉴定培养基(法国CHROMAgar公司)、Cary-Blair氏运送培养基,双糖铁(KIA)/动力吲哚尿素(MIU)(上海CDC)、脑心浸液/M-H琼脂,药敏纸片及分配器(英国OXOID公司)、API20E肠杆菌科细菌鉴定板条(法国bioMérieux公司)、沙门菌诊断血清,鞭毛诱导软琼脂(丹麦SSI公司)。
3. 方法:
(1)沙门菌的分离培养与生化鉴定:采集病例粪便拭子插入Cary-Blair氏运送培养基中送至实验室,接种于5 ml亚硒酸盐煌绿增菌液37 ℃培养12 h后沙门菌科玛嘉鉴定培养基三区划线,37 ℃培养过夜(16~18 h);挑取疑似菌落(紫红色、突起、光滑、湿润),做进一步生化鉴定。用无菌接种针挑取疑似菌落分别穿刺接种于克氏双糖(KIA)和动力/吲哚/尿素培养基(MIU)上,37 ℃培养18~24 h。对于符合发酵葡萄糖不发酵乳糖(K/A)、产气(gas+)、硫化氢阳性(H2S+)、动力阳性(Mov+)和吲哚阴性(-)、尿素酶阴性(URE-)的菌株可初步判定为沙门菌,API20E系统生化板条最终确认。
(2)血清学分型:鉴定后的沙门菌转种于哥伦比亚营养琼脂,37 ℃培养过夜(16~18 h)。用一次性接种环挑取小半环菌落于载玻片上,滴加1滴菌体抗原(O抗原)分型血清充分研磨,1 min内出现颗粒凝集判为阳性,生理盐水作为自凝对照;0.4%鞭毛诱导软琼脂点种,37 ℃培养16 h后取远端菌苔进行鞭毛Ⅰ与Ⅱ相(H:1/2相)诱导与血清凝集试验,根据K-W血清分型表确定对应血清型别。
(3)药敏试验:参照WHO推荐的Kirby-Bauer法,将沙门菌转种脑心浸液琼脂平板,37 ℃培养16 h后,0.85%生理盐水制成0.5麦氏单位悬液。用无菌棉拭子蘸取菌液均匀涂布于M-H平板表面,用分配器将药敏纸片压盖其上,15 min内送37 ℃温箱培养16~18 h后,测量各药敏纸片抑菌圈直径,参照美国临床实验室标准化协会(CLSI)2009年标准进行耐药表型判定,大肠埃希菌ATCC25922作为质控菌株[2]。
结 果1. 菌株来源:1 351株非伤寒沙门菌病例男女性别比例为1.5 ∶ 1(811 ∶ 540);年龄分布为0~5岁815例(60.3%),5~18岁74例(5.5%),18~30岁373例(27.6%),30~60岁20例(1.5%),>60岁69例(5.1%),以低龄儿童和青壮年为主;分离时间多集中于5-10月,具有较典型的春夏季节特征。
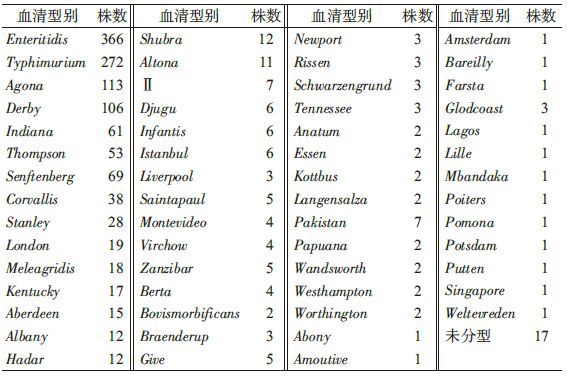
2. 血清型别鉴定:1 351株非伤寒沙门菌经血清学分型共分为58个血清型,位居前7位的是肠炎(S. enteritidis)、鼠伤寒(S. typhimurium)、阿贡那(S. agona)、德尔比(S. derby)、印第安纳(S. indiana)、森芬伯格(S. senftenberg)、汤普森(S. thompson)沙门菌,另外有17株未能分型,见表 1。
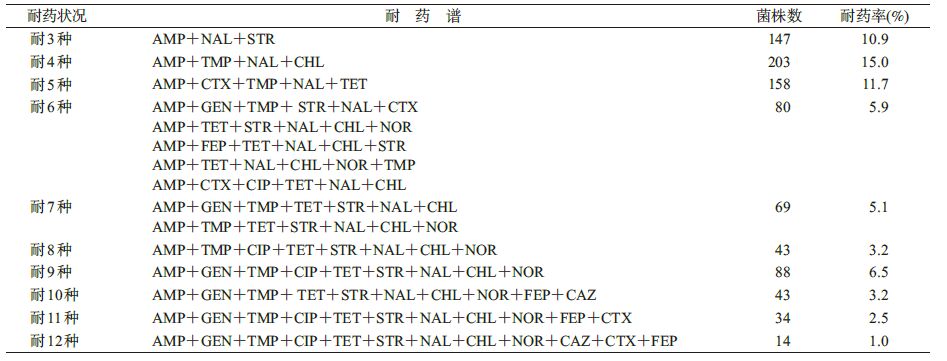
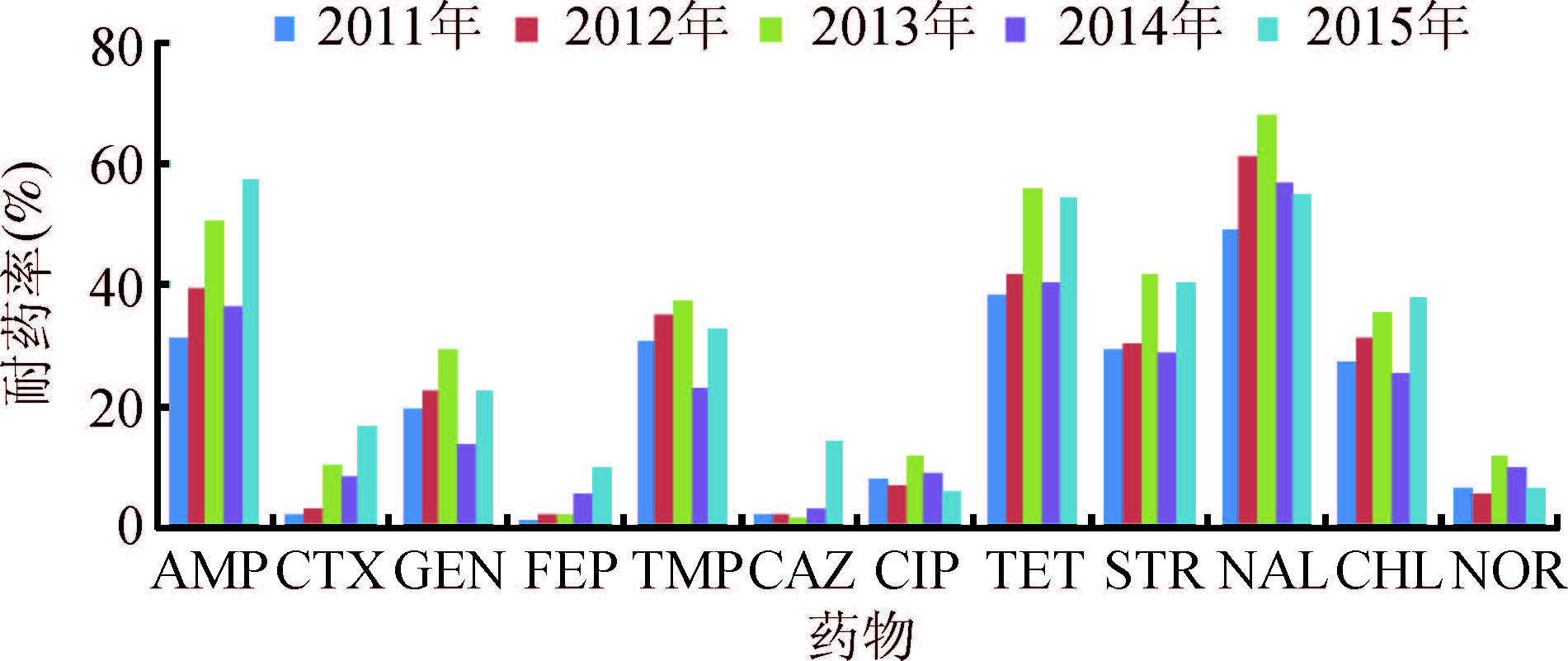
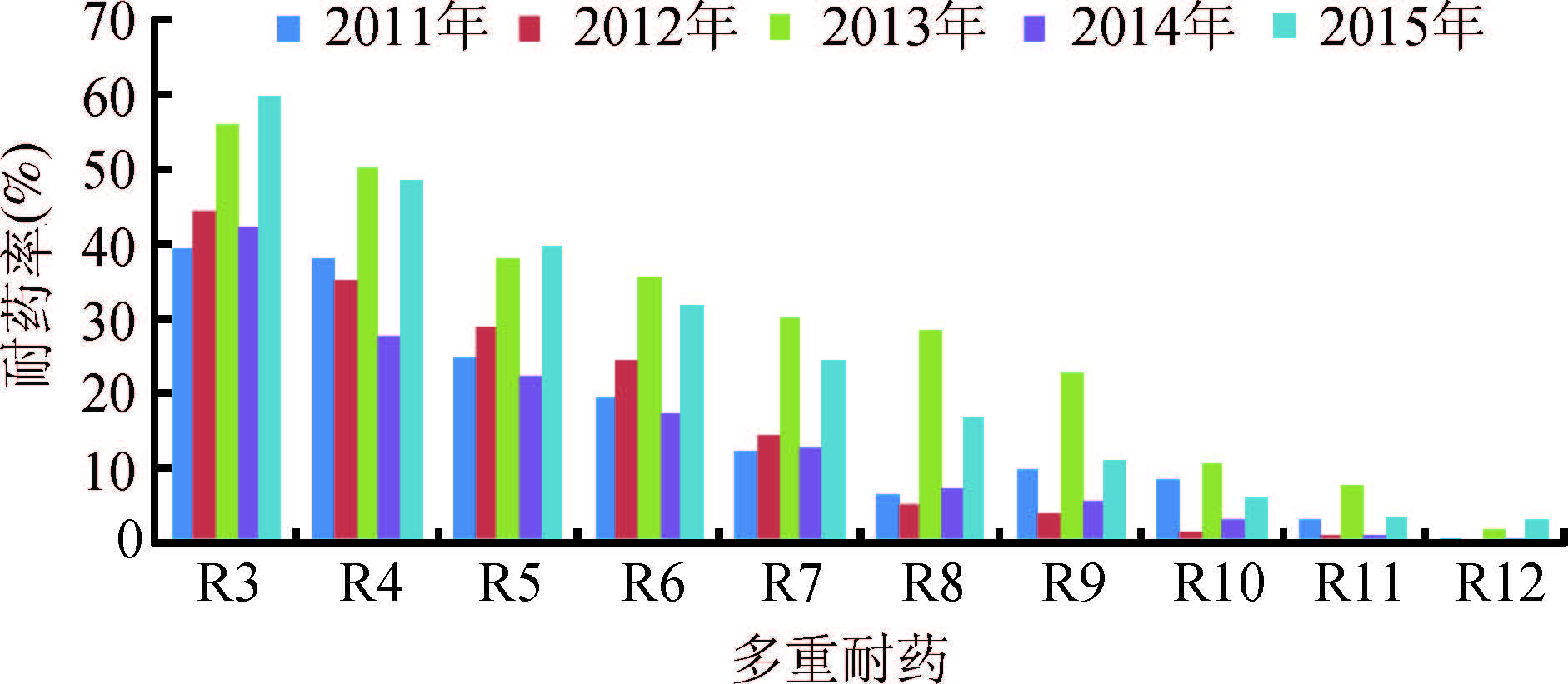
3. 药敏测试:1 351株非伤寒沙门菌对广谱合成类青霉素氨苄西林(AMP)的耐药率为46.1%;对三代头孢类抗生素头孢他啶(CAZ)、头孢噻肟(CTX)的耐药率为19.5%和21.2%,对四代头孢类抗生素头孢吡肟(FEP)的耐药率为8.8%;对一代喹诺酮类抗生素萘啶酸(NAL)的耐药率为58.7%,对三代氟喹诺酮类抗生素环丙沙星(CIP)、诺氟沙星(NOR)的耐药率为14.7%和14.7%;对氨基糖苷类抗生素庆大霉素(GEN)、链霉素(STR)的耐药率为25.0%和35.6%;对氯霉素类抗生素(CHL)的耐药率为35.4%;对增效磺胺类抗生素甲氧苄氨嘧啶(TMP)的耐药率为31.7%;对四环素(TET)的耐药率为37.8%,菌株对三代、四代头孢类抗生素的耐药率呈逐年上升趋势(表 2、图 1)。菌株多重耐药状况比较严重,1 351株非伤寒沙门菌中耐3种以上抗生素的多重耐药菌株为879株(65.1%):其中耐3~4种的为350株(25.9%),耐5~7种的为309株(22.9%),耐8~10种的为174株(12.9%),耐11~12种的为48株(3.6%)(表 3,图 2)。
|
| 图 1 2011-2015年河南省非伤寒沙门菌耐药率 |
|
| 图 2 2011-2015年河南省非伤寒沙门菌多重耐药率 |
据WHO的报告,自21世纪以来,在世界范围内,由沙门菌感染确诊的患病人数显著增加。在我国内陆地区,由非伤寒沙门菌感染引起的食物中毒屡居首位[3-4]。据资料统计,在我国细菌性食物中毒事件中,70%~80%是由非伤寒沙门菌引起,其已成为我国食源性疾病暴发疫情中最主要的病原体[5-7]。沙门菌血清型别众多,我国目前已报道的有100余种。血清学分型在沙门菌病原学监测工作中占据着非常重要的地位,也是目前全球微生物学实验室面临的挑战之一,其受试剂、技术、人员素质、经验等多方面因素制约。从河南省近几年的研究看,非伤寒沙门菌H相诱导缺失是实验室面临的主要难题,以鼠伤寒沙门菌2相缺失(1,4,5,12:i:-)最为突出,尽管我们采取了复壮、加强1相鞭毛抗原抑制、更换血清和诱导方法等措施,仍无法从根本上解决问题,分析可能存在鞭毛蛋白编码基因缺失或重组等可能性,需要进一步从分子机制上加强研究。另外还有56株未分型沙门菌,除了技术本身的局限外,是否存在新的血清型别,值得特别关注。从本研究中可以发现,河南省沙门菌的优势血清型别仍以肠炎、鼠伤寒沙门菌为主,这和其他部分省(市)的研究结果相同[8-10],但阿贡那、德尔比、印第安纳等血清型也占据着重要的位置,特别是一些罕见血清型引起的暴发疫情和聚集性病例(如2012年河南省Stanley沙门菌暴发疫情)。建立快速、高通量、高灵敏度、精准度高的血清学分型或分子分型技术平台并开展方法学比较研究,是下一步的工作重点和方向。
细菌耐药是近年来医疗卫生机构面临的重大问题。由于临床过度治疗与抗生素的滥用,病原菌的耐药现象日益严重[11-12]。从本研究药敏测试结果可以看出,河南省以非伤寒沙门菌为代表的肠道致病菌耐药问题比较严重,其对8类12种抗生素均存在不同程度的耐药,比较严重的有青霉素类、磺胺类、四环素类、氯霉素类、氨基糖苷类以及一代喹诺酮类,对临床常用药物三代头孢类及喹诺酮类抗生素耐药率比较低,但也呈上升趋势。非伤寒沙门菌的多重耐药情况也非常严重,临床分离菌株近半数对3~12种抗生素耐药,虽然其时间增高趋势并不显著,但这些耐药菌株多分离自5岁以下的低龄儿童,不仅增加了医疗成本,而且从公共卫生角度更值得关注。
| [1] | 何冬梅, 柯碧霞, 邓小玲, 等. 2010年广东省沙门菌监测及其病原学特征分析[J]. 中华预防医学杂志 , 2012, 46 (5) : 424–429 DOI:10.3760/cma.j.issn.0253-9624.2012.05.010 D M, Ke BX, Deng XL, et al. Surveillance and analysis on the pathogenic features of Salmonella in Guangdong province in 2010[J]. Chin J Prev Med , 2012, 46 (5) : 424–429 DOI:10.3760/cma.j.issn.0253-9624.2012.05.010 |
| [2] | Petrovska L, Mather AE, AbuOun M, et al. Microevolution of monophasic Salmonella typhimurium during epidemic,United Kingdom,2005-2010[J]. Emerg Infect Dis , 2016, 22 (4) : 617–624 DOI:10.3201/eid2204.150531 |
| [3] | Rivoal K, Protais J, Quéguiner S, et al. Use of pulsed-field gel electrophoresis to characterize the heterogeneity and clonality of Salmonella serotype enteritidis,typhimurium and infantis isolates obtained from whole liquid eggs[J]. Int J Food Microbiol , 2009, 129 (2) : 180–186 DOI:10.1016/j.ijfoodmicro.2008.11.021 |
| [4] | Petrov P, Hendriksen RS, Kantardjiev T, et al. Occurrence and characterization of Salmonella enterica subspecies enterica serovar 9,12:l,v:-strains from bulgaria,denmark,and the united states[J]. Eur J Clin Microbiol Infect Dis , 2009, 28 (5) : 473–479 DOI:10.1007/s10096-008-0653-9 |
| [5] | Chen MH, Hwang WZ, Wang SW, et al. Pulsed field gel electrophoresis (pfge) analysis for multidrug resistant Salmonella enterica serovar schwarzengrund isolates collected in six years (2000-2005) from retail chicken meat in taiwan[J]. Food Microbiol , 2011, 28 (3) : 399–405 DOI:10.1016/j.fm.2010.10.002 |
| [6] | Huang X, Huang Q, Dun ZJ, et al. Nontyphoidal Salmonella infection,Guangdong province,China,2012[J]. Emerg Infect Dis , 2016, 22 (4) : 726–729 DOI:10.3201/eid2204.151372 |
| [7] | Liu X, Liu Q, Xiao K, et al. Attenuated Salmonella typhimurium delivery of a novel DNA vaccine induces immune responses and provides protection against duck enteritis virus[J]. Vet Microbiol , 2016, 186 : 189–198 DOI:10.1016/j.vetmic.2016.03.001 |
| [8] | 李柏生, 柯碧霞, 何冬梅, 等. 广东省腹泻病例非伤寒沙门菌耐药谱和PFGE分型研究[J]. 中华微生物学和免疫学杂志 , 2012, 32 (6) : 542–548 DOI:10.3760/cma.j.issn.0254-5101.2012.06.012 B S, Ke BX, He DM, et al. Antimicrobial resistance patterning and pulsed field gel electrophoresis (PFGE) typing for non-typhoidal Salmonella isolated from diarrhea cases in Guangdong province,China[J]. Chin J Microbiol Immunol , 2012, 32 (6) : 542–548 DOI:10.3760/cma.j.issn.0254-5101.2012.06.012 |
| [9] | 戴月, 朱谦让, 周翌婧, 等. 2013年江苏省食源性非伤寒沙门菌疾病负担研究[J]. 江苏预防医学 , 2014, 25 (4) : 20–22 DOI:10.13668/j.issn.1006-9070.2014.04.008 Y, Zhu QR, Zhou YJ, et al. Investigation on burden of food-bourne non-typhoidal Salmonella infections in Jiangsu province[J]. Jiangsu J Prev Med , 2014, 25 (4) : 20–22 DOI:10.13668/j.issn.1006-9070.2014.04.008 |
| [10] | 于国慧, 董方, 刘锡清, 等. 2009年北京地区儿童感染性腹泻病原学及耐药性分析[J]. 中国小儿急救医学 , 2011, 18 (1) : 33–35 DOI:10.3760/cma.j.issn.1673-4912.2011.01.012 G H, Dong F, Liu XQ, et al. Analysis of etiology and drug resistance of infectious diarrhea among children in Beijing area in 2009[J]. Chin Pediatr Emerg Med , 2011, 18 (1) : 33–35 DOI:10.3760/cma.j.issn.1673-4912.2011.01.012 |
| [11] | Frink S, Morales C, Kiang D. Draft whole-genome sequences of Salmonella enterica subsp.enterica serovars enteritidis,veneziana,and salford,isolated from herbs[J]. Genome Announc , 2016, 4 (2) : e00134–16 DOI:10.1128/genomeA.00134-16 |
| [12] | Yamazaki W, Uemura R, Sekiguchi S, et al. Campylobacter and Salmonella are prevalent in broiler farms in kyushu,Japan:results of a 2-year distribution and circulation dynamics audit[J]. Appl Microbiol , 2016, 120 (6) : 1711–1722 DOI:10.1111/jam.13141 |
 2016, Vol. 37
2016, Vol. 37