文章信息
- 何寒青, 张兵, 严睿, 李倩, 符剑, 唐学雯, 周洋, 邓璇, 谢淑云 .
- He Hanqing, Zhang Bing, Yan Rui, Li Qian, Fu Jian, Tang Xuewen, Zhou Yang, Deng Xuan, Xie Shuyun .
- 不同免疫程序接种2剂麻疹-流行性腮腺炎-风疹联合减毒活疫苗的卫生经济学评价
- Economic evaluation on different two-dose-vaccination-strategies related to Measles, Mumps and Rubella Combined Attenuated Live Vaccine
- 中华流行病学杂志, 2016, 37(8): 1121-1126
- CHINESE JOURNAL OF EPIDEMIOLOGY, 2016, 37(8): 1121-1126
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2016.08.014
-
文章历史
收稿日期: 2016-01-30
麻疹-流行性腮腺炎-风疹联合减毒活疫苗(MMR)虽使相应疾病负担明显下降,但目前全球每年依然有上百万儿童受到感染[1-2]。浙江省自2007年开始采用8月龄接种1剂麻疹-风疹联合减毒活疫苗(MR)和18月龄接种1剂MMR策略后,麻疹和风疹的发病水平持续下降(2010-2015年均发病率<2/10万),但是流行性腮腺炎发病率却始终维持>30/10万,且2010-2015年报告的突发公共卫生事件达25起,可能与仅接种1剂流行性腮腺炎成分疫苗无法提供足够的保护有关[3-4]。为同步加强流行性腮腺炎控制,确保儿童能接种有2剂次流行性腮腺炎成分的疫苗,浙江省可采用接种MMR替换现有免疫规划中的8月龄接种MR;也可参考北京、上海、天津和山东等地对4~6岁儿童额外增加接种1剂MMR[5]。为此,本研究通过拟合数学模型,对浙江省可能采用的两种2剂MMR备选策略进行卫生经济学评价。
资料与方法1. 发病资料: 浙江省麻疹、流行性腮腺炎和风疹的发病数据源于“中国疾病预防控制信息系统”,查询条件为发病日期在“2014年1月1日至2014年12月31日”,现住址为“浙江省”,从而导出病例数再计算各年龄组发病率。
2. 成本计算:根据中国CDC开展的麻疹、流行性腮腺炎和风疹经济学负担调查结果[6],以及WHO推荐的发展中国家贴现率<10%范围标准[7],再结合我国医疗费用研究报道计算疾病成本[8],其中对疾病费用采用5%贴现计算得2014年每例麻疹、流行性腮腺炎和风疹的疾病经济负担成本分别为4 246.53、1 232.42和1 404.92元。疫苗和注射器成本根据2014年浙江省招标采购价格计算。根据浙江省县、乡和村级免疫规划服务成本调查结果[9],结合卢莉等[10]对浙江省计划免疫服务成本的调查及WHO推荐的成本贴现3%标准[7],计算2014年浙江省、市、县、乡镇和村级免疫规划服务成本合计为6.49元/剂次。
3. 卫生经济学评价: 本研究假定70万出生队列的封闭人群(N),从出生开始进行演变,时间节点(i)按照免疫策略不同设定为0、8、18月龄和4周岁,直至一个生命周期结束(75岁)。设定3种备选策略:现有的8月龄接种MR和18月龄接种MMR(策略1);8和18月龄均接种MMR(策略2);8月龄接种MR、18月龄和4岁均接种MMR(策略3)。不同剂次接种率用Ji,接种后保护率用Ei表示,期间发病风险(年均发病率)为Ii,Ti表示第i阶段的时间长度。并假定接种后保护率仅与剂次数有关[11],到某一接种年龄后即接种,各时间节点时接种疫苗的保护者(Vi) 、病例数(Ci) 和剩余易感者(Si)演变如图 1。

|
| 图 1 不同人群在各时间状态下的演变情况 |
采用增量成本效果比(incremental cost- effectiveness ratio,ICER)、增量成本效益比(incremental cost-benefit ratio,ICBR)和增量净收益(incremental net benefit,INB)方法,分别将策略2、3与策略1比较,计算方法为
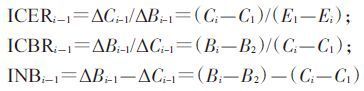
其中C(cost)为接种成本=∑(疫苗+注射器)单价(元/人份) ×损耗系数×接种数量+每剂次工作成本(元/剂次)×接种数量×接种率;E(effectiveness)为效果=∑(麻疹+流行性腮腺炎+风疹)发病数;B(benefit)为效益=∑(麻疹+流行性腮腺炎+风疹)疾病经济负担。
4. 统计学分析:采用Microsoft Excel和R软件。经济学评价均贴现(3%)至2014年。敏感性分析包括对不同免疫策略接种率、疫苗保护效果(VE)进行浮动调整,以及对发病风险、疾病成本、疫苗价格和接种成本(按±5%、±10%等比例)的调整。
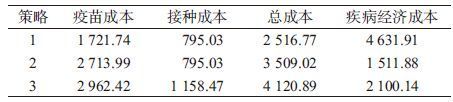
结 果1. 不同免疫策略的成本:假定8、18月龄和4岁的接种率分别为90%、85%和80%[12],按MR 5.8元/人份、MMR 20.8元/人份、注射器0.3元/人份,损耗系数采用1.05测算不同策略的接种成本。策略1接种成本为2 516.77万元、策略2为3 509.02万元、策略3为4 120.89万元。在设定条件下测算70万队列人群观察75年后,按策略1的条件下发生麻疹、流行性腮腺炎和风疹的人数分别为423、6 859和98人;策略2分别为423、1 929和98人;策略3分别为422、3 077和97人。策略1、策略2和策略3发生病例的经济成本合计分别为4 631.91、1 511.88和2 100.14万元(表 1)。
2. 不同免疫策略的卫生经济学评价:与策略1相比,策略2和3的 ICER分别为2 012.51 ∶ 1和4 238.72 ∶ 1,即与策略1比,策略2每增加2 012.51元可减少1例病例的发生,策略3则是增加4 238.72元投入可减少1例病例。ICBR2-1 和ICBR3-1分别为1 ∶ 3.14和1 ∶ 1.58,即与策略1比,每增加1元投入,策略2和策略3实施后可分别减少3.14元和1.58元疾病负担损失,均符合成本效益。根据INB结果,与策略1相比,实施策略2和3均为正效益,INB分别为2 127.78万元和927.65万元。
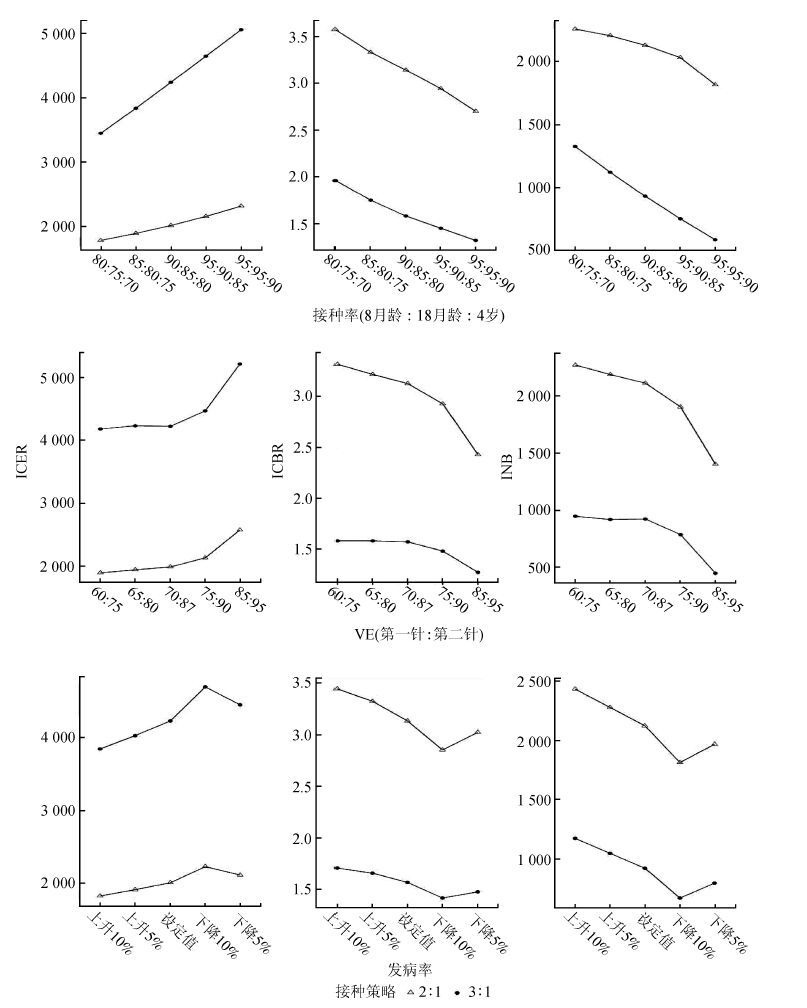
3. 卫生经济学评价结果的敏感性分析:在接种率、VE、发病率、疾病负担、疫苗和接种成本的变化下,与策略1相比,策略2的 ICER、ICBR均低于策略3,但INB高于策略3(图 2)。
|
| 图 2 不同MMR免疫策略的接种率、VE和发病率卫生经济学评价的敏感性分析 |
调整接种率(70%~95%)后,ICER2-1变化在1 780.83~2 313.51元/例、ICER3-1在3 445.67~5 056.06元/例;ICBR2-1在1 ∶ 2.70 ~3.57,ICBR3-1在1 ∶ 1.32 ~1.96; INB2-1在1 813.22~2 255.78万元,INB3-1在582.48~1 322.60万元。对VE敏感性分析显示[13-14],麻疹、风疹疫苗的VE(75.0%~99.5%)变化后各指标基本不变(仅ICER3-1、INB3-1有1%范围内变化)。调整流行性腮腺炎疫苗的VE(60%~95%)后,ICER2-1变化在1 917.95~2 597.12元/例,ICER3-1在4 197.06~5 225.83元/例;ICBR2-1在1 ∶ 2.44~3.33,ICBR3-1在1 ∶ 1.28~1.59; INB2-1在1 411.76~2 287.61万元,INB3-1在449.72~952.77万元。发病风险的敏感性分析(按±5%、±10%),ICER2-1变化在1 830.43~2 235.06元/例,ICER3-1在3 854.79~4 707.97元/例;ICBR2-1在1 ∶ 2.86~3.45,ICBR3-1为1 ∶ 1.43~1.72; INB2-1在1 817.88~2 437.22万元,INB3-1在675.94~1 179.04万元(图 3)。

|
| 图 3 不同MMR免疫策略的疾病成本、疫苗价格和接种成本卫生经济学评价结果的敏感性分析 |
对疾病成本、疫苗价格和接种成本敏感性分析(按±5%、±10%)显示,疾病成本变化后ICER均保持不变,ICBR2-1变化在1 ∶ 2.86~3.45,ICBR3-1在1 ∶ 1.43~1.72; INB2-1在1 815.78~2 439.79万元,INB3-1在674.48~1 180.83万元。疫苗价格调整后,ICER2-1变化在1 811.26~2 213.76元/例,ICER3-1在3 910.88~4 566.56元/例;ICBR2-1在1 ∶ 2.86~3.45,ICBR3-1在1 ∶ 1.47~1.72; INB2-1在2 028.56~2 227.01万元,INB3-1在803.58~1 051.72万元。接种成本变化后ICER2-1、ICBR2-1和INB2-1均不变,ICER3-1在4 142.69~4 334.76元/例,ICBR3-1在1∶1.54~1.61,INB3-1在891.31~964.00万元。
讨 论本研究在当前国家免疫规划策略基础上,对设定的两种不同免疫接种策略建立模型并进行卫生经济学评价。结果显示,采用策略3(8月龄接种MR+18月龄接种MMR+4岁接种MMR)的接种成本最高,实施策略2则发病总人数最少及疾病经济负担最低。与策略1相比,减少1例病例,策略3的增量投入是策略2的2.11倍;策略2的ICBR为1 ∶ 3.14,也优于策略3的1 ∶ 1.58;策略2的INB为2127.78万元,是策略3的2.29倍。就各项指标评价结果而言,策略2的各项指标结果均优于策略3,且敏感性分析结果也与此一致,卫生经济学评价结果更优。
实施接种2剂MMR符合成本效益,是免疫规划发展的趋势。但考虑到母传抗体等因素,WHO推荐在满12月龄后开始接种MMR。近年来很多研究报道儿童在6月龄后麻疹[15]、流行性腮腺炎和风疹母传抗体已基本消失[16]。2011年浙江省发生小年龄组儿童麻疹暴发疫情,证实8月龄儿童已是高危易感染人群[17]。一些发达国家也有关于婴幼儿母传抗体早期消失的报道,尤其来自接种疫苗获得保护的妇女其婴幼儿母传抗体下降更快[18-19]。近期研究表明6月龄婴儿接种MMR也能提供与12月龄时接种获得的相同细胞免疫保护[20-21],虽然体液免疫保护略有差异,但同样能有效减低麻疹、流行性腮腺炎的发病和死亡[22]。浙江省对接种MMR后随访1年观察表明,8月龄和12月龄儿童具有相同的免疫原性和安全性[11]。由于婴幼儿感染发病后更易出现并发症而发生重症病例[23],在疾病负担较高的地方,可采用早期接种MMR的策略[24],如学龄前儿童在幼儿园的传播风险较大,建议在2岁内接种第2剂[25]。本研究中策略3提供了2剂流行性腮腺炎疫苗的保护,但由于接种时间较晚(第1剂在18月龄,第2剂在4岁),依然有较多儿童在接种第2剂MMR前发病[14]。
本研究存在局限性。如评价仅是基于一个封闭人群的发病测算,许多参数都是理论性的或基于假设,其结果的外推存在一定缺陷。但敏感性分析表明,对主要参数调整后,评价指标变化均不大,且结论均一致,表明本研究结果还是较为稳定。
综上所述,采用2针次MMR免疫策略是全国免疫规划的发展趋势,从目前的8月龄接种MR和18月龄接种MMR免疫策略调整为8和18月龄均接种MMR,或4岁时增加1剂MMR均符合卫生经济学要求。当前情况下,与4岁额外增加接种1剂次MMR相比,调整为8和18月龄均接种MMR的策略更具有卫生经济学意义。
| [1] | Papania MJ, Wallace GS, Rota PA, et al. Elimination of endemic measles,rubella,and congenital rubella syndrome from the western hemisphere:the US experience[J]. JAMA Pediatr , 2014, 168 (2) : 148–155 DOI:10.1001/jamapediatrics.2013.4342 |
| [2] | White SJ, Boldt KL, Holditch SJ, et al. Measles,mumps,and rubella[J]. Clin Obstet Gynecol , 2012, 55 (2) : 550–559 DOI:10.1097/GRF.0b013e31824df256 |
| [3] | 符剑, 陈恩富, 李倩, 等. 2005-2009年浙江省流行性腮腺炎监测和暴发疫情分析[J]. 疾病监测 , 2011, 26 (4) : 284–286 DOI:10.3784/j.issn.1003-9961.2011.04.009 Fu J, Chen EF, Li Q, et al. Surveillance of mumps in Zhejiang province,2005-2009[J]. Dis Surveill , 2011, 26 (4) : 284–286 DOI:10.3784/j.issn.1003-9961.2011.04.009 |
| [4] | Hviid A, Rubin S, Mühlemann K. Mumps[J]. Lancet , 2008, 371 (9616) : 932–944 DOI:10.1016/S0140-6736(08)60419-5 |
| [5] | 刘隽, 苏琪茹, 马超, 等. 不同免疫策略下流行性腮腺炎发病特征的初步比较分析[J]. 中国疫苗和免疫 , 2014, 20 (6) : 519–522 Liu J, Su QR, Ma C, et al. Preliminary comparative analysis of epidemic characteristics of mumps with different vaccination strategies in China[J]. Chin J Vacc Immunizat , 2014, 20 (6) : 519–522 |
| [6] | 郭世成, 梁晓峰, 左树岩. 2004年全国麻疹风疹流行性腮腺炎经济负担调查分析[J]. 中国疫苗和免疫 , 2008, 14 (1) : 32–36 Guo SC, Liang XF, Zuo SY. Economical burden on measles,rubbella,and mumps cases in China in 2004[J]. Chin J Vacc Immunizat , 2008, 14 (1) : 32–36 |
| [7] | World Health Organization.WHO guide for standardization of economic evaluations of immunization programmes[M].Geneva: WHO Document Production Services, 2008: 56–57 |
| [8] | 易伟愿, 庞军, 李智华. 2001-2010年广西中医医院人均医疗费用情况分析[J]. 广西医学 , 2013, 35 (1) : 88–90 DOI:10.11675/j.issn.0253-4304.2013.01.32 Yi WY, Pang J, Li ZH. Analysis on the per capita medical expenditure of Guangxi traditional Chinese medicine hospital from 2001 to 2010[J]. Guangxi Med J , 2013, 35 (1) : 88–90 DOI:10.11675/j.issn.0253-4304.2013.01.32 |
| [9] | 何寒青, 陈恩富, 李倩, 等. 浙江省1978-2007年计划免疫卫生经济学评价[J]. 中国农村卫生事业管理 , 2010, 30 (10) : 835–837 He HQ, Chen EF, Li Q, et al. Health economic appraisal for 30-year expanded program on immunization in Zhejiang province[J]. Chin Rural Health Service Administrat , 2010, 30 (10) : 835–837 |
| [10] | 卢莉, 金水高, 于竞进, 等. 不同经济水平地区计划免服务成本的筹资现状分析[J]. 中国计划免疫 , 2005, 11 (3) : 217–220 DOI:10.3969/j.issn.1006-916X.2005.03.014 Lu L, Jin SG, Yu JJ, et al. Financing situation of expanded programme on immunization in areas at different economic levels[J]. Chin J Vacc Immunizat , 2005, 11 (3) : 217–220 DOI:10.3969/j.issn.1006-916X.2005.03.014 |
| [11] | He HQ, Chen EF, Chen HP, et al. Similar immunogenicity of measles-mumps-rubella (MMR) vaccine administrated at 8 months versus 12 months age in children[J]. Vaccine , 2014, 32 (31) : 4001–4005 DOI:10.1016/j.vaccine.2014.04.044 |
| [12] | 郑景山, 曹雷, 郭世成, 等. 2013年全国省级抽查以乡为单位适龄儿童国家免疫规划疫苗接种率分析[J]. 中国疫苗和免疫 , 2014, 20 (6) : 492–498 Zheng JS, Cao L, Guo SC, et al. Immunization coverage of the National Immunization Program vaccines at the township level,based on a survey conducted by provincial CDCs in China,2013[J]. Chin J Vacc Immunizat , 2014, 20 (6) : 492–498 |
| [13] | Uzicanin A, Zimmerman L. Field effectiveness of live attenuated measles-containing vaccines:a review of published literature[J]. J Infect Dis , 2011, 204 (Suppl 1) : S133–149 DOI:10.1093/infdis/jir102 |
| [14] | Wang HQ, Hu YM, Zhang GM, et al. Meta-analysis of vaccine effectiveness of mumps-containing vaccine under different immunization srategies in China[J]. Vaccine , 2014, 32 (37) : 4806–4812 DOI:10.1016/j.vaccine.2014.05.061 |
| [15] | He HQ, Chen EF, Li Q, et al. Waning immunity to measles in young adults and booster effects of revaccination in secondary school students[J]. Vaccine , 2013, 31 (3) : 533–537 DOI:10.1016/j.vaccine.2012.11.014 |
| [16] | Wang ZF, Yan R, He HQ, et al. Difficulties in eliminating measles and controlling rubella and mumps:a cross-sectional study of a first measles and rubella vaccination and a second measles,mumps,and tubella vaccination[J]. PLoS One , 2014, 9 (2) : e89361 DOI:10.1371/journal.pone.0089361 |
| [17] | Gao J, Chen EF, Wang ZG, et al. Epidemic of measles following the nationwide mass immunization campaign[J]. BMC Infect Dis , 2013, 13 (1) : 139 DOI:10.1186/1471-2334-13-139 |
| [18] | Leuridan E, Hens N, Hutse V, et al. Early waning of maternal measles antibodies in era of measles elimination:longitudinal study[J]. BMJ , 2010, 340 : c1626 DOI:10.1136/bmj.c1626 |
| [19] | Leineweber B, Grote V, Schaad UB, et al. Transplacentally acquired immunoglobulin G antibodies against measles,mumps,rubella and varicella-zoster virus in preterm and full term newborns[J]. Pediatr Infect Dis J , 2004, 23 (4) : 361–363 DOI:10.1097/00006454-200404000-00019 |
| [20] | Gans HA, Ren JY, Yasukawa LL, et al. Humoral and cell-mediated immune responses to an early 2-dose measles vaccination regimen in the United States[J]. J Infect Dis , 2004, 190 (1) : 83–90 DOI:10.1086/421032 |
| [21] | Njie-Jobe J, Nyamweya S, Miles DJC, et al. Immunological impact of an additional early measles vaccine in Gambian children:responses to a boost at 3 years[J]. Vaccine , 2012, 30 (15) : 2543–2550 DOI:10.1016/j.vaccine.2012.01.083 |
| [22] | Gans H, Yasukawa L, Rinki M, et al. Immune responses to measles and mumps vaccination of infants at 6,9,and 12 months[J]. J Infect Dis , 2001, 184 (7) : 817–826 DOI:10.1086/323346 |
| [23] | Wolfson LJ, Grais RF, Luquero FJ, et al. Estimates of measles case fatality ratios:a comprehensive review of community-based studies[J]. Int J Epidemiol , 2009, 38 (1) : 192–205 DOI:10.1093/ije/dyn224 |
| [24] | Hutchins SS, Dezayas A, Le Blond K, et al. Evaluation of an early two-dose measles vaccination schedule[J]. Am J Epidemiol , 2001, 154 (11) : 1064–1071 DOI:10.1093/aje/154.11.1064 |
| [25] | Sever AE, Rainey JJ, Zell ER, et al. Measles elimination in the Americas:a comparison between countries with a one-dose and two-dose routine vaccination schedule[J]. J Infect Dis , 2011, 204 : S748–755 DOI:10.1093/infdis/jir445 |
 2016, Vol. 37
2016, Vol. 37