文章信息
- 陈诗娴, 周玲, 陈永忠, 潘洪秋, 唐少文.
- Chen Shixian, Zhou Ling, Chen Yongzhong, Pan Hongqiu, Tang Shaowen.
- 住院抗结核治疗患者药物性肝炎发生及转归研究
- Incidence and outcome of anti-tuberculosis drug-induced hepatotoxicity in tuberculosis inpatients
- 中华流行病学杂志, 2016, 37(7): 930-934
- Chinese Journal of Epidemiology, 2016, 37(7): 930-934
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2016.07.005
-
文章历史
- 投稿日期: 2016-02-28
2. 212005 镇江市第三人民医院结核病科
2. Department of Tuberculosis, The Third People's Hospital of Zhenjiang Affiliated to Jiangsu University, Zhenjiang 212005, China
结核病是由结核分枝杆菌引起的慢性呼吸道传染病,为全球重大公共卫生问题。由于长时间、多种药物的联合使用,结核病患者会出现不同程度的不良反应,其中以抗结核药致肝损伤(anti-tuberculosis drug-induced hepatotoxicity,ATDH)较为常见且最为严重[1]。本研究基于江苏省镇江市第三人民医院2006-2012年住院结核患者病案资料及出院后门诊随访记录,描述和分析抗结核治疗患者的ATDH发生及其转归,从而为ATDH的预防诊断及治疗提供临床依据。
对象与方法1. 研究对象:2006年1月至2012年7月间曾在镇江市第三人民医院住院接受抗结核治疗的患者。纳入标准:符合《肺结核诊断和治疗指南》[2]和《肺外结核的诊断和治疗》[3]的诊断标准,且住院治疗患者。排除标准:治疗期间无肝功能检测或只有基线肝功能检测的患者。
2. 资料收集:根据住院抗结核治疗患者的病历,收集患者的人口学资料、疾病相关资料、用药资料及ATDH情况,同时收集肝功能检测记录,包括ALT、AST、总胆红素(TBIL)等指标。
3. ATDH诊断:采用两种标准:①国际共识会议标准[4]:ALT >2倍的正常值上限(ULN)(2×ULN),或AST和TBIL联合升高,且其中之一升高>2×ULN,并排除其他原因引起的肝功能异常。②美国胸科协会标准[5]:ALT>3×ULN且伴有相关症状;或AST>3×ULN且伴有相关症状;或ALT>5×ULN伴有或不伴有相关症状;或AST>5×ULN伴有或不伴有相关症状;或TBIL>2×ULN。采用RUCAM(Roussel Uclaf Causality Assessment Method)简化评分系统来判断因果关系[6],且≥3分者判断为ATDH。其中,ALT及AST的ULN为40 U/L,TBIL的ULN为20 μmol/L。
4. 统计学分析:应用EpiData 3.1软件建立录入系统,并进行双轨录入和一致性核查。使用SPSS 20.0软件进行统计学分析,定量正态分布资料采用x±s表示,偏态分布资料采用M(QR)表示;定性资料采用构成比或率表示。对两组或多组定性资料的比较采用 χ2检验。
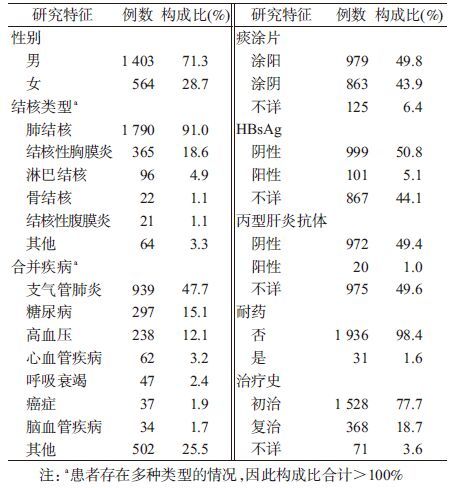
结 果1. 人口学特征:共纳入住院抗结核治疗患者1 967例,其中男性1 403例(71.3%);年龄在9~90岁,平均年龄为(48.26±19.4)岁[男性(50.34±19.2)岁,女性(43.08±19.1)岁]。
2. 疾病情况:在1 967例患者中,肺结核最多(占91.0%),同时有两种及以上类型结核的患者377例(占19.2%),65.9%的患者合并其他疾病(表1)。
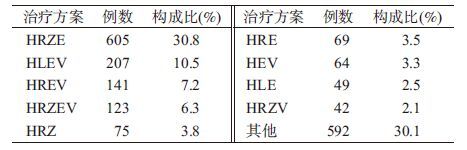
3. 治疗情况:在1 967例患者中,1 804例患者常规住院治疗,163例(16.7%)患者在住院前已接受抗结核治疗,其中21例(12.9%)因治疗效果不佳住院、30例(18.5%)因出现不良反应住院、112例(68.7%)因症状(咳嗽、咳痰、咯血)明显加重住院。住院抗结核药物主要有异烟肼(H)、利福平(R)、利福喷丁(L)、吡嗪酰胺(Z)、乙胺丁醇(E)、左氧氟沙星(V)等,治疗方案构成见表2。患者平均住院天数为37(M=30),肝功能检测次数M为7(QR:4~11),最多50次。治疗前初始ALT均值为22.8 U/L,AST均值为26.8 U/L,TBIL均值为10.9 μmol/L。
治疗过程中,78.3%的患者全程服用预防性保肝药,83.5%的患者使用一种保肝药,使用频次较高的为慢肝养阴胶囊、水飞蓟宾葡甲胺片、复方甘草酸苷等(表3)。
住院期间,19例患者发生死亡(15例为呼吸衰竭或伴有循环衰竭,2例为窒息,1例为心源性猝死,1例为全身衰竭)。
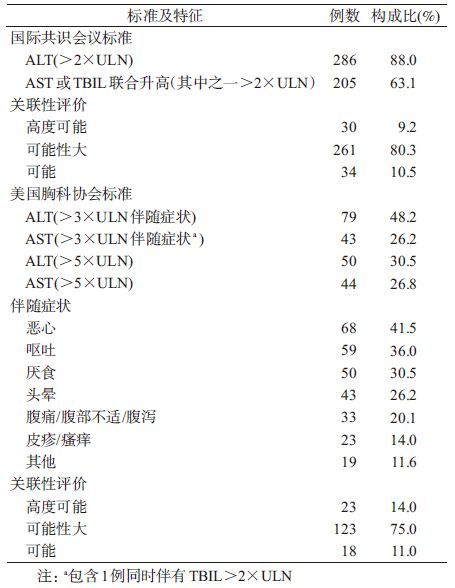
4. ATDH的发生:依据国际共识会议标准,325例患者被判断为ATDH,发生率为16.5%,发生时间为25 d(QR:12~46.5 d)。依据美国胸科协会标准,164例患者被判定为ATDH,发生率为8.3%,发生时间为23 d(QR:13~44 d)。具体构成见表4。
在两种判断标准下,男性ATDH发生率均高于女性,差异有统计学意义(P<0.05),使用HRZE治疗方案ATDH发生率高于其他方案,差异有统计学意义(P<0.05),但不同年龄、有无合并疾病、有无使用保肝药以及初复治的ATDH发生率差异均无统计学意义(P>0.05),见表5。
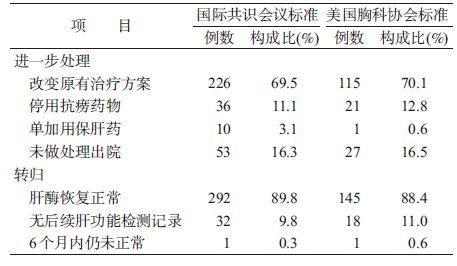
5. ATDH的转归:在两种判断标准下,ATDH发生后进一步处理主要是改变原有治疗方案或停药等,大部分患者肝酶恢复正常(表6)。依据治疗方案变动情况,可疑药物依次为利福平(134例)、吡嗪酰胺(119例)、异烟肼(109例)、利福喷丁(20例)、百生肼(8例)、丙硫异烟胺(7例)、丁胺卡那霉素(7例)。
ATDH是在抗结核治疗过程中发生频率最高且最为严重的不良反应,导致患者服药的不规律性、结核治疗的中断进而治疗失败,同时也会增加结核耐药性的发生,甚至演变为肝衰竭危及患者生命[7]。因此,分析住院抗结核治疗患者ATDH的发生及转归将有助于针对性的预防和控制。
本研究结果显示,基于国际共识会议标准ATDH的发生率为16.5%,基于美国胸科协会标准的ATDH发生率为8.3%,两种诊断标准下的ATDH发生率差异有统计学意义( χ2=60.532,P<0.000 1)。既往文献报道ATDH发生率在2%~28%之间,除与采用的诊断标准不尽相同外,还与种族、地区、肝功能检测频率、社会经济状况、病毒性肝炎流行、预防性治疗等因素相关[1]。同样是中国人群,以大样本社区抗结核治疗人群为研究对象,中国人群ATDH发生率为2.55%(美国胸科协会标准)[8]。但周丽莎和耿文奎[9]对781例住院抗结核治疗患者进行研究,160例出现肝损害(国际共识会议标准),发生率为20.5%。Shu等[10]对来自台湾大学医院连续五年的926例肺结核患者进行回顾性研究,ATDH发生率为12.0%(国际共识会议标准)。而夏愔愔和詹思延[11]综合不同诊断标准下的117篇文献,其结果表明ATDH发生率为11.9%。本研究纳入连续七年的住院病例,病情相对较重,65.9%的患者合并其他疾病,且29.0%患者有肺外结核,这可能是住院患者ATDH发生率高的原因。
既往研究显示ATDH的危险因素主要是人口学因素(女性、高龄)、HIV/AIDS、既往肝病史、基因、饮酒、服药方式等[12]。但本研究显示,两种诊断标准下男性发生率均高于女性。这与吴玉华和武谦虎[13]研究结果相一致,后者也提示男性发生率高于女性。这可能与男性病情相对较重,用药量较大有关。同样,本研究还显示≥50岁与<50岁患者的ATDH发生率差异无统计学意义。对于高龄危险因素,国内学者的研究也不尽相同,许光辉等[14]研究发现ATDH的发生与年龄无统计学关联。
本研究显示,在两种标准下HRZE治疗方案ATDH发生率高于其他方案组(P<0.05)。既往有研究表明,服用HRZE/HRZ方案的结核患者的ATDH发生率为20.5%(国际共识会议标准)[9]。虽然ATDH产生机制尚未明确,但异烟肼、利福平、吡嗪酰胺被认为是引起ATDH的主要药物,HRZ联合应用时对肝脏损害更为严重[1]。有研究显示应用HRZE方案组ATDH发生率为46.1%,明显高于HLAMKO方案组[15]。Chang等[16]也发现HRZ治疗方案ATDH发生率(2.6%)高于HR方案(0.8%)。本研究也未发现耐药结核患者与非耐药患者ATDH的发生率差异有统计学意义(P>0.05),与Sun等[17]结果相一致(P=0.086)。
本研究的住院抗结核治疗患者ATDH的中位发生时间为25 d,83.7%患者发生ATDH在开始治疗后的前2个月内,与吴玉华和武谦虎[13]研究显示发病时间为用药后7~60 d、平均天数为36 d相接近。Shu等[10]在台湾地区研究显示ATDH发生的中位时间是38 d。ATDH的发生一般都在抗结核治疗的强化期,用药种类多,用药量大,但不同研究间具体发生时间尚存在一定差异。本研究ATDH发生时间短于其他研究,与本研究纳入患者例数较多及病情相对较重有关。从导致肝损伤的药物来看,频率最高的为利福平,其次为吡嗪酰胺、异烟肼、利福喷丁,与相关综述中描述的大致相同[18]。
进一步分析预防性保肝药对ATDH发生的影响,在两种判断标准下,服用组与未服用组的发生率差异均无统计学意义(国际共识会议标准,16.9% vs. 15.2%,χ2=0.669,P=0.716;美国胸科协会标准,8.2% vs. 8.6%,χ2=0.523,P=0.770)。目前,多篇文献提示保肝药物对ATDH的发生无预防作用[19, 20]。保肝药物种类数量繁多,对其作用机制仍缺乏了解,鲜有大样本随机对照试验评估各种保肝药物对ATDH的预防作用,对何时进行预防性保肝也有一定争议[21],过量使用保肝药可能加重患者肝脏负担。因此,对抗结核患者使用保肝药的种类、时间、剂量迫切需要规范化。
本研究纳入连续七年的住院抗结核治疗病例资料,样本量大,用药信息详实,基本排除了饮酒等混杂因素,ATDH的判断采用两种通用标准,有助于不同地区不同标准研究的比较。但本研究也存在一定局限性,如未检测乙型肝炎和丙型肝炎等。住院抗结核治疗的方案调整相对频繁,本研究尚有17.7%的其他方案,因例数少未能分析其与ATDH的关系。
利益冲突 无
| [1] Tostmann A,Boeree MJ,Aarnoutse RE,et al. Antituberculosis drug-induced hepatotoxicity:Concise up-to-date review[J]. J. DOI:J Gastroen Hepatol,2008,23(2):192-202.x. |
| [2] 中华医学会结核病学分会. 肺结核诊断和治疗指南[J]. 中华结核和呼吸杂志,2001,24(2):70-74. Tuberculosis Branch of the Chinese Medical Association. Tuberculosis diagnosis and treatment guidelines[J]. Chin J Tuberc Respir Dis,2001,24(2):70-74. |
| [3] 许绍发,端木宏谨. 肺外结核的诊断和治疗[J]. 中华结核和呼吸杂志,1997,20(3):131-132. Xu SF,Duanmu HJ. The diagnosis and treatment of extrapulmonary tuberculosis[J]. Chin J Tuberc Respir Dis,1997,20(3):131-132. |
| [4] Benichou C. Criteria of drug-induced liver disorders. Report of an international consensus meeting[J]. J. DOI:J Hepatol,1990,11(2):272-276.1016/0168-8278(90)90124-A. |
| [5] Saukkonen JJ,Cohn DL,Jasmer RM,et al. An official ATS statement:hepatotoxicity of antituberculosis therapy[J]. A. DOI:Am J Respir Crit Care Med,2006,174(8):935-952.200510-1666ST. |
| [6] Aithal GP,Watkins PB,Andrade RJ,et al. Case definition and phenotype standardization in drug-induced liver injury[J]. Clin Pharmacol Ther,2011,89(6):806-815. DOI:10.1038/clpt. 2011.58. |
| [7] Lv XZ,Tang SW,Xia YY,et al. Adverse reactions due to directly observed treatment strategy therapy in Chinese tuberculosis patients:a prospective study[J]. PLoS One,2013,8(6):e65037. DOI:10.1371/journal.pone.0065037. |
| [8] Shang PH,Xia YY,Liu FY,et al. Incidence,clinical features and impact on anti-tuberculosis treatment of anti-tuberculosis drug induced liver injury (ATLI)in China[J]. PLoS One,2011,6(7):e21836. DOI:10.1371/journal.pone.0021836. |
| [9] 周丽莎,耿文奎. 初治肺结核住院患者发生肝损害的危险因素分析[J]. 内科,2009,4(2):184-187. DOI:10.3969/j.issn. 1673-7768.2009.02.009. Zhou LS,Geng WK. A research of drug-induced liver injury of tuberculosis patients hospitalized for initial treatment[J]. Internal Med China,2009,4(2):184-187. DOI:10.3969/j.issn.1673-7768.2009.02.009. |
| [10] Shu CC,Lee CH,Lee MC,et al. Hepatotoxicity due to first-line anti-tuberculosis drugs:a five-year experience in a Taiwan medical centre[J]. Int J Tuberc Lung Dis,2013,17(7):934-939. DOI:10.5588/ijtld.12.0782. |
| [11] 夏愔愔,詹思延. 国内抗结核药物不良反应发生率的综合分析[J]. 中华结核和呼吸杂志,2007,30(6):419-423. DOI:10. 3760/cma.j.issn.1001-0939.2007.06.007. Xia YY,Zhan SY. Systematic review of anti-tuberculosis drug induced adverse reactions in China[J]. Chin J Tuberc Respir Dis,2007,30(6):419-423. DOI:10.3760/cma.j.issn.1001-0939.2007. 06.007. |
| [12] Ramappa V,Aithal GP. Hepatotoxicity related to anti-tuberculosis drugs:mechanisms and management[J]. J Clin Exp Hepatol,2013,3(1):37-49. DOI:10.1016/j.jceh.2012.12.001. |
| [13] 吴玉华,武谦虎. 抗结核药致肝损害1949例文献分析[J]. 西北药学杂志,2015,30(6):750-753. DOI:10.3969/j.issn.1004-2407.2015.06.028. Wu YH,Wu QH. Literature analysis of 1949 cases liver injury induced by anti-TB drugs[J]. Northwest Pharm J,2015,30(6):750-753. DOI:10.3969/j.issn.1004-2407.2015.06.028. |
| [14] 许光辉,陈维清,陈华,等. 抗结核药物诱导肝损伤的影响因素探讨[J]. 药物流行病学杂志,2008,17(6):377-380. DOI:10.3969/j.issn.1005-0698.2008.06.010. Xu GH,Chen WQ,Chen H,et al. Influence factors of liver injury induced by anti-tuberculosis drugs[J]. Chin J Pharmacoepidemiol,2008,17(6):377-380. DOI:10.3969/j.issn.1005-0698.2008. 06.010. |
| [15] 陈琳,贾战生,傅恩清,等. 两种抗结核化疗方案对肺结核患者肝功能影响的比较[J]. 第四军医大学学报,2002,23(13):1228-1230. DOI:10.3321/j.issn.1000-2790.2002.13.022. Chen L,Jia ZS,Fu EQ,et al. Comparison of the effects two treatments for tuberculosis on liver function in patients with pulmonary tuberculosis[J]. J Fourth Mil Med Univ,2002,23(13):1228-1230. DOI:10.3321/j.issn.1000-2790.2002.13.022. |
| [16] Chang KC,Leung CC,Yew WW,et al. Hepatotoxicity of pyrazinamide:cohort and case-control analyses[J]. Am J Respir Crit Care Med,2008,177(12):1391-1396. DOI:10.1164/rccm.200802-355OC. |
| [17] Sun Q,Zhang Q,Gu J,et al. Prevalence,risk factors,management,and treatment outcomes of first-line antituberculous drug-induced liver injury:a prospective cohort study[J]. Pharmacoepidemiol Drug Saf,2016. DOI:10.1002/pds.3988. |
| [18] 肖和平. 抗结核治疗时预防性保肝用药的是与非[J]. 中华结核和呼吸杂志,2013,36(10):722-723. DOI:10.3760/cma.j.issn.1001-0939.2013.10.002. Xiao HP. Preventive use of hepatoprotectors during anti-tuberculosis treatment[J].Chin J Tuberc Respir Dis,2013,36(10):722-723. DOI:10.3760/cma.j.issn.1001-0939.2013. 10.002. |
| [19] Zhang SM,Pan HQ,Peng XZ,et al. Preventive use of a hepatoprotectant against anti-tuberculosis drug-induced liver injury:A randomized controlled trial[J]. J Gastroen Hepatol,2016,31(2):409-416. DOI:10.1111/jgh.13070. |
| [20] Wu SS,Xia YY,Lv XZ,et al. Preventive use of hepatoprotectors yields limited efficacy on the liver toxicity of anti-tuberculosis agents in a large cohort of Chinese patients[J]. J Gastroenterol Hepatol,2015,30(3):540-545. DOI:10.1111/jgh.12717. |
| [21] 缪晓辉. 如何防护抗结核药所致肝损伤[J]. 中华结核和呼吸杂志,2013,36(10):729-731. DOI:10.3760/cma.j.issn.1001-0939.2013.10.006. Miao XH. How to protect anti-tuberculosis drug induced-liver injury[J].Chin J Tuber Respirc Dis,2013,36(10):729-731. DOI:10.3760/cma.j.issn.1001-0939.2013.10.006. |
 2016, Vol. 37
2016, Vol. 37