文章信息
- 刘佳, 许巍, 何翠, 燕晶, 邢辉, 薛秀娟, 孙定勇, 朱谦, 王哲.
- Liu Jia, Xu Wei, He Cui, Yan Jing, Xing Hui, Xue Xiujuan, Sun Dingyong, Zhu Qian, Wang Zhe.
- 河南省新确证HIV感染者中HIV原发耐药状况研究
- The prevalence of primary HIV-1 drug resistance in newly reported HIV infections in Henan
- 中华流行病学杂志, 2016, 37(5): 643-647
- Chinese Journal of Epidemiology, 2016, 37(5): 643-647
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2016.05.011
-
文章历史
- 投稿日期: 2015-11-23
2. 102206 北京, 中国疾病预防控制中心性病艾滋病预防控制中心
2. National Center for AIDS/STD Control and Prevention, Chinese Center for Disease Control and Prevention, Beijing 102206, China
艾滋病抗病毒治疗(antiretroviral treatment,ART)的广泛开展有效降低艾滋病的病死率,提高患者的生存质量[1],但同时也导致耐药株的产生。如果未治疗感染者初始感染HIV是耐药株则为原发耐药。随着HIV流行和抗病毒治疗的扩大,原发耐药的问题已经凸显,国外的研究文献显示,欧美发达国家新报告HIV感染人群中的原发耐药率达到10%~20%[2],艾滋病耐药毒株的传播已经成为一个全球性的公共卫生问题。
河南省从2003 年开始在全省实施免费ART,截止2013年底河南省ART在治人数已有33 000人。2010和2011年对河南省ART病毒学失败(接受治疗1年以上,病毒载量≥1 000 拷贝/ml)的3 235例艾滋病患者的调查发现,耐药发生率达到了68.48%[3]。治疗时间长,治疗人数多和高耐药发生率增加了河南省HIV耐药株的传播风险,且目前还不能对每个患者进行个体化耐药基因型检测,而抗病毒治疗药物的种类和来源十分有限,一旦出现耐药株的流行,将对河南省的抗病毒治疗产生不利影响。因此,在未治疗患者中开展原发耐药的监测对于抗病毒治疗以及艾滋病的防治工作有着十分重要的意义。本研究对河南省2013和2014年新确证未接受抗病毒治疗的HIV感染者进行耐药检测,对其耐药株的流行情况进行分析。
对象与方法1. 研究对象和样本来源:整理河南省6个城市(南阳、漯河、平顶山、商丘、许昌和郑州)2013年1-6月和2014年1-6月新确证上报的HIV感染者传染病报告卡信息和网络直报信息资料,主要包括基本人口学信息、接触史、性病史、感染途径、样本来源以及治疗信息等;在2013年6-10月和2014年6-10月由全省各级CDC负责采集病例的血样。本研究已通过河南省CDC伦理委员会的批准和审核(2015-KY-005-01)。
2. 基因型耐药检测和序列分析:使用In-house方法进行基因型耐药检测[4, 5]。使用QIAGEN公司QIAamp® Viral RNA Mini Kit 按照说明书提取RNA。经过反转录和PCR扩增获得片段并测序,引物设计参照国际标准株HXB2株(全基因1~9 719 bp)。
第一轮 PCR:外侧上游引物MAW 26:5′- TTGGAAATGTGGAAAGGAAGGAC-3′HXB2 2 028~2 050;外侧下游引物RT21:5′-CTGTA TTTCTGCTATTAAGTCTTTTGATGGG-3′HXB2 3 509~3 539;第二轮 PCR:内侧上游引物 PRO-1:5′- CAGAGCCAACAGCCCCACCA-3′HXB2 2 147~2 166; 内侧下游引物 RT20:5′-CTGCCAGTTC TAGCTCTGCTTC-3′HXB2 3 441~3 462;测序引物:正向测序引物PROS3:5′-GCCAACAGCCC CACCA-3′;RTAS:5′-CTCAGATTGGTTGCAC- 3′;RT-B:5′-CCTAGTATAAACAATGAGACA C-3′;反向测序引物PROC1S:5′-GCTGGGTGTGGTATT CC-3′;RT20S3:5′-GTTCTAGCTCTGCTT C-3′。
对扩增片段测序后使用Vector NIT advance 10软件进行序列的编辑和拼接,使用Bio-edit软件对样本序列和标准参考株序列进行比对和校正。所得片段长约1.3 kb,涵盖HIV整个蛋白酶区(1~99 密码子)和反转录酶基因前300个氨基酸(1~300 密码子)。将所得序列输入斯坦福大学HIV耐药数据库(http://hivdb.stanford.edu/)在线对HIV耐药突变、耐药性和亚型情况进行分析。
3. HIV耐药株的流行水平分级:按照WHO耐药监测指南[6, 7],低流行:原发耐药发生率<5%,中度流行:原发耐药发生率为5%~15%,高度流行:原发耐药发生率>15%。
4. 统计学分析:采用Excel 2010软件整理数据,统计分析采用SPSS 19.0软件。采用 χ2检验比较不同变量间出现耐药株的差别(检验水准 α=0.05),采用多因素非条件logistic回归模型分析耐药株传播的影响因素(α入=0.05,α出=0.1)。
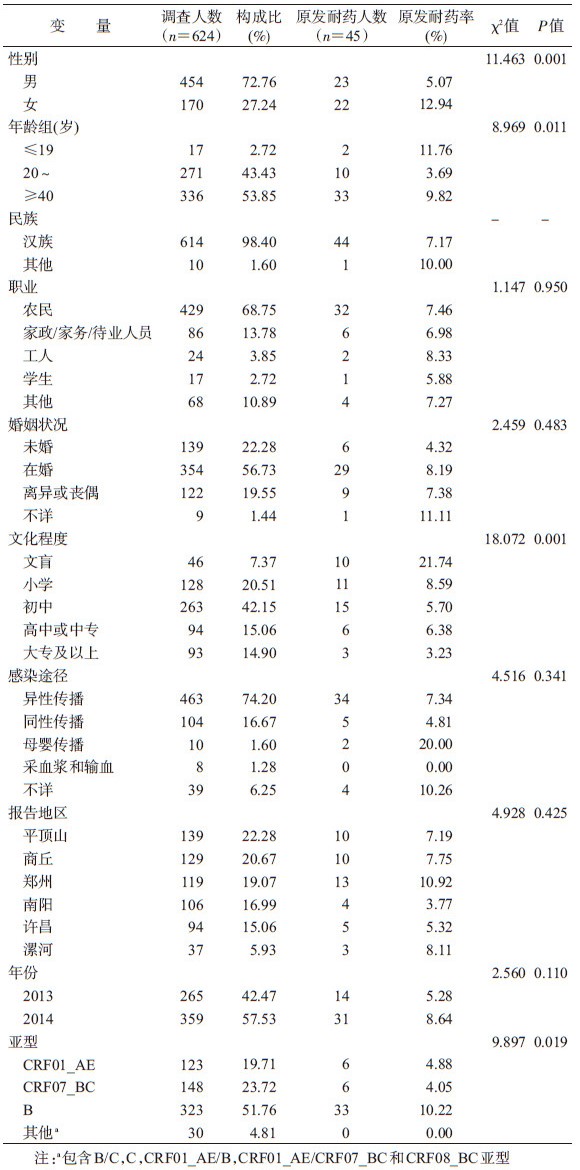
结果1. 一般情况:调查812例HIV感染者共有624例检测数据有效(其中,20例发生溶血情况未检测,168例未能扩增出或扩增结果不完整)。男性占72.76%(454/624);40岁以上的病例占53.85%(336/624),M=41岁(最小年龄2岁,最大年龄86岁);汉族为主,占98.40%(614/624);农民占68.75%(429/624);在婚56.73%(354/624);初中文化程度者多(42.15%,263/624);感染途径多为异性性传播(74.20%,463/624)。其中B亚型占51.76%(323/624),CRF07_ BC亚型占23.72%(148/624),CRF01_AE亚型占19.71%(123/624),其他亚型包括CRF01_AE/B(16例,占2.53%),CR F08_BC(7例,占1.11%),CRF01_AE/CRF07_BC(3例,占0.47%),C(3例,占0.47%)和B/C(1例,占0.16%)(表 1)。
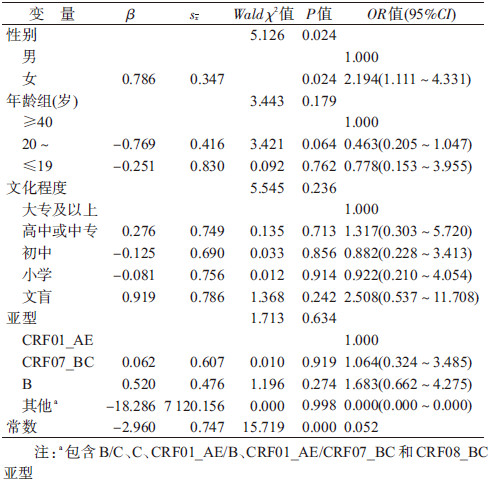
2. 耐药株的流行情况和风险因素分析:624例患者中有45例检测到耐药株,原发耐药率为7.21%。其中女性的原发耐药率高于男性(χ2=11.463,P=0.001),≤19岁病例的原发耐药率高于其他年龄段(χ2=8.969,P=0.011),文盲的原发耐药率最高,达到21.74%(χ2=18.072,P=0.001),B亚型的原发耐药率高于其他亚型(χ2=9.897,P=0.019)。根据单因素分析结果,以P<0.05的检验水准筛选自变量,符合条件的因素为性别、年龄、文化程度和亚型;以是否有原发耐药发生为因变量纳入非条件logistic回归模型进行分析,结果显示:性别是原发耐药的影响因素,女性发生原发耐药的风险高于男性(OR=2.194,95%CI:1.111~ 4.331);年龄、文化程度和基因亚型对原发耐药率没有影响(表 2)。
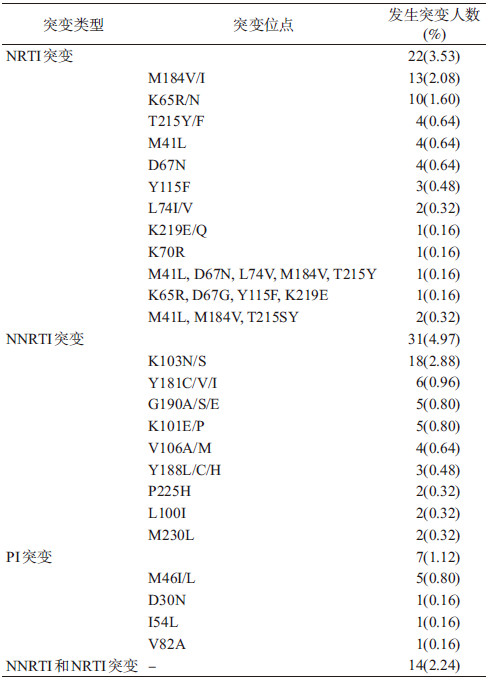
3. 耐药突变位点的发生情况:624例患者中核苷类反转录酶抑制剂(NRTI)耐药突变的病例有22例,发生率为3.53%。M184V/I是出现最多的NRTI耐药突变,其次是K65R/N。其中有4例出现了多个NRTI耐药突变,其中1例同时含有M41L、D67N、L74V、M184V和T215Y,1例同时含有K65R、D67G、Y115F和K219E,还有2例同时含有M41L、 M184V和T215SY。非核苷类反转录酶抑制剂(NNRTI)耐药突变的病例有31例,发生率为4.97%。K103N/S是出现最多的NNRTI耐药突变。蛋白酶抑制剂(PI)耐药的病例有7例,发生率为1.12%。同时存在NNRTI和NRTI突变的病例有14例,发生率为2.24%(表 3)。
HIV耐药株的出现使患者ART的效果下降,同时耐药株在未治疗人群中的传播也会给ART的长期实施带来更多障碍。本研究对河南省2013-2014年新确证未治疗HIV感染者的原发耐药情况进行了研究。
河南省早期的感染者多为B亚型,在近几年的研究中也表明B亚型仍然是河南省流行的HIV毒株中最主要的亚型,占90%以上[8, 9, 10, 11, 12]。但在本研究中通过对HIV部分POL区序列的分型却发现2013和2014年新上报HIV感染者中B以外的亚型占48.24%,其中CRF07_BC和 CRF01_AE亚型分别占23.72%和19.71%,更有多种其他亚型(CRF01_AE/B、CRF08_ BC、CRF01_AE/CRF07_BC、C和B/C)被发现。提示随着HIV流行方式的变化,河南省的HIV亚型情况也发生了改变,需要进行分子流行病学研究来全面了解其变化和发展规律。
河南省2013-2014年新确证HIV感染者的原发耐药率为7.21%,根据WHO耐药监测指南的标准已经达到中等程度的流行。其中女性的原发耐药率高,且经过多因素非条件logistic回归模型分析发现女性发生原发耐药的风险也高。研究发现在接受治疗后有一定比例的HIV感染者虽然血浆中检测不到病毒,但在男性的精子中仍能检测到病毒[13],因此在治疗的情况下男性仍然存在感染性伴侣的可能,复制的病毒很可能就是耐药毒株,这可能就是女性原发耐药发生风险高的原因。本文文盲和年龄≤19岁人群的原发耐药率显著高于其他人群,但由于样本例数太少,结果可能会产生偏倚,需谨慎对待。本研究显示B亚型的原发耐药率远高于其他亚型,ART治疗失败后被检测到耐药的患者绝大多数是B亚型[14],且已证明向普通人群传播[15],说明因ART失败发生耐药的患者将自身耐药毒株传给新的感染者,可能是河南省耐药株流行的主要原因。
耐药突变位点的出现是导致HIV耐药的根本因素,本研究对耐药突变的发生情况进行了统计分析,研究表明出现NNRTI耐药突变的病例最多,且M184V/I是最常见的NRTI耐药突变,K103N/S是最常见的NNRTI耐药突变,这说明河南省新确证病例中原发耐药株的耐药突变与河南省ART失败患者的耐药突变的模式一致[3],也印证了新确证病例中原发耐药株的来源主要是ART失败出现耐药的患者。本研究发现有4例患者出现了多NRTI耐药突变,多重耐药突变很可能使常规的一线药物无法有效抑制患者体内的病毒,就需要使用更高级别的ART方案。二线方案就是目前河南省最常用的较之一线方案更高级别的ART方案,它包含一种PI类药物,一线方案治疗效果不好的患者在更换二线治疗方案后能取得好的治疗效果[14]。但在本研究同时还发现了7例含有PI耐药突变的新确证病例,预示着二线ART方案也达不到理想的效果。提示我们在提供充足二线药物的同时还需要引入更多种类的ART药物,并应具备开展个性化治疗的能力。
B亚型的原发耐药率高,在下一步的研究中需要使用更精确的检测方法来明确是“B”还是“B′”亚型,这对于推断原发耐药毒株的来源十分重要。此外,本研究仅有两年的原发耐药监测数据,不能充分反映河南省HIV原发耐药的变化和发展趋势,因此还需要进行更连贯的监测。
综上所述,河南省应该定期开展未治疗HIV感染者的耐药性监测,并应具备为特定人群提供治疗前耐药检测和个性化用药指导的能力,从而保证河南省ART的有效进行。
| [1] Zhao Y,Li C,Sun X,et al. Mortality and treatment outcomes of China's National Pediatric antiretroviral therapy program[J]. Clin Infect Dis,2013,56(5):735-744. DOI:10.1093/cid/cis941. |
| [2] World Health Organization. HIV drug resistance report 2012[DB/OL]. Geneva:WHO,2012:20-27.[2015-10-10]. http://www. who.int/hiv/pub/drugresistance/report2012/en/. |
| [3] Liu J,Wu YS,Yang WJ,et al. Population-based human immunodeficiency virus 1 drug resistance profiles among individuals who experienced virological failure to first-line antiretroviral therapy in Henan,China during 2010-2011[J]. AIDS Res Ther,2015,12(1):22. DOI:10.1186/s12981-015-0062-y. |
| [4] Liao L,Xing H,Shang H,et al. The prevalence of transmitted antiretroviral drug resistance in treatment-naive HIV-infected individuals in China[J]. J Acquir Immune Defic Syndr,2010,53 Suppl 1:S10-14. DOI:10.1097/QAI.0b013e3181c7d363. |
| [5] Zhong P,Pan QC,Ning Z,et al. Genetic diversity and drug resistance of human immunodeficiency virus type 1(HIV-1) strains circulating in Shanghai[J]. AIDS Res Hum Retroviruses,2007,23(7):847-856. DOI:10.1089/aid.2006.0196. |
| [6] Bennett DE,Myatt M,Bertagnolio S,et al. Recommendations for surveillance of transmitted HIV drug resistance in countries scaling up antiretroviral treatment[J]. Antivir Ther,2008,13 Suppl 2:S25-36. |
| [7] Myatt M,Bennett DE. A novel sequential sampling technique for the surveillance of transmitted HIV drug resistance by cross-sectional survey for use in low resource settings[J]. Antivir Ther,2008,13 Suppl 2:S37-48. DOI:10.1074/jbc.270. 43.25363. |
| [8] Wu ZY,Liu ZY,Detels R. HIV-1 infection in commercial plasma donors in China[J]. Lancet,1995,346(8966):61-62. DOI:10.1016/S0140-6736(95)92698-4. |
| [9] Li Z,He X,Wang Z,et al. Tracing the origin and history of HIV-1 subtype B'epidemic by near full-length genome analyses[J]. AIDS,2012,26(7):877-884. DOI:10.1097/QAD.0b013 e328351430d. |
| [10] Li L,Sun GQ,Liang SJ,et al. Different distribution of HIV-1 subtype and drug resistance were found among treatment naïve individuals in Henan,Guangxi,and Yunnan province of China[J]. PLoS One,2013,8(10):e75777. DOI:10.1371/journal.pone.0075777. |
| [11] Su B,Liu L,Wang FS,et al. HIV-1 subtype B'dictates the AIDS epidemic among paid blood donors in the Henan and Hubei provinces of China[J]. AIDS,2003,17(17):2515-2520. DOI:10.1097/01.aids.0000088229.55968.a2. |
| [12] Li LN,Sun BL,Zeng HY,et al. Relatively high prevalence of drug resistance among antiretroviral-naive patients from Henan,Central China[J]. AIDS Res Hum Retroviruses,2014,30(2):160-164. DOI:10.1089/AID.2013.0144. |
| [13] Lambert-Niclot S,Tubiana R,Beaudoux C,et al. Detection of HIV-1 RNA in seminal plasma samples from treated patients with undetectable HIV-1 RNA in blood plasma on a 2002-2011 survey[J]. AIDS,2012,26(8):971-975. DOI:10.1097/QAD. 0b013e328352ae09. |
| [14] Wang J,Wang Z,Liu J,et al. Efficacy and HIV drug resistance profile of second-line ART among patients having received long-term first-line regimens in rural China[J]. Sci Rep,2015,5:14823. DOI:10.1038/srep14823. |
| [15] Li L,Sun GQ,Zhong P,et al. HIV-1 Thai B strain has spread out of former plasma donors into general population through sexual contact in Henan,China[J]. J Med Virol,2016,88(4):614-621. DOI:10.1002/jmv.24383. |
 2016, Vol. 37
2016, Vol. 37