文章信息
- 张兵, 严睿, 何寒青, 李倩, 胡昱, 陈雅萍, 谢淑云.
- Zhang Bing, Yan Rui, He Hanqing, Li Qian, Hu Yu, Chen Yaping, Xie Shuyun.
- 浙江省2013年麻疹疫情时空分布特征
- Spatial-temporal distribution feature of measles in Zhejiang province, 2013
- 中华流行病学杂志, 2016, 37(4): 548-552
- Chinese Journal of Epidemiology, 2016, 37(4): 548-552
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2016.04.022
-
文章历史
- 收稿日期: 2015-09-06
麻疹是导致儿童残疾和死亡的重要原因。全球推行了一系列消除麻疹的措施,2010年麻疹归因死亡人数相比2000年下降了74.0%,但部分发展中国家的麻疹形势依然很严峻[1]。我国自1978年将麻疹疫苗纳入儿童计划免疫后,麻疹疫情得到了有效控制;但2013年麻疹疫情在成年人和低年龄组儿童中出现反弹,提示我国消除麻疹任务依然任重而道远[2]。已有众多学者从时间、空间或时空等层面对麻疹的蔓延方式进行了相关研究[3, 4, 5]。经典的易感者-感染者-移出者模型可从时间维度来描述麻疹的发生发展规律,并评估强化免疫等措施对麻疹疫情的控制效果[6]。人作为麻疹病毒的唯一自然宿主,因而人口迁徙模式与麻疹的空间蔓延规律紧密相关[2, 7]。考虑到人口迁徙数据的难获取性和复杂性,Simini等[8]提出了辐射模型,较好地克服了传统重力模型对交通数据的依赖且存在系统预测偏差的缺陷。Marguta和Parisi[3]更是将辐射模型运用到麻疹时空传播机制研究中,发现麻疹疫情呈现周期性是局部人口密度和人群迁徙相互作用的结果。然而,也有学者发现基于Power-law算法来模拟传染病的时空蔓延规律也能取得较好效果[9]。本研究采用基于Power-law算法的时空多成分模型探讨浙江省麻疹疫情的时空流行特征。
资料与方法1. 数据来源:浙江省2013年麻疹个案数据来源于中国疾病预防控制信息系统;各县(市、区)含麻疹成分(含麻类)疫苗报告接种率来源于全国常规免疫接种率报告。人口数据来源于中国免疫规划信息管理系统。考虑到分析方法的可行性,西湖风景区和温州经济开发区分别并入西湖区和龙湾区处理。
2. 研究方法:
(1)时空多成分模型:时空多成分模型是在考虑人群迁入的泊松分支过程的基础上,加入了季节效应、长期趋势和过度离散特性,广泛应用于多区域时序数据分析中。假设研究区域分为n块,对于区域i(i∈1,2,3,…,n)在时间t(t∈1,2,3,…,m)的发病人数为Yi,t,时空多成分模型可写成:
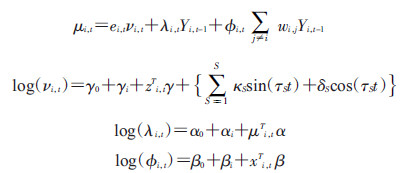
式中,μi,t是Yi,t作为负二项分布的条件均值;ei,t代表区域i在时间t的偏移变量,本研究采用各区域在不同时间段的人群密度作为偏移变量;νi,t、λi,t和φi,t分别定义了模型中的局部特性成分、时间自相关成分和空间流行成分;γ0、α0和β0分别代表了三成分的截距,γi、αi和βi分别代表三成分的随机效应,服从均值为0的正态分布;γ、α和 β分别代表了协变量zi,tT、 μi,tT和 xi,tT对局部特性成分、时间自相关成分和空间流行成分的作用强度。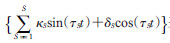 表示季节效应,τS=2πS/freq,其中S和freq分别代表周期数和频率。考虑到流动儿童对麻疹传播有较大影响[10],本研究纳入各县(市、区)流动儿童接种数与本地儿童接种数的比值,分别代入协变量μi,tT和zi,tT中,通过赤池信息量准则(AIC)和得分准则来评价模型拟合效果。
表示季节效应,τS=2πS/freq,其中S和freq分别代表周期数和频率。考虑到流动儿童对麻疹传播有较大影响[10],本研究纳入各县(市、区)流动儿童接种数与本地儿童接种数的比值,分别代入协变量μi,tT和zi,tT中,通过赤池信息量准则(AIC)和得分准则来评价模型拟合效果。
(2)空间权重矩阵:wi,j代表空间权重矩阵,反映区域i和j的邻近关系,其中一阶确定性邻接矩阵为:若i和j有共同边界,则Wi,j=Oi,j=1,否则为0。考虑到麻疹传播的长拖尾性,本研究采用Power-law算法对空间邻接矩阵Oi,j加权后构建空间权重矩阵,与确定性高阶邻近关系搭建空间权重矩阵相比,Power- law在复杂模型中更易得到确定性结果[9]。若区域i和区域j是K阶相邻且衰减系数为d,则Wi,j=Oi,j-d。对于独立县(市、区)(包括洞头县、岱山县和嵊泗县)则从新定义其邻近关系。相关参数推导基于惩罚最大似然比法,分析采用R软件的surveillance程序包[11]。
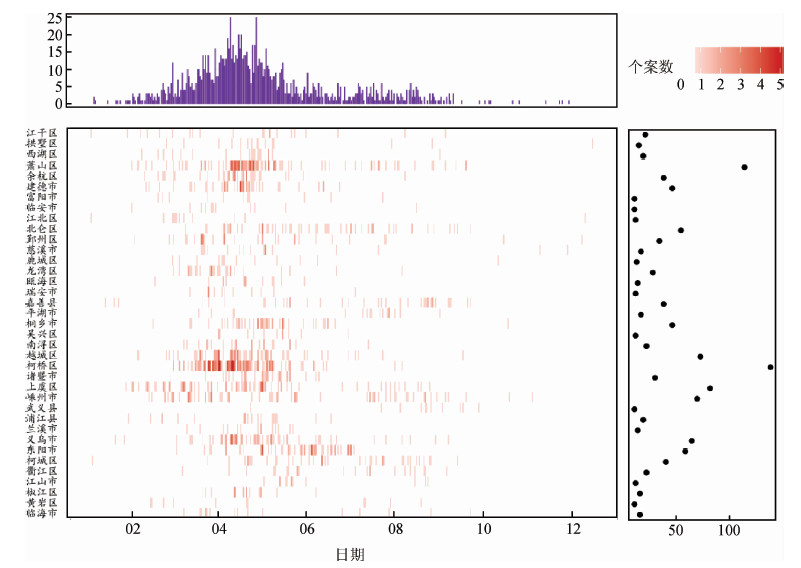
结 果1. 各县(市、区)麻疹发病情况:2013年浙江省共报告麻疹1 494例,报告发病率为2.72/10万,除开化县、龙泉市、嵊泗县、松阳县、遂昌县及云和县外均存在麻疹个案,其中柯桥区、萧山区和上虞区年麻疹个案数相对较多,分别为137、113和81例。麻疹病例主要集中出现在3-5月,占年总病例数的88.5%(3、4和5月全省麻疹例数分别为267、473和311),见图 1。
|
| 注:图中左下列出麻疹个案数>10的县(市、区),按照国标码进行排列;格子颜色越深,说明该地区该时间麻疹病例数越多;左上是市日病例总数,右下是病例总数 图 1 2013年浙江省各县(市、区)麻疹发病情况 |
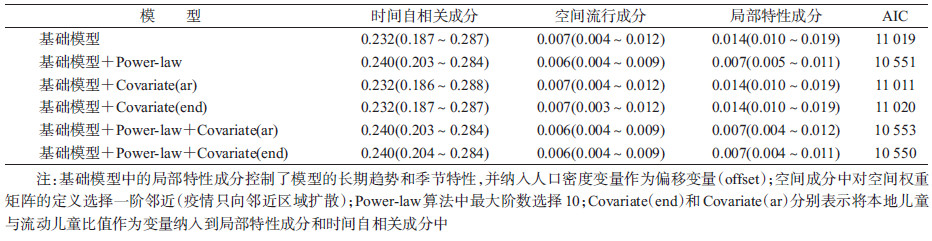
2. 时空多成分模型:Power-law时空多成分模型的AIC在10 550~10 553之间,为兼顾模型的简便性,本研究选择不含协变量的Power-law时空多成分模型,此时时间自相关成分、局部特性成分和空间流行成分分别为0.240(95%CI:0.203~0.284)、0.006(95%CI:0.004~0.009)和0.007(95%CI:0.005~0.011),见表 1。
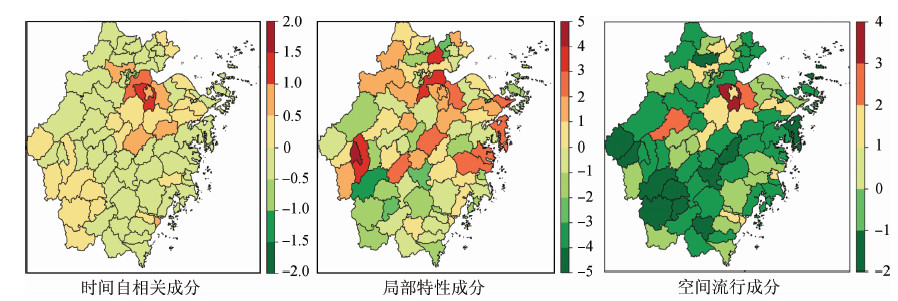
3. 随机效应模型:基于Power-law算法的随机效应时空多成分模型分析显示,对时间自相关成分而言,杭州市西南、绍兴、宁波中部和温州中部等县(市、区)的麻疹疫情受先前时段疫情的影响较大,如柯桥区、萧山区和越城区,其时间自相关成分值分别为1.39、0.88和0.77;在控制季节效应后,柯桥区、衢江区、萧山区、桐乡市的局部特性成分较大,分别为4.06、3.74、3.55和3.40,提示这些县(市、区)麻疹发病的本地风险水平高;对空间流行成分而言,柯桥区、上虞区、建德市和义乌市较大,其值分别为3.08、2.54、2.21和1.98,提示这些县(市、区)麻疹疫情受邻近县(市、区)影响较大,见图 2。
|
| 注:基础模型中的局部特性成分控制了模型的长期趋势和季节特性,并纳入人口密度变量作为偏移变量(offset);空间成分中对空间权重矩阵的定义选择一阶邻近(疫情只向邻近区域扩散);Power-law算法中最大阶数选择10;Covariate(end)和Covariate(ar)分别表示将本地儿童与流动儿童比值作为变量纳入到局部特性成分和时间自相关成分中 图 2 2013年浙江省各县(市、区)基于Power-law的随机效应模型中时间自相关、局部特性和空间流行成分分析 |
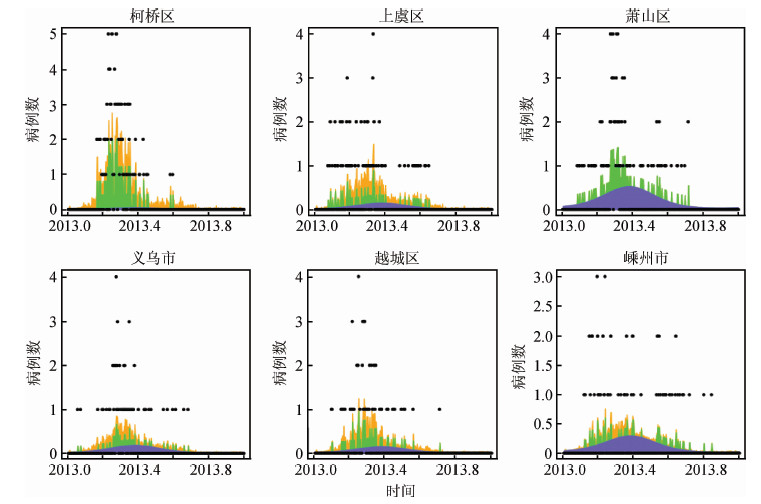
4. 高疫情地区的多成分模型:县(市、区)年麻疹例数超过60的时空多成分模型拟合结果显示,柯桥区的空间流行成分和时间自相关成分较大,而局部特性成分接近0,提示该区的麻疹疫情受邻近县(市、区)和先前时段麻疹疫情的影响;上虞区和越城区的空间流行成分和时间自相关成分均大于局部特性成分,提示这两个地区的麻疹疫情受本地先前暴发疫情和邻近县(市、区)的影响大于本地发病风险,且时间段主要集中在4-5月;萧山区和嵊州市的局部特性成分较大且高值出现在5月,提示这两个地区在5月麻疹发生的本地风险水平高,见图 3。
|
| 注:图中横轴日期是当前日期在1年的百分比位置,即2013.4代表2013年第146天(0.4×365); 绿色代表空间自相关成分,棕色代表空间流行成分,蓝色代表局部特性成分 图 3 2013年浙江省麻疹疫情超过60例的各县(市、区)时空多成分模型 |
基于多时序多研究区域的传染病监测数据,时空多成分模型可有效地捕捉各研究区域传染病疫情的时空演变规律并采取针对性的防控措施,但模型所需基础数据相对较多且分析结果对研究区域数目较敏感。本研究基于时空多成分模型分析浙江省各县(市、区)麻疹疫情的分布特征和流行特征。总体而言,浙江省麻疹疫情离消除麻疹目标依然有一定差距,部分地区麻疹疫情相对高发,如绍兴的柯桥区、上虞区和杭州的萧山区等,但这些地区疫情的时空组成成分不一,故针对性地采取措施更能有效控制麻疹疫情。对于空间流行成分和时间自相关成分较大的柯桥区,控制麻疹疫情不仅需加强本地麻疹疫情应急处置工作进而降低麻疹暴发疫情的后续影响,也需其邻近区域如越城区和上虞区等采取相关措施进行联合防控才能降低疫情的跨区域传播;而萧山区麻疹疫情成分中本地风险值高,因而需强化本地的免疫屏障,降低免疫空白人群比例。
人口流动、免疫空白和医院暴露等是浙江省小年龄组儿童麻疹疫情发生的主要危险因素[12],前者会导致麻疹疫情的跨区域传播,后两者会增大麻疹疫情的本地风险值。接种含麻类疫苗提高人群抗体水平是建立高水平免疫屏障和阻断麻疹病毒传播的有效措施,尤其是对于流动儿童中的免疫空白人群[10]。尽管本研究显示控制时空成分后,流动儿童与本地儿童数比值这一变量并不对麻疹疫情产生显著影响,但总体上流动儿童的接种率与常住人口相比仍偏低,因而提高流动儿童接种率并降低免疫空白人数仍是整个免疫规划工作中的重点。同时,儿童在综合性医院发生院内感染的可能性大,即便医院采取了发热预检制度,拥挤的诊疗场所也会导致麻疹的传播,因而根据医院实际情况采取相应措施来降低麻疹病毒的院内感染对于控制低年龄儿童麻疹发病具有重要意义[12]。
随着含麻类疫苗接种策略的调整,打破了以往麻疹疫情的流行规律,而成年人麻疹疫情的反弹,也给消除麻疹目标带来了艰巨挑战[2]。浙江省对高年级学生进行强化免疫并于2011年将初三学生含麻类疫苗接种纳入常规免疫,显著提高了高年龄儿童的麻疹抗体水平,并逐步降低了成年人麻疹疫苗的空白人群比例[13]。当然,部分研究表明针对麻疹高危成年人进行常规接种可有效降低麻疹疫情[2],但对于高危人群的定义及如何在高危人群中实施科学接种,进而提高整个人群的麻疹抗体水平仍需进一步研究。
利益冲突 无| [1] Durrheim DN,Strebel PM. Measles vaccine still saves children's lives[J]. Lancet,2015,385(9965):327. DOI:10.1016/S0140-6736(15)60114-3. |
| [2] Chen M,Zhang Y,Huang F,et al. Endemic and imported measles virus-associated outbreaks among adults,Beijing,China,2013[J]. Emerg Infect Dis,2015,21(3):477-479. DOI:10. 3201/eid2103.140646. |
| [3] Marguta R,Parisi A. Impact of human mobility on the periodicities and mechanisms underlying measles dynamics[J]. J R Soc Interface,2015,12(104):20141317. DOI:10.1098/rsif. 2014.1317. |
| [4] Cauchemez S,Ferguson NM. Likelihood-based estimation of continuous-time epidemic models from time-series data:application to measles transmission in London[J]. J R Soc Interface,2008,5(25):885-897. DOI:10.1098/rsif.2007.1292. |
| [5] Bauch CT,Szusz E,Garrison LP. Scheduling of measles vaccination in low-income countries:Projections of a dynamic model[J]. Vaccine,2009,27(31):4090:4098. |
| [6] Verguet S,Johri M,Morris SK,et al. Controlling measles using supplemental immunization activities:A mathematical model to inform optimal policy[J]. Vaccine,2015,33(10):1291-1296. DOI:10.1016/j.vaccine.2014.11.050. |
| [7] González MC,Hidalgo CA,Barabási AL. Understanding individual human mobility patterns[J]. Nature,2008,453(7196):779-782. DOI:10.1038/nature06958. |
| [8] Simini F,González MC,Maritan A,et al. A universal model for mobility and migration patterns[J]. Nature,2012,484(7392):96-100. DOI:10.1038/nature10856. |
| [9] Geilhufe M,Held L,Skrøvseth SO,et al. Power law approximations of movement network data for modeling infectious disease spread[J]. Biom J,2014,56(3):363-382. DOI:10.1002/bimj.201200262. |
| [10] Herzog SA,Paul M,Held L. Heterogeneity in vaccination coverage explains the size and occurrence of measles epidemics in German surveillance data[J]. Epidemiol Infect,2011,139(4):505-515. DOI:10.1017/S0950268810001664. |
| [11] Meyer S,Held L. Power-law models for infectious disease spread[J]. Ann Appl Stat,2014,8(3):1612-1639. DOI:10.1214/14-AOAS743. |
| [12] 陈恩富,何寒青,李倩,等. 浙江省2008年麻疹流行因素的病例对照研究[J]. 中国疫苗和免疫,2010,16(1):11-14. Chen EF,He HQ,Li Q,et al. Case-control study on epidemiology factors of measles in Zhejiang Province in 2008[J]. Chin J Vacc Immun,2010,16(1):11-14. |
| [13] He H,Chen EF,Li Q,et al. Waning immunity to measles in young adults and booster effects of revaccination in secondary school students[J]. Vaccine,2013,31(3):533-537. DOI:10. 1016/j.vaccine.2012.11.014. |
 2016, Vol. 37
2016, Vol. 37