文章信息
- 孙树柳, 高玉琦, 尹娟, 庄贵华.
- Sun Shuliu, Gao Yuqi, Yin Juan, Zhuang Guihua.
- 中国婴幼儿普遍接种轮状病毒疫苗的成本效果分析
- A cost-effectiveness analysis on universal infant rotavirus vaccination strategy in China
- 中华流行病学杂志, 2016, 37(2): 238-242
- Chinese Journal of Epidemiology, 2016, 37(2): 238-242
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2016.02.018
-
文章历史
- 收稿日期: 2015-06-29
轮状病毒(RV)是全球<5岁儿童发生重型腹泻的首要原因[1]。研究报道[2, 3],全球每年大约有2 500万RV感染患儿需要接受门诊治疗,其中200万患儿需要住院治疗,且约有45万患儿因RV腹泻死亡。中国<5岁婴幼儿每年因RV腹泻就诊超过300万人,约损失直接成本20亿元、社会成本27亿元[4]。由于目前尚无有效的抗病毒治疗方法,且普通对症治疗收效有限,故接种疫苗成为降低RV腹泻发病率和降低疾病负担最为安全有效的方法。全球已有多个国家将RV疫苗纳入该国免疫规划,研究显示疾病负担显著降低[5, 6]。但目前中国尚未制定相关的指导意见。为此本研究旨在从卫生经济学角度探讨中国现阶段进行RV疫苗普遍接种的成本效果及何种RV疫苗更适合在国内推广,为国家制定相关政策提供理论依据。
对象与方法1. 研究对象:以中国2012年出生的1 634万新生儿为研究对象(数据来源于《2013年中国统计年鉴》)。
2. 决策树-Markov模型:决策树模型用来直观地比较不同方案的优劣;Markov模型用来模拟各策略下RV腹泻的感染与进程,并计算其相关的成本和效果期望值。
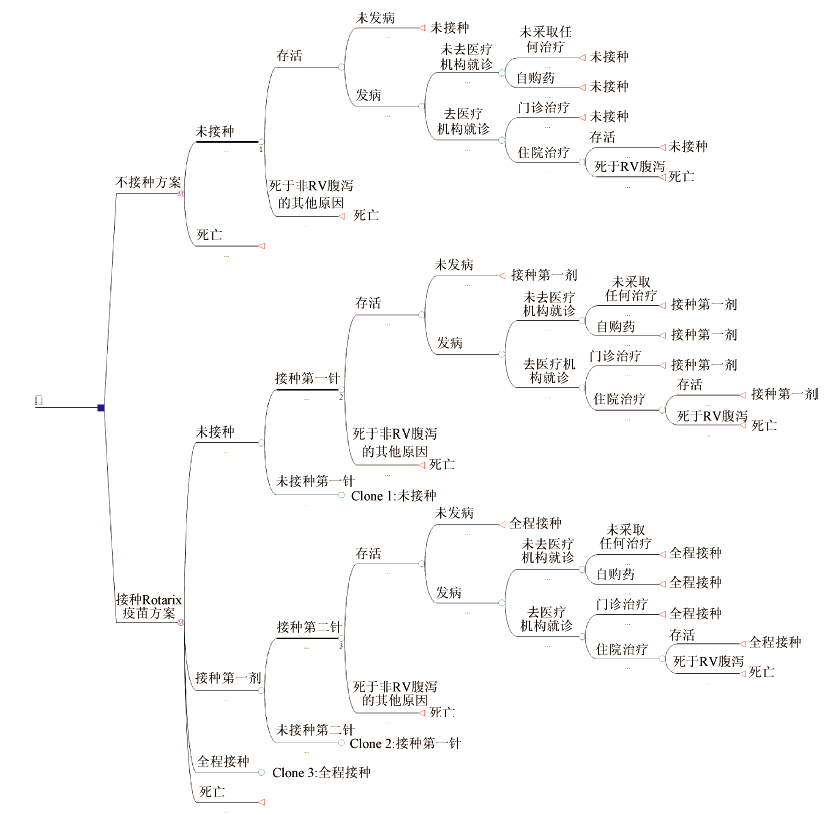
本研究决策树模型有3种方案:不接种疫苗、接种Rotarix疫苗和接种Rotateq疫苗。按照WHO推荐的指导意见:Rotarix疫苗在婴儿3、4月龄接种,Rotateq疫苗在婴儿3、4、5月龄接种。由于RV腹泻为急性肠道传染病,病程约为1周,且个体可多次感染,本研究Markov模型借鉴哥伦比亚学者的建模思想[7],根据队列人群接种疫苗的情况划分Markov状态:①对于不接种方案,模型只有2个Markov状态,即“未接种”和“死亡”,人群初始均处于“未接种”状态,此后分出“存活”和“死于非RV腹泻的其他原因”2个分支,“死于非RV腹泻的其他原因”转归至“死亡”状态,而“存活”再分出“未发病”和“发病”2个分支(图 1);②对于接种Rotarix疫苗方案,模型包括4个Markov状态:“未接种”、“接种第一剂”、“全程接种”、“死亡”,人群初始均处于“未接种”状态,3月龄时队列中部分婴儿接种第一剂Rotarix疫苗,转至“接种第一剂”状态,未接种婴儿转至“未接种”状态,之后“接种第一剂”的婴儿部分继续接种第二剂疫苗,进入“全程接种”状态,未接种第二剂疫苗的婴儿则转归至“接种第一剂”状态,在此过程中均可发生RV腹泻及就医活动(图 1);③对于接种Rotateq疫苗方案,由于该疫苗全程接种需要3剂次,故与Rotarix疫苗方案相比仅多一个“接种第二剂”的Markov状态。模型模拟时间为5年,Markov循环周期定为1个月。
|
| 注:Ⓜ为Markov节点;○ 为机会节点;△为终结点 图 1 不接种方案与接种Rotarix疫苗方案的Markov模型示意图 |
3. 参数设定:模型中的各项参数主要通过查阅国内流行病学调查数据,统计年鉴和广泛检索国内外期刊论文等途径确定。部分参数,如疫苗购置成本、接种率等根据相关依据合理假设(表 1)。
(1)成本相关指标:分为直接成本和间接成本。其中直接成本包括直接医疗成本(如门诊费用、住院费用、自购药治疗费用等)和直接非医疗成本(如就医的交通费、住宿费等),间接成本主要考虑监护人陪护RV腹泻患儿造成的生产力损失。在计算ICER时,为避免重复计算仅考虑直接成本。成本的年贴现率为3%,且均贴现至基准年2012年。
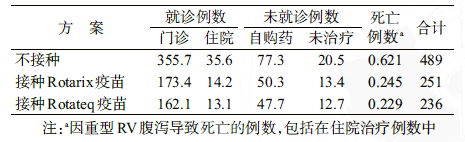
(2)效果相关指标:分为直接效果指标和综合效果指标。直接效果指标为各种方案下,因RV腹泻接受门诊治疗、住院治疗、自购药治疗及因RV腹泻死亡的病例数;综合效果指标采用失能调整寿命年(DALY),包括疾病导致伤残和过早死亡损失的寿命年。通过年龄和时间贴现,以增加与其他研究的可比性,贴现率仍定为3%。
4. 卫生经济学评价指标:两种方案的优劣比较主要采用ICER指标,即两种方案的成本差与效果差的比值,表示每避免1个DALY损失所需要费用的成本。本文ICER基于WHO推荐标准[23](若ICER<0,则该方案不仅效果更好且节约成本;若ICER<该国1倍人均GDP,则该方案具有高的成本效果;若ICER介于该国1~3倍人均GDP,则该方案具有成本效果;若ICER>该国3倍人均GDP,则该方案不具有成本效果)比较确定最优方案。由统计年鉴得到2012年我国人均GDP为38 420元。
5. 灵敏性分析:采用确定性的灵敏性分析方法。通过单因素灵敏性分析龙卷风图可以显示各参数取值发生变化时ICER的变化幅度,同时发现对模型影响相对较大的重要参数。重要参数可能导致最优方案发生改变,故继续对这些参数进一步进行灵敏性分析。
6. 统计学分析:模型建立和数据分析采用决策分析软件TreeAge Pro 2012 和Excel 2010。
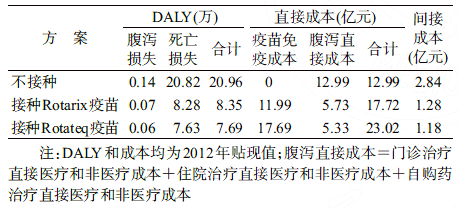
结 果1. 不接种与接种RV疫苗的疾病负担:根据模型模拟得到2012年中国新生儿0~4岁有关RV腹泻的结局及损失的DALY和社会成本(表 2,3)。在不接种RV腹泻疫苗的情况下,2012年中国新生儿发生489万例RV腹泻,因RV腹泻损失约21万个DALY,共损失社会成本15.83亿元。 同年,通过普遍接种Rotarix疫苗和Rotateq疫苗,可分别减少238万和253万例RV腹泻的发生,避免12.6万和13.3万个DALY的损失,RV腹泻相关的疾病负担减少60.2%和63.3%。
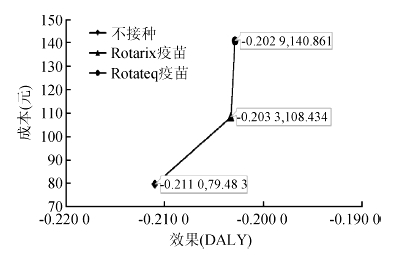
2. RV疫苗接种后的成本效果分析:如图 2所示,与不接种方案相比,接种Rotarix疫苗和Rotateq疫苗方案的ICER值为3 760元/DALY和7 578元/DALY,均远小于中国2012年人均GDP(38 420元)。从卫生经济学角度分析,接种该两种疫苗方案均具有高的成本效果。两种疫苗接种方案相比,Rotateq疫苗保护效果略优,但需要支付更多的疫苗免疫费用。与Rotarix疫苗方案相比,接种Rotateq疫苗方案的ICER为81 068元/DALY(介于1倍与3倍人均GDP之间),在基线情况下认为Rotateq疫苗方案与Rotarix疫苗方案相比具有成本效果。
|
| 图 2 三种方案的成本效果分析 |
3. 单因素灵敏性分析:随着各参数在预先设定的灵敏性分析范围内变动时,Rotarix疫苗接种方案和Rotateq疫苗接种方案与不接种方案相比的ICER值始终小于中国2012年人均GDP(38 420元),结果非常稳定。同时发现RV腹泻发病率和疫苗免疫成本两个参数对模型影响相对最大。
对两种疫苗接种方案的成本效果比较进行单因素灵敏性分析发现,结果并不稳定。RV腹泻发病率、Rotateq疫苗与Rotarix疫苗相比的保护率差值、单剂疫苗免疫成本、门诊与住院治疗患儿比例4个参数取值不同时,最优方案可能会发生变化。
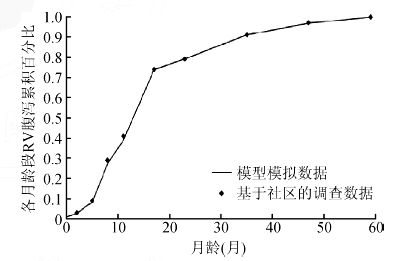
4. 模型拟合效果分析:通过文献搜索,在中国仅找到一篇关于<5岁儿童RV腹泻的现况调查[8]。经比较,该实际调查与模型模拟的结果相近(图 3)。
|
| 注:图中数值是通过模拟固定队列0~4岁各月龄段发生RV腹泻的病例数以及总发病例数计算获得;实线为不接种方案下,Markov模型模拟固定队列发生RV腹泻的例数占总发病例数的累计百分比;实点为河北省卢龙县基于社区调查获得的RV腹泻年龄分布数据 图 3 Markov模型模拟结果与实际调查数据的比较 |
本研究结果表明,RV腹泻可导致大量医疗卫生资源的损失。而从卫生经济学分析,不管是2剂的Rotarix疫苗还是3剂的Rotateq疫苗,与不接种疫苗方案相比均具有高的成本效果,灵敏性分析显示结果稳定可靠。
中国目前已有两项关于RV疫苗的卫生经济学评价[24, 25],其中一篇利用河北省正定县农村地区RV腹泻调查数据探讨RV疫苗在我国农村地区的适用性;另一篇基于统计数据估计2剂次RV疫苗在中国的成本效果。两项研究结果均表明两剂RV疫苗具有较好的成本效果,与本研究结论一致。Aballéa等[22]广泛检索2001-2011年全球发表的关于RV疫苗的卫生经济学研究开展系统评价,发现在众多的发展中国家,由于较低的疫苗购置价格和较严重的疾病负担,RV疫苗普遍具有较好的成本效果。而根据巴西、墨西哥等国在开展RV疫苗普遍接种之后的监测数据显示,RV腹泻乃至整体腹泻的发病率明显降低[26]。提示中国应该考虑将RV疫苗纳入免疫规划。
在基线情况下,Rotateq疫苗与Rotarix疫苗接种方案相比,每避免1个DALY损失平均需要花费81 068元。虽然认为具有成本效果,但考虑到中国目前还未将任何RV疫苗纳入免疫规划,且Rotateq疫苗方案灵敏性分析的不稳定和不确定性,以及Rotateq疫苗需要多接种一剂,与Rotarix疫苗相比更难于大规模实施。综上所述,在中国现阶段可能更适宜推广Rotarix疫苗。
本研究存在不足。研究中采用的决策树Markov模型是一个静态、确定、整体、封闭的模型。静态模型未考虑免疫屏障对未接种儿童的间接保护作用,相对于动态模型而言,静态模型会低估疫苗的保护效果;由于一些参数无法确定其分布,研究中只进行了确定性灵敏性分析而未进行概率灵敏性分析。研究中的部分参数如RV腹泻患儿就诊率、治疗费用等依据局部地区的流行病学调查结果估计,可能存在一定偏倚。
| [1] Bernstein DI.Rotavirus overview[J].Pediatr Infect Dis J, 2009, 28(3):S50-53.DOI:10.1097/INF.0b013e3181967bee. |
| [2] Parashar UD, Hummelman EG, Bresee JS, et al.Global illness and deaths caused by rotavirus disease in children[J].Emerg Infect Dis, 2003, 9(5):565-572.DOI:10.3201/eid0905.020562. |
| [3] Tate JE, Burton AH, Boschi-Pinto C, et al.2008 estimate of worldwide rotavirus-associated mortality in children younger than 5 years before the introduction of universal rotavirus vaccination programmes:a systematic review and meta-analysis[J].Lancet Infect Dis, 2012, 12(2):136-141.DOI:10.1016/S1473-3099(11) 70253-5. |
| [4] Jin H, Wang B, Fang ZY, et al.Hospital-based study of the economic burden associated with rotavirus diarrhea in eastern China[J].Vaccine, 2011, 29(44):7801-7806.DOI:10.1016/j.vaccine.2011.07.104. |
| [5] Glass RI, Parashar U, Patel M, et al.Rotavirus vaccines:successes and challenges[J].J Infect, 2014, 68(S1):S9-18.DOI:10.1016/j.jinf.2013.09.010. |
| [6] Patel MM, Glass R, Desai R, et al.Fulfilling the promise of rotavirus vaccines:how far have we come since licensure?[J].Lancet Infect Dis, 2012, 12(7):561-570.DOI:10.1016/S1473-3099(12)70029-4. |
| [7] De La Hoz F, Alvis N, Narváez J, et al.Potential epidemiological and economical impact of two rotavirus vaccines in Colombia[J].Vaccine, 2010, 28(22):3856-3864.DOI:10.1016/j.vaccine.2010.03.004. |
| [8] 张丽杰.我国六地区婴幼儿轮状病毒腹泻监测和分子流行病学研究[D].北京:中国疾病预防控制中心, 2005.Zhang LJ.Rotavirus surveillance and molecular epidemiology among children with acute diarrhea in six areas of China[D].Beijing:Chinese Center for Disease Control and Prevention, 2005. |
| [9] 张静, 刘民.广东、河南、甘肃三省12县区腹泻病例就诊模式调查[J].中华流行病学杂志, 2008, 29(10):989-993.DOI:10.3321/j.issn:0254-6450.2008.10.009.Zhang J, Liu M.Current situation on the treatment modules of diarrhea cases in 12 counties/cities of Guangdong, Henan and Gansu provinces in China[J].Chin J Epidemol, 2008, 29(10):989-993.DOI:10.3321/j.issn:0254-6450.2008.10.009. |
| [10] 方肇寅, 张丽杰, 唐景裕, 等.中国河北省卢龙县儿童轮状病毒腹泻研究[J].病毒学报, 2005, 21(1):21-26.DOI:10.3321/j.issn:1000-8721.2005.01.005.Fang ZY, Zhang LJ, Tang JY, et al.Rotavirus diarrhea among children in Lulong County, Hebei Province, China[J].Chin J Virol, 2005, 21(1):21-26.DOI:10.3321/j.issn:1000-8721.2005.01.005. |
| [11] Lou JT, Xu XJ, Wu YD, et al.Epidemiology and burden of rotavirus infection among children in Hangzhou, China[J].J Clin Virol, 2011, 50(1):84-87.DOI:10.1016/j.jcv.2010.10.003. |
| [12] 肖生彬, 颜虹, 党少农, 等.西部农村婴幼儿常见病就诊现状及影响因素分析[J].现代预防医学, 2012, 39(18):4704-4706, 4715.Xiao SB, Yan H, Dang SN, et al.Analysis on medical care utilization among rural younger children in west China and its influencing factors[J].Mod Prev Med, 2012, 39(18):4704-4706, 4715. |
| [13] Black RE, Cousens S, Johnson HL, et al.Global, regional, and national causes of child mortality in 2008:a systematic analysis[J].Lancet, 2010, 375(9730):1969-1987.DOI:10.1016/S0140-6736(10)60549-1. |
| [14] 杨素华, 王宏, 刘娜, 等.2006-2007年我国五岁以下住院儿童轮状病毒流行病学研究[J].中华实验和临床病毒学杂志, 2009, 23(3):168-170.DOI:10.3760/cma.j.issn.1003-9279.2009.03.003.Yang SH, Wang H, Liu N, et al.Molecular epidemiology of rotavirus among children under 5 years old hospitalized for diarrhea in China[J].Chin J Exp Clin Virol, 2009, 23(3):168-170.DOI:10.3760/cma.j.issn.1003-9279.2009.03.003. |
| [15] Li RC, Huang T, Li YP, et al.Human rotavirus vaccine(RIX4414) efficacy in the first two years of life:a randomized, placebo-controlled trial in China[J].Hum Vaccine Immunother, 2014, 10(1):11-18.DOI:10.4161/hv.26319. |
| [16] Castilla J, Beristain X, Martínez-Artola V, et al.Effectiveness of rotavirus vaccines in preventing cases and hospitalizations due to rotavirus gastroenteritis in Navarre, Spain[J].Vaccine, 2012, 30(3):539-543.DOI:10.1016/j.vaccine.2011.11.071. |
| [17] Chang WC, Yen C, Wu FT, et al.Effectiveness of 2 rotavirus vaccines against rotavirus disease in Taiwanese infants[J].Pediatr Infect Dis J, 2014, 33(3):e81-e86.DOI:10.1097/INF.0000000000000105. |
| [18] El Khoury AC, Mast TC, Ciarlet M, et al.Projecting the effectiveness of RotaTeq(r) against rotavirus-related hospitalisations in Brazil[J].Mem Inst Oswaldo Cruz, 2011, 106(5):541-545. |
| [19] 方鹤松.中国七省一市小儿急性腹泻病研究的进展[J].临床消化病杂志, 1991(3):120-122.Fang HS.Progesses in the study of acute diavrhea in children in seven provinces and one city in China[J].Chin J Clini Gastroenterol, 1991(3):120-122. |
| [20] 柴程良.腹泻病流行特征与经济负担研究[D].杭州:浙江大学, 2010.Chai CL.Study on epidemic characteristics and disease background burden of diarrhea[D].Hangzhou:Zhejiang University, 2010. |
| [21] Murray CJ, Lopez AD.The Global Burden of Disease:a comprehensive assessment of mortality and disability from diseases, injuries, and risk factors in 1990 and projected to 2020[M].Cambridge, MA:Harvard School of Public Health, 1996. |
| [22] Aballéa S, Millier A, Quilici S, et al.A critical literature review of health economic evaluations of rotavirus vaccination[J].Hum Vaccine Immunother, 2013, 9(6):1272-1288.DOI:10.4161/hv.24253. |
| [23] Guilbert JJ.The world health report 2002:reducing risks, promoting healthy life[J].Educat Health, 2003, 16(2):230.DOI:10.1080/1357628031000116808. |
| [24] Wang XY, Riewpaiboon A, Von Seidlein L, et al.Potential cost-effectiveness of a rotavirus immunization program in rural China[J].Clin Infect Dis, 2009, 49(8):1202-1210.DOI:10.1086/605632. |
| [25] Liu N, Yen C, Fang ZY, et al.Projected health impact and cost-effectiveness of rotavirus vaccination among children<5 years of age in China[J].Vaccine, 2012, 30(48):6940-6945.DOI:10.1016/j.vaccine.2012.05.084. |
| [26] Lanzieri TM, Costa I, Shafi FA, et al.Trends in hospitalizations from all-cause gastroenteritis in children younger than 5 years of age in Brazil before and after human rotavirus vaccine introduction, 1998-2007[J].Pediatr Infect Dis J, 2010, 29(7):673-675.DOI:10.1097/INF.0b013e3181da8f23. |
 2016, Vol. 37
2016, Vol. 37