文章信息
- 姜涛, 赵光宇, 韩剑峰, 辛文文, 庄道民, 谭亚芳, 何君, 高荣保, 王宏, 陈操, 王峰, 高波, 房彤宇.
- Jiang Tao, Zhao Guangyu, Han Jianfeng, Xin Wenwen, Zhuang Daomin, Tan Yafang, He Jun, Gao Rongbao, Wang Hong, Chen Cao, Wang Feng, Gao Bo, Fang Tongyu.
- 塞拉利昂埃博拉病毒病疫情中13个国际检测实验室的比较以及对我国的启示
- Comparison of international Ebola virus testing laboratories in Ebola virus disease outbreak in Sierra Leone
- 中华流行病学杂志, 2015, 36(9): 1034-1037
- Chinese Journal of Epidemiology, 2015, 36(9): 1034-1037
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2015.09.030
-
文章历史
- 投稿日期: 2015-05-06
2. 病原微生物和生物安全国家重点实验室;
3. 中国疾病预防控制中心病毒病预防控制所;
4. 军事医学科学院微生物流行病研究所
2 State Key Laboratory of Pathogen and Biosecurity;
3 National Institute for Viral Disease Control and Prevention, Chinese Center for Disease Control and Prevention;
4 Institute of Microbiology and Epidemiology, Academy of Military Medical Science
西非埃博拉疫情防控中,感染者的早期发现、实验室快速确认和及时隔离治疗是有效阻止埃博拉病毒病传播的关键环节。其中,实验室确认是开展疑似患者甄别与治疗以及后续疫情控制措施的基础。西非三国本身并无病原检测实验室,也缺乏相应的检测技术人员,国际援助的检测实验室在疫情防控中发挥了举足轻重的作用。系统梳理国际援助塞拉利昂的各检测实验室情况,并与中国援塞移动实验室进行比较与分析,从而总结国外疫情应急检测的先进经验以及中国当前的缺项与不足,为中国公共卫生事件中应急检测能力建设提供启示。
1. 基本情况:西非埃博拉疫情自2013年12月暴发于几内亚Gueckedou和Macenta,并迅速跨过边境传入相邻的塞拉利昂和利比里亚[1]。WHO于2014年3月23日正式收到埃博拉疫情暴发的通报。随着疫情的迅速蔓延与加剧,WHO于8月8日宣布此次疫情为“国际关注的突发公共卫生事件”[2]。塞拉利昂的埃博拉疫情在2014年5月首次出现与几内亚接壤的Kenema和Kailahun地区,并迅速蔓延至全国[1]。截止2015年3月22日,塞拉利昂共有8 518例确诊埃博拉病例,其中3 356例死亡。
2014年9月前,塞拉利昂仅有两家埃博拉检测实验室,检测能力严重不足,覆盖范围也极为有限。一家实验室位于Kailahun,自2014年6月开展埃博拉检测工作,为加拿大公共卫生署援助和运行,另一家实验室位于Kenema,为美国提供资金与技术援助。
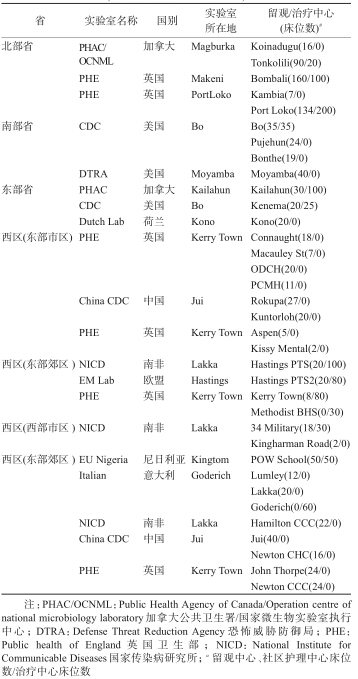
中国在2014年9月16日派遣移动生物安全实验室抵达塞拉利昂首都弗里敦帮助开展埃博拉检测工作,并迅速成为埃博拉检测的核心力量。2014年10月底,包括中国在内的6家检测实验室开展埃博拉病毒检测工作。至2015年初,由中、美、意、英、南非、加拿大、欧盟和尼日利亚等援助的检测实验室已达13家,其中西区6家、北部省3家、东部省2家、南部省2家,基本覆盖了塞拉利昂所有行政区和主要交通枢纽[3]。这些检测实验室依托塞拉利昂各行政区的埃博拉治疗中心(Ebola Treatment Centre,ETC)和/或留观中心(Ebola Holding Centre,EHC)开展工作,收取依托医疗机构以及周边留观与治疗中心、社区诊疗中心(Community Care Centre,CCC)的埃博拉疑似病例及不明死者的样本开展埃博拉病原检测(表 1)。在各国检测实验室的共同努力下,单日样本检测能力最高时达到1 500份样本,基本实现了新发现疑似病例在24 h内得到检测确认和临床诊断,为早发现、早诊断和早隔离提供必要的技术支撑。
2. 各国埃博拉检测实验室检测技术比较:检测实验室来自各国,在检测技术、生物安全理念以及实验室设计上各有特色,反映了不同国家在重大疫情现场快速检测能力建设上的理念差异与侧重。现分别从病毒检测技术、生物安全以及实验室能力等在塞拉利昂检测实验室进行比较分析,以期有所借鉴。
(1)病毒检测技术:此次塞拉利昂国际援助检测实验室的检测技术呈现3个特点:
一是自动化核酸纯化成为高通量样本处理的主流。基于固定设施的实验室和现场实验室大多采用自动化核酸纯化装置,以满足快速高效处理大量样本的需求。例如中国、美国和南非采用Life Technologies公司的MagMax Express 96®核酸自动提取仪,该仪器采用磁珠法原理,可一次从96份临床样本纯化病毒核酸。英国Kerrytown等3家实验室则各采用2台Qiagen公司生产的14通量的EZ1核酸自动提取仪。MagMax核酸提取仪的优势在于通量高,可在30 min内完成96份样本的核酸制备;EZ1核酸自动提取仪的优势在于成本控制,当样本数小于50份样本,EZ1更为灵活经济,耗材与试剂损耗较少。与核酸自动提取仪相比,手工提取病毒核酸花费时间一般要超过2 h,当样本数超过50份以上时,在样本灭活处理、信息核对与核酸制备环节花费的时间总共约需5 h,严重影响检测效率。中国第二批和第三批移动实验室检测队配备全自动核酸制备仪器后,样本处理与核酸制备时间可控制在2 h内,加上核酸检测的时间,整个检测环节仅需3~4 h。欧盟移动实验室则偏重机动性能,牺牲了实验室高通量样本处理能力,在疫情高峰期处理大量样本时效率较低。意大利以及尼日利亚等实验室也有类似问题。
二是实时PCR仍是病原检测确认的主体检测技术。虽然近些年来病毒传染病的快速检测方法飞速发展,但在突发疫情现场实验室检测需求上,实时PCR检测方法仍是首要之选。它虽然对仪器以及操作人员的专业性有着较高的要求,但其高灵敏性、高特异性、不开盖交叉污染低等优点仍使得它成为实验室病原确认的最佳选择。胶体金等传统快检方法、微流体芯片等技术或灵敏度低或囿于成本难以满足应急检测的需求。从表 2可以看出,在塞拉利昂各国家检测实验室主要采用商业化埃博拉检测试剂盒,或者实验室检测方法(In-house assay),在技术水平上区别不大。塞拉利昂卫生部第二次检测实验室外部质量考核也显示实验室检测能力差异甚微。但各实验室在检测仪器的选择上则侧重不同。中国和美国采用的是实验室级别的96通道实时定量PCR仪,特点是高通量,缺点是光路元件较为脆弱,机动运输能力差,使用前可能需要光路校正。而英国、欧盟等实验室则更多基于考虑机动性与灵活性的考虑,采用Cepheid公司的SmartCycler®实时PCR仪。该仪器具有16个反应模块,具有独立的光学以及热学校准,可分别开展检测反应,当样本量较少时,检测更为灵活机动。
三是分区操作是临床核酸检测的根本要求。即便此次埃博拉疫情应急检测的特殊性质以及基础条件不足的限制,各国际援助实验室仍将分区操作作为临床核酸检测质量的根本保证。各固定或半固定现场实验室在建设过程中,已将分区考虑在内。例如美国Bo城实验室分设了3个房间(试剂准备、核酸制备与模板添加以及PCR室)和室外一个单独的样本处理区;实验服为各房间专用,试剂与样本也分别储藏在各自专用冰箱内。英国Kerrytown实验室在样本处理与核酸制备外,又单独设立了试剂准备、模板添加与PCR室3个小房间,并在房间内设置了洁净柜以进一步避免交叉污染的可能。意大利的Goderich实验室仅设有试剂准备、加样与PCR 3个分区,没有单独的房间,空间是联通的。为解决这一问题,该实验室采用PE材质的简易隔离手套箱用于核酸制备、扩增试剂准备两个关键环节,以实现基本的空间隔离。总之,各援塞检测实验室麻雀虽然囿于条件所限,无法实现定向气流与人流,但采用房间空间间隔或采用手套箱实现基本的空间隔离,有效避免核酸检测交叉污染问题。
(2)生物安全:按WHO埃博拉病毒病诊断实验室诊断指南要求,埃博拉样本的处理与核酸检测应符合下列生物安全要求[4]。方案一:具备BSL-3/4生物安全设施的检测实验室时:病毒分离应在BSL-4实验室开展。应确保病毒分离物和样本妥善的处理和保管,避免无意或恶意的泄露;样本的灭活操作应在BSL-3实验室条件下进行;非灭活的样本,须在BSL-3实验室内开展RT-PCR以及ELISA检测。样本灭活(例如裂解)后,可在BSL-2实验室内开展RT-PCR以及ELISA检测。方案二:缺乏BSL-3/4相关设施的检测实验室:PCR或ELISA检测的样本处理应在单独实验室区域内的三级生物安全柜(手套箱)内进行;样本灭活后,可从手套箱内取出在BSL-2实验室条件下开展后续检测工作;处理未经灭活的样本时,应佩戴必要的个人防护装置,包括手套、N95口罩或电动空气过滤系统,全脸面屏和一次性防水外罩衣。
各国援助塞拉利昂检测实验室主要包括三种生物安全方案:中国移动BSL-3实验室具备BSL-3级条件,采用WHO第一种生物安全方案。在操作流程上,一是样本经过双重灭活,二是样本、人员与环境三重防护,即样本在生物安全柜中操作,人员着正压防护头罩,三是样本处理与核酸制备在BSL-3负压环境内进行,保障了人员与环境的双重安全。美国则采用的第二种的替换方案,即仅依赖个人正压防护的生物安全策略:即在检测实验室区域外10 m的空地处设立了一个单独的开放式样本处理室,房间围墙约1.8 m处围挡约有30 cm是与外接联通开放;样本直接在实验台面操作而未采用手套箱;个人防护采用带电动送风的正压防护头罩(PARP);除可能操作时发生样本沾染的一次性外罩衣外,其余防护用具均反复使用。这显示美国完全认定埃博拉病毒主要通过接触而非飞沫或气溶胶传染,其所有的操作规程与生物安全要求均基于这一基本科学认定。其余国家的援塞实验室则均采用WHO第二种基于负压手套箱的生物安全方案。意大利实验室的手套箱为硬结构外排式的,生物安全系数最高;欧盟移动实验室采用的是简易折叠手套箱,采用商业化生防过滤罐作为空气过滤方案,每2周更换一次。其余实验室的手套箱为固定框架下的柔式手套箱,易于运输和展开。南非在手套箱操作区域外增加了负压隔离装置,通过定向气流实现13~18 Pa的负压,并将装置内区域视为半污染区,人员入内操作需着正压防护防护。各国检测实验室的生物安全方案详见表 3。
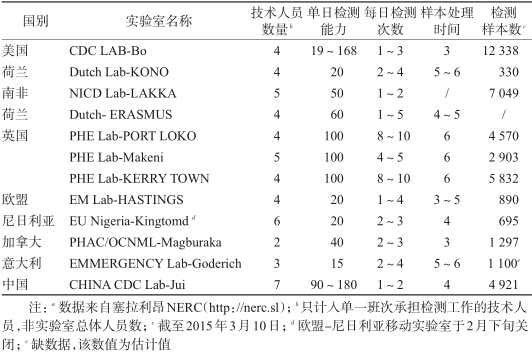
(3)实验室能力:各国人力资源使用大致相同,4人是较为通用的方案,这主要依赖于工作的分配,常规上一人负责样本接收、一人负责样本处理与核酸制备、一人负责PCR反应、一人负责信息上报。当人数<4人时,任务则相应合并。中国因需2~3人进行移动车载BSL-3实验室保障,因此人员配备较其他检测实验室为多,但承担检测核心任务的人员与其他实验室相同。援塞各国检测实验室的检测能力见表 4。值得借鉴的是,欧美等国检测实验室普遍不自行承担仪器保障,而采用直接运回国内维修保养方式,减少了人员配备,避免实验人员额外的工作压力。
各实验室的单日检测能力与检测速度主要与其核酸制备能力相对应。中国、美国、英国等采用自动化核酸设备,每日可完成超过100份样本的检测工作,单轮检测时间<4 h。中国检测实验室曾于2014年12月2日达到124份的单日最高检测量,总检测量接近5 000例(截至2015年3月10日)。其他实验室则囿于核酸手工提取的局限,单日检测量一般不超过50份。
(4)机动能力:援塞国际检测实验室主要分为现场实验室(Field Lab)、移动实验室(Mobile Lab)和固定实验室(Fixed Lab)。一般来说,移动实验室主要是指基于车载的实验室或者可通过机动运输展开的实验室。在西非,除中国的车载实验室系统外,其他所有的移动实验室则均为装备与耗材模块箱组化的实验室。欧美国家的移动实验室有多种装备组合,例如车载检测实验室、集装箱式实验室、模块化箱组实验室等。针对城市疫情与反恐应急,多采用车载实验室;而针对需要远程机动性的疫情应急处置,则多选择集装箱式实验室或模块化箱组类的移动实验室,其原因一是易于运输,二是能源损耗小,对展开环境要求低。相对于国外的模块化机动实验室,中国援塞的移动BSL-3实验室则暴露出一些问题:一是由于初始设计是针对城市疫情与生物恐怖处置的目的,因此仅具备常规陆路机动能力,更适合城市作业;二是功能有限,由于车载实验室仅包括BSL-3实验室,从功能分区与生物安全角度,需在车载实验室外另设PCR检测实验室,这就削弱了实验室的移动特点,同时车组缺少必要的仪器与试剂耗材运输能力,无法实现车组到位即时展开并开展检测工作。
3. 启示:此次西非埃博拉疫情,中国派出了以车载移动BSL-3实验室为核心的检测实验室赴塞拉利昂开展埃博拉病毒检测工作,高水平的完成了援塞抗埃任务,展现了中国在生物安全与传染病防控上的巨大进步,但在执行任务中,也暴露出中国应急检测力量建设与欧美等国的差距与不足。
(1)移动生物安全实验室的理念与经验仍存较大差距:自2003年SARS疫情后,我国对传染病的再认识从整体上推动了疫情防控的发展。而国内外多起实验室生物安全事故也有效推动了我国生物安全立法和相关认证认可的发展。2003年以来,《病原微生物实验室生物安全管理条例》等管理条例、相关标准和实验室生物安全认可制度相继发布实施。我国高等级生物实验室的建设进入了稳步发展阶段。公众生物安全意识、从业人员素质和管理水平得到提高;高等级生物安全实验室设计、建设、施工工艺和技术日趋成熟。特别是随着近年来H1N1、H7N9禽流感、MERS以及西非埃博拉疫情的暴发与处置,我国上下整体对生物安全的重视提到一个前所未有的高度,对固定实验室的建设、管理与应用经验非常丰富。
但此次援塞抗埃任务也暴露出应急现场或移动实验室生物安全理念落后与经验不足的问题。这种不足体现在:一是生物安全防护机械照搬固定实验室防护模式,而不是针对埃博拉病毒风险评估而制定的有针对性防护措施;二是移动实验室的设计与建设基本脱胎于固定实验室,而没有充分考虑其特殊的工作性质和现场开展工作的局限性,未集成核酸检测能力,缺少必要的物资运输能力,无法实现即时展开和迅速开展工作。三是机械照搬国内临床核酸检测的方案,特别是采用生物安全柜作为基本操作载体,难以满足现场实验室和机动实验室需要。四是由于缺少真正实战的检验,移动BSL-3实验室的一些设计与应用与实战需求脱节,表现在对水电要求高,污水处理、高压灭菌与淋浴不实用等问题。而欧美国家采用可拆卸手套箱作为现场实验室的生物安全替代方案,易于实现;采用简单分区甚至采用微型洁净柜实现核酸检测的分区操作,易于改造;采用适合机动的实时PCR仪而非普通的商业化PCR仪,易于机动。欧美等移动实验室这些从生物安全防护到核酸检测,从工作流程到检测方案,在各个环节充分考虑了生物安全与现场应急检测的统一,给我国公共卫生事件的应急处置提供了极好的借鉴。
(2)亟需加强核心技术研发:此次援塞抗埃任务极好地展现了我国的技术实力,但也暴露出我国在核心技术上的差距,例如BSL-3双扉高压锅、HEPA滤材、高生物安全等级手套箱、负压隔离装置、实时PCR仪、自动核酸提取仪等关键装置仍需进口。这一问题不解决,我国生物安全领域的发展、公共卫生的应急处置领域仍将受制于他国。从某种程度上,我国在此次援塞任务中不得不采用大型车载BSL-3的生物安全方式,除了理念上的问题,也有非车载机动实验室由于关键与核心技术的缺乏而举步维艰的原因。因此,迫切需要加大技术研发,提升生物安全装备自主创新能力,尽快实现生物安全核心技术与核心装备的吸收转化与自我保障。
(3)亟待推进关键应用性系统研究:虽然我国在生物安全以及疫情防控领域开展很多研究,但关键的应用基础性系统研究仍较为缺乏。例如针对高等级生物安全病原体,其灭活与生物安全废弃物的安全处理方法?实验室操作导致病毒飞沫或气溶胶产生的风险?在生物安全柜与手套箱操作埃博拉或者其他可形成气溶胶并导致感染的病原体的导致泄漏的风险?防护服表面埃博拉病毒潜在沾染的风险评估及其消毒处理?不同消毒剂对烈性病原体的消杀方法及效果?这些问题或相关领域的问题不解决,在未来类似埃博拉病毒病等烈性传染病防控中,仍会囿于关键原理不明、要素不清,而导致认识不清而处置失当,风险评估不当而引起过度防护或防护不当,资源配比不清而引起人力与物力浪费。
| [1] Baize S, Pannetier D, Oestereich L,et al. Emergence of Zaire Ebola virus disease in Guinea[J]. N Engl J Med,2014,371(15):1418-1425. |
| [2] WHO. Statement on the 1st meeting of the IHR Emergency Committee on the 2014 Ebola outbreak in West Africa[EB/OL]. (2014-08-08)[2015-05-01]. http://www.who.int/mediacentre/news/statements/2014/ebola-20140808/en/. |
| [3] UNMEER. Sierra Leone:Ebola emergency weekly situation report No. 12,5-11 January 2015[R]. Government of Sierra Leone,UN Mission for Ebola Emergency Response,2015. |
| [4] WHO. Laboratory diagnosis of Ebola virus disease[EB/OL]. (2014-09-19)[2015-05-01]. http://www.who.int/iris/bitstream/10665/134009/1/WHO_EVD_GUIDANCE_LAB_14.1_eng.pdf. |
 2015, Vol. 36
2015, Vol. 36