文章信息
- 汪宁, 钟平. 2014.
- Wang Ning, Zhong Ping. 2014.
- 中国HIV分子流行病学30年
- Molecular epidemiology of HIV in China:1985-2015
- 中华流行病学杂志, 2015, 36(6): 541-546
- Chinese Journal of Epidemiology, 2015, 36(6): 541-546
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2015.06.001
-
文章历史
- 投稿日期:2015-05-04
2. 上海市疾病预防控制中心
2. Shanghai Center for Disease Control and Prevention
1981年6月5日,美国疾病预防控制中心《发病率与病死率周报》(MMWR)[1]发表了Gottlied报告洛杉矶5名年轻男同性恋者感染罕见的卡氏肺囊虫肺炎,尽管该报告当时并未引起关注,但该日被定为艾滋病发现日。1982年9月,美国疾病预防控制中心首次正式在MMWR将此病症命名为AIDS。1983年法国病毒学家Barre-Sinoussi等[2]从1例AIDS患者淋巴结中分离出一种新的人类反转录病毒(LAV);同时,美国病毒学家Gallo等[3]报告他们分离到的新人类反转录病毒(HTLV-Ⅲ)可能是AIDS病原体。1986年国际微生物学会及国际病毒分类学会将这类病毒统一命名为HIV。
我国1985年在北京诊断了中国境内首例AIDS患者(阿根廷籍)[4]。同年在杭州血友病患者中发现了首例中国本土居民感染HIV的事件[5]。依据临床发现病例而言,2015年是中国发现艾滋病并开展防治及科学研究30周年。 1. 我国HIV分子流行病学的发展及对防治工作的贡献。
(1)运用分子水平的生物标志物研究我国HIV传入时间和来源。我国科学家采用血清学技术对中国首批HIV感染者做流行病学调查,溯源研究发现HIV经血液制品1982年由美国传入中国,1983年感染了我国部分使用受染血液制品者[6]。1989年我国首次在云南省德宏州注射吸毒(IDU)人群中发现HIV暴发流行[7, 8]。之后,对该阳性人群进行分子流行病学研究,显示该地区IDU人群HIV-1为B亚型(欧洲B亚型)及B’亚型(泰国B亚型),由缅甸传入[9]。次年,在泰国遣返回中国云南的暗娼(FSW)中发现了CRF01_AE亚型[10]。1995年首次报道了在中国德宏州1992-1993年收集的IDU人群样本中发现由印度传入的C亚型毒株[11]。我国于1999年在福建省发现首例HIV-2感染者[12]。泰国、印度以及越南的B亚型、C亚型和CRF01_AE通过贩毒和IDU以及性交易途径越过边界进入我国并在不同的时间阶段成为我国主要的流行毒株[13, 14, 15, 16];可见,运用分子水平的生物标志物(抗体、病毒抗原和核酸等)研究我国HIV感染溯源和传播轨迹等方面的流行病学问题起步较早。
(2)全面系统地按统一设计方案开展全国HIV-1流行亚型分布与变迁的调查和监测。为及时掌握我国不同时期、不同地区、不同高危人群HIV-1亚型流行分布情况,了解我国主要流行毒株的消长趋势及新重组毒株的传播和相关影响因素,我国共进行过3次全国HIV分子流行病学调查。1996-1998年进行的第一次调查显示,我国HIV-1主要流行的亚型有B’(47.5%)、C(34.3%)及CRF01_AE亚型(9.6%)[13]。2002-2003年第二次调查显示,我国HIV-1流行的亚型以BC重组毒株、B’和CRF01_AE为主,并且在国际上首次报告了中国独特的CRF07_BC和CRF08_BC重组毒株[17]。2006-2007年第三次调查结果显示,我国存在至少12种HIV-1基因型,已经成为全球HIV-1基因亚型最多的国家之一;当时我国HIV-1流行的亚型主要有CRF07_BC(35.5%)、CRF01_AE(27.6%)、CRF08_BC(20.1%)和B’(9.6%),占HIV感染者总数的92.8%;该调查还发现BC、BC/CRF01_AE、CRF01_AE/C、CRF01_AE/BC、CRF01_AE/B和C/CRF01_AE等多种重组基因型毒株在不同地区和不同高危人群开始流行;与早期全国HIV-1主要流行亚型的分布有了很大改变[18]。揭示我国HIV扩散途径,反映我国HIV流行优势株在各地区各高危人群都随时间而变化。通过对近20多年来我国HIV-1基因亚型(簇)分布特征及流行变迁趋势进行系统分析,可以清楚地看到我国HIV-1新的变异和重组的流行毒株越来越多,传播的速度也越来越快,HIV-1的基因型种类和流行模式越来越复杂。虽然各地区和主要高危人群中的HIV-1主要流行优势毒株的构成存在一些特点,但其差异性随着时间变化而趋于减弱,特别是在性传播途径HIV感染者中和以性传播途径为主的地区更加明显,传播途径比地域对HIV基因多样性的影响更强[19]。这些信息强烈提示,我国的HIV/AIDS及其高危人群之间无保护性行为是最近一段时期我国HIV-1亚型多样化的“孵化器”和“加速器”。目前正进行第四次全国HIV-1分子流行病学调查,期待能有更新的发现。
(3)我国科学家在世界上首先发现和鉴定了一批新的HIV-1流行毒株,丰富了全球重组病毒库,并且对这些新发现的流行毒株的流行病学意义进行了较深入的研究。从1996-1997年云南德宏、广西南宁、新疆乌鲁木齐等地区IDU人群HIV-1中发现2种B/C重组亚型(CRF07_BC和CRF08_BC)[17, 20, 21, 22]。这是最早在中国发现、并被美国国家生物技术中心基因库(GenBank)收入的HIV-1重组亚型。它是由在云南同时流行的B亚型和C亚型毒株经复杂重组后传播远至新疆和全国各地[18, 19, 23, 24, 25]。最新的研究表明CRF07_BC分成2个进化支,经由不同的毒品转运途径,一支从新疆传播至辽宁、江苏、黑龙江、北京、广东等地,另一支从云南传播至台湾;而CRF08_BC亚型从云南自1994年前后向东北传播到辽宁,1995年前后向东传播到广西[26]。这两个中国重组毒株已传播其他亚洲国家和欧美国家[27]。
第二次全国分子流行病学调查之后是我国分子流行病学蓬勃发展期。从2007年深圳地区MSM人群HIV感染者中首次发现CRF55_01B[28]。目前我国南方部分地区已发现CRF55_01B占MSM HIV感染者的10%以上[29]。从2008年辽宁、广东、云南、湖南等地区的MSM人群样品中首次发现CRF59_01B[30]。在MSM人群中发现的新型HIV重组株CRF55_01B和CRF59_01B,是继我国IDU人群中检出CRF07_BC和CRF08_BC两株重组株以来,我国鉴定的最重要的新HIV重组毒株,为监测HIV传播提供了新靶标[28, 31]。从2008年吉林和福建等地的异性性传播人群HIV感染者中首次发现CRF61_BC[32]。从2009年云南地区IDU和/或异性性传播人群HIV感染者中首次发现CRF57_BC[33]、CRF62_BC[34]、CRF64_BC[35]、CRF65_cpx[36]。从2009年广西异性性传播人群中发现并命名新型CRF01_AE变异毒株CRF01_AE-v[37],现广泛流行于国内许多地区;2007年发表了详尽解析的05CNHB_hp3毒株,该毒株被GenBank选为HIV-1国际标准参考序列广泛参考应用[38]。我国科学家首次发现并报告多个新的二代重组病毒均被GenBank收入并得到正式命名。
CRF01_AE毒株最早在1994-1996年云南、广西等地FSW人群和IDU人员中检测到的,现已广泛播散到全国的不同地区和人群,异性性传播和静脉吸毒传播是其流行的主要传播途径,分别占50.2%和38.9%[18, 19]。中国至少存在7个独立的进化簇,其中簇1、2和3主要在中国华南和西南部省份异性性传播和IDU人群中流行;簇4和5主要在北方部分城市中的MSM人群中流行;簇6和7则分别在福建和云南的异性性传播人群中流行,7个独特的AE流行簇已经在我国不同的高危人群中迅速形成和流行[39]。尚红教授团队在国内最早对MSM人群中HIV传播规律进行系统研究,发现我国9个大、中城市MSM人群75%以上的HIV感染是由CRF01_AE和1株CRF07_BC引起的,并通过系统进化和贝叶斯方法估算了3个毒株的起源、传播路线、影响范围和规模,对我国控制HIV传播和疫苗研究具有重要意义[40, 41]。对中国CRF01_AE流行起始时间分析的结果表明,所有的CRF01_AE进化簇都在20世纪90年代中期从泰国进人中国[39]。
分子流行病学在这些重组病毒新发现以及追踪流行轨迹方面发挥了关键的作用,对我国的艾滋病防治工作有科学指导意义。
(4)在发现HIV耐药的发生、监测HIV耐药的流行动向、提出应对策略等方面做出贡献。2008年以来的分子流行病学监测的实践为我国建立HIV耐药监测网络奠定了坚实的基础,我国在北京、上海和沈阳分别建立了四个HIV耐药监测核心实验室和一个亚太区域级HIV耐药实验室,以及遍及全国省会城 市省级耐药监测网络实验室,这是全球最大的国家HIV耐药监测网络,在国内和国际上产出一批较好的研究成果[42, 43, 44, 45, 46, 47, 48]。我国HIV/AIDS获得性耐药的发生率随抗病毒治疗时间而增长趋势的速度快于欧美国家,主要问题在于服药患者的依从性不够、训练有素的医生数量不够,病毒载量和耐药检测密度不够等[49]。另一个值得警惕的是我国传播性耐药HIV株的流行已在一些高流行地区和大城市出现流行,特别在MSM人群中更明显[50]。我国部分城市MSM人群中HIV传播性耐药率已达5%以上,非核苷类药物引起的耐药株传播明显上升,在我国HIV新型重组株中也检出耐药,急需加强MSM人群耐药监测及治疗前检测[47]。提示在扩大治疗实践中决不能忽视艾滋病相关高危行为干预工作,一定要慎重对待HIV耐药株流行的后果。最近有我国科学家参与的由美国斯坦福大学牵头,联合 32个国家的63个团队,针对 2000-2013年发表的 287 篇HIV耐药性研究论文(涵盖111个国家的 50 870个样本)展开了全球性HIV-1的RT耐药基因突变的详尽分析,是一篇非常有学术参考价值的综述性论文[51]。
(5)监测我国流行的不同亚型HIV毒株的致病性变化,发现某些HIV-1重组株的毒力显著增强,加速宿主CD4细胞耗损,疾病进程显著加快。研究认为,HIV的病毒亚型和病毒嗜性可能是影响HIV进展的重要因素[52]。例如B’亚型占HIV-1感染基因型95%的我国中部地区经既往有偿采供血感染HIV人群[19],其从感染HIV至发病的中位潜伏期约为8.5~9.6年[53, 54, 55]。而当前在我国性传播人群中流行的优势株CRF01_AE则具有较强致病性[56]。一项国内12家医院参与的研究,通过对MSM队列HIV-1阳转者CD4+T淋巴细胞计数消长情况随访发现,感染CRF01_AE亚型的患者较非CRF01_AE亚型组患者疾病进展更快(病程4.8年vs. 6.4年)[57]。通过从临床、流行病学以及基础研究的不同角度鉴定和分析了在我国流行多年的CRF01_AE重组病毒,首次提出了目前在我国广泛流行的CRF01_AE重组病毒是加快疾病进展和导致感染人群平均在4~5年内进入艾滋病期的主要原因,解释了大量低CD4+T淋巴细胞计数的新感染者现象[56, 57],为早诊断早治疗的方案提供了科学支持,同时也为准确估计我国经性 (特别是MSM人群)感染HIV的疾病进程以及正确评价防治效果提供重要的校正参数。
(6)将分子水平检测技术用于判断HIV-1感染时间、追查传播来源和传播途径做出的贡献。目前已有10余种HIV-1新近感染的检测方法[58],其中应用最为广泛的是BED捕获酶免疫实验(BED capture enzyme immunoassay,BED-CEIA)法,其原理是通过检测HIV-1感染后人体内抗HIV IgG增加的水平区分HIV-1近期感染和长期感染。BED- CEIA适用于多种HIV-1 亚型,在横断面研究或者哨点监测的HIV-1新发感染率研究中应用广泛[59, 60, 61]。我国的研究表明,确认HIV-1阳性的样本经BED- CEIA检测后,如果An值≥1.2则为长期感染(感染时间>168 d),An值≤0.8时,则为近期感染(感染时间<168 d)[62, 63]。采用BED-CEIA对MSM、FSW人群中HIV-1新发感染检测显示,我国MSM人群中HIV的新发感染率在7.0%~8.0%之间[64, 65],FSW人群中HIV的新发感染率在0.5%~4.4%之间[66, 67, 68]。
HIV的一个显著特点是其基因的高度变异性,HIV在传播过程中产生许多亚型并形成一定的地区分布特点。各亚型之间基因核苷酸序列差异较大,而HIV毒株在一个地区流行起始时其基因变异在 0%~2%之间,然后平均每年以 0.5%~1%的速度变异,据此,可以根据基因离散率推算某一基因型在某一地区的流行时间[9, 69, 70]。HIV-1的基因遗传多样性(diversity)与感染时间存在相关关系:在未治疗的情况下,如果病毒载量在检测值102 copies/ml以上,HIV-1的遗传多样性与感染时间成正比即感染时间越长遗传多样性越大;这种线性关系在Fiebig Stages Ⅰ~Ⅴ期之间比较稳定,感染5年以后这种复杂度的上升会到一个平台期[71]。因此在感染时间处于一定范围内可以通过病毒的序列变异度预测感染时间[72]。但是随着进化会产生适应性强的优势毒株,HIV-1遗传多样性会进入新的动态平衡状态[73]。系统进化树分析已被证明是提供HIV-1传播史(链)证据的有用方法。 2. 中国HIV分子流行病学面临的挑战与机遇。
(1)30年来我国艾滋病的流行形势发生了很大的变化,在正确地认识疫情特点和科学地判断疫情走势等方面都需要分子流行病学更精准的信息。该时期我国每年新报告HIV/AIDS例数逐年上升,HIV主要传播途径有了明显改变,以血液传播(涉及的人群和地区都很局限)转变到性传播(涉及的人群和地区都很广泛)为主,传播途径多样化,受累人群由高危人群为主到高危及一般人群并重的巨大变化(图 1);流行地区由农村为主到城乡并行,2004-2005年对部分地区部分人群大筛查,检出大量既往HIV感染(20世纪90年代中期的不安全采供血,以及90年代后期IDU)。近几年,每年新报告HIV/AIDS者中仍有40%左右的中晚期感染者(CD4+T淋巴细胞计数<200 cells/μl)[74],使得基于阳性样本检测调查所得HIV-1亚型分布状态与现实情况相比,有可能呈现一定时滞性。目前,高危行为人群规模及其交往密度的扩大,使得HIV毒株变异、重组机会更易发生,新的毒株扩散和传播更加容易。给我国的艾滋病防控提出了新的急需解决的问题。
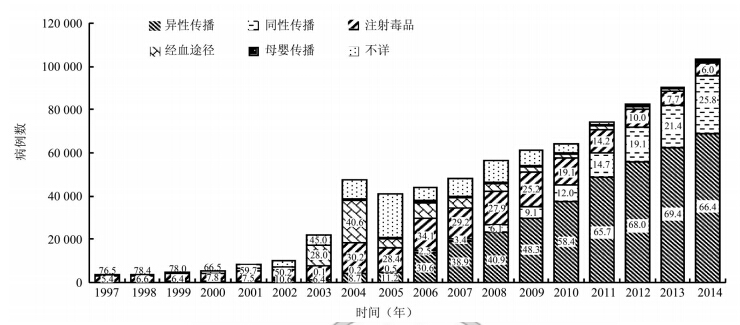 |
| 图 1 我国历年新报告 HIV/AIDS人数及其传播途径 |
(2)随着大数据时代到来,我们应该及时引进、开发、推广分子流行病学的新技术新方法,充分地利用实验室结果与流行病学信息对接整合,甚至将HIV亚型变异与AIDS相关社会生态因素综合分析。在传统流行病学调查和艾滋病防治领域大数据资源的基础上,广泛应用分子系统进化并推演分析、系统进化发生地理学理论和技术以及近年来发展的贝叶斯合并理论推演方法,在准确和精确地解决HIV-1起源、传播方向、时空流行分析以及人际间传播等方面无疑能起到决定性的作用,充分发挥分子流行病学研究和监测结果的指导作用。
(3)将HIV分子亚型监测、分子系统动力学与抗病毒治疗的工作目标相结合,对不同地域和不同高危人群的HIV进行分子动力学以及病毒传播网分析,及时发现新的重组毒株(特别是新的耐药毒株)和快速成簇的毒株或快速发展簇的毒株,针对这些病毒特征的HIV感染者需要特别关注,优先和强化对他们的抗病毒治疗,即所谓的强关联者治疗概念,实施“簇内监测、干预、治疗”有效干预方式。在2014年和2015年的“反转录病毒和机会性感染大会”上,国际专家们继续着重聚焦于HIV传播链/传播簇和传播网络的监测分析,强调将分子系统进化动力学与宏观流行病学结合,对HIV-1分子传播网络监测和网络内高危人群活动模式的重视,为精准和有效的干预提供科学依据。美国建立圣地亚哥HIV-1分子传播网络评分,发现高网络评分与基线高危行为高度相关,可以预测传播危险;对高网络评分的HIV感染个体(即强关联者)进行优先抗病毒治疗,可大大降低HIV传播率,显著降低HIV传播的网络水平[75]。这些研究还包括“HIV传播网络结构揭示了桥梁人群的特征”、“美国2007-2012年传播簇的增长和地域播散”、“比较确认和非确认的流行病学伴侣HIV传播网络”和“固定性伴侣和HIV基因关联伴侣的HIV传播网络”等,最新进展对指导我国的HIV-1传播链和传播网络监测、确定传播性较强且高危行为较频繁的HIV感染者为优先治疗者、评估和指导当地抗病毒治疗的预防干预有效性等方面都具有重要参考价值。
| [1] Center for Disease Control. Pneumocystis pneumonia—Los Angeles[J]. MMWR Morb Mortal Wkly Rep, 1981, 30(21):250-252. |
| [2] Barre-Sinoussi F, Chermann JC, Rey F, et al. Isolation of a T-lymphotropic retrovirus from a patient at risk for acquired immune deficiency syndrome (AIDS)[J]. Science,1983,220(4599):868-871. |
| [3] Gallo RC,Sarin PS,Gelmann EP,et al. Isolation of human T-cell leukemia virus in acquired immune deficiency syndrome (AIDS)[J]. Science,1983,220(4599):865-867. |
| [4] Zheng YY. First case of AIDS diagnosed in China[J]. Natl Med J Chin,1988,68(1):5-6. (in Chinese) 郑育英. 我国诊断的首例艾滋病[J]. 中华医学杂志,1988,68(1):5-6. |
| [5] Zeng Y, Fan J,Zhang Q,et al. Detection of antibody to LAV/HTLV-Ⅲ in sera from hemophiliacs in China[J]. AIDS Res,1986,2 Suppl 1:S147-149. |
| [6] Zeng Y. Serological screening of HIV antibody in China[J]. Chin J Epidemiol,1988,9(3):138-140. (in Chinese) 曾毅. 艾滋病的血清流行病学调查研究[J].中华流行病学杂志,1988,9(3):138-140. |
| [7] Ma Y,Li ZZ,Zhang KX,et al. First detection of HIV infection in drug users in China[J]. Chin J Epidemiol,1990,11(3):184- 图1 我国历年新报告HIV/AIDS人数及其传播途径 185. (in Chinese) 马瑛,李祖正,张开祥,等. 首次在我国吸毒人群中发现艾滋病病毒感染者[J]. 中华流行病学杂志,1990,11(3):184-185. |
| [8] Zhao SD,Cheng HH,Zhang JP,et al. AIDS surveillance in Yunnan province in China (1986-1990)[J]. Chin J Epidemiol,1991,12(2):72-74. (in Chinese) 赵尚德,程何荷,张家鹏,等. 云南省艾滋病监测报告(1986-1990)[J]. 中华流行病学杂志,1991,12(2):72-74. |
| [9] Weniger BG,Takebe Y,Ou CY,et al. The molecular epidemiology of HIV in Asia[J]. AIDS,1994,8 Suppl 2:S13-28. |
| [10] Cheng H,Zhang J,Capizzi J,et al. HIV-1 subtype E in Yunnan,China[J]. Lancet,1994,344(8927):953-954. |
| [11] Luo CC,Tian C,Hu DJ, et al. HIV-1 subtype C in China[J]. Lancet,1995,345(8956):1051-1052. |
| [12] Yan YS, Zheng ZS,Chen G,et al. First case of HIV-2 diagnosed in Fujian[J]. Str J Prev Med,1999,3(1):6-7. (in Chinese) 严延生,郑兆双,陈舸,等. 福建发现首例HIV-2感染者[J]. 海峡预防医学杂志,1999,3(1):6-7. |
| [13] Shao YM,Su L,Xing H,et al. HIV molecular epidemic research in China[J]. Bull Med Res,2000,29(11):19-20. (in Chinese) 邵一鸣,苏玲,邢辉,等. 全国范围艾滋病毒分子流行病学研究[J]. 医学研究通讯,2000,29(11):19-20. |
| [14] Liao HN, Tee KK, Hase S, et al. Phylodynamic analysis of the dissemination of HIV-1 CRF01_AE in Vietnam[J]. Virology,2009,391(1):51-56. |
| [15] Li Y, Uenishi R, Hase S, et al. Explosive HIV-1 subtype B'epidemics in Asia driven by geographic and risk group founder events[J]. Virology,2010,402(2):223-227. |
| [16] Li Z, He X, Wang Z, et al. Tracing the origin and history of HIV-1 subtype B' epidemic by near full-length genome analyses[J]. AIDS,2012,26(7):877-884. |
| [17] Group for HIV Molecular Epidemiologic Survey. Project summary for national HIV molecular epidemiology and database establishment[Z]. 2004. (in Chinese) “全国艾滋病毒分子流行病学调查及数据库的建立”项目组. “全国艾滋病毒分子流行病学调查及数据库的建立”项目总结[Z]. 2004. |
| [18] He X, Xing H, Ruan YH, et al. A comprehensive mapping of HIV-1 genotypes in various risk groups and regions across China based on a nationwide molecular epidemiologic survey[J]. PLoS One,2012,7(10):e47289. |
| [19] Su YY,Liu HX,Wu J,et al. Distribution of HIV-1 genotypes in China:a systematic review[J]. Chin J Epidemiol,2014,35(10):1164-1168. (in Chinese) 苏迎盈,刘慧鑫,吴静,等. 中国HIV-1基因亚型分布及流行趋势[J]. 中华流行病学杂志,2014,35(10):1164-1168. |
| [20] Su L,Graf M,Zhang YZ,et al. Characterization of a virtually full-length human immunodeficiency virus type 1 genome of a prevalent intersubtype (C/B') recombinant strain in China[J]. J Virol,2000,74(23):11367-11376. |
| [21] Piyasirisilp S,McCutchan FE,Carr JK,et al. A recent outbreak of human immunodeficiency virus type 1 infection in southern China was initiated by two highly homogeneous,geographically separated strains,circulating recombinant form AE and a novel BC recombinant[J]. J Virol,2000,74(23):11286-11295. |
| [22] Yang RG,Kusagawa S, Zhang CY, et al. Identification and characterization of a new class of human immunodeficiency virus type 1 recombinants comprised of two circulating recombinant forms,CRF07_BC and CRF08_BC,in China[J]. J Virol,2003,77(1):685-695. |
| [23] Yu XF,Liu W,Chen J,et al. Rapid dissemination of a novel B/C recombinant HIV-1 among injection drug users in southern China[J]. AIDS,2001,15(4):523-525. |
| [24] Ning CY,He X,Feng Y,et al. Epidemiological features and research progress of HIV-1 genotypes distribution in China[J]. Chin J Prev Med,2013,47(11):1060-1062. (in Chinese) 宁传艺,何翔,冯毅,等. 中国HIV-1主要基因型分布和流行特征研究进展[J]. 中华预防医学杂志,2013,47(11):1060-1062. |
| [25] Xin RL,He X,Xing H, et al. Genetic and temporal dynamics of human immunodeficiency virus type 1 CRF07_BC in Xinjiang,China[J]. J Gen Virol,2009,90(Pt 7):1757-1761. |
| [26] Liu J,Zhang CY. Phylogeographic analyses reveal a crucial role of Xinjiang in HIV-1 CRF07_BC and HCV 3a transmissions in Asia[J]. PLoS One,2011,6(8):e23347. |
| [27] Tee KK,Pybus OG,Li XJ, et al. Temporal and spatial dynamics of human immunodeficiency virus type 1 circulating recombinant forms 08_BC and 07_BC in Asia[J]. J Virol,2008,82(18):9206-9215. |
| [28] Han XX,An MH,Zhang WQ,et al. Genome sequences of a novel HIV-1 circulating recombinant form,CRF55_01B,identified in China[J]. Genome Announc,2013,1(1):e00050-12. |
| [29] Zhao J,Cai WD,Zheng CL,et al. Origin and outbreak of HIV-1 CRF55_01B among MSM in Shenzhen,China[J]. J Acquir Immune Defic Syndr,2014,66(3):e65-67. |
| [30] Zhang WQ, Han XX, An MH, et al. Identification and characterization of a novel HIV-1 circulating recombinant form (CRF59_01B) identified among men-who-have-sex-with-men in China[J]. PLoS One,2014,9(6):e99693. |
| [31] Han XX, An MH, Zhang WQ,et al. Genome sequences of a novel HIV-1 circulating recombinant form (CRF59_01B) identified among men who have sex with men in northeastern China[J]. Genome Announc,2013,1(3):e00315-13. |
| [32] Li XG,Ning CY,He X,et al. Genome sequences of a novel HIV-1 circulating recombinant form (CRF61_BC) Identified among Heterosexuals in China[J].Genome Announc,2013,1(3):e00326-13. |
| [33] Wei HM,Liu YJ,Feng Y,et al. Genome sequence of a novel HIV-1 circulating recombinant form (CRF57_BC) identified from Yunnan,China[J]. AIDS Res Hum Retroviruses,2014,30(4):384-388. |
| [34] Wei HM,His J,Feng Y,et al. Identification of a novel HIV-1 circulating recombinant form (CRF62_BC) in western Yunnan of China[J]. AIDS Res Hum Retroviruses,2014,30(4):380-383. |
| [35] Hsi J,Wei HM,Xing H,et al. Genome sequence of a novel HIV-1 circulating recombinant form (CRF64_BC) identified from Yunnan,China[J]. AIDS Res Hum Retroviruses,2014,30(4):389-393. |
| [36] Feng Y,Wei HM,Hsi J,et al. Identification of a novel HIV type 1 circulating recombinant form (CRF65_cpx) composed of CRF01_AE and subtypes B and C in Western Yunnan,China[J]. AIDS Res Hum Retroviruses,2014,30(6):598-602. |
| [37] Zeng HY,Sun ZW, Liang SJ, et al. Emergence of a new HIV type 1 CRF01_AE variant in Guangxi,Southern China[J]. AIDS Res Hum Retroviruses,2012,28(10):1352-1356. |
| [38] Tan JX, Kang XJ, Zhang W, et al. Full-length clone and characterization of a human immunodeficiency virus type 1 subtype B' isolated from Hubei province,China[J]. Chin Med J (Engl),2007,120(9):831-833. |
| [39] Feng Y,He X,Hsi JH, et al. The rapidly expanding CRF01_AE epidemic in China is driven by multiple lineages of HIV-1 viruses introduced in the 1990s[J]. AIDS,2013,27(11):1793-1802. |
| [40] An MH, Han XX, Xu JJ, et al. Reconstituting the epidemic history of HIV strain CRF01_AE among men who have sex with men (MSM) in Liaoning,northeastern China:implications for the expanding epidemic among MSM in China[J]. J Virol,2012,86(22):12402-12406. |
| [41] Han XX,An MH,Zhang M,et al. Identification of 3 distinct HIV-1 founding strains responsible for expanding epidemic among men who have sex with men in 9 Chinese cities[J]. J Acquir Immune Defic Syndr,2013,64(1):16-24. |
| [42] Liao LJ,Xing H,Su B,et al. Impact of HIV drug resistance on virologic and immunologic failure and mortality in a cohort of patients on antiretroviral therapy in China[J]. AIDS,2013,27(11):1815-1824. |
| [43] Liao LJ, Xing H, Dong YH, et al. Surveys of transmitted HIV drug resistance in 7 geographic Regions in China,2008-2009[J]. Clin Infect Dis,2012,54 Suppl 4:S320-S323. |
| [44] Xing H,Wang X,Liao LJ,et al. Incidence and associated factors of HIV drug resistance in Chinese HIV-infected patients receiving antiretroviral treatment[J]. PLoS One,2013,8(4):e62408. |
| [45] Xing H,Ruan YH,Li J,et al. HIV drug resistance and its impact on antiretroviral therapy in Chinese HIV-infected patients[J]. PLoS One,2013,8(2):e54917. |
| [46] Wang J, He C, Hsi JH, et al. Virological outcomes and drug resistance in Chinese patients after 12 months of 3TC-based first-line antiretroviral treatment,2011-2012[J]. PLoS One,2014,9(2):e88305. |
| [47] Zhao B,Han XX,Xu JJ,et al. Increase of RT-related transmitted drug resistance in non-CRF01_AE among HIV type 1-infected men who have sex with men in the 7 cities of China[J]. J Acquir Immune Defic Syndr,2015,68(3):250-255. |
| [48] Li L,Sun GQ,Liang SJ,et al. Different distribution of HIV-1 subtype and drug resistance were found among treatment naive individuals in Henan,Guangxi,and Yunnan province of China[J]. PLoS One,2013,8(10):e75777. |
| [49] Liu HX,Ma Y,Su YY,et al. Emerging trends of HIV drug resistance in Chinese HIV-infected patients receiving first-line highly active antiretroviral therapy:a systematic review and meta-analysis[J]. Clin Infect Dis,2014,59(10):1495-1502. |
| [50] Su YY,Zhang FJ,Liu HX,et al. The prevalence of HIV-1 drug resistance among antiretroviral treatment naive individuals in mainland China:a meta-analysis[J]. PLoS One,2014,9(10):e110652. |
| [51] Rhee SY,Blanco JL,Jordan MR,et al. Geographic and temporal trends in the molecular epidemiology and genetic mechanisms of transmitted HIV-1 drug resistance:an individual-patient- and sequence-level meta-analysis[J]. PLoS Med,2015,12(4):e1001810. |
| [52] Langford SE,Ananworanich J,Cooper DA. Predictors of disease progression in HIV infection:a review[J]. AIDS Res Ther,2007,4:11. |
| [53] Zhang FJ,Dou ZH,Yu L,et al. An ambispective cohort studv of the naturaI history of HlV infection among former unsafe commercial blood and plasma donors[J]. Chin J Epidemiol,2008,29(1):9-12. (in Chinese) 张福杰,豆智慧,于兰,等. 中国既往不安全有偿供血感染HIV者自然史双向性队列研究[J]. 中华流行病学杂志,2008,29(1):9-12. |
| [54] Li DM,Wang L,Gao X,et al. Study on the natural history of HIV among former commercial plasma donors caused by contaminated plasma donation in central China[J]. Chin J Epidemiol,2010,31(6):633-637. (in Chinese) 李东民,王璐,高省,等. 中国中部地区经不安全采供血感染艾滋病毒的自然病程研究[J]. 中华流行病学杂志,2010,31(6):633-637. |
| [55] Liu HX, Wang L,Qin QQ,et al. Impact of delayed diagnoses bias on the estimation of AIDS incubation[J]. Chin J Epidemiol,2011,32(9):892-895. (in Chinese) 刘慧鑫,王璐,秦倩倩,等. 滞后诊断偏倚对判断艾滋病潜伏期的影响[J]. 中华流行病学杂志,2011,32(9):892-895. |
| [56] Li X, Xue Y,Zhou L,et al. Evidence that HIV-1 CRF01_AE is associated with low CD4+T cell count and CXCR4 co-receptor usage in recently infected young men who have sex with men (MSM) in Shanghai,China[J]. PLoS One,2014,9(2):e89462. |
| [57] Li YJ,Han Y,Xie J,et al. CRF01_AE subtype is associated with X4 tropism and fast HIV progression in Chinese patients infected through sexual transmission[J]. AIDS,2014,28(4):521-530. |
| [58] Shen S,Jiang Y. Advances on the assays for newly infected HIV cases[J]. Chin J Epidemiol,2010,31(4):462-465. (in Chinese) 沈圣,蒋岩. HIV 新近感染检测方法研究进展[J]. 中华流行病学杂志,2010,31(4):462-465. |
| [59] Parekh BS,Kennedy MS,Dobbs T,et al. Quantitative detection of increasing HIV type 1 antibodies after seroconversion:a simple assay for detecting recent HIV infection and estimating incidence[J]. AIDS Res Hum Retroviruses,2002,18(4):295-307. |
| [60] Hu DJ, Vanichseni S, Mock PA, et al. HIV type 1 incidence estimates by detection of recent infection from a cross-sectional sampling of injection drug users in Bangkok:use of the IgG capture BED enzyme immunoassay[J]. AIDS Res Hum Retroviruses,2003,19(9):727-730. |
| [61] Nesheim S,Parekh B,Sullivan K,et al. Temporal trends in HIV type 1 incidence among inner-city childbearing women in Atlanta:use of the IgG-capture BED-enzyme immunoassay[J]. AIDS Res Hum Retroviruses,2005,21(6):537-544. |
| [62] Jiang Y,Wang M,Ni M, et al. HIV-1 incidence estimates using IgG-capture BED-enzyme immunoassay from surveillance sites of injection drug users in three cities of China[J]. AIDS,2007,21 Suppl 8:S47-51. |
| [63] Li SW,Zhang XY,Li XX,et al. Detection of recent HIV-1 infections among men who have sex with men in Beijing during 2005-2006[J]. Chin Med J (Engl),2008,121(12):1105-1108. |
| [64] Li XF,Lu HY,Cox C,et al. Changing the landscape of the HIV epidemic among MSM in China:results from three consecutive respondent-driven sampling surveys from 2009 to 2011[J]. Biomed Res Int,2014,2014:563517. |
| [65] Yang L, Yang CJ, Chen HC, et al. HIV incidence in MSM in Yunnan,2008-2011[J]. Mod Prev Med,2015,42(1):137-139,156. (in Chinese) 杨莉,杨朝军,陈会超,等.2008-2011年云南省男男性行为人群HIV新发感染率调查[J] . 现代预防医学,2015,42(1):137-139,156. |
| [66] Yang CJ,Ma YL,Chen HC,et al. Application of BED for HIV-1 incidence research in female sex workers (FSW) in Yunnan province[J]. Chin J Prev Med,2015,49(1):70-71. (in Chinese) 杨朝军,马艳玲,陈会超,等. 应用BED方法对云南省暗娼人群进行HIV-1新发感染率研究[J].中华预防医学杂志,2015,49(1):70-71. |
| [67] Duan S,Shen S,Bulterys M, et al. Estimation of HIV-1 incidence among five focal populations in Dehong,Yunnan:a hard hit area along a major drug trafficking route[J]. BMC Public Health,2010,10:180. |
| [68] Xu J,Smith MK,Ding G,et al. Drug use and sex work:competing risk factors for newly acquired HIV in Yunnan,China[J]. PLoS One,2013,8(3):e59050. |
| [69] Myers G, Korber B, Smith RF, et al. Human retroviruses and AIDS[M]. Los Alamos,New Mexico:Los Alamos National Laboratory,1993. |
| [70] Janssens W, Heyndrickx L, Fransen K, et al. Genetic and phylogenetic analysis of env subtypes G and H in central Africa[J]. AIDS Res Hum Retroviruses,1994,10(7):877-879. |
| [71] Keele BF,Giorgi EE, Salazar-Gonzalez JF, et al. Identification and characterization of transmitted and early founder virus envelopes in primary HIV-1 infection[J]. Proc Natl Acad Sci USA,2008,105(21):7552-7557. |
| [72] Giorgi EE,Funkhouser B,Athreya G,et al. Estimating time since infection in early homogeneous HIV-1 samples using a poisson model[J]. BMC Bioinformatics,2010,11:532. |
| [73] Buzon MJ, Sun H,Li C,et al. HIV-1 persistence in CD4+T cells with stem cell-like properties[J]. Nat Med,2014,20(2):139- 142. |
| [74] Tang H,Mao Y,Shi CX,et al. Baseline CD4 cell counts of newly diagnosed HIV cases in China:2006-2012[J]. PLoS One,2014,9(6):e96098. |
| [75] Little SJ,Kosakovsky Pond SL,Anderson CM,et al. Using HIV networks to inform real time prevention interventions[J]. PLoS One,2014,9(6):e98443. |
 2015, Vol. 36
2015, Vol. 36


