文章信息
- 汪永禄, 李凤娟, 王多春, 张萍, 陶勇, 王利, 王艳. 2014.
- Wang Yonglu, Li Fengjuan, Wang Duochun, Zhang Ping, Tao Yong, Wang Li, Wang Yan. 2014.
- 马鞍山地区耐甲氧西林金黄色葡萄球菌的分子特征研究
- Study of molecular characteristics of methicillin-resistant Staphylococcus aureus in Maanshan area
- 中华流行病学杂志, 2015, 36(3): 285-289
- Chinese Journal of Epidemiology, 2015, 36(3): 285-289
- http://dx.doi.org/10.3760/cma.j.issn.0254-6450.2015.03.020
-
文章历史
- 投稿日期:2014-9-10
2. 中国疾病预防控制中心传染病预防控制所;
3. 河南省疾病预防控制中心;
4. 北京市通州区疾病预防控制中心
2. National Institute for Communicable Diseases Control and Prevention, Chinese CDC
3. CDC of Henan Province;
4. CDC of Tongzhou District, Beijing
金黄色葡萄球菌(金葡菌)能够产生溶血毒素、肠毒素、杀白细胞素等多种毒力因子,引起一系列感染性疾病[1]。近年来,由于耐甲氧西林金葡菌(methicillin-resistant Staphylococcus aureus,MRSA)的大量出现,使疾病治疗变得更加困难和棘手[2]。MRSA作为医院感染的重要病原菌,得到越来越多的关注。由于抗生素滥用,我国已经成MRSA高度流行的国家。由于MRSA起源、进化和流行具有区域特点,有必要对患者来源和食品来源菌株进行分子生物学研究。本研究对2008-2012年马鞍山地区分离的210株金葡菌的肠毒素和溶血素基因进行检测,并对34株MRSA及3株甲氧西林敏感金葡菌(MSSA)进行多位点序列分型(MLST)分析,探讨菌株间遗传进化关系。 材料与方法
1. 实验菌株:共210株,其中食品来源菌株127株,分别为2010年40株、2011年57株、2012年30株;患者来源菌株83株,分别为2008年55株、2011年20株、2012年8株。所有菌株均为革兰阳性菌、过氧化氢酶和血浆凝固酶阳性,经细菌自动仪鉴定为金葡菌;同时对每株菌株耐热核酸酶基因进行PCR检测以进一步确定。
2. 肠毒素检测:使用法国梅里埃公司生产的miniVIDAS全自动荧光免疫分析仪及肠毒素检测试剂盒检测肠毒素基因。菌株经肉汤培养过夜后,离心,取上清液上机。操作按仪器手册进行。同时设置阳性和阴性对照。
3. 溶血素基因与MLST基因的检测:根据在NCBI上查的序列,利用Primer 5.0软件,设计溶血素基因nuc、hla、hlb以及MLST的引物序列,PCR引物由生工生物工程(上海)股份有限公司合成,见表 1。
溶血素基因PCR条件:94 ℃预变性5 min;94 ℃ 40 s,49 ℃ 40 s(hla基因)或54 ℃ 40 s(hlb基因),72℃ 1 min,30个循环;72 ℃ 10 min。MLST分析的PCR条件:94 ℃预变性5 min;94 ℃ 30 s,53 ℃ 30 s,72 ℃ 60 s,30个循环,72 ℃ 10 min。PCR产物进行琼脂凝胶电泳后成像。
4. MLST分析:通过PCR扩增金葡菌arcc、aroe、glpf、gmk、pta、tpi、yqil七个管家基因,将扩增产物直接送公司纯化和双向测序。测序结果用Vector NTI suite 6软件进行分析和校对后,将7个管家基因序列进行网上数据库比对,得到每个菌株的等位基因号。将已有的7个基因序列作为参照,使用DNAStar的MegAlign软件对序列进行分析,并将整理好的序列上传至MLST数据库网站(http://saureus.mlst.net),得到每个等位基因相对应的序号并获得序列型(ST),根据eBURST对ST进行亲缘性分析。
5. 甲氧西林抗性检测和药敏试验:甲氧西林抗性检测采用纸片扩散法,依据美国临床实验室标准化协会(CLSI)的标准[3],利用苯唑青霉素平板筛选试验进行检测,在平板上有单菌落生长,则判定为苯唑青霉素或甲氧西林抗性阳性。每个菌株重复测定3次,以金葡菌ATCC29213作为质控菌株。药敏试验按CLSI标准,采用琼脂稀释法,制备含相应抗生素系列稀释梯度的MH琼脂平板。抗生素包括青霉素、苯唑西林、庆大霉素、红霉素、去甲万古霉素、四环素、氯霉素、利福平、环丙沙星、氯林可霉素、呋喃妥因。结果判断以抑制细菌生长的最低药物浓度为MIC。 结果
1. 甲氧西林抗性检测:采用纸片扩散法对210株菌株进行检测,51株为MRSA(24.3%),包含食品来源25株(19.7%,25/127)及患者来源26株(31.3%,26/83)。
2. 肠毒素检测:210株金葡菌中107株为肠毒素阳性(50.9%)。不同年份菌株的肠毒素阳性率分别为2008年54.6%(30/55),2009年42.5%(17/40),2011年57.1%(44/77)和2012年42.1%(16/38),不同年份之间肠毒素阳性率差异无统计学意义(P=0.284)。51株MRSA中有46株肠毒素阳性(90.2%),其中25株食品来源MRSA有22株阳性(88.0%);26株患者来源MRSA中24株阳性(92.3%),差异无统计学意义(P=0.963)。
3. 溶血素基因分布:
(1)nuc:210株菌株经PCR扩增均检测到nuc基因,阳性率为100%。
(2)hla、hlb:根据PCR检测结果,210株菌中198株含有hla、hlb中的1~2种基因(94.3%),其中hla、hlb同时检出率为31.4%,hla基因检出率为32.4%,hlb基因检出率为30.5%(表 2)。统计学分析显示,食品来源和患者来源菌株各基因阳性率差异无统计学意义(χ2=2.807,P=0.422)。食品来源的127株菌株中检出溶血素基因120株,检出率为94.5%;83株患者来源菌株中78株检出溶血素基因,检出率为94.0%,见表 3。51株MRSA检出hla、hlb中的1~2种基因,检出率为100%。
4. MLST:选取34株MRSA和3株MSSA进行MLST分析,得到14个等位基因,11个ST,以ST239为主(43.2%),ST5次之(16.2%),其他型别为散发状态,分别是ST7(5-4-1-4-4-6-3)为10.8%,ST188(3-1-1-8-1-1-1)为8.1%,ST88(22-1-14-23-12- 4-31)为8.1%,其余型别(ST1、97、243、585、630和1281)均为2.7%,见图 1。
 |
| 图 1 马鞍山地区37株MRSA MLST聚类 |
菌株的ST比较分散,主要以ST239为主,占47.1%(16/34),其次为ST5,占17.6%(6/34),这两个主要型别的菌株均为MRSA。在ST188、ST1281和ST7三种ST的菌株中各有1株是耐甲氧西林凝固酶阴性的菌株(MRCNS),其余34株菌为MRSA,见图 2。
 |
| 图 2 马鞍山地区MRSA和MSSA的MLST |
17株患者来源菌株有6个ST,以ST239为主要型别(35.3%,6/17),其次为ST5(29.4%,5/17);20株食品来源菌株有9个型别,以ST239为主(45.0%,9/20),其次为ST7(15.0%,3/20)。在几个主要的ST中菌株来源既包括患者来源也包括食品来源,见图 3。
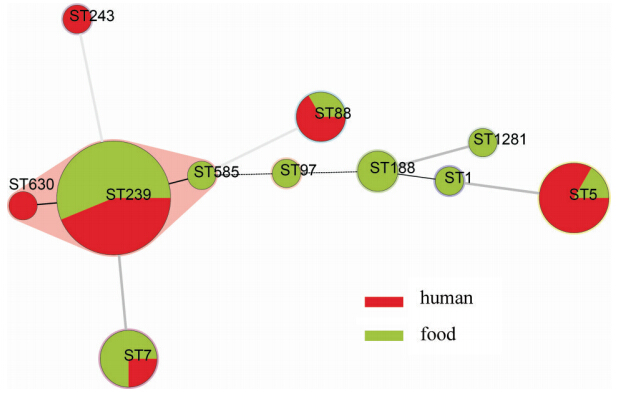 |
| 图 3 马鞍山地区不同来源金葡菌的MLST |
eBURST软件分析显示(图 4),ST585、ST239以及ST630亲缘关系较近,其余ST之间亲缘关系较远。
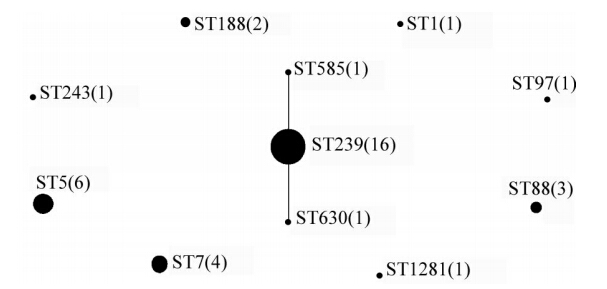 |
| 图 4 马鞍山地区37株MRSA的eBURST分析 |
5. 药敏试验:食品和患者来源的菌株对青霉素、苯唑西林、氨苄西林、庆大霉素和红霉素的耐药率最高,均高于90.0%,耐药率较高的为四环素、环丙沙星、氯林可霉素和利福平,均高于50.0%,所有菌株对氯霉素、呋喃妥因和去甲万古霉素有较低的耐药率。食品和患者来源菌株耐药率差异无统计学意义,见表 3。 讨论
金葡菌为人类重要的致病菌之一,能够产生溶血毒素、肠毒素、杀白细胞素等多种毒力因子,可引起人皮肤软组织感染、肺炎和中毒性休克综合征等一系列感染性疾病,严重危害着人类的健康[4]。本研究对210株金葡菌溶血素基因检测,阳性率达94.3%,说明溶血素在该菌中普遍存在。对51株MRSA进行溶血素检测,发现均携带hla或hlb基因。因本研究菌株数较少,MRSA耐药是否与携带溶血素基因有关,有待进一步研究证实。
近年来,随着抗生素滥用,动物源性MRSA菌株在全世界范围内已有报道[5]。本研究中20株食品来源菌株分离自马鞍山地区的禽畜类和水产品,17株则分离自住院患者。根据37株菌株的MLST结果可以看出,在这些菌株中,共有11个ST,以ST239为主要型别,ST5次之。根据20株食品来源菌株的MLST进行分析,有9个型别,以ST239为主要型,ST7次之;金葡菌是社区获得性感染和医院内感染的主要致病菌之一,因此国内外的报道多以分离自患者的菌株为多见,而对于分离自食品的菌株较少。本次食品来源菌株以ST239为主要型别。由于金葡菌也是食源性致病菌,有必要对我国食品中MRSA的流行情况进行MLST分析,以建立统一的分子数据库。此外,17株患者来源菌株则分布为6个型别,也以ST239为主要型,ST5次之。根据我国相关医院内MRSA的流行病学调查发现,ST5和ST239型是我国医院感染中最为常见[6]。其中ST239-MRSA 在阿根廷[7]、印度[8]和中国香港[9]等地也报道ST239为主要克隆群。而ST5这一克隆在日本[10]和韩国[11]也是其优势菌群,这些报道都与本研究结果一致。
从结果中可以看出,11种ST亲缘关系较远,提示不同来源的37株菌存在克隆多样性,34株MRSA共分为10个ST,以ST239和ST5为优势型别;而3株MSSA分别为ST188、ST1281和ST7,提示ST239和ST5可以作为MRSA鉴定的候选型别。
药敏试验结果显示,51株MRSA对青霉素、苯唑西林、氨苄西林的耐药率均高于95%,对庆大霉素、红霉素、四环素的耐药率高于90%,仅对去甲万古霉素、呋喃妥因有较好的敏感性,提示MRSA呈多重耐药的情况较为严重。目前,由于抗生素在临床治疗中长期大量使用,致使MRSA已经成为医院内及社区获得性感染的主要致病菌,其来源普遍,检出频繁,致病力和耐药性也越来越强。同时,食源性动物中MRSA的产生也与抗菌药物在养殖场的广泛应用密切相关,长期低剂量的抗菌药物添加到饮水或饲料中,可能是导致细菌产生耐药性的主要原因之一[12]。因此,临床上应进一步控制和对症使用抗生素治疗MRSA引起的疾病,在养殖业中,应合理规范动物饲料抗生素添加剂的使用,加强抗生素的管理及耐药性的监测,以防止多耐药菌株的产生。
| [1] Lowy FD. Staphylococcus aureus infections[J]. N Engl J Med,1998,339(8):520-532. |
| [2] Su GG,Yu YS,Lin J,et al. Homology analysis of 19 strains of methicillinresistant Staphylococcus aureus[J]. Chin J Epidemiol,2004,25(12):1084-1085. (in Chinese) 苏关关,俞云松,林洁,等. 19株甲氧西林耐药金黄色葡萄球菌的同源性分析[J]. 中华流行病学杂志,2004,25(12):1084- 1085. |
| [3] Klevens RM,Morrison MA,Nadle J,et al.Invasive methicillin- resistant Staphylococcus aureus infections in the United States[J]. JAMA,2007,298(15):1763-1771. |
| [4] Han XL,Liu LS, Li Y, et al. Detection and analysis of food poisoning with Staphylococcus aureus enterotoxin A,C[J]. Chin J Epidemiol,2004,25(6):547. (in Chinese) 韩秀兰,柳连顺,李云,等. 一起金黄色葡萄球菌A、C肠毒素引起食品中毒的检测分析[J]. 中华流行病学杂志,2004,25(6): 547. |
| [5] Wang XM,Yao JN,Li BB,et al. Antimicrobial susceptibility and SCCmec typing of methicillin-resistant Staphylococcus aureus isolates from swine[J]. Chin J Zoonoses,2013,29(9):841-845. (in Chinese) 王雪敏,姚建楠,李蓓蓓,等. 猪源耐甲氧西林金黄色葡萄球菌的耐药表型及其SCCmec基因分型研究[J]. 中国人兽共患病学报,2013,29(9):841-845. |
| [6] Zhang W, Shen X,Zhang H,et al. Molecular epidemiological analysis of methicillin-resiseant Staphylococcus aureus isolates from Chinese pediatric patients[J]. Clin Microbiol Infect Dis,2009,12(10):57-69. |
| [7] Sola C, Cortes P, Saka HA, et al. Evolution and molecular characterzation of methicillin-resistant Staphylococcus aureus epidemic and sporadic clones in Coedoba,Argentina[J]. J Clin Microbiol,2006,44(1):192-200. |
| [8] Chongtrakool P, Ito T, Ma XX, et al. Staphylococcal Cassette Chromosome mec(SCCmec) typing of methicillin-resistant Staphylococcus aureus strains isolated in 11 Asia countries:a proposal for a new nomenclature for SCCmec elements[J]. Antimicrob Agents Chemother,2006,50(3):1001-1012. |
| [9] Ip M,Yung RW,Ng TK,et al. Contenporary methicillin-resistant Staphylococcus aureus clone in Hong Kong[J]. J Clin Microbiol,2005,43(10):5069-5073. |
| [10] Zaraket H,Otsuka T,Saito K,et al. Molecular characterization of methicillin-resistant Staphylococcus aureus in hospitals in Niigata,Japan:divergence and transmission[J]. Microbiol Immunol,2007,51(2):171-176. |
| [11] Ko KS,Kim YS,Song JH,et al. Genotypic diversity of methicillin- resistant Staphylococcus aureus isolates in Korean Hospitals[J]. Antimicrob Agents Chemother,2005,49(8):3583-3585. |
| [12] Dai FW,Ke XF,Zhou SS,et al. The epidemiology of methicillin- resistant Staphylococcus aureus(MRSA) in animals[J]. Chin J Compar Med,2010,20(7):81-85. (in Chinese) 戴方伟,柯贤福,周莎桑,等. 耐甲氧西林金黄色葡萄球菌在动物流行病学中的研究进展[J]. 中国比较医学杂志,2010,20(7):81-85. |
 2015, Vol. 36
2015, Vol. 36





