超临界CO2(scCO2)微乳液是热力学稳定光学透明的系统,由极性内核、CO2连续相以及聚集在水核周围的表面活性剂分子组成[1]。因为超临界CO2微乳液可以溶解极性分子或离子,并且具有特殊的内部结构,因此在萃取、反应及纳米材料制备领域均有广泛应用[2-8]。相行为实验和大型仪器测试是研究scCO2微乳液的常用方法,近些年,分子动力学(molecular dynamics, MD)模拟技术的发展,为研究scCO2微乳液的微观性质提供了新途径[9-11]。然而,大量关于scCO2微乳液的研究都是基于含氟表面活性剂[12-15],对不含氟碳氢表面活性剂[16]的报道较少。相比于含氟表面活性剂,碳氢表面活性剂成本低、低毒性,因此有助于scCO2微乳液技术的发展[17]。另外,scCO2微乳液应用的拓展和深化,需要深入研究其内部的微观结构信息及影响因素。文中通过实验测试了基于不含氟碳氢表面活性剂LS-45微乳液的临界微乳液浓度(critical microemulsion concentration, CMC),以及体系对水的溶解能力。同时,使用MD模拟在分子级别上研究了scCO2微乳液的形成过程和微观结构。另外,考察了表面活性剂浓度对微乳液聚团聚集过程的影响。
1 实验原料及研究方法 1.1 实验原料LS-45表面活性剂(纯度99.5%),上海尤文化工有限公司;CO2(纯度99%),大连光明气体公司;二次蒸馏水为实验室自制。LS-45分子结构如图 1所示。
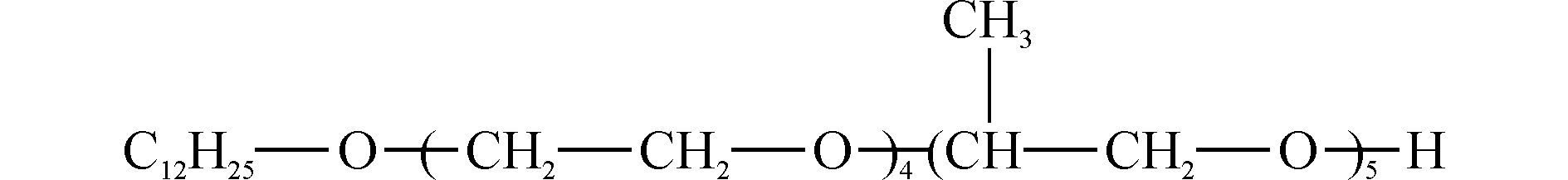
|
图 1 LS-45分子结构示意 |
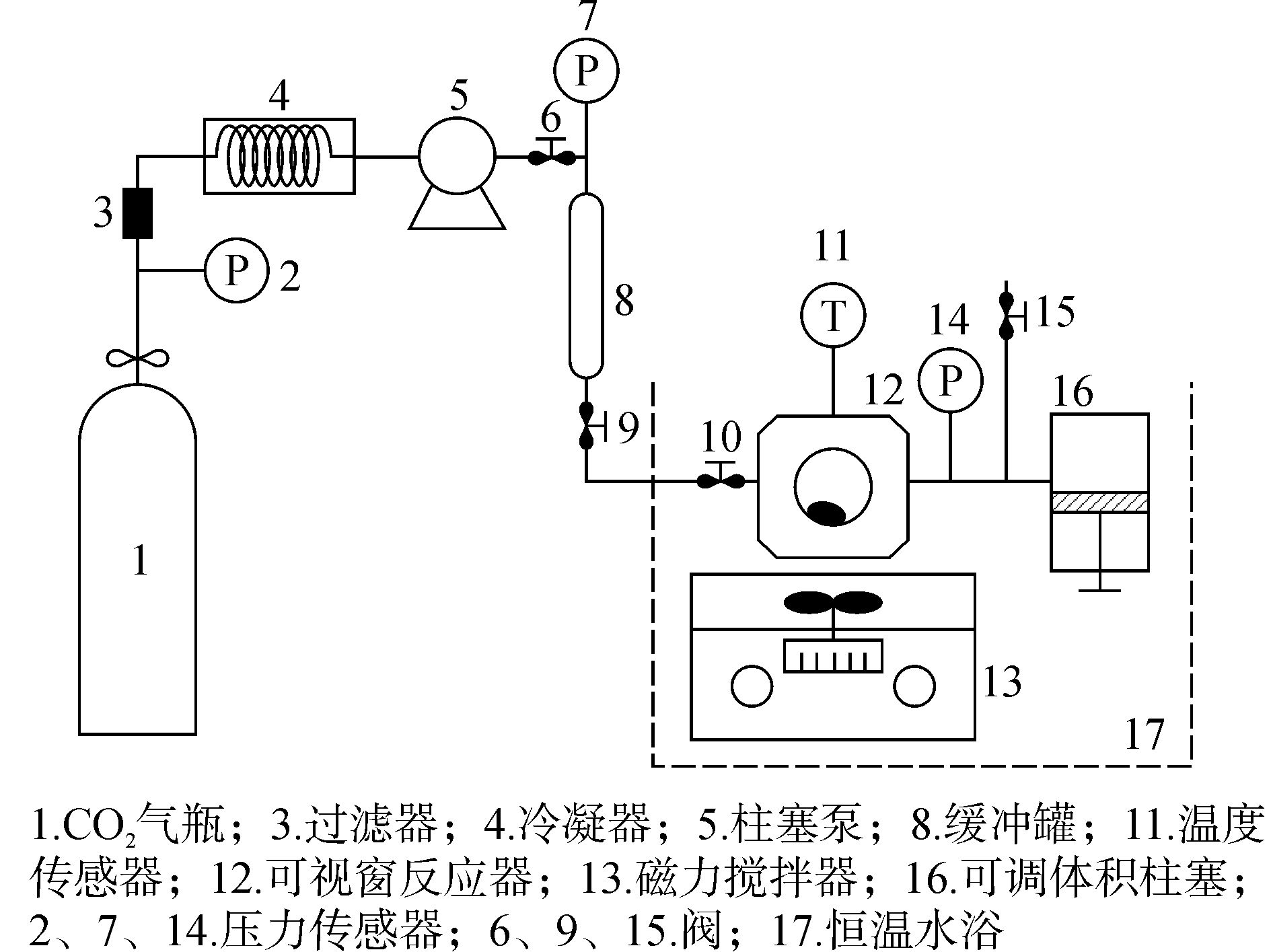
相行为实验流程如图 2所示。实验装置主要包括体积为30.16 mL带可视窗的高压反应器、体积可调活塞(调节范围0~1.5 mL)、恒温水浴锅、高效液相色谱(high performance liquid chromatography, HPLC)泵以及CO2储罐。系统压力通过压力传感器(DG1300-BZ-A-2-40) 测试,精度为±0.01 MPa。温度由K型热电偶进行测量,精度为±0.1 ℃。实验时,用微量注射器将表面活性剂和水注入反应器,连接装置并将柱塞调零。微调阀9、10用CO2置换系统的空气后关闭阀15。打开恒温水浴锅对系统加热,待系统温度升至设定值后打开HPLC泵进行加压,直到观察到体系澄清透明时,停止打压。缓慢调节活塞,当体系出现浑浊时,停止调节并将此时的压力和温度记录,该压力称为浊点压力。每组实验重复3次,取平均值。
|
图 2 高压流体相行为实验流程 |
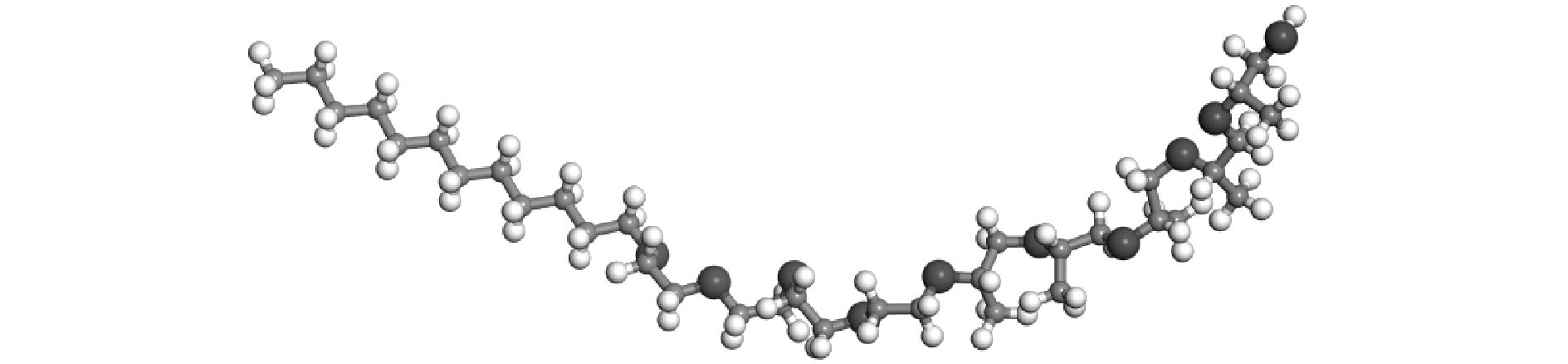
首先在MS-STUDIO软件中将CO2、水以及表面活性剂等分子进行建模,然后将分子模型导入GROMACS 4.6.2程序进行计算。所有计算均采用NPT系综,使用Sarkar恒温器[18]控制体系温度,Berendsen恒压器[19]控制体系压力。温度调节器的弛豫时间设置为0.5 ps,压力控制器的弛豫时间设置为1 ps,压缩系数设置为4.5×10-5 bar-1。将全部分子放置在一个立方体盒子中,并将盒子各方向上设置成周期边界。为了消除初始条件对运算结果的影响,进一步提高计算准确性,所有分子均随机放置于盒子中,各原子间没有约束。MD运动方程选用Gromacs中SD算法求解,并设定初始步长1 fs。通过颗粒化网格Ewald方法[20]来计算静电相互作用力,设置Lennard-Jones(LJ)交互作用截断距离为1.2 nm。线性约束求解算法求解时,限制了氢与重原子之间的键长。表面活性剂分子LS-45选用CHARMM通用力场(CGenFF) [21]参数编译。二氧化碳分子采用EPM2模型[22]进行编译,水分子使用SPC模型[23]进行编译。图 3为LS-45表面活性剂的分子示意图。
|
图 3 LS-45分子示意应 |
临界微乳液浓度表示形成微乳液所需要的最低的表面活性剂浓度,是判断微乳液形成与否的重要参数。表面活性剂溶液体相的一系列性质,如表面张力、渗透压、摩尔电导率、增溶以及去污力等的突变被归结为溶液体相中发生了表面活性剂聚集。从理论上讲,因胶束形成而产生不连续变化的性质均可以被用来测定CMC[24]。本文考察了系统中的浊点压性质的变化来找到体系的突变点,继而得到体系的CMC。
在所考察的LS-45/H2O/CO2三元体系中,水的浓度固定为0.018 4 mol/L,通过测试不同表面活性剂浓度的浊点压,来考察体系性质的突变,结果如图 4所示。随着表面活性剂浓度的增大,体系的浊点压力首先增加到一个极大值点,然后有微小下降,随后再继续增大。因此,浊点压力在一个窄浓度范围里剧烈波动,本文选取波动开始的点——极大值点作为临界点。在临界点两侧,浊点压曲线的斜率有较明显变化,说明系统内部的性质发生了变化,因此可将此点对应的浓度定义为临界微乳液浓度。对于LS-45构成的微乳液体系,CMC为0.002 71 mol/L,并发现在实验条件范围内CMC对温度的变化并不敏感。

|
图 4 LS-45浓度和浊点压关系曲线 |
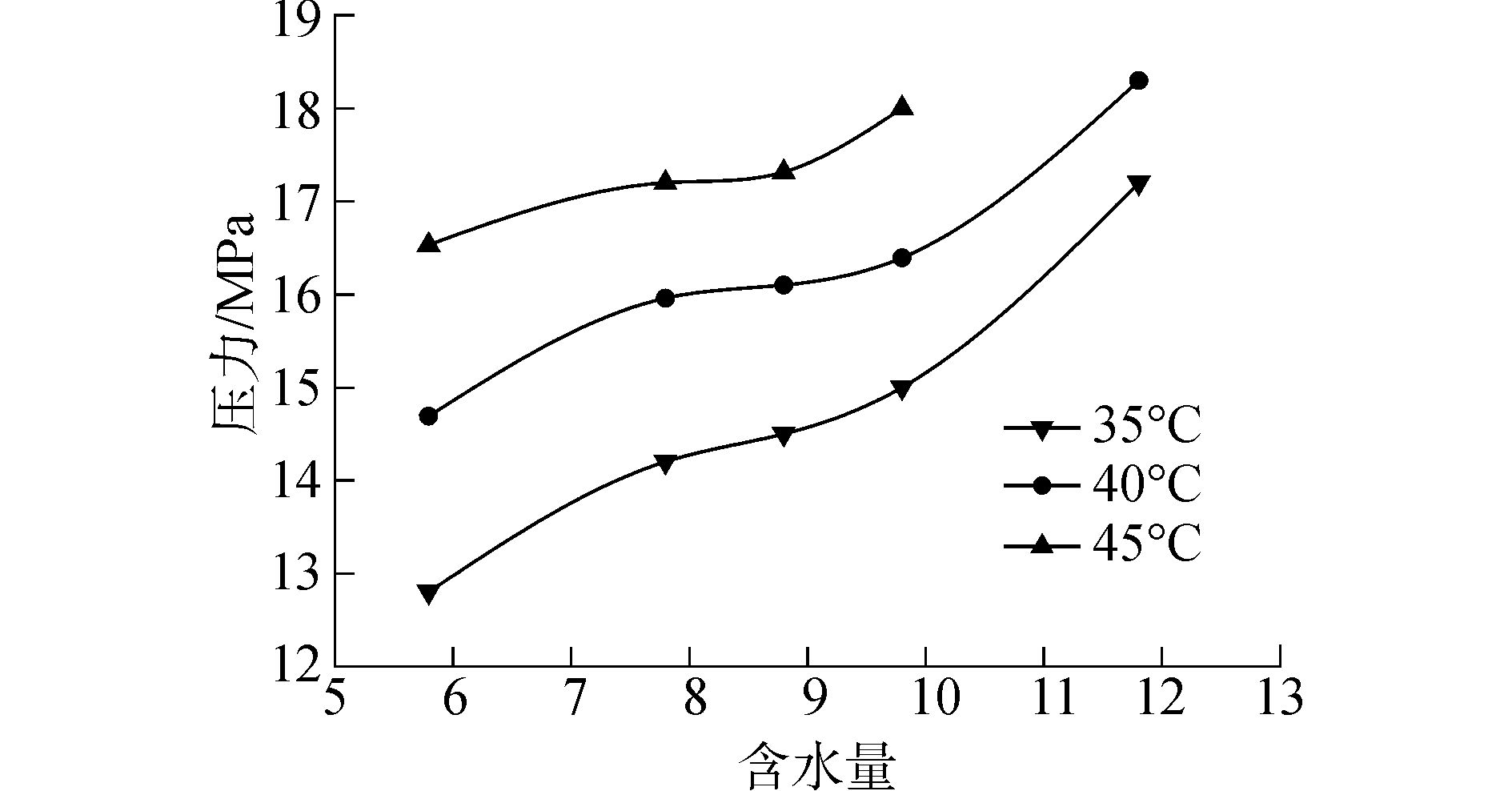
含水量(W0)为体系中水与表面活性剂的摩尔比,是微乳液结构调控的重要参数,通常反映了微乳液聚团尺寸的大小。W0越大,微乳聚团越大,微乳液内核极性越强,从而溶解极性物质的能力也越强。实验选取的表面活性剂浓度0.008 4 mol/L大于CMC,考察了体系浊点压与W0的关系曲线,结果如图 5所示。由图 5可以看出,体系浊点压力随W0的增大而增大。这是因为随着压力的增加,体系中CO2密度随之增加,因此溶剂能力也得到了提升。
|
图 5 LS-45体系含水量和浊点压关系曲线 |
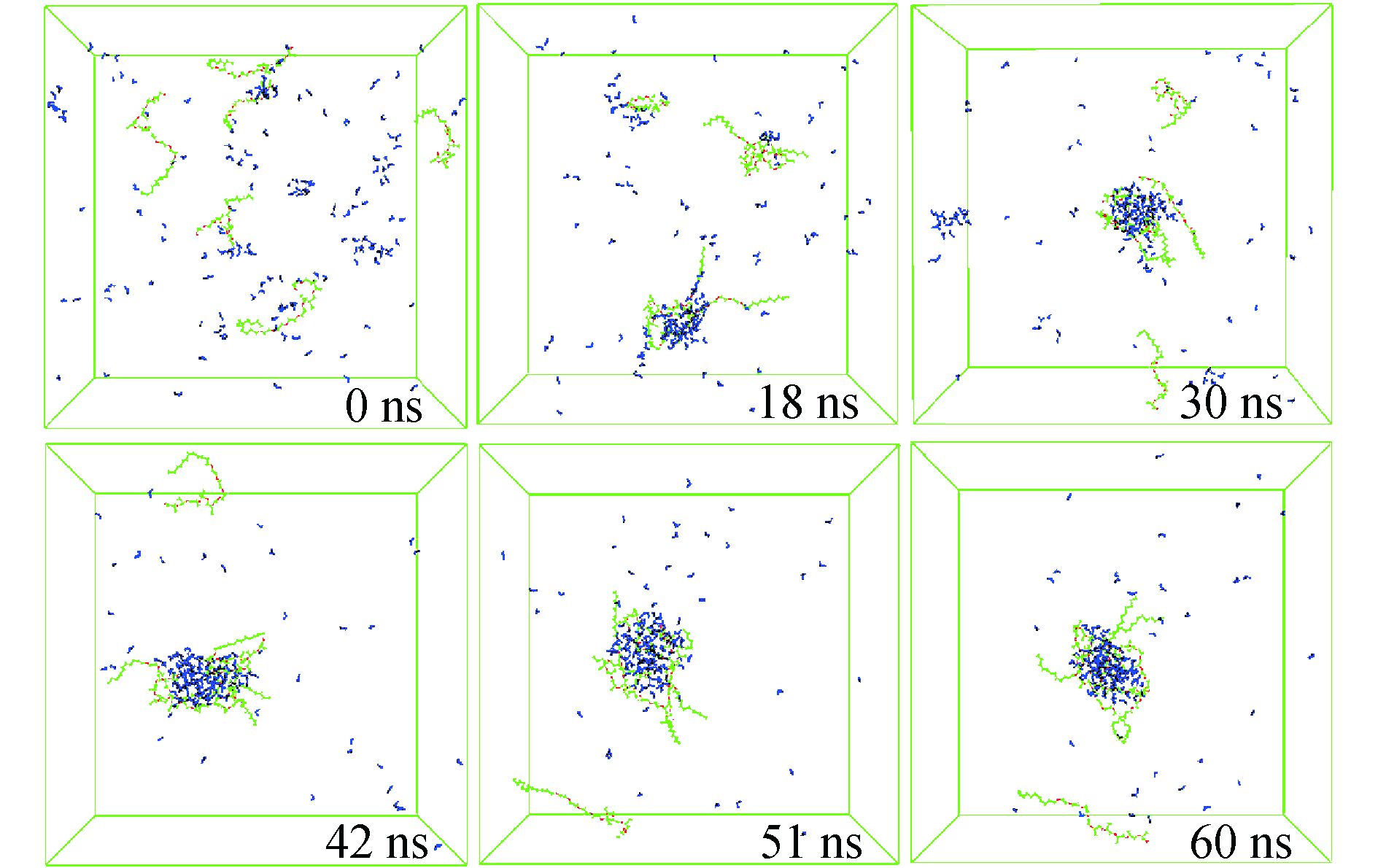
MD模拟可以直观地反映纳米级别微乳液聚团的结构。通过MD模拟可以为微乳液的形成提供较为直观的判据,并可以进一步探究微乳液聚集过程和内部信息。以实验选取的表面活性剂浓度0.008 4 mol/L为基础,考察了6LS-45/160H2O/12 000CO2(数字代表分子个数)三元体系在温度35 ℃、压力23 MPa条件下的聚集过程,结果如图 6所示。其中CO2分子被设置为隐藏,以便于清楚地观测聚团状态。由图 6所示,在0 ns时,表面活性剂和水分子均随机分布在盒子里,代表聚集的初始状态;18 ns时,水分子首先形成初始聚集,并吸引了部分表面活性剂分子;30 ns时,水核尺寸继续增大,并吸引了更多表面活性剂;在42 ns时,水核尺寸进一步增大,并吸引了5个表面活性剂分子;51 ns时和60 ns时,聚团聚集情况基本稳定,微乳液聚团中包含5个表面活性剂分子,另有一个表面活性剂游离于连续相中。
|
图 6 6LS-45/160H2 O/12 000CO2三元体系计算轨迹 |
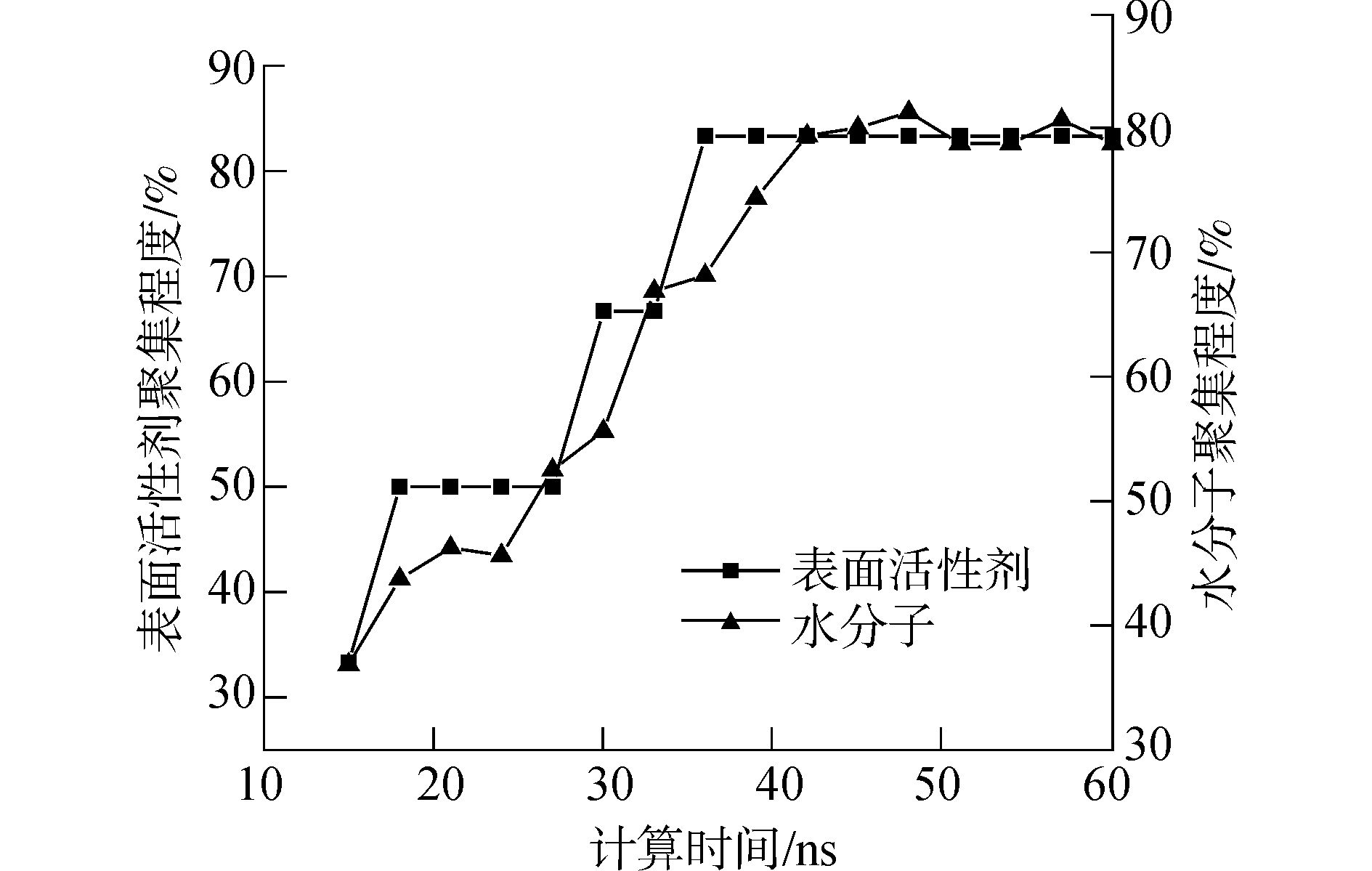
从模拟过程中开始出现表面活性剂聚集为起点,间隔3 ns进行取样,并分析每个取样点状态下聚团结构信息,结果如图 7所示。其中,左侧纵坐标表示微乳液聚团中表面活性剂数量与表面活性剂总数之比。右侧纵坐标表示聚团内水分子数占全部水分子数量的百分比。横坐标为计算时间,单位为ns。由图 7可知,随计算时间的增长,水分子和表面活性剂的聚集程度均随之增加,并在达到一定计算时间后趋于稳定。当聚团稳定后,表面活性剂聚集程度可达83.3%,水分子为80%左右。从图中可以看出水分子与表面活性剂分子的聚集轨迹基本一致,这可能是由于水核与表面活性剂分子极性头基间的氢键作用使两者紧密结合,同步增长。
|
图 7 6LS-45+160H2O+12 000CO2体系中聚团聚集信息随计算时间变化规律 |
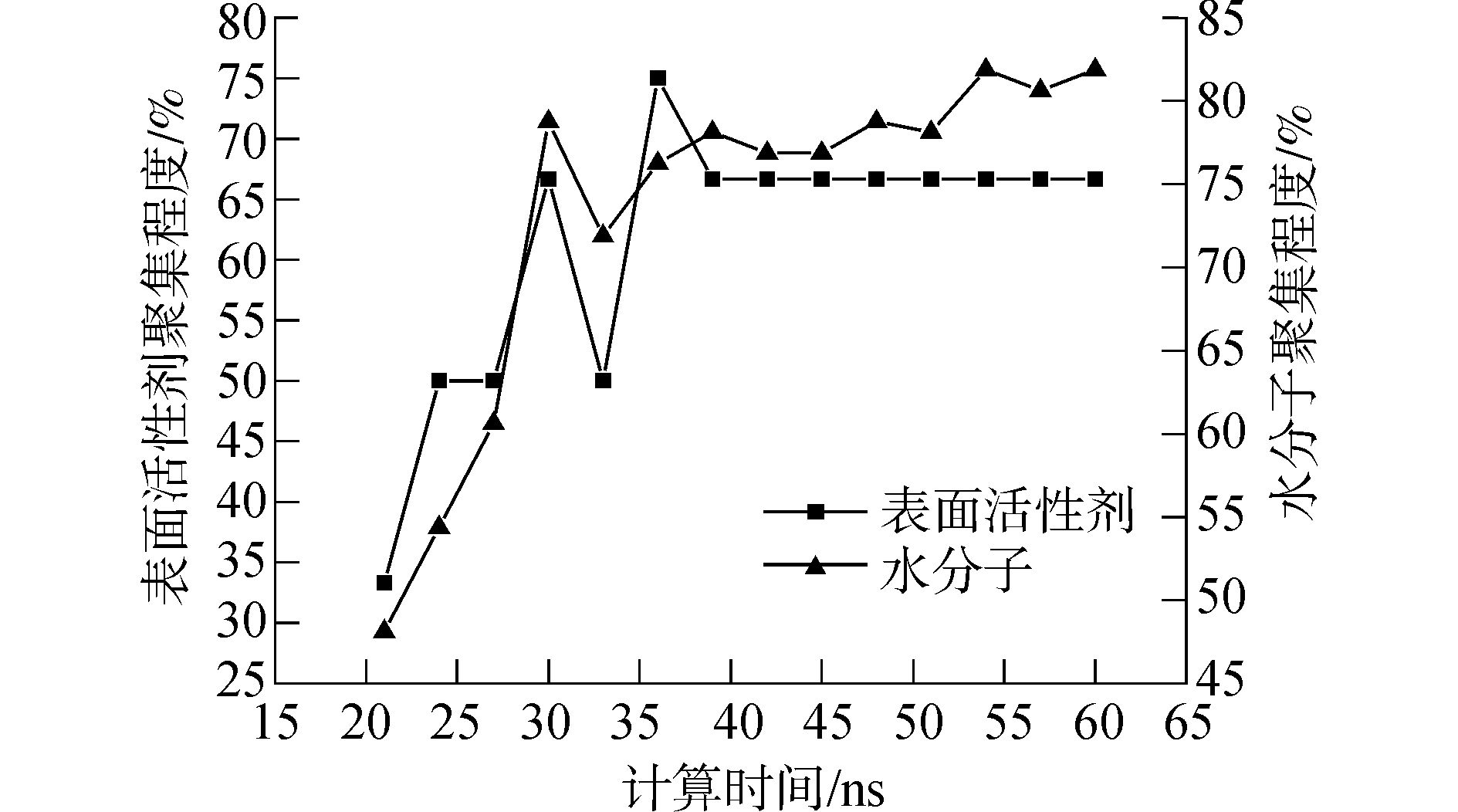
另外,展开了12LS-45/160H2O/12 000CO2三元体系在温度35℃、压力23.37 MPa条件下的过程取样分析,结果如图 8所示。其中,模拟条件取自韩布兴课题组的实验数据[25]。由图 8可以看出,表面活性剂聚集稳定后达到66.67%,水分子可达到80%左右。
|
图 8 12LS-45+160H2O+12 000CO2体系中聚团聚集信息随计算时间变化规律 |
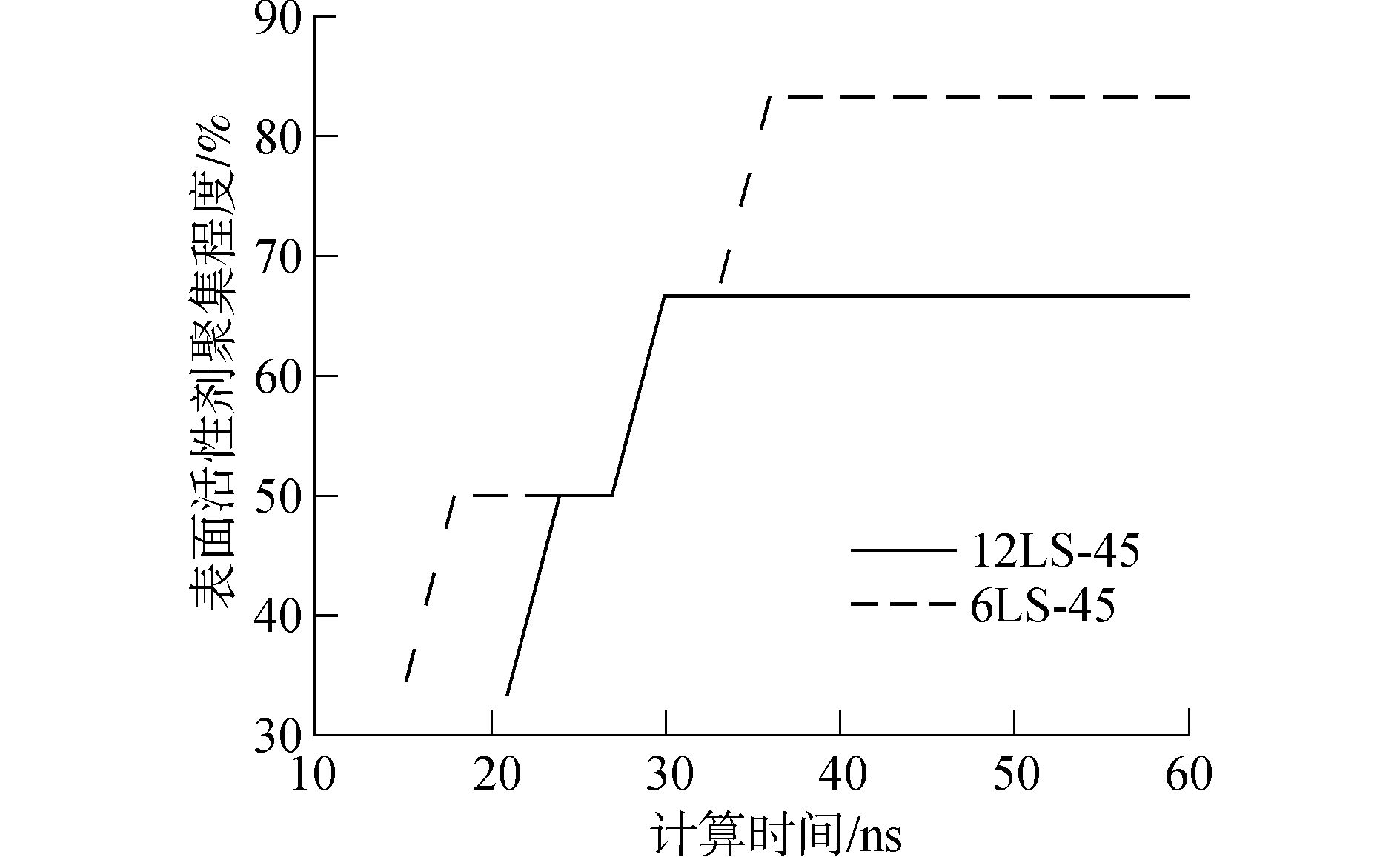
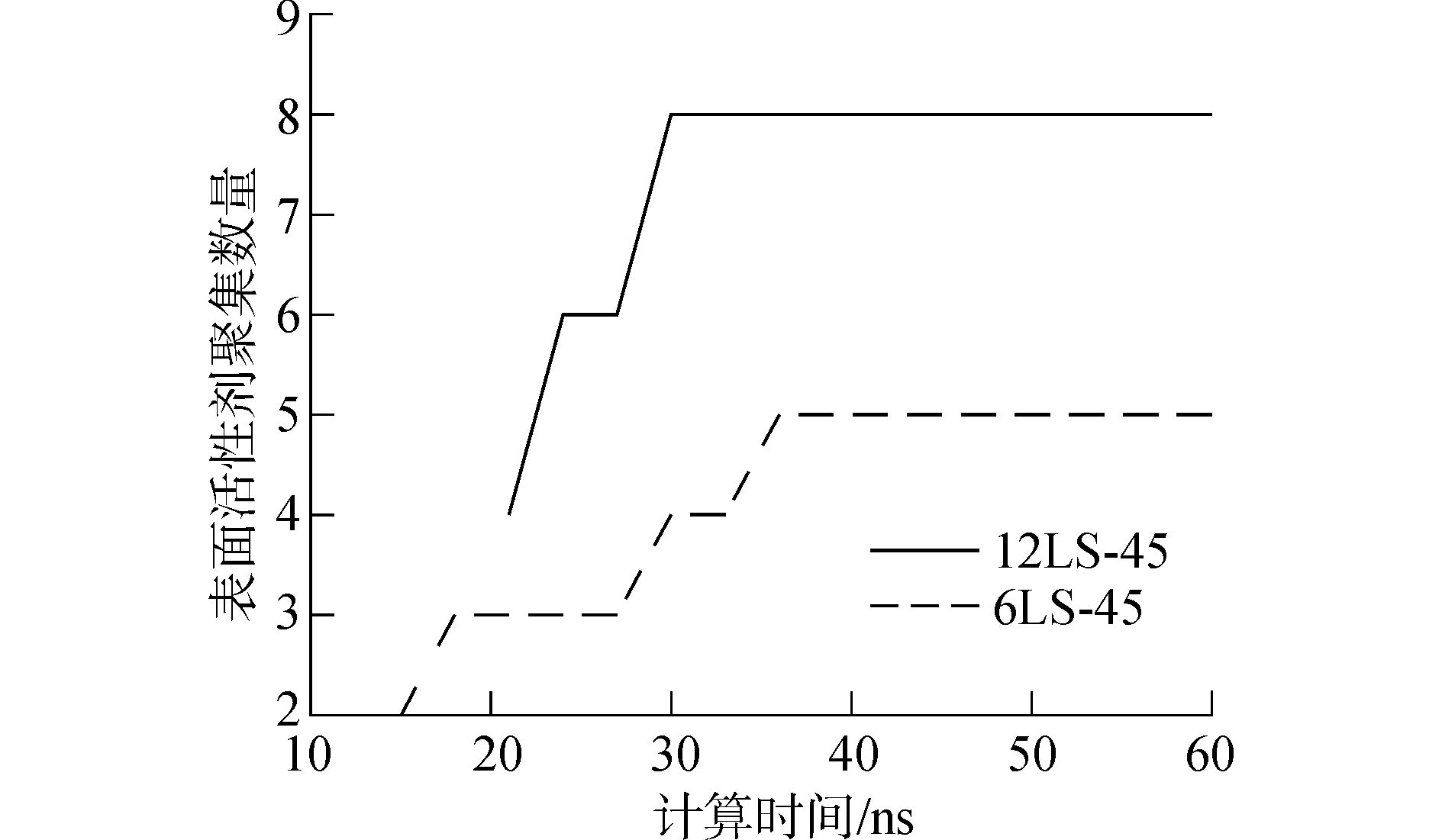
通过MD模拟考察了不同表面活性剂浓度对微乳液聚集过程的影响。在体系水量一定、温度在35 ℃的情况下,分析了表面活性剂数量分别为6个和12个时聚团中表面活性剂的聚集情况,结果如图 9、10所示。由图 9、10可以看出表面活性剂聚集程度随计算时间的增加而增加,然后趋于稳定。另外,当体系中表面活性剂数量较大时,聚团在达到稳定后表面活性剂聚集百分比较小,然而聚团中表面活性剂的绝对数量较大。这说明体系中表面活性剂数量较大时,形成的微乳液聚团规模也较大。
|
图 9 nLS-45+160H2O+12 000CO2体系中表面活性剂浓度对微乳液聚集程度(百分比)的影响 |
|
图 10 nLS-45+160H2O+12 000CO2体系中表面活性剂浓度对微乳液聚集程度(绝对数量)的影响 |
当体系中水分子数量及体系温度(35 ℃)一定时,表面活性剂数量对聚团内水核聚集过程的影响如图 11所示。由图可知,水分子聚集百分比随计算时间的增长而增大。其中,表面活性剂数量较高的体系,水分子聚集程度较大。当计算时间继续增加,两曲线趋于稳定,并基本重合。这说明,表面活性剂数量对微乳液内水核的最终聚集情况影响不大。

|
图 11 nLS-45+160H2O+12 000CO2体系中表面活性剂浓度对微乳液中水分子聚集过程的影响 |
文中对不含氟碳氢表面活性剂LS-45构成的微乳液体系进行了相行为测试,得到了体系的CMC以及W0,并运用MD模拟和过程取样分析,研究了表面活性剂自组装过程中的微观结构信息。主要得出以下结论:
1) 微乳液体系的溶水能力随压力的增加而增大;
2) 微乳液聚集过程中,表面活性剂分子与水分子的聚集轨迹基本一致;
3) 表面活性剂数量对微乳液内水核的最终聚集程度影响不大。
| [1] |
FULTON J L, SMITH R D. Reverse micelle and microemulsion phases in supercritical fluids[J]. Journal of physical chemistry, 1988, 92(10): 2903-2907. DOI:10.1021/j100321a039 ( 0) 0)
|
| [2] |
OHDE H, YE X-R, WAI C M, et al. Synthesizing silver halide nanoparticles in supercritical carbon dioxide utilizing a water-in-CO2 microemulsion[J]. Chemical communications, 2000, 23: 2353-2354. ( 0) 0)
|
| [3] |
WANG J S, CHIU K. Metal extraction from solid matrices using a two-surfactant microemulsion in neat supercritical carbon dioxide[J]. Microchimica acta, 2009, 167(1/2): 61-65. ( 0) 0)
|
| [4] |
WANG J S F, WAI C M. Transporting metal ions using reverse micelles in alcohol modified supercritical carbon dioxide[J]. Journal of supercritical fluids, 2007, 40(2): 176-182. DOI:10.1016/j.supflu.2006.06.003 ( 0) 0)
|
| [5] |
YU W, ZHOU D, YIN J Z, et al. Phase behavior of supercritical CO2 microemulsion with AOT and its solubilization properties of 1, 3-propanediol[J]. Separation science and technology, 2013, 48(13): 1982-1986. DOI:10.1080/01496395.2013.791854 ( 0) 0)
|
| [6] |
YU W, ZHOU D, YIN J-Z, et al. Selective solubilization of 1, 3-propanediol using a water-supercritical CO2 microemulsion with LS-45 as surfactant[J]. Rsc advances, 2013, 3(20): 7585. DOI:10.1039/c3ra23429k ( 0) 0)
|
| [7] |
YU W, ZHOU D, YIN J-Z, et al. Phase behavior of supercritical CO2 microemulsions with surfactant Ls-36 and selective solubilization of propane-1, 3-diol[J]. Journal of chemical & engineering data, 2013, 58(3): 814-820. ( 0) 0)
|
| [8] |
LIU J, CHENG S, ZHANG J, et al. Reverse micelles in carbon dioxide with ionic-liquid domains[J]. Angew chem int ed engl, 2007, 46(18): 3313-3315. DOI:10.1002/(ISSN)1521-3773 ( 0) 0)
|
| [9] |
SALANIWAL S, CUI S T, CUMMINGS P T, et al. Self-assembly of reverse micelles in water/surfactant/carbon dioxide systems by molecular simulation[J]. Langmuir, 1999, 15(16): 5188-5192. DOI:10.1021/la9904556 ( 0) 0)
|
| [10] |
LU L Y, BERKOWITZ M L. Molecular dynamics simulation of a reverse micelle self assembly in supercritical CO2[J]. Journal of the american chemical society, 2004, 126(33): 10254-10255. DOI:10.1021/ja048670i ( 0) 0)
|
| [11] |
CHAITANYA V S V, SENAPATI S. Self-assembled reverse micelles in Supercritical CO2 entrap protein in native state[J]. Journal of the american chemical society, 2008, 130(6): 1866-1870. DOI:10.1021/ja0739234 ( 0) 0)
|
| [12] |
SAGISAKA M, KOIKE D, MASHIMO Y, et al. Water/supercritical CO2 microemulsions with mixed surfactant systems[J]. Langmuir, 2008, 24(18): 10116-10122. DOI:10.1021/la8014145 ( 0) 0)
|
| [13] |
MOHAMED A, ARDYANI T, SAGISAKA M, et al. Economical and efficient hybrid surfactant with low fluorine content for the stabilisation of water-in-CO2 microemulsions[J]. Journal of supercritical fluids, 2015, 98: 127-136. DOI:10.1016/j.supflu.2015.01.012 ( 0) 0)
|
| [14] |
MOHAMED A, SAGISAKA M, HOLLAMBY M, et al. Hybrid CO2-philic surfactants with low fluorine content[J]. Langmuir, 2012, 28(15): 6299-6306. DOI:10.1021/la3005322 ( 0) 0)
|
| [15] |
SAGISAKA M, IWAMA S, ONO S, et al. Nanostructures in water-in-CO2 microemulsions stabilized by double-chain fluorocarbon solubilizers[J]. Langmuir, 2013, 29(25): 7618-7628. DOI:10.1021/la400376g ( 0) 0)
|
| [16] |
EASTOE J, PAUL A, NAVE S, et al. Micellization of hydrocarbon surfactants in supercritical carbon dioxide[J]. Journal of the American chemical society, 2001, 123(5): 988-989. DOI:10.1021/ja005795o ( 0) 0)
|
| [17] |
HOLLAMBY M J, TRICKETT K, MOHAMED A, et al. Tri-chain hydrocarbon surfactants as designed micellar modifiers for supercritical CO2[J]. Angew chem int ed engl, 2009, 48(27): 4993-4995. DOI:10.1002/anie.v48:27 ( 0) 0)
|
| [18] |
SARKAR B, ADHIKARI S, BAER M. Space-time contours to treat intense field-dressed molecular states. Ⅱ. Applications[J]. J chem phys, 2007, 127(1): 014302. DOI:10.1063/1.2743438 ( 0) 0)
|
| [19] |
BERENDSEN H J C, POSTMA J P M, VAN GUNSTEREN W F, et al. Molecular dynamics with coupling to an external bath[J]. J chem phys, 1984, 81(8): 3684. DOI:10.1063/1.448118 ( 0) 0)
|
| [20] |
DARDEN T, YORK D, PEDERSEN L. Particle mesh ewald:an N·log(N) method for ewald sums in large systems[J]. J chem phys, 1993, 98(12): 10089. DOI:10.1063/1.464397 ( 0) 0)
|
| [21] |
VANOMMESLAEGHE K, HATCHER E, ACHARYA C, et al. CHARMM general force field:a force field for drug-like molecules compatible with the CHARMM all-atom additive biological force fields[J]. Journal of computational chemistry, 2010, 31(4): 671-690. ( 0) 0)
|
| [22] |
HARRIS J G, YUNG K H. Carbon dioxides liquid-vapor coexistence curve and critical properties as predicted by a simple molecular-model[J]. Journal of physical chemistry, 1995, 99(31): 12021-12024. DOI:10.1021/j100031a034 ( 0) 0)
|
| [23] |
BERENDSEN H J C, GRIGERA J R, STRAATSMA T P. The missing term in effective pair potentials[J]. The journal of physical chemistry, 1987, 91(24): 6269-6271. DOI:10.1021/j100308a038 ( 0) 0)
|
| [24] |
崔正刚. 表面活性剂、胶体与界面化学基础[M]. 北京: 化学工业出版社, 2013.
( 0) 0)
|
| [25] |
LIU J C, HAN B X, WANG Z W, et al. Solubility of Ls-36 and LS-45 surfactants in supercritical CO2 and loading water in the CO2/water/surfactant systems[J]. Langmuir, 2002, 18(8): 3086-3089. DOI:10.1021/la011721u ( 0) 0)
|
 2017, Vol. 44
2017, Vol. 44


