苯甲酸又称安息香酸,分子式为C6H5COOH,是苯环上的1个氢被羧基(-COOH)取代形成的化合物,其以游离酸、酯或其衍生物的形式广泛存在于自然界中,主要用于抗真菌及消毒防腐,用于医药、染料载体、增塑剂、香料和食品防腐剂等的生产,也用于醇酸树脂涂料的性能改进,也作为钢铁设备的防锈剂、农业化学品。
苯甲酸收载于2015年版《中华人民共和国药典》(简称《中国药典》)二部[1]、食品添加剂标准[2]、饲料添加剂标准[3]、欧洲药典(EP)9.0版[4]、美国药典(USP)41-国家处方集(NF)36版[5]、英国药典(BP)2018年版[6]、日本药局方(JP)17版[7]以及食品化学法典(FCC)第5版[8]中,但各国药典均未对苯甲酸有关物质进行检查,仅食品添加剂及饲料添加剂的标准对5种联苯类物质(联苯、2-甲基联苯、3-甲基联苯、4-甲基联苯、苯甲酸苄酯)进行了控制。
苯甲酸的工业生产方法主要为甲苯液相空气氧化法[9],此外还有三氯甲苯水解法以及邻苯二甲酸酐脱羧法等[10]。苯甲酸的合成过程中容易引入甲苯、苯甲醛、苯甲醇以及联苯类杂质等,其直接影响到产品的安全性。目前,文献报道的检测方法主要为气相色谱(GC)法[11-15]、高效液相色谱(HPLC)法[16-19]等,但仅限于检测其中1~3个杂质成分,尚未见文献报道同时测定苯甲酸有关物质(甲苯、苯甲醛、苯甲醇以及联苯类)的测定方法。本文在前人工作基础上,建立了GC法同时测定苯甲酸有关物质(甲苯、苯甲醛、苯甲醇以及联苯类)的方法。结果表明,所建立的方法简便、快捷、结果准确,能有效控制药品质量。
1 仪器与试药 1.1 仪器安捷伦7890B气相色谱仪,梅特勒XP205电子分析天平。
1.2 药品与试剂苯甲酸样品:样品1(厂家A,批号1160701,原料药),样品2(厂家A,批号1180103,原料药),样品3(厂家B,批号170901,辅料),样品4(厂家B,批号170902,辅料),样品5(厂家C,批号B803148,化学试剂),样品6(厂家D,批号1FK0073,进口辅料);溶剂:N,N-二甲基甲酰胺(国药集团化学试剂有限公司,批号81007718,分析纯);对照品:甲苯(Dr. Ehrenstorfer GmbH,批号30914,含量99.9%),苯甲醛(中国食品药品检定研究院,批号111650-201303,含量99.9 %),苯甲醇(中国食品药品检定研究院,批号190019-201702,含量99.8%),联苯(Stanford Chemicals,批号BPB-081078,含量99.51%),2-甲基联苯(TCI,批号OE5XH,含量98.9%),3-甲基联苯(TCI,批号ONWVE,含量95.3%),4-甲基联苯(TCI,批号4LSKC,含量98.4%),苯甲酸苄酯(Stanford Chemicals,批号BYB-577800,含量99.90%)。
2 方法与结果 2.1 色谱条件色谱柱:Aglient DB-FFAP毛细管柱(30 m×0.32 mm,0.25 μm);柱温:起始温度为100 ℃,保持1 min,以5 ℃·min-1升温至230℃,保持5 min;进样口温度:270 ℃;氢火焰检测器温度:300 ℃;空气流量:400 mL·min-1;氢气流量:30 mL·min-1;载气(N2)流速:1.0 mL·min-1,分流比10:1,进样量:1 μL。
2.2 溶液的制备 2.2.1 混合对照品储备液及混合对照品溶液精密称取甲苯、苯甲醛、苯甲醇、联苯、2-甲基联苯、3-甲基联苯、4-甲基联苯、苯甲酸苄酯的对照品各约20 mg,放于预先盛有约3 mL N,N-二甲基甲酰胺(DMF)的10 mL量瓶中混合,然后加DMF稀释制成每1 mL中约含2 mg的混合对照品储备液。精密量取混合对照品储备液1.0 mL于100 mL量瓶中,加DMF稀释至刻度,摇匀,即成每1 mL中约含20 μg的混合对照品溶液。
2.2.2 供试品溶液取样品0.5 g,精密称定,置25 mL量瓶中,加DMF溶解并稀释制成每1 mL中约含20 mg的溶液,作为供试品溶液。
2.2.3 空白溶液空白溶液为DMF。
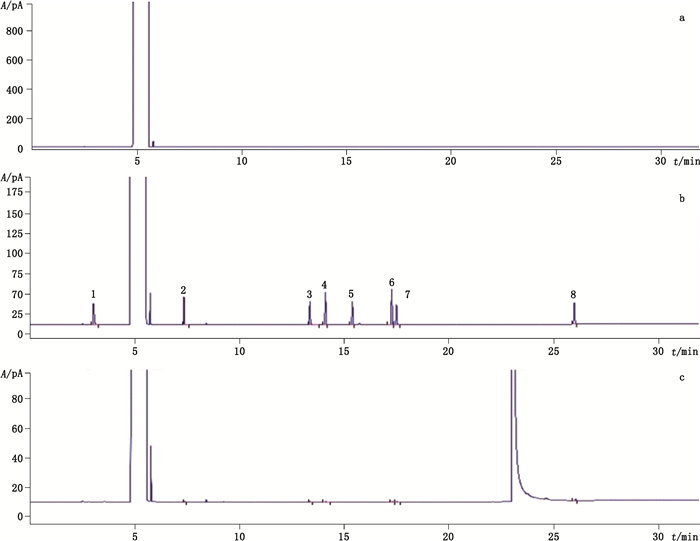
2.3 系统适用性试验取“2.2”项下的空白溶液、对照品溶液和供试品溶液(样品批号1160701)各1 μL,在“2.1”项色谱条件下分别进样,记录色谱图。结果显示,空白溶剂不影响测定,各溶液色谱图中相邻的峰间分离度良好,均大于2.0(图 1);甲苯、苯甲醛、苯甲醇、联苯、2-甲基联苯、3-甲基联苯、4-甲基联苯、苯甲酸苄酯的理论塔板数均大于10 000。
|
1.甲苯(methylbenzene)2.苯甲醛(phenylaldehyde)3.苯甲醇(benzyl alcohol)4. 2-甲基联苯(2-methyl biphenyl)5.联苯(biphenyl)6. 3-甲基联苯(3-methyl biphenyl)7. 4-甲基联苯(4-methyl biphenyl)8.苯甲酸苄酯(benzyl benzoate) a. DMF b.对照品溶液(solution of reference substances)c.供试品溶液(sample solution) 图 1 GC色谱图 Fig.1 GC chromatograms |
精密量取混合对照品储备液5、50、100、500、1 000、1 500 μL,分别置50 mL量瓶中,加DMF稀释至刻度,摇匀,即得线性溶液①~⑥,按上述色谱条件进样分析。以浓度X(μg·mL-1)为横坐标,峰面积Y为纵坐标进行线性回归,结果见表 1。
|
|
表 1 8个化合物线性关系 Tab.1 Linear relationships of 8 compounds |
将“2.4”项下的线性溶液⑥用DMF逐级稀释,进样测定。结果当信噪比约为3时,测得检测下限;当信噪比约为10时,测得定量下限。结果如表 1。
2.6 精密度试验精密量取线性溶液⑤1 μL,按“2.1”项下的色谱条件,连续进样测定6次,记录色谱图及峰面积值。结果测得甲苯、苯甲醛、苯甲醇、联苯、2-甲基联苯、3-甲基联苯、4-甲基联苯、苯甲酸苄酯峰面积的RSD(n=6)分别为0.31%、0.26%、0.43%、0.23%、0.24%、0.22%、0.29%、0.28%,说明仪器进样精密度良好。
2.7 稳定性试验精密量取线性溶液⑤1 μL,分别于0、8、16、24 h,按“2.1”项下的色谱条件进样测定,记录色谱图及峰面积值。结果测得甲苯、苯甲醛、联苯、2-甲基联苯、3-甲基联苯、4-甲基联苯、苯甲酸苄酯峰面积在24 h内的RSD分别为1.0%、0.40%、0.26%、0.33%、0.23%、0.33%、0.26%,说明其溶液在24 h内基本保持稳定,苯甲醇的峰面积在16 h内的RSD为0.12%,说明其溶液在16 h内基本保持稳定。
2.8 加样回收试验分别精密称取已知含量的样品(批号170901)约0.5 g,共9份,依次加入“2.2.1”项下的混合对照品储备液0.20、0.25、0.30 mL,各3份,再分别加DMF稀释至25 mL,即得低、中、高3个质量浓度的供试溶液,按上述色谱条件进样测定并计算回收率。结果如表 2,表明各成分的低、中、高3个浓度回收率均在95.5%~100.4%之间,RSD在0.09%~0.98%之间,说明本方法准确度良好。
|
|
表 2 回收率试验结果 Tab.2 Results of recovery tests |
取6批样品,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,结果见表 3。
|
|
表 3 6批样品中有关物质测定结果(%) Tab.3 Results of related substances in 6 samples |
由于所要检测的有关物质较多,而且3-甲基联苯、4-甲基联苯的沸点与极性相近,难以分离,在本试验中选择不同的毛细管柱进行测定,在选择PE-wax柱时,3-甲基联苯与4-甲基联苯的分离度达不到要求,在使用安捷伦-waxetr柱时,各成分分离度均达到要求,但分析时间较长,而使用安捷伦-DB-FFAP柱时,各成分分离度不仅达到要求,且分析时间控制在30 min内。
3.2 色谱条件的选择本试验检测的有关物质包括甲苯、苯甲醛、苯甲醇、联苯、2-甲基联苯、3-甲基联苯、4-甲基联苯、苯甲酸苄酯8个化合物,沸点范围为110~324 ℃,因此本试验采用程序升温使8个化合物在较短时间内达到良好的分离。
3.3 结论为了进一步控制苯甲酸原料药的质量,对原料药中有关物质进行测定,考虑检出的已知杂质成分的量均较小,结合2015年版《中国药典》对有关物质的限度要求与ICH杂质研究指导原则最低限度要求,甲苯的限度设为不得过0.089%,其余成分设为不得过0.1%。
本文建立了不同级别苯甲酸中有关物质甲苯、苯甲醛、苯甲醇、联苯、2-甲基联苯、3-甲基联苯、4-甲基联苯、苯甲酸苄酯的检查方法,并规定其限度,与已有方法相比,该方法简便、灵敏、专属性强,能同时测定8个成分。此外,苯甲酸在2015年版《中国药典》标准中没有设立有关物质检查项,故本法的建立有利于药品质量的有效控制。
| [1] |
中华人民共和国药典2015年版.二部[S].2015: 50 ChP 2015.Vol Ⅱ[S].2015: 50 |
| [2] |
GB 1886.183-2016食品添加剂苯甲酸[S].2016 GB 1886.183-2016 Food Additive Benzoic Acid[S].2016 |
| [3] |
NY/T 1447-2007饲料添加剂苯甲酸[S].2007 NY/T 1447-2007 Feed Additive Benzoic Acid[S].2007 |
| [4] |
EP 9.0[S].2017: 1818
|
| [5] |
USP 41-NF 36[S].2018: 486
|
| [6] |
BP 2018.Vol Ⅰ[S].2018: 276
|
| [7] |
JP 17[S].2016: 447
|
| [8] |
FCC Ⅵ[S].2008: 46
|
| [9] |
王忠元, 张艳熹. 甲苯液相空气氧化制苯甲酸[J]. 黑龙江石油化工, 1996(1): 1. WANG ZY, ZHANG YX. Toluene liquid phase air oxidation to benzoic acid[J]. Heilongjiang Petrochem Technol, 1996(1): 1. |
| [10] |
吴鑫干, 陈舒伐. 苯甲酸的合成和精制[J]. 现代化工, 2000, 20(8): 10. WU XG, CHEN SF. Synthesis and purification of benzoic acid[J]. Mod Chem Ind, 2000, 20(8): 10. DOI:10.3321/j.issn:0253-4320.2000.08.004 |
| [11] |
张冲, 徐爱霞, 王海琳, 等. 气相色谱法测定苯甲醇注射液的有关物质[J]. 药物生物技术, 2016, 23(3): 241. ZHANG C, XU AX, WANG HL, et al. GC determination of related substances of benzyl alcohol injection[J]. Pharm Biotechnol, 2016, 23(3): 241. |
| [12] |
葛红莉, 吴爱莉. 气相色谱法测定药用辅料苯甲醇含量[J]. 化工时刊, 2017, 31(9): 12. GE HL, WU AL. Determination of benzyl alcohol by gas chromatography[J]. Chem Ind Times, 2017, 31(9): 12. DOI:10.16597/j.cnki.issn.1002-154x.2017.09.005 |
| [13] |
谭平华, 唐盛伟, 刘长军, 等. 气相色谱法同时测定苯甲醛、苯甲醇和苯甲酸[J]. 天然气化工, 2007, 32(2): 64. TAN PH, TANG SW, LIU CJ, et al. The simultaneous determination of benzaldehyde, benzyl alcohol and benzoic acid by gas chromatography[J]. Nat Gas Chem Ind, 2007, 32(2): 64. DOI:10.3969/j.issn.1001-9219.2007.02.016 |
| [14] |
孙远华, 张同来, 张建国, 等. 气相色谱法测定甲苯氧化产物中的甲苯及苯甲醛[J]. 分析科学学报, 2005, 21(2): 229. SUN YH, ZHANG TL, ZHANG JG, et al. Determination of toluene and benzaldehyde in toluene oxidation products by gas chromatography[J]. J Anal Sci, 2005, 21(2): 229. DOI:10.3969/j.issn.1006-6144.2005.02.036 |
| [15] |
刘敬兰, 周鸿娟, 陈连文, 等. 气相色谱法测定甲苯氧化产物中的苯甲醛及苯甲酸[J]. 色谱, 1996, 14(1): 79. LIU JL, ZHOU HJ, CHEN LW, et al. Determination of benzaldehyde and benzoic acid in toluene oxidation products by gas chromatography[J]. Chin J Chromatogr, 1996, 14(1): 79. DOI:10.1007/BF02009548 |
| [16] |
章家伟, 王辉, 孙庆荣, 等. RP-HPLC法同时测定苯甲酸原料药中有关物质苯甲醛和甲苯的含量[J]. 中国药房, 2013, 24(29): 2754. ZHANG JW, WANG H, SUN QR, et al. Simultaneous determination of related substances benzaldehyde and toluene in benzoic acid crude drug by RP-HPLC[J]. China Pharm, 2013, 24(29): 2754. |
| [17] |
粟贵, 刘雁鸣, 李兰, 等. 高效液相色谱法测定药用辅料苯甲醇中苯甲酸和苯甲醛含量[J]. 中南药学, 2014, 12(12): 1239. SU G, LIU YM, LI L, et al. Determination of benzoic acid and benzaldehyde in pharmaceutical excipients benzyl alcohol by HPLC[J]. Cent South Pharm, 2014, 12(12): 1239. DOI:10.7539/j.issn.1672-2981.2014.12.021 |
| [18] |
张波, 张谦, 程晓平, 等. 苯甲醇注射液含量的高效液相色谱法测定[J]. 济宁医学院学报, 2008, 31(2): 139. ZHANG B, ZHANG Q, CHEN XP, et al. Determination of benzyl alcohol injection by high performance liquid chromatography[J]. J Jining Med College, 2008, 31(2): 139. DOI:10.3969/j.issn.1000-9760.2008.02.024 |
| [19] |
徐辉. 高效液相色谱法测定药用辅料苯甲醇中苯甲酸和苯甲醛的含量[J]. 中国新技术新产品, 2017(4): 62. XU H. Determination of benzoic acid and benzaldehyde in benzyl alcohol by high performance liquid chromatography[J]. New Technol New Prod China, 2017(4): 62. DOI:10.3969/j.issn.1673-9957.2017.04.039 |
 2020, Vol. 40
2020, Vol. 40 