2. 甘肃省中藏药检验检测技术工程实验室, 兰州 730070;
3. 甘肃省河西制药有限责任公司, 张掖 734000
2. Gansu Inspection and Testing Technical Engineering Laboratory for Chinese Herbal and Tibetan Medicine, Lanzhou 730070, China;
3. Gansu Hexi Pharmaceutical Co., Ltd, Zhangye 734000, China
栀子金花丸收载于《中华人民共和国药典》(简称《中国药典》)2015年版一部,是由栀子、黄连、黄芩、黄柏、大黄、金银花、知母和天花粉8味中药制成的中药复方制剂,具有清热泻火、凉血解毒的功效,用于肺胃热盛、口舌生疮、牙龈肿痛、目赤眩晕、咽喉肿痛、吐血衄血和大便秘结的治疗[1]。方中黄芩中含有黄芩苷等黄酮类化合物,金银花中主要含有绿原酸、槲皮素、木犀草素、木犀草苷等有机酸、黄酮和三萜皂苷类成分,知母中含芒果苷,栀子中含有栀子苷等环烯醚萜类成分及三萜类、黄酮类成分,其中小檗碱是黄连、黄柏中的共有成分,小檗碱、黄柏碱等生物碱成分具有较强的抗菌、消炎作用,栀子中的栀子苷具有保肝利胆、抗炎、抗氧化等多种作用[2]。
对于栀子金花丸的测定,《中国药典》2015年版仅以栀子苷为指标进行含量测定,文献[3-10]采用同一波长进行测定。本文参考文献[11-15],建立HPLC-DAD法,利用DAD检测器设定3个检测通道,同时采用不同结构的化合物在不同紫外波长处检测,对栀子金花丸中含量较高的栀子苷、绿原酸、黄芩苷、芒果苷、小檗碱、黄柏碱、大黄酸、大黄素、芦荟大黄素和大黄酚10个活性成分进行含量测定,为全面评价栀子金花丸的质量以及今后质量标准的提高提供参考。
1 仪器与试药 1.1 仪器Waters 2695型高效液相色谱仪(2695溶剂管理系统,2996二极管阵列检测器,Empower Ⅲ色谱工作站,Waters公司);KQ-250型超声波提取器(昆山市超声仪器有限公司);XR205SM-DR型十万分之一分析天平(Pricisa公司)。
1.2 对照品、样品及试剂对照品栀子苷(批号110749-201718,含量97.6%)、绿原酸(批号110753-201817,含量96.8%)、黄芩苷(批号110715-201016,含量94.4%)、芒果苷(批号110607-201702,含量100.0%)、盐酸小檗碱(批号110713-201814,含量96.7%)、盐酸黄柏碱(批号111895-201504,含量98.0%)、大黄酸(批号110756-201607,含量99.3%)、大黄素(批号110796-201512,含量98.7%)、芦荟大黄素(批号110795-201710,含量98.1%)、大黄酚(批号110796-201621,含量99.2%)均购自中国食品药品检定研究院;栀子金花丸,批号181203、181204、181205、180901、180902,由甘肃河西制药有限公司提供。
甲醇、乙腈为色谱纯(Merck公司),水为超纯水,其余试剂(国药集团化学试剂有限公司)均为分析纯。
2 方法与结果 2.1 色谱条件采用Luna C18色谱柱(4.6 mm×250 mm,5 µm),以乙腈(A)-0.2%醋酸水溶液(B)为流动相,梯度洗脱(0~15 min,8%A→40%A;15~20 min,40%A→ 60%A;20~30 min,60%A→90%A;30~40 min,90%A→8%A),流速1.0 mL·min-1,柱温35 ℃,检测波长258 nm(检测栀子苷、芒果苷、大黄酸、大黄素、芦荟大黄素和大黄酚)、280 nm(检测黄芩苷、黄柏碱)、345 nm(检测绿原酸、小檗碱),进样量10 µL。
2.2 溶液的制备 2.2.1 混合对照品储备液分别精密称取栀子苷、绿原酸、黄芩苷、芒果苷、盐酸小檗碱、盐酸黄柏碱、大黄酸、大黄素、芦荟大黄素和大黄酚的对照品适量,加甲醇溶解并制成每1 mL分别含栀子苷657.0 μg,绿原酸418.0 μg,黄芩苷301.0 μg,芒果苷632.0 μg,盐酸小檗碱668.0 μg(小檗碱的量=盐酸小檗碱的量/1.1087),盐酸黄柏碱71.0 μg(黄柏碱的量=盐酸黄柏碱的量/1.1066),大黄酸271.0 μg,大黄素73.0 μg,芦荟大黄素41.0 μg,大黄酚101.0 μg的混合溶液,即得。
2.2.2 供试品溶液取本品适量,研细,取约0.5 g,精密称定,置锥形瓶中,精密加入甲醇50 mL,密塞,称量,超声处理(功率300 W,频率50 kHz)20 min,放冷,再称量,用甲醇补足减失的量,摇匀,滤过,精密量取续滤液10 mL,置25 mL量瓶中,加甲醇至刻度,摇匀,用0.45 μm微孔滤膜滤过,取续滤液,即得。
2.2.3 阴性样品溶液按照栀子金花丸的处方比例分别制备不含大黄、黄连和黄柏、黄芩、金银花、知母、栀子以及只含天花粉(无栀子苷、绿原酸、黄芩苷、芒果苷、小檗碱、黄柏碱、大黄酸、大黄素、芦荟大黄素和大黄酚10个成分)的7种阴性样品,按“2.2.2”项下方法操作,即得。
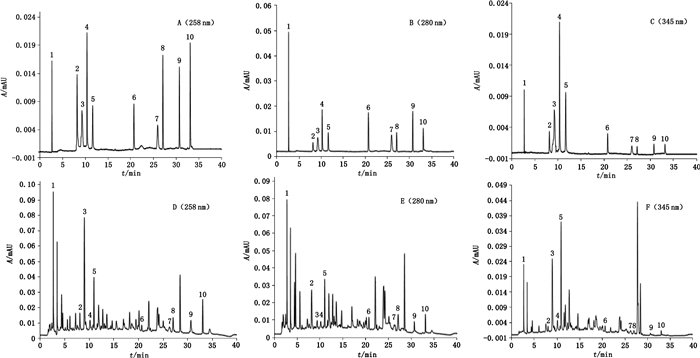
2.3 专属性试验精密吸取“2.2.1”项下混合对照品储备液适量,用甲醇稀释100倍,配制成混合对照品溶液。精密吸取上述混合对照品溶液及“2.2.2”项下的供试品溶液及“2.2.3”项下的阴性样品溶液各10 μL,按“2.1”项下色谱条件进行试验,结果见图 1、2。在上述色谱条件下,栀子金花丸中10个被测成分均达到基线分离,与其他成分之间均无明显干扰。
|
1.黄柏碱(phellodendrine)2.芒果苷(mangiferin)3.小檗碱(berberine)4.栀子苷(geniposide)5.绿原酸(chlorogenic acid)6.黄芩苷(baicalin)7.芦荟大黄素(aloe emodin)8.大黄酸(rhein)9.大黄素(emodin)10.大黄酚(chrysophanol) A.混合对照品(mixed reference substances,258 nm)B.混合对照品(mixed reference substances,280 nm)C.混合对照品(mixed reference substances,345 nm)D.样品(sample,258 nm)E.样品(sample,280 nm)F.样品(sample,345 nm) 图 1 混合对照品及样品的HPLC色谱图 Fig.1 HPLC chromatograms of mixed reference substances and sample |

|
1~10.同图 1(same as G.只含天花粉阴性样品(negative sample without ten ingredients,258 nm)H.只含天花粉阴性样品(negative sample without ten ingredients,280 nm)I.只含天花粉阴性样品(negative sample without ten ingredients,345 nm)J.缺黄柏和黄连阴性样品(negative sample without Coptidis Rhizoma and Phelldendri Cortex,345 nm)K.缺金银花阴性样品(negative sample without Lonicerae Japonicae Flos,345 nm)L.缺知母阴性样品(negative sample without Anemarrhena Rhizoma,258 nm)M.缺栀子阴性样品(negative sample without Gardeniae Fructus,258 nm)N.缺黄芩阴性样品(negative sample without Scutellariae Radix,280 nm)O.缺大黄阴性样品(negative sample without Rhei Radix et Rhizoma,258 nm) 图 2 阴性样品的HPLC色谱图 Fig.2 HPLC chromatograms of negative samples |
分别精密吸取上述混合对照品储备液适量,用甲醇逐级稀释,配制成6个不同浓度的混合对照品溶液,按“2.1”项下色谱条件进样,测定峰面积,每个浓度进样2次;以对照品的进样量X(μg)为横坐标,峰面积Y为纵坐标,进行线性回归,回归方程、相关系数及线性范围见表 1。取混合对照品溶液,逐级稀释并进样测定,以仪器的信噪比S/N为3时计算检测下限(LOD),以仪器的信噪比S/N为10时计算定量下限(LOQ),结果见表 1。
|
|
表 1 10个成分的线性关系、检测限和定量限结果 Tab.1 Linear relationship, LOD and LOQ of ten constituents |
吸取“2.2.1”项下混合对照品储备液适量,用甲醇稀释100倍,配制成的混合对照品溶液,按“2.1”项下色谱条件下连续重复进样6次,测得栀子苷、绿原酸、黄芩苷、芒果苷、小檗碱、黄柏碱、大黄酸、大黄素、芦荟大黄素和大黄酚峰面积RSD依次分别为1.3%、0.45%、1.2%、0.63%、0.32%、1.8%、0.64%、1.3%、1.6%和0.86%,表明仪器精密度良好。
2.6 稳定性试验取同一供试品溶液,室温下于0、2、4、6、8、10 h分别按“2.1”项下色谱条件进样测定,测得栀子苷、绿原酸、黄芩苷、芒果苷、小檗碱、黄柏碱、大黄酸、大黄素、芦荟大黄素和大黄酚峰面积RSD依次分别为1.5%、0.73%、1.1%、1.1%、1.4%、1.2%、1.6%、1.2%、0.92%和0.74%,表明供试品溶液在10 h内测定,稳定性良好。
2.7 重复性试验取同一批栀子金花丸(批号181203),按“2.2.2”项下方法制备供试品溶液6份,按“2.1”项下色谱条件进样测定,测得栀子苷、绿原酸、黄芩苷、芒果苷、小檗碱、黄柏碱、大黄酸、大黄素、芦荟大黄素和大黄酚平均含量分别为3.68、2.32、1.71、3.52、3.51、0.35、1.46、0.44、0.23、0.54 mg·g-1,RSD分别为2.0%、1.3%、2.6%、1.0%、1.6%、1.6%、2.3%、1.6%、2.2%和1.4%,表明该方法重复性良好。
2.8 加样回收率试验精密量取已知含量的栀子金花丸(批号181203)9份,每份0.25 g,精密称定,置具塞锥形瓶中,每3份一组,分别精密加入10个被测成分的混合对照品溶液适量,按“2.2.2”项下方法,自“加入甲醇50 mL”起操作,制得低、中、高3个浓度的供试溶液各3份。按“2.1”项下色谱条件进样测定,结果见表 2,表明回收率良好。
|
|
表 2 10个成分的加样回收率 Tab.2 Recovery for ten components |
目前,本地市场上销售的栀子金花丸均为甘肃河西制药有限公司产品,因条件所限,仅从该公司收集到5批样品,按“2.1”项方法进行10个成分的测定,外标法计算各成分的含量,结果见表 3。
|
|
表 3 栀子金花丸中10个成分的含量(mg·g-1,n=3) Tab.3 Determination results of ten components in Zhizi Jinhua pills |
在现行栀子金花丸的质量标准中,仅以栀子苷为指标进行定量质控,不能全面反映该药物中多组分共同作用起效的特点,本实验以栀子金花丸处方中的主要成分栀子苷、绿原酸、黄芩苷、芒果苷、盐酸小檗碱、盐酸黄柏碱、大黄酸、大黄素、芦荟大黄素和大黄酚10个测定成分作为栀子、金银花、黄芩、知母、黄柏、黄连、大黄7个中药材法定质量评价指标。通过方法学的研究,建立了栀子金花丸中栀子苷、绿原酸等10个活性成分的测定指标。
3.2 色谱柱和流动相的选择本实验分别比较了3种不同品牌不同型号的色谱柱[Agilent ZORBAX SB C18(4.6 mm×150 mm,5 μm)、Agilent Eclipse XDB C18(4.6 mm×250 mm,5 μm)和Luna C18(4.6 mm×250 mm,5 µm)]。由3名实验人员,分别采用3种不同色谱柱分别对同一批样品进行测定,测定样品栀子苷含量的RSD(n=9)为1.1%,结果表明Luna C18色谱柱对栀子金花丸水溶性成分的分离效果最佳。
其次本试验测定指标为生物碱盐、有机酸和苷类,故分别对流动相中的酸(磷酸、甲酸、醋酸)进行了考察,将流动相体系的pH由低到高调节至不同值进行分析,最终确定采用0.2%醋酸(pH约3)酸度较为适宜,故选择乙腈-0.2%醋酸溶液作为流动相。
3.3 DAD检测波长的选择栀子金花丸中栀子苷、绿原酸、黄芩苷、芒果苷、小檗碱、黄柏碱、大黄酸、大黄素、芦荟大黄素和大黄酚的紫外吸收波长差异较大[1],栀子苷在238 nm,大黄酸、大黄素、芦荟大黄素和大黄酚在254 nm,黄芩苷、黄柏碱在280 nm,绿原酸和小檗碱在345 nm有强吸收,为使这些成分在一次进样中同时得到测定,本研究综合考虑,利用DAD检测器进行全波长扫描后,设定258、280和345 nm 3个检测通道,有效地分离并定量了栀子金花丸中的10个成分,经方法学考察,证实了该方法的准确性与可靠性,从而为栀子金花丸更全面的质量评价和控制提供了参考。
3.4 小结含量测定结果表明,栀子苷、绿原酸、黄芩苷、芒果苷、小檗碱、黄柏碱、大黄酸、大黄素、芦荟大黄素和大黄酚10个成分为不同批次栀子金花丸,栀子苷含量均符合《中国药典》2015年版一部该品种项下规定(不得低于2.0 mg·g-1),5批次样品的HPLC色谱行为相似度较高,各批次样品间待测成分含量差异较小,说明栀子金花丸的药材来源和生产工艺均较为稳定。
本研究采用3个不同波长切换,一种色谱条件和系统适用性试验,同时测定,有良好的分离效果,样品提取方法简便,可作为该产品质量考察和控制的参考。
| [1] |
中华人民共和国药典2015年版.一部[S].2015: 1538 ChP 2015.Vol Ⅰ[S].2015: 1538 |
| [2] |
肖培根, 李大鹏, 杨世林. 新编中药志.第三卷[M]. 北京: 化学工业出版社, 2002. XIAO PG, LI DP, YANG SL. Modern Chinese Materia Medica.Vol Ⅲ[M]. Beijng: Chemical Industry Press, 2002. |
| [3] |
曲蕃升, 邢丽媛, 许丽娜. 栀子金花丸多指标成分HPLC含量测定方法研究[J]. 现代中药研究与实践, 2017, 31(1): 56. QU FS, XING LY, XU LN. Multiple compounds determination of Zhizi-Jinhua pills by high-performance liquid chromatography[J]. Res Pract Chin Med, 2017, 31(1): 56. |
| [4] |
赵倩, 冯伟红, 张启伟, 等. "一测多评"法用于栀子金花丸多成分含量测定的可行性研究[J]. 中国中药杂志, 2014, 39(10): 1826. ZHAO Q, FENG WH, ZHANG QW, et al. Feasibility study of QAMS for quantitative analysis of multiple structural types of ingredients in Zhizi Jinhua pill[J]. China J Chin Mater Med, 2014, 39(10): 1826. DOI:10.4268/cjcmm20141015 |
| [5] |
陈帅, 王慧竹, 薛健飞, 等. 栀子金花丸HPLC指纹图谱及其与体外抗氧化活性的相关性分析[J]. 中国药房, 2016, 27(22): 3077. CHEN S, WANG HZ, XUE JF, et al. Analysis of the relationship of HPLC fingerprint of Zhizi Jinhua pills with its in vitro antioxidant activity[J]. China Pharm, 2016, 27(22): 3077. DOI:10.6039/j.issn.1001-0408.2016.22.16 |
| [6] |
黎晓玲, 彭瑞光. HPLC同时测定栀子金花丸中4种成分的含量[J]. 安徽农业科学, 2014, 42(6): 1665. LI XL, PENG RG. Simultaneous determination of 4 components in Zhizijinhua pill by HPLC[J]. J Anhui Agric Sci, 2014, 42(6): 1665. DOI:10.3969/j.issn.0517-6611.2014.06.030 |
| [7] |
蒋范任, 蔡洪鲲, 周翀, 等. 反相高效液相色谱法同时测定栀子金花丸中栀子苷、小檗碱、黄芩苷、大黄酸、大黄素、大黄酚的含量[J]. 中南药学, 2015, 13(2): 172. JIANG FR, CAI HK, ZHOU C, et al. Determination of geniposide, berberine, baicalin, rhein, emodin and chrysophanol in Zhizi Jinhua pill by RP-HPLC[J]. Cent South Pharm, 2015, 13(2): 172. |
| [8] |
高晓燕, 卢建秋. 栀子金花丸中栀子苷、黄芩苷、番泻苷A和番泻苷B的含量测定方法研究[J]. 中国中药杂志, 2009, 34(20): 2649. GAO XY, LU JQ. Study on determination of geniposide, baicalin, sennoside A and sennoside B in Zhizijinhua Wan[J]. China J Chin Mater Med, 2009, 34(20): 2649. DOI:10.3321/j.issn:1001-5302.2009.20.023 |
| [9] |
温金莲, 周清, 宋粉云. RP-HPLC测定栀子金花丸中芒果苷的含量[J]. 中国实验方剂学杂志, 2011, 17(17): 65. WEN JL, ZHOU Q, SONG FY. Determination of mangiferin in Zhizi Jinhua Wan by RP-HPLC[J]. Chin J Exp Tradit Med Form, 2011, 17(17): 65. DOI:10.3969/j.issn.1005-9903.2011.17.020 |
| [10] |
郑峰, 徐成志. HPLC法测定栀子金花丸中大黄素和大黄酚的含量[J]. 安徽医药, 2007, 1(11): 1006. ZHENG F, XU CZ. Determination of emodin and chrysophanol in Zhizijinhua Wan by HPLC[J]. Anhui Med Pharm J, 2007, 1(11): 1006. DOI:10.3969/j.issn.1009-6469.2007.11.028 |
| [11] |
何昱, 周惠芬, 黄丽娜, 等. HPLC-DAD法同时测定谷红注射液中7个组分的含量[J]. 药物分析杂志, 2015, 35(6): 954. HE Y, ZHOU HF, HUANG LN, et al. Simultaneous quantification of seven components in Guhong injection by HPLC-DAD[J]. Chin J Pharm Anal, 2015, 35(6): 954. |
| [12] |
郭小龙, 蔡敏, 陈勇, 等. 液相色谱法同时测定栀子金花丸中栀子苷和盐酸小檗碱的含量[J]. 湖北大学学报(自然科学版), 2007, 29(3): 283. GUO XL, CAI M, CHEN Y, et al. Simultaneous determination of geniposide and berberine hydrochloride in Zhizijinhua Wan by high performance liquid chromatography[J]. J Hubei Univ(Nat Sci), 2007, 29(3): 283. DOI:10.3969/j.issn.1000-2375.2007.03.018 |
| [13] |
王常顺, 刘永利, 段吉平, 等. 双波长-UPLC法同时测定知柏地黄丸中6个成分的含量[J]. 药物分析杂志, 2018, 38(2): 256. WANG CS, LIU YL, DUAN JP, et al. Simultaneous quantification of six components in Zhibai Dihuang pills by dual-wavelength UPLC[J]. Chin J Pharm Anal, 2018, 38(2): 256. |
| [14] |
郝乘仪, 于蕾, 昌盛, 等. HPLC-DAD法同时测定栀芩清热合剂中多指标成分含量[J]. 药物分析杂志, 2018, 38(9): 1601. HAO CY, YU L, CHANG S, et al. Simultaneous determination of index compounds in Zhiqin Qingre mixture by HPLC-DAD[J]. Chin J Pharm Anal, 2018, 38(9): 1601. |
| [15] |
陈晓虎, 苏晶, 王慧, 等. UPLC法同时测定栀子金花丸中11种成分[J]. 中草药, 2014, 45(6): 955. CHEN XH, SU J, WANG H, et al. Simultaneous determination of 11 components in Zhizijinhua pill by UPLC[J]. China Tradit Herb Drugs, 2014, 45(6): 955. DOI:10.7501/j.issn.0253-2670.2014.7.011 |
 2020, Vol. 40
2020, Vol. 40 
