2. 北京茗泽中和药物研究有限公司, 北京 102629;
3. 河北省药物化工中心, 石家庄 050018
2. Beijing minzezhonghe pharmaceutical research Co., Ltd., Beijing 102629, China;
3. Hebei Research Center of Pharmaceutical and Chemical Engineering, Shijiazhuang 050018, China
铝镁加混悬液是中和胃酸药,文献报道其对提高胃液pH,减少胃液总酸度有明显的疗效,可用于治疗胃及十二指肠溃疡或胃酸过多引起的反酸、烧心、疼痛、腹胀等症状[1-2]。铝镁加,1984年由西班牙Amirall公司首次上市销售,目前,韩国一洋药品株式会社生产的原料药在中国上市[3]。本研究以在西班牙、德国等欧洲国家上市的铝镁加混悬液(Almax Forte)为参比制剂进行仿制研究。
在药物质量研究过程中,除了关注活性成分的指标外,近年来对其杂质研究也越来越深入,同时还需要对抑菌剂、氧化剂等特殊辅料进行控制。另外基因毒性杂质,是影响药物安全性的主要因素,应重点关注[4-6]。本研究参照原研制剂Almax Forte[7],选用醋酸氯己定作为本品辅料中的抑菌剂。
醋酸氯己定是口服液体制剂的常规辅料,最大用量为0.01%,其降解杂质对氯苯胺为基因毒性杂质[8-9]。关于醋酸氯己定的含量测定,《中华人民共和国药典》2015年版二部中收载了高氯酸非水滴定法和紫外可见分光光度法[10]。但本品中仅含0.01%的醋酸氯己定,药典方法的专属性和精密度不能满足铝镁加混悬液中醋酸氯己定含量测定的要求,而且药典方法不含有醋酸氯己定降解杂质对氯苯胺的含量测定,需要重新建立方法。本研究参考美国药典[11]、欧洲药典[12]及相关文献[13-16]建立了一种高效液相色谱法,可同时测定铝镁加混悬液中醋酸氯己定及其降解杂质对氯苯胺的含量,该方法专属性、精密度、准确度均可满足要求。
1 仪器与试药 1.1 仪器Waters 2695-2487高效液相色谱仪(Waters公司);QUINTIX125D-1CN/BT125D型电子分析天平(赛多利斯科学仪器有限公司);PHSJ-5型pH计(上海雷磁-上海仪电科学仪器股份有限公司);SB25-12DTD型超声波清洗器(宁波新芝生物科技有限公司);5415D型离心机(上海心亮实业有限公司);Exceed-Ad-型艾柯超纯水机(成都康氏康宁科技发展有限公司)。
1.2 试药对照品醋酸氯己定(中国食品药品检定研究院,使用前不需干燥处理,按C22H30OCl2N10·2C2H4O2计,供HPLC法测定含量为96.3%,批号100183-201604)、对氯苯胺对照品(中国食品药品检定研究院,使用前不需干燥处理,供HPLC法系统适用性及显色法检查用,按C6H6ClN计,含量为100%,批号101398-201601)、铝镁加混悬液(自制,批号20180201、20180201、20180301,规格15 mL:1.5 g);Almax Forte(原研制剂,批号32M,Amirail公司);甲醇、乙腈均为色谱纯(上海星可高纯试剂有限公司);水为纯化水;其他试剂均为分析纯。
2 方法与结果 2.1 溶液的制备 2.1.1 醋酸氯己定对照品溶液精密称取醋酸氯己定对照品溶液10 mg置于20 mL量瓶中,用溶剂(流动相A)溶解并稀释至刻度,摇匀得储备液①,从储备液①中量取1 mL用溶剂稀释至10 mL,摇匀即得50 μg·mL-1的溶液,冰箱(2~8 ℃)保存。
2.1.2 对氯苯胺对照品溶液称取对氯苯胺对照品10 mg置于100 mL量瓶中,用溶剂溶解并定容,摇匀得储备液②,精密量取储备液②1 mL置于100 mL量瓶中,用溶剂稀释至刻度,摇匀即得1 µg·mL-1的对氯苯胺溶液,冰箱(2~8 ℃)保存。
2.1.3 系统适用性溶液分别精密称取醋酸氯己定对照品和对氯苯胺对照品各10 mg,用溶剂制成醋酸氯己定10 µg·mL-1和对氯苯胺0.1 µg·mL-1的混合溶液。
2.1.4 供试品溶液前处理精密称取铝镁加混悬液5 g置于50 mL量瓶中,加溶剂稀释至约40 mL,超声(500 W,40 kHz)并辅助振摇10 min,取出放冷至室温,用溶剂稀释至刻度,离心(13 000 r·min-1,10 min),取上清液,即得。
2.1.5 空白辅料溶液精密称取空白辅料5 g置于50 mL量瓶中,加溶剂稀释至约40 mL,超声(500 W,40 kHz)并辅助振摇10 min,取出放冷至室温,用溶剂稀释至刻度,离心(13 000 r·min-1,10 min),取上清液,即得。
2.1.6 空白溶剂溶液流动相A:磷酸盐溶液(取磷酸二氢钠27.6 g,加三乙胺10 mL,加水1 500 mL,搅拌使溶解后,用磷酸调节pH 3.0,用水稀释至2 000 mL)-乙腈(70:30)。
2.2 色谱条件色谱柱为WondaSil C18 Superb柱(4.6 mm×250 mm,5 µm),以磷酸盐溶液(取磷酸二氢钠27.6 g,加三乙胺10 mL,加水1 500 mL,搅拌使溶解后,用磷酸调节pH3.00,用水稀释至2 000 mL)-乙腈(70:30)为流动相A,乙腈为流动相B,梯度洗脱条件见表 1,流速为1.5 mL·min-1,检测波长239 nm,柱温40 ℃,进样量为200 µL。
|
|
表 1 流动相梯度洗脱条件 Tab.1 Mobile phase gradient elution conditions |
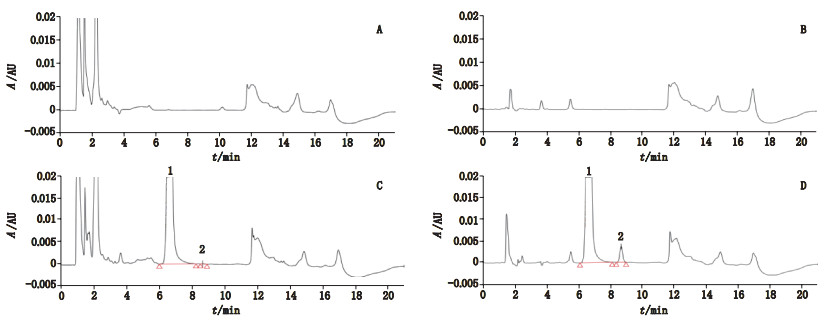
分别精密量取系统适用性溶液、供试品溶液和空白辅料溶液及空白溶剂溶液各200 µL,按“2.2”项下的色谱条件进样分析,结果见图 1。系统适用性溶液中醋酸氯己定和对氯苯胺的保留时间分别为6.624 min和8.681 min,且醋酸氯己定与其降解杂质对氯苯胺分离度良好,最小分离度均大于要求的3.0,理论板数以醋酸氯己定计峰不低于7 000,空白溶剂、空白辅料不干扰本品中醋酸氯己定的检测。
|
1.醋酸氯已定(chlorhexidine acetate)2.对氯苯胺(p-chloroaniline) 图 1 空白辅料(A)、空白溶剂(B)、铝镁加混悬液自制品(C)、系统适用性溶液(D)高效液相色谱图 Fig.1 HPLC chromatograms of excipients(A), blank solvent(B), almagate suspension product(C), system suitability solution(D) |
分别精密量取“2.1.1”项下的醋酸氯己定对照品溶液和“2.1.2”项下的对氯苯胺对照品溶液适量,配制成系列浓度的线性溶液,按“2.2”项下的色谱条件分别进样分析测定其峰面积。以质量浓度(X,µg·mL-1)为横坐标,峰面积(Y)为纵坐标,绘制标准曲线。得醋酸氯己定和对氯苯胺回归方程:
| $Y=3.387 \times 10^{5} X+547.7 \quad r^{2}=1.000\\ Y=4.420 \times 10^{5} X-191.0 \quad r^{2}=0.995\;2 $ |
醋酸氯己定和对氯苯胺质量浓度分别在0.982~ 13.76 µg·mL-1和0.002~0.042 µg·mL-1范围内与峰面积线性关系良好。
2.5 精密度试验分别精密量取“2.1.1”项下的醋酸氯己定对照品溶液和“2.1.2”项下的对氯苯胺对照品溶液适量,分别配制成10 µg·mL-1的醋酸氯己定对照品溶液和0.05 µg·mL-1的对氯苯胺对照品溶液,按“2.2”项下的色谱条件连续进样6次,测定醋酸氯己定和对氯苯胺峰面积和保留时间,计算其RSD(n=6)。醋酸氯己定的保留时间的RSD为0.11%,峰面积的RSD为0.065%;对氯苯胺的保留时间RSD为0.042%,峰面积RSD为2.3%。结果表明本法测定醋酸氯己定和对氯苯胺精密度良好。
2.6 稳定性试验以“2.1”项下方法制备供试品溶液,按照“2.2”项下的色谱条件于制备后放置0、2、4、6、8、10、26、45 h进样测定其醋酸氯己定和对氯苯胺的峰面积,计算RSD分别为0.070%和10.6%。随着供试品溶液放置时间的延长,对氯苯胺峰面积有增长趋势。在0、2、4、6、8 h时其峰面积RSD分别为0.21%和2.8%,相对0 h的变化值在20%以内,符合要求,故供试品溶液需在室温8 h内完成检测。
2.7 重复性试验取20180301批次铝镁加混悬液,以“2.1”项下方法平行制备6份供试品溶液,按照“2.2”项下的色谱条件依次进行测定,混悬液中醋酸氯己定和对氯苯胺的平均含量分别为82.5%和0.015%(以醋酸氯己定的标示量计),RSD(n=6)分别为1.1%和5.3%,表明该方法的重复性良好。
2.8 回收率试验取20180301批次铝镁加混悬液,按“2.1”项下方法高、中、低每个浓度制备各3份供试溶液,按照“2.2”项下的色谱条件测定,计算9份供试品的平均回收率和RSD,结果见表 2。试验表明该方法准确性良好。计算公式如下:
|
|
表 2 回收率实验结果(n=9) Tab.2 Results of the recovery test |
| ${\rm{回收率 = }}\left( {{m_{\rm{测 }}} - {m_{{\rm{ 本底量}}}}} \right)/{m_{\rm{加}}} \times 100\% $ |
| $m_{\mathrm{加}}=C_{\mathrm{D}} \times C_{\mathrm{X}}=\frac{m_{\mathrm{D}} \times P_{1} \times V_{\mathrm{X}}}{m_{\mathrm{D}}} $ |
| ${m_{{\rm{测}}}} = \frac{{{A_{\rm{Y}}} \times {m_{\rm{D}}} \times {P_1} \times {V_{\rm{Y}}}}}{{{A_{\rm{D}}} \times {V_{\rm{D}}}}};{m_{{\rm{本底量}}}} = {m_{\rm{D}}} \times x $ |
CD:对照品的浓度;AY:供试品中醋酸氯己定或对氯苯胺峰面积;AD:醋酸氯己定或对氯苯胺对照品峰面积;VY:供试品稀释体积(mL);VD:对照品稀释体积(mL);VX:加入贮备液的体积(mL);mY:供试品称样量(g);mD:对照品称样量(mg);P1:对照品纯度(%);x:目标组分的含量(空白辅料中无醋酸氯己定,故本底量为0)
2.9 定量下限与检测下限取“2.1.1”项下的醋酸氯己定对照品溶液和“2.1.2”项下的对氯苯胺对照品溶液,逐级稀释后进样,以色谱峰峰高为基线噪音3倍计算醋酸氯己定和对氯苯胺的检测下限质量浓度分别为0.001 03 μg·mL-1和0.001 2 μg·mL-1,其中,对氯苯胺的检测下限为0.25 ng,占限度浓度的0.006 3%;以色谱峰峰高为基线噪音10倍计算醋酸氯己定和对氯苯胺的定量下限质量浓度分别为0.003 4 µg·mL-1和0.002 5 μg·mL-1,其中,对氯苯胺的定量下限为0.50 ng,占限度浓度的0.012 5%,满足分析方法的要求。
2.10 样品的测定取3批样品,分别按照“2.1”项下方法制备供试品溶液,按照“2.2”项下的色谱条件依次对本品进行测定,按标示量计算,结果见表 3。
|
|
表 3 铝镁加混悬液样品测定结果 Tab.3 Determination results of almagate suspension |
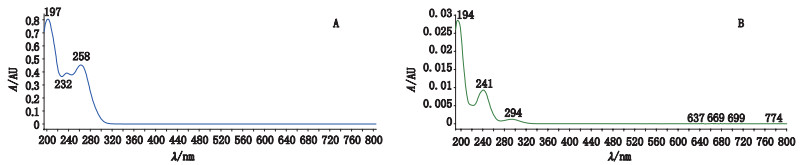
精密量取“2.1”项下对照品溶液适量,注入液相色谱仪(二极管阵列检测器,190~800 nm),记录色谱图,考察其吸收波长。结果见图 2。图谱表明在239 nm处醋酸氯己定与对氯苯胺均有较强吸收,故选用239 nm作为检测波长。
|
图 2 醋酸氯己定(A)和对氯苯胺(B)的紫外吸收图谱 Fig.2 Ultraviolet absorption spectra of chlorhexidine acetate(A)and p-chloroaniline(B) |
考察了不同流速(1.7、1.3、1.5、1.0 mL·min-1)对醋酸氯己定和对氯苯胺的检测影响,结果表明流速为1.0 mL·min-1时,未能检测到对氯苯胺的色谱峰,流速为1.7、1.5、1.3 mL·min-1时均符合检测要求,考虑方法的耐用性,确定流速为1.5 mL·min-1。
3.1.3 进样量的选择考察了不同进样量(50、100、150、200 μL)对醋酸氯己定和对氯苯胺的检测影响。不同的进样量结果对比说明,选择200 μL更能满足检测需求。
3.2 样品前处理提取条件的考察由于样品为混悬液,其中醋酸氯己定仅占0.01%,混悬液辅料中不溶组分较多,样品无法直接进样检测,实验过程中发现其体系黏度过大,不利于过滤,故选择样品前处理方式为离心并超声提取。为了提高其提取效率和检测的准确性,本研究对醋酸氯己定的前处理提取方法进行了考察并优化。
3.2.1 离心条件研究了不同的离心条件对醋酸氯己定的提取结果影响,表 4为不同离心条件下供试品中醋酸氯己定的提取结果。试验表明,延长离心时间的同时增加离心转速,有利于提高醋酸氯己定的提取效率;在离心时间为10 min,离心转速为13 000 r·min-1时,能获得澄清的上清液。
|
|
表 4 离心条件的考察结果 Tab.4 Results of centrifugation conditions |
研究了不同的超声条件对醋酸氯己定的提取效率的影响。试验表明超声时间分别为5、10、20 min时对本品中醋酸氯己定含量测定结果无影响,为保证样品提取完全且提高醋酸氯己定的前处理提取效率,选择超声条件为超声并辅助振摇10 min。
3.3 色谱条件耐用性试验分别考察了不同的流动相(A-B)比例(71:29、69.5:30.5)、不同的流动相pH(2.80、3.20)、不同检测波长(234、244 nm)、不同的流速(1.3、1.7 mL·min-1)以及不同的柱温(35、45 ℃)对醋酸氯己定和对氯苯胺含量测定的影响。结果表明上述各条件与原条件相比,含量结果基本一致,该检测方法耐用性良好。
3.4 小结本研究针对铝镁加混悬液中防腐剂醋酸氯己定及其降解杂质对氯苯胺进行研究。优化并建立了前处理提取方法,有效地提高了检测准确性。建立了同时测定铝镁加混悬液中醋酸氯己定和其降解杂质对氯苯胺含量的HPLC法,该方法简便、快捷,专属性和准确性良好,为铝镁加混悬液的质量研究提供了指导和参考。
| [1] |
夏永红, 钱平安, 厉旭光. 泮托拉唑、伊托必利和铝镁加联合治疗胃食管反流病疗效分析[J]. 药物与临床, 2011, 49(6): 59. XIA YH, QIAN PA, LI XG. Analysis on the curative effect of pantoprazole, itopril and aluminum magnesium combined in the treatment of gastroesophageal reflux disease[J]. Drugs Clin, 2011, 49(6): 59. |
| [2] |
王娟, 单桂芹, 曹嘉伽, 等. 康复新液联合铝镁加混悬液治疗放射性食管炎的疗效分析[J]. 现代肿瘤医学, 2018, 26(5): 699. WANG J, SHAN GQ, CAO JJ, et al. Curative effect analysis of Kangfuxinye combined with Al-Mg and suspension in the treatment of radiation esophagitis[J]. J Mod Oncol, 2018, 26(5): 699. DOI:10.3969/j.issn.1672-4992.2018.05.012 |
| [3] |
杨波.新型抗酸剂铝镁加的研究[D].沈阳: 沈阳药科大学, 2001 YANG B. Study on the Addition of Aluminum-magnesium as a New Antacid Agent[D]. Shenyan: Shenyang Pharmaceutical University, 2001 |
| [4] |
胡向青, 郝福, 李志刚, 等. 药物中杂质及有害物质控制限度的研究进展[J]. 现代药物与临床, 2014, 29(9): 953. HU XQ, HAO F, LI ZG, et al. Research progress on control limits of impurities and harmful substances in drugs[J]. Mod Med Clin Pract, 2014, 29(9): 953. |
| [5] |
陈震. 有关物质的研究与新药注册[J]. 中国医药工业杂志, 2010, 41(11): 872. CHEN Z. Research on related substances and registration of new drugs[J]. Chin J Pharm, 2010, 41(11): 872. DOI:10.3969/j.issn.1001-8255.2010.11.020 |
| [6] |
张哲峰. 药物杂质研究中风险控制的几个关键问题[J]. 现代药物与临床, 2010, 25(5): 327. ZHANG ZF. Several key problems of risk control in drug impurity research[J]. Mod Med Clin Pract, 2010, 25(5): 327. |
| [7] |
Almax F. Drug Instructions[EB/OL]. Amirail. Spain: 1984 (1993- 05-19). [2018-09-15]: https://detail.youzan.com/show/goods?alias=360gex8gu1hcu
|
| [8] |
ROWE RC, SHESKEY PJ, QUINN ME. Handbook of Pharmaceutical Excipients[M]. Milford: Pharmaceutical Press, 2009: 162.
|
| [9] |
ICH. M7: Assment and Control of DNA Reactive(Mutagenic)Impurities in Pharmaceuticals to Limit Potential Carcinogenic Risk[S]. 2010: 36
|
| [10] |
中华人民共和国药典2015年版.二部[S]. 2015: 1543 ChP 2015. Vol Ⅱ[S]. 2015: 1543 |
| [11] |
USP 40-NF 35. Vol Ⅱ[S]. 2017: 3364
|
| [12] |
EP 9. 0. Vol Ⅱ[S]. 2016: 2037
|
| [13] |
秦春华, 姜从良. 肤康凝胶中醋酸氯己定含量的测定[J]. 湖北中医杂志, 2015, 3(5): 63. QIN CH, JIANG CL. Determination of chlorhexidine acetate in Fukang gel[J]. Hubei J Tradit Chin Med, 2015, 3(5): 63. |
| [14] |
李小荣. 高效液相色谱法测定醋酸氯己定缓释凝胶中醋酸氯己定的含量[J]. 中国医院药学杂志, 2008, 10(19): 1727. LI XR. Determination of chlorhexidine acetate in sustained release gel of chlorhexidine acetate by high performance liquid chromatography[J]. Chin J Hosp Pharm, 2008, 10(19): 1727. DOI:10.3321/j.issn:1001-5213.2008.19.041 |
| [15] |
解素华, 闫阅. 高效液相色谱法测定脂质体制剂中醋酸氯己定的含量[J]. 药物分析杂志, 2006, 26(2): 263. XIE SH, YAN Y. Determination of chlorhexidine acetate in liposome preparation by high performance liquid chromatography[J]. Chin J Pharm Anal, 2006, 26(2): 263. |
| [16] |
姜韧, 柯可, 刘刚, 等. HPLC测定皮湿霜中苯佐卡因、地塞米松磷酸钠和醋酸氯己定含量[J]. 药物分析杂志, 2005, 25(11): 1336. JIANG R, KE K, LIU G, et al. Determination of benzocaine, dexamethasone sodium phosphate and chlorhexidine acetate in Pishi cream by HPLC[J]. Chin J Pharm Anal, 2005, 25(11): 1336. |
 2019, Vol. 39
2019, Vol. 39 
