2. 陕西瑞奇生物科技有限公司, 西安 710075;
3. 陕西省食品药品检验所, 西安 710065
2. Shaanxi Ruiqi Biotechnology Co., Ltd., Xi'an 710075, China;
3. Shaanxi Food and Drug Inspection Institute, Xi'an 710065, China
二氧化硫是一种无色,易溶于水,有刺激性气味的气体,其化学性质比较活泼,既具有氧化性又具有还原性,因此,常被用作保鲜剂和防腐剂。但过量的二氧化硫残留,易使服用者产生恶心、呕吐等胃肠道反应及眼、鼻黏膜刺激症状,严重时易产生喉头痉挛水肿等[1]。此外,硫熏对中药材有效成分产生影响:会导致百合中的有效成分含量都显著减少[2];也可以使当归的品质受到很大影响,阿魏酸含量由于硫熏降低[3-4];硫熏后黄芩中黄酮苷类成分呈下降趋势,黄芩苷含量变化明显[5]。同时,硫熏会使中药的pH下降,改变中药的性味归属[6]。调查结果[7-8]显示,中药材中二氧化硫残留量超标已经成为普遍现象。
为了严格控制中药材安全问题,国家制订了二氧化硫限量标准及检测方法。2015年版《中华人民共和国药典》中二氧化硫残留量测定法有3种方法,包括酸碱滴定法(第一法)、气相色谱法(第二法)和离子色谱法(第三法)。基于酸碱中和的滴定碘量法操作简单方便,但是对于有机酸含量高的样本,会导致滴定终点难以判定[9];比色法最常见的是盐酸副玫瑰苯胺法和蒸馏-比色法,由于其使用的试剂污染环境,而且本身有颜色的样本在比色分析时会产生干扰[10-12];气相色谱法及离子色谱法检测结果准确,但对实验人员和仪器要求高[13-14]。当然,还有其他的方法,如:示波极谱法,需要专业技术人员和昂贵的仪器设备[15];荧光法,易受溶液浓度、酸性强度等干扰,而且还需要荧光检测仪器[16]。因此,目前,市场上急需一种简单、便捷、易于携带的快速检测方法,能够快速检测出中药材中二氧化硫的残留量,为中药材使用企业和监管部门提供便利。
气体法是一种利用亚硫酸盐还原产生的硫化氢与醋酸铅反应生成硫化铅黑色示踪物,从而对中药材及中药饮片中二氧化硫残留进行检测的方法[17-18],它具有操作简单、灵敏度高和选择性好等优点,但通常存在使用的装置体积较大,材质易碎,不易携带,醋酸铅反应膜为手工制作,稳定性差等缺点。因此,本研究通过设计硅胶材质的专用反应瓶盖,将醋酸铅反应膜制备成试纸条,优化实验条件等改进措施,建立了一种操作简便,结果稳定的二氧化硫半定量快速检测试剂盒。
1 材料与方法 1.1 仪器和试药卷式贴膜一体机CTM 850、数控感应斩切机(上海金标有限公司生产);Milli-Q制水系统(密理博公司)。
锌粒、亚硫酸钠、氢氧化钠、盐酸,均为分析纯,国药集团化学试剂有限公司产品;5%(m/v)醋酸铅反应膜,由上海金标有限公司定制;二氧化硫反应瓶盖为陕西瑞奇生物科技有限公司专利产品(专利号:ZL201620703797.6)。
白芷、当归、茯苓、枸杞子、红花等74批次中药材来自于2016年9月至2018年9月陕西省食品药品检验所抽检留样。
1.2 方法 1.2.1 二氧化硫残留快速检测试剂盒的制备试剂盒的组成:0.125%(m/v)氢氧化钠、20%(v/v)盐酸溶液、锌粒;耗材:反应瓶盖、试纸条、反应瓶。
制备醋酸铅检测试纸条:在55 mm宽的聚氯乙烯(PVC)板上,在距1边9 mm处先覆盖1道双面胶。再每间隔7 mm,在双面胶上打一直径为5 mm的孔,同时在距同一边4 mm处打一直径为3 mm的小孔;然后将定制的已裁成9 mm宽的用5%醋酸铅浸泡的醋酸铅检测膜条粘到双面胶上,再在反应膜两边贴上单面胶,最后用裁切机以两个圆孔为检测试纸条中心将PVC板切成7 mm宽的试纸条,即得。
1.2.2 实验样品的制备取白芷、当归、茯苓、枸杞子、红花、沙苑子、黄柏、鸡血藤、灵芝、番泻叶、益母草、淫羊藿、紫苏叶、山药、天麻、白术、党参等共74种不同批次的样品,粉碎,分别称取1.0 g溶于5 mL 0.125% (m/v)氢氧化钠水溶液,水浴80 ℃,浸泡20 min,取出静置分层,取上清液作为待测样品。
1.2.3 气体法检测实验过程用移液枪准确吸取1 mL待测样品至反应瓶中,加入2粒锌粒(约0.7 g),将试纸条定位孔端插入反应瓶盖上定位,反应孔自然固定在瓶盖正中间,用7 μL双蒸水浸湿醋酸铅检测试纸条的检测膜,再加入20%(v/v)盐酸溶液1 mL,立即盖上反应瓶盖,25 ℃条件下,反应10 min,得到硫化铅深浅不同的斑点。
1.2.4 标准溶液的制备亚硫酸钠标准溶液:准确称取亚硫酸钠1 g至100 mL量瓶中,准确加超纯水至刻度,得10 g·kg-1溶液。分别量取10 g·kg-1的溶液0.2、0.6、1、1.6、3 mL至100 mL量瓶中,准确加超纯水至刻度,即可得浓度为20、60、100、160、300 mg·kg-1的亚硫酸钠标准溶液,对应的二氧化硫浓度即为10、30、50、80、150 mg·kg-1。
1.2.5 检测试剂盒线性范围及敏感度的确定向反应瓶中分别加上述不同浓度的标准溶液,按照“1.2.3”项下实验方法操作,得到不同浓度下的斑点,用Bandscan5.0软件分析灰度值,得到灰度与含量曲线。
1.2.6 试剂盒的稳定性试验将制备好的试剂盒常温下保存,每2个月用0、300、800 mg·kg-1的亚硫酸钠标准品(折合二氧化硫含量为0、150、400 mg·kg-1),按“1.2.3”项下实验方法检测。得到放置不同时间试剂对亚硝酸钠的检测灰度斑点,用Bandscan 5.0软件分析灰度值,考察试剂盒的稳定性。
1.2.7 样品测定称取74份中药材样品,按方法“1.2.2”项下方法制备供试品溶液,按方法“1.2.3”项下方法测定,将所得的灰度斑点,用试剂盒标准色卡对比,半定量读值。同时按2015年版《中华人民共和国药典》第三法(离子色谱法)做平行测定,然后进行对比。
2 结果 2.1 二氧化硫检测试纸条的制备在洁净车间控温控湿,利用卷式贴膜一体机CTM 850,将PVC板、双面胶、醋酸铅反应膜、单面胶、一次性粘贴打孔做成试纸条,用数控感应斩切机,当感应到定位孔后,对试纸条进行斩切,试纸条结构见图 1。

|
1. PVC薄板(PVC sheet) 2.单面胶(one-sided gum) 3.醋酸铅反应膜(lead acetate reaction film) 4.双面胶(double-sided gum) 5.反应孔(reaction hole) 6.定位孔(positioning hole) 图 1 醋酸铅检测试纸条结构示意图 Fig.1 Structure diagram of the lead acetate test strip |
试剂盒反应后得到不同浓度下的显色斑点(见图 2),用Bandscan 5.0软件分析灰度值,以灰度Y为纵坐标,二氧化硫含量X为横坐标,进行线性回归,得回归方程:
| $ Y=59.45 X-93.39 \quad r^{2}=0.9979 $ |

|
1. 0 mg·kg-1 2. 10 mg·kg-1 3. 30 mg·kg-1 4. 50 mg·kg-1 5. 80 mg·kg-1 6. 120 mg·kg-1 图 2 不同浓度二氧化硫斑点图 Fig.2 The speckle diagrams of SO2 different concentration |
二氧化硫含量线性范围10~150 mg·kg-1。
2.3 试剂盒敏感度的确定试剂盒对二氧化硫检测的灰度与含量线性范围为10~150 mg·kg-1,样本经过5倍稀释后,试剂盒的检测范围可以扩大为10~750 mg·kg-1,试剂盒的敏感度为10 mg·kg-1。参考2010年版《中华人民共和国药典》第二增补本中对中药材中二氧化硫的限量要求[19],制作二氧化硫半定量检测标准色卡(见图 3)。

|
图 3 二氧化硫半定量标准色卡 Fig.3 Sulfur dioxide semi-quantitative standard color cards |
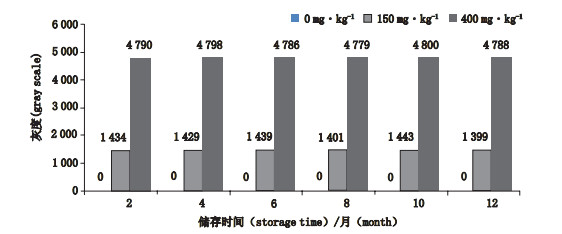
将试剂盒在常温下储存12个月,用0、300、800 mg·kg-1的亚硫酸钠标准品(折合二氧化硫浓度为0、150、400 mg·kg-1)每2个月检测1次,将显色斑点用Bandscan 5.0软件进行灰度分析,其检测值基本保持一致(见图 4)。
|
图 4 二氧化硫灰度与储存时间关系 Fig.4 Greyscale of sulphur dioxide and its storage time |
将74批次的中药饮片,用本试剂盒检测,每批次测定2次,取其灰度平均值,用标准曲线换成二氧化硫含量。同时按照2015年版《中华人民共和国药典》第三法(离子色谱法)对中药饮片进行检测,每批次测定2次,取其结果平均值,将2种方法的测定结果进行对比判定,结果见表 1。
|
|
表 1 试剂盒检测结果与2015年版《中华人民共和国药典》第三法检测结果比较 Tab.1 Comparison between the results of this kit and the third method of Chinese Pharmacopoeia 2015 |
二氧化硫熏蒸不但影响中药材的质量,而且对使用者产生严重的不良反应。2010年版《中华人民共和国药典》第二增补本对二氧化硫的限量规定:中药材及饮片(矿物来源的中草药材除外)中亚硫酸盐残留量(以二氧化硫计)不得超过150 mg·kg-1,山药、牛膝、粉葛、天冬、天麻、天花粉、白及、白芍、白术、党参等10种中药材及其饮片中亚硫酸盐残留量不得超过400 mg·kg-1。因此,中药材中二氧化硫残留快速检测试剂盒的建立具有十分重要的现实意义。本研究建立的快速检测试剂盒通过氢氧化钠将熏蒸的二氧化硫提取出来形成亚硫酸盐,在酸性条件下,与锌和盐酸反应生成硫化氢气体,硫化氢再与湿润的醋酸铅试纸反应生成硫化铅黑色沉淀在试纸条上,根据显色灰度的深浅可半定量地快速确定药材中二氧化硫的残留量。检测反应原理方程式:
| $ \begin{aligned} \mathrm{SO}_{2}+2 \mathrm{NaOH}=\mathrm{Na}_{2} \mathrm{SO}_{3}+\mathrm{H}_{2} \mathrm{O} \\ 8 \mathrm{HCl}+3 \mathrm{Zn}+\mathrm{Na}_{2} \mathrm{SO}_{3}=3 \mathrm{ZnCl}_{2}+2 \mathrm{NaCl}+\mathrm{H}_{2} \mathrm{S} \uparrow+3 \mathrm{H}_{2} \mathrm{O} \\ \mathrm{H}_{2} \mathrm{S}+\mathrm{Pb}(\mathrm{Ac})_{2}=\mathrm{PbS} \downarrow+2 \mathrm{HAc} \end{aligned} $ |
试剂盒中的反应瓶盖专用设计,硅胶材质,可以有效避免酸碱等化学试剂腐蚀;瓶盖上有试纸条插槽,插槽与瓶体联通,它们构成一个整体,无需组装可稳定固定试纸条,有利于瓶内气体与试纸条上的醋酸铅反应膜准确充分地反应。醋酸铅试纸条是检测的关键,试纸条显色的深浅体现了二氧化硫残留量的多少。为了保证试纸条的精度,专门定制醋酸铅反应膜,保证试纸每个横截面的浸泡时间和浓度一致。由于醋酸铅反应膜较软,在操作时容易损坏,在生产时,先覆盖双面胶,再打孔,然后贴醋酸铅检测膜。考虑到试纸条是以插拔的方式固定到反应瓶盖上,因此试纸条两头贴上单面胶(图 1),防止反应膜在插入反应瓶盖的过程中被损坏。定位孔在裁切成条时起到识别作用,在插入瓶盖时,起到定位作用。在生产检测试纸条时控制温湿度条件,由机器精密组装、定位和裁切,保证试纸条的质量稳定可靠。通过检测组件的定制,缩小反应体积,优化实验过程,使检测操作模块化,大大缩短了反应时间,整个检测过程可在30 min内完成。
从二氧化硫含量与灰度标准曲线可知,当二氧化硫含量在0~150 mg·kg-1范围内时线性良好,但当二氧化硫含量等于或低于10 mg·kg-1时,斑点灰度很浅,用Bandscan 5.0软件分析时,灰度值为0,所以确定检测下限为10 mg·kg-1;当二氧化硫实际含量大于150 mg·kg-1时会出现斑点显色过深无法判读,可将样品稀释5倍,检测后换算的浓度再乘以5。最终试剂盒检测范围扩展为10~750 mg·kg-1,敏感度为10 mg·kg-1,同时制备的半定量标准色卡(图 4)范围也包括了2015年版《中华人民共和国药典》对中药材二氧化硫限量的2个最高限150 mg·kg-1和400 mg·kg-1,便于在实际应用中检测结果的快速判定。
试剂盒常温储存12个月,每2个月检测1次,用Bandscan 5.0软件分析检测的斑点灰度可以精确地判断试剂盒稳定性是否有变化。结果表明,试剂盒对高、中、低含量的亚硫酸钠检测结果均保持稳定(图 4)。这是因为试剂盒所用的试纸条属于干化学物质,自然环境下稳定;所用的试剂稀氢氧化钠溶液(密闭塑料瓶保存)、浓盐酸(密闭玻璃瓶保存)和锌粒,其在密闭的环境内也都相当稳定,从而保证了试剂盒整体检测效果的稳定性。
本方法的检测目标是二氧化硫,自然界中与硫相似属性的元素是氧,在本检测方法条件下,不会反应生成硫化铅而显色。由反应原理来分析,可能干扰检测反应的是中药材内源性的硫,但通过文献查得内源性的硫一般以氨基硫的形式存在,在本检测方法条件下,不会反应显色。从本次74种不同批次的中药材样品的对比验证结果来看,本检测方法与药典中离子色谱法的检测结果一致,没有干扰出现。所以,本试剂盒只针对外源添加的二氧化硫进行半定量检测,所以该检测方法对二氧化硫的检测是高度特异的。
通过74种不同批次的中药材样品的对比验证,试剂盒检测结果与2015年版《中华人民共和国药典》方法检测的结果基本一致。其中有2个样本(枸杞子和党参)由于二氧化硫的含量超过试剂盒的检测上限(表 1),斑点显色极深,已经超出标准色卡检测上限,所以与2015年版《中华人民共和国药典》第三法检测的浓度值相差非常大,但两者判定结果是一致的。因此,本研究建立的二氧化硫残留快速检测试剂盒,不但在数10 min内只需简单的几步即可完成对中药材二氧化硫残留的半定量检测,而且可有效地排除中药材本身颜色的干扰,是一种稳定可靠、便捷快速的中药材二氧化硫半定量检测工具。
| [1] |
薛雯, 薛健, 孙晖, 等. 中药材二氧化硫残留的危害及检测研究[J]. 辽宁中医杂志, 2011, 38(12): 2431. XUE W, XUE J, SUN H, et al. Harmfulness and research of the sulfur dioxide residue in Chinese herbal medicine[J]. Liaoning J Traditi Chin Med, 2011, 38(12): 2431. |
| [2] |
李林, 张志杰, 蔡宝昌, 等. 硫熏对百合有效成分的影响[J]. 上海中医药大学学报, 2006, 20(1): 64. LI L, ZHANG ZJ, CAI BC, et al. Effect of sulphur fumigation on the effective components of Lily[J]. Acta Univ Tradit Med Sin Pharm Shanghai, 2006, 20(1): 64. DOI:10.3969/j.issn.1008-861X.2006.01.021 |
| [3] |
拱健婷, 王大仟, 张金霞, 等. 硫磺熏蒸对当归品质影响及其替代技术研究进展[J]. 中南药学, 2018, 16(6): 793. GONG JT, WANG DQ, ZHANG JX, et al. Effect of sulfur-fumigation on the quality of Angelica sinensis and research advance in alternative technology[J]. Central South Pharm, 2018, 16(6): 793. |
| [4] |
李成义, 王延惠, 李硕, 等. 硫熏对不同等级当归中阿魏酸含量的影响[J]. 中国现代中药, 2011, 13(12): 36. LI CY, WANG YH, LI S, et al. Effect of sulphur fumigation on the contents of ferulic acid inangelicae Sinensis Radix of different levels[J]. Mod Chin Med, 2011, 13(12): 36. DOI:10.3969/j.issn.1673-4890.2011.12.009 |
| [5] |
肖凌, 姜涛, 聂晶, 等. 硫磺熏蒸对黄芩药材及饮片质量影响分析[J]. 中国中药杂志, 2016, 41(12): 2216. XIAO L, JIANG T, NIE J, et al. Impact of sulfur fumigation on quality of Scutellariae Radix[J]. China J Chin Mater Med, 2016, 41(12): 2216. |
| [6] |
谢云龙, 雪鹏. 硫磺熏对10味中药pH值的影响[J]. 中国现代医学杂志, 2001, 11(7): 95. XIE YL, XUE P. Effect of sulphur fumigation on the pH of 10 traditional Chinese medicines[J]. China J Mod Med, 2001, 11(7): 95. DOI:10.3969/j.issn.1005-8982.2001.07.049 |
| [7] |
陈琴鸣, 周海燕, 吴应春.23种市售中药材中二氧化硫残留量的测定与分析[C].第二届浙江中西部科技论文集(药学分卷), 2005: 95 CHEN QM, ZHOU HY, WU YC.Determination of Sulfur Dioxide in 23 Chinese Medicinal Materials from Markets by Optimized Monier-Williams Method[C]. The Second Collection of Science and Technology in Central and Western Zhejiang Province(Drug Credit Volume), 2005: 95 |
| [8] |
孙磊, 金红宇, 马双成, 等. 中药中二氧化硫残留的检测方法与最大残留限量分析[J]. 中国药品标准, 2012, 13(1): 16. SUN L, JIN HY, MA SC, et al. Determination method and maximum residue limit of sulfur dioxide in traditional Chinese medicine[J]. Drug Stand China, 2012, 13(1): 16. DOI:10.3969/j.issn.1009-3656.2012.01.006 |
| [9] |
周晓琴. 食品中亚硫酸盐测定方法的改进)[J]. 凯里学院学报, 2010, 28(3): 58. ZHOU XQ. Improvement of the determination of sulfurous acid salt in the food[J]. J Kaili Univ, 2010, 28(3): 58. DOI:10.3969/j.issn.1673-9329.2010.03.20 |
| [10] |
刘宏芳, 许卓望. 无汞吸收盐酸副玫瑰苯胺比色法快速测定硫磺熏蒸食品中二氧化硫[J]. 中国调味品, 2006, 5(5): 21. LIU HF, XU ZW. Rapid determination of sulfur dioxide content in sulfur-smoked foods by pararosaniline hydrocloride with non-mercury absorption treatment[J]. China Condim, 2006, 5(5): 21. DOI:10.3969/j.issn.1000-9973.2006.05.005 |
| [11] |
郎涛. 无汞吸收-盐酸副玫瑰苯胺比色法测定食品中的亚硫酸盐[J]. 食品工业科技, 2009, 6: 348. LANG T. Determination of sulfite in foods by pararosaniline hydrocloride with non-mercury absorption treatment[J]. Sci Technol Food Ind, 2009, 6: 348. DOI:10.3969/j.issn.1673-9078.2009.04.002 |
| [12] |
杨娜, 李辉. 盐酸副玫瑰苯胺比色法测定红枣中亚硫酸盐含量方法及注意事项[J]. 食品安全导刊, 2015(27): 166. YANG N, LI H. Method and note for determination of sulfate in central Asia of Jujube[J]. China Food Saf Mag, 2015(27): 166. |
| [13] |
车镇涛, 宗玉英. 离子色谱法测定常用药食两用中药材中的二氧化硫含量[J]. 中药材, 2006, 29(5): 444. CHE ZT, ZONG YY. Determination of sulphur dioxide in commonly used Chinese herbal medicines with both food and medicine function for health care by ion-chromatographic method[J]. J Chin Med Mater, 2006, 29(5): 444. DOI:10.3321/j.issn:1001-4454.2006.05.014 |
| [14] |
吴越, 王玉, 梅雪艳, 等. 在线渗析-离子色谱法检测中药材中二氧化硫残留量[J]. 药物分析杂志, 2014, 34(1): 155. WU Y, WANG Y, MEI XY, et al. Determination of sulfur dioxide residues in Chinese materia medica by inline dialysis-ion chromatography[J]. Chin J Pharm Anal, 2014, 34(1): 155. |
| [15] |
张添, 周心怡, 于涛. 示波极谱法测定食品中的二氧化硫[J]. 无锡轻工大学学报, 2003, 5(22): 72. ZHANG T, ZHOU XY, YU T. Determination of sulfur dioxide in food by oscilloscopic polarography[J]. J Wuxi Univ Light Ind, 2003, 5(22): 72. |
| [16] |
YE Z, DUAN C, SHENG R, et al. A novel colorimetric and ratiometric fluorescent probe for visualizing SO2 derivatives in environment and living cells[J]. Talanta, 2018, 176: 389. DOI:10.1016/j.talanta.2017.08.054 |
| [17] |
陈寿春. 重要无机化学反应[M]. 上海: 上海科学技术出版社, 1986: 917. CHEN SC. Important Inorganic Chemical Reactions[M]. Shanghai: Shanghai Science Technology Press, 1986: 917. |
| [18] |
郝延军, 徐秋阳, 桑育黎, 等. 硫熏中药材的快速检测方法研究[J]. 中国中药杂志, 2012, 37(3): 335. HAO YJ, XU QY, SANG YL, et al. Study on the rapid detection method of Chinese materia medica with sulphur[J]. China J Chin Mater Med, 2012, 37(3): 335. |
| [19] |
中华人民共和国药典2010年版.第二增补本[S]. 2010: 179 ChP 2010.Supl Ⅱ[S]. 2010: 179 |
 2019, Vol. 39
2019, Vol. 39 
