2. 中国人民解放军空军军医大学第一附属医院药剂科, 西安 710032
2. Department of Pharmacy, the First Affiliated Hospital of PLA Air Force Military Medical University, Xi'an 710032, China
复方他扎罗汀丙酸氯倍他索软膏是一种新型复方外用制剂,其主成分为他扎罗汀(tazarotene,图 1),即6-[(3,4-二氢-4,4-二甲基-2H-1-苯并噻喃-6-基)乙炔基]-3-吡啶羧酸乙酯,和丙酸氯倍他索(clobetasol propionate,图 1),即16β-甲基- 11β-羟基-17-(1-氧代丙基)-9-氟-21-氯-孕留-1,4-二烯-3,20-二酮,用于治疗寻常型银屑病。他扎罗汀是原药,在体外无活性,体内经酯酶水解为活性代谢产物他扎罗汀酸,而他扎罗汀酸主要作用于皮肤,选择性高,是最适合皮肤外用的维A酸类药物[1-3]。丙酸氯倍他索作为高效局部外用糖皮质激素类药物,在临床上应用广泛,常制成外用制剂用于银屑病的治疗[4-5],并且常与其他外用制剂或治疗方法联合使用,如他扎罗汀乳膏、窄谱中波紫外线疗法(NB-UVB疗法),从而提高疗效[6-8]。本文的研究对象即为该新型复方外用制剂,名为复方他扎罗汀丙酸氯倍他索软膏,为我国自主研制,已申请发明专利[9],未见文献报道和研究。欧洲药典9.0版及《中华人民共和国药典》二部(2015年版)已收载丙酸氯倍他索质量标准,他扎罗汀质量标准仅在《中华人民共和国药典》二部(2015年版)有收载[10-11]。他扎罗汀、丙酸氯倍他索的质量研究已分别有文献报道[12-15],但复方他扎罗汀丙酸氯倍他索软膏有关物质的系统研究及鉴定未见报道。
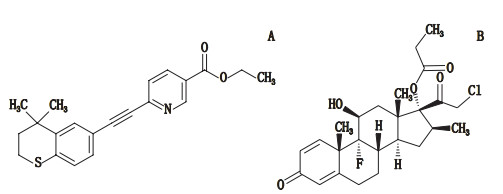
|
图 1 他扎罗汀(A)及与丙酸氯倍他索(B)化学结构图 Fig.1 Chemical structures of tazarotene(A) and clobetasol propionate(B) |
本研究建立了适用于复方他扎罗汀丙酸氯倍他索软膏有关物质检查的色谱-质谱联用分析方法,通过ESI+-TOF/MS测定其有关物质的精密相对分子质量及分子式,结合MS/MS的子离子特征,综合鉴定其有关物质的结构,为复方他扎罗汀丙酸氯倍他索软膏的质量控制提供了参考依据。
1 仪器、药品与试剂 1.1 仪器Agilent 1290 Infinity液相色谱-6224飞行时间质谱仪,Agilent Mass Hunter Qualitative Analysis软件(Agilent公司);Thermo Dionex Ultimate 3000高效液相色谱-TSQ Quantum Ultra型LC-MS/MS联用仪,Xcalibur 3.0数据处理系统(Thermo Fisher公司),BS 21S分析天平(Sartorius公司)。
1.2 药品与试剂复方他扎罗汀丙酸氯倍他索软膏(批号20180115,江苏知原药业有限公司);有关物质对照品(他扎罗汀亚砜、氯倍他索、17α-螺环化合物,加拿大TRC Research Chemicals Inc;他扎罗汀酸,江苏小林制药有限公司合成)。乙酸铵、甲酸(分析纯,南京化学试剂有限公司),甲醇(色谱纯,TEDIA公司),乙腈(色谱纯,TEDIA公司),水(市售娃哈哈纯净水)。
2 方法 2.1 色谱条件采用Phecda C18(4.6 mm×250 mm,5 μm)色谱柱,以0.1%乙酸铵/0.2%甲酸水溶液-甲醇-乙腈(70:21:9)为流动相A,甲醇-乙腈(70:30)为流动相B,线性梯度洗脱[0~35 min,A-B(40:60)→A-B(20:80);35~37 min,A-B(20:80)→A-B(0:100);37~47 min,A-B(0:100);47~48 min,A-B(0:100)→A-B(40:60);48~55 min,A-B(40:60)],流速1.0 mL·min-1,柱温25 ℃,检测波长240 nm(用于检测丙酸氯倍他索有关物质)和325 nm(用于检测他扎罗汀有关物质),进样量20 μL,分流比1:1进行MS检测。
2.2 质谱条件电喷雾正离子化,TOF/MS测定喷雾电压3.5 kV,雾化氮气压力275 kPa,流量10 L·min-1,温度350 ℃,碎片电压135 V,参比离子m/z 121.050 8(质子化嘌呤,C5H5N4+)和m/z 922.009 8(质子化氟代膦嗪HP-921,C18H19O6N3P3F24+),质量数扫描范围m/z 100~1 000。MS/MS测定的喷雾电压4 kV,雾化气压力300 kPa,辅助气压力35 kPa,毛细管温度350 ℃,二级质谱扫描碰撞氩气压力0.16 Pa,碰撞能量10~30 eV。
2.3 溶液配制 2.3.1 供试品溶液取复方他扎罗汀丙酸氯倍他索软膏1 g,精密称定,置10 mL量瓶中,精密加甲醇5 mL,55 ℃加热5 min并充分振摇使他扎罗汀和丙酸氯倍他索溶解,冰浴30 min后取上清液,以0.45 μm有机系滤膜过滤,取续滤液即得。
2.3.2 混合有关物质对照品溶液取有关物质他扎罗汀亚砜、他扎罗汀酸、氯倍他索、17α-螺环化合物的对照品适量,精密称定,加甲醇溶解并定量稀释成质量浓度均约为1.0 μg·mL-1的溶液,即得。
2.3.3 强制降解试验溶液精密称取复方他扎罗汀丙酸氯倍他索软膏1 g,置10 mL量瓶中,分别经1.0 mL酸(0.1 mol·L-1盐酸甲醇溶液)60 ℃水浴5 h,0.5 mL碱(0.01 mol·L-1氢氧化钠甲醇溶液)60 ℃水浴15 min,0.5 mL 3%过氧化氢甲醇溶液60 ℃水浴30 min,高温(90 ℃)水浴12 h,光照(4 500 lx)条件下照射12 h处理,然后均加入甲醇5 mL,55 ℃加热5 min并充分振摇使他扎罗汀和丙酸氯倍他索溶解,冰浴30 min后取上清液,使用0.45 μm有机系滤膜迅速过滤,取续滤液作为他扎罗汀质量浓度约为200 μg·mL-1和丙酸氯倍他索质量浓度约为100 μg·mL-1的强制降解试验溶液。同法配制空白溶液。
3 结果 3.1 有关物质检查建立的复方他扎罗汀丙酸氯倍他索软膏有关物质挥发性流动相HPLC检查方法适用于质谱联用鉴定。图 2、3分别为复方他扎罗汀丙酸氯倍他索软膏供试品溶液及强制降解试验溶液的325 nm(他扎罗汀)和240 nm(丙酸氯倍他索)HPLC叠加色谱图,共检出12个主要有关物质,分别按各自波长下保留时间从小到大顺序编号,325 nm下检出有关物质1~7,240 nm下检出有关物质8~12。
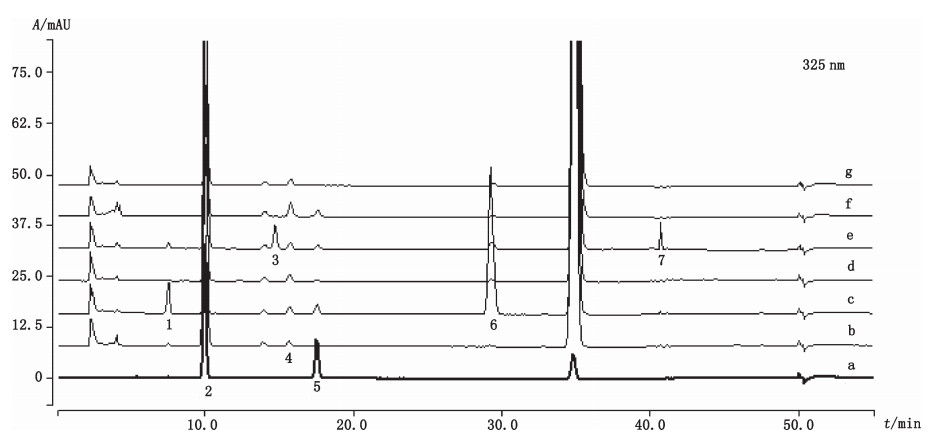
|
1~7.同表 1(same as Tab. 1) a.对照品溶液(reference solution)b.氧化破坏溶液(forced degradation solution under oxidation stress)c.碱破坏溶液(forced degradation solution under base stress)d.光照破坏溶液(forced degradation solution under photolysis stress)e.酸破坏溶液(forced degradation solution under acid stress)f.高温破坏溶液(forced degradation solution under heat stress)g.供试品溶液(test sample solution) 图 2 复方他扎罗汀丙酸氯倍他索软膏及其强制降解试验溶液的高效液相色谱图(325 nm) Fig.2 HPLC chromatograms of compound tazarotene and clobetasol propionate ointment and its forced degradation solutions (325 nm) |
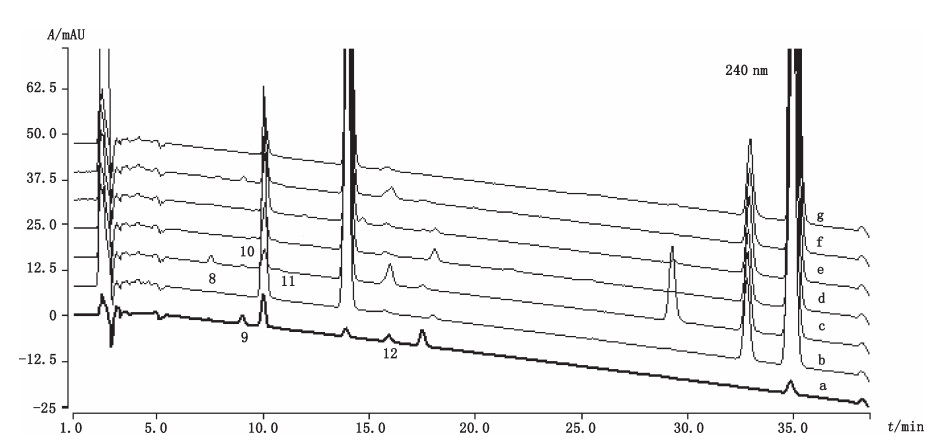
|
8~12.同表 1(same as Tab. 1) a~f.同图 2(same as Fig. 2) 图 3 复方他扎罗汀丙酸氯倍他索软膏及其强制降解试验溶液的高效液相色谱图(240 nm) Fig.3 HPLC chromatograms of compound tazarotene and clobetasol propionate ointment and its forced degradation solutions (240 nm) |
复方他扎罗汀丙酸氯倍他索软膏样品共检出3个有关物质,为有关物质2、4、6,均为325 nm下他扎罗汀的有关物质,而240 nm下未见明显有关物质。强制降解试验表明,复方他扎罗汀丙酸氯倍他索软膏中他扎罗汀稳定性较差,在强制降解试验中主要降解为有关物质1~7,根据与混合有关物质对照品溶液的比较,确定有关物质2为他扎罗汀亚砜,有关物质5为他扎罗汀酸,同时根据二级碎片离子特征解析出有关物质6为文献中报道的他扎罗汀酸甲酯[16]。丙酸氯倍他索较稳定,强制降解条件较剧烈,而产生有关物质含量较低,主要为有关物质8~12,根据与混合有关物质对照品溶液的比较,确定有关物质9为氯倍他索,有关物质12为17α-螺环化合物,同时根据二级碎片离子特征解析出有关物质8和11分别为欧洲药典记载的有关物质A(倍他米松17-丙酸酯)和K(倍他米松21-丙酸酯)。酸破坏检测到7个降解产物(有关物质1~7),碱破坏检测到9个降解产物(有关物质1、2、4~6、8、9、11和12),光照破坏检测到4个降解产物(有关物质2、4、6和10),氧化破坏检测到4个降解产物(有关物质1、2、4和12),高温破坏检测到5个降解产物(有关物质2、4、5、9和12)。
3.2 有关物质的结构鉴定采用TOF/MS测得各有关物质母离子的准确质量和分子式,三重四极杆获得二级质谱碎片信息,通过与主成分及已知有关物质质谱特征的对比分析,鉴定各有关物质的结构,结果见表 1和图 4。
|
|
表 1 复方他扎罗汀丙酸氯倍他索软膏有关物质结构的液质联用鉴定结果 Tab.1 The structures of the related substances of compound tazarotene and clobetasol propionate ointment identified by LC-MS |

|
图 4 复方他扎罗汀丙酸氯倍他索软膏有关物质1~12化学结构图 Fig.4 Chemical structures of the related substances 1-12 of compound tazarotene and clobetasol propionate ointment |
通过对他扎罗汀及有关物质2(他扎罗汀亚砜)和有关物质5(他扎罗汀酸)的一级质谱母离子准确质量、二级质谱特征碎片离子和裂解途径(图 5和图 6)的分析,可以辅助其未知有关物质结构的推断与鉴定。
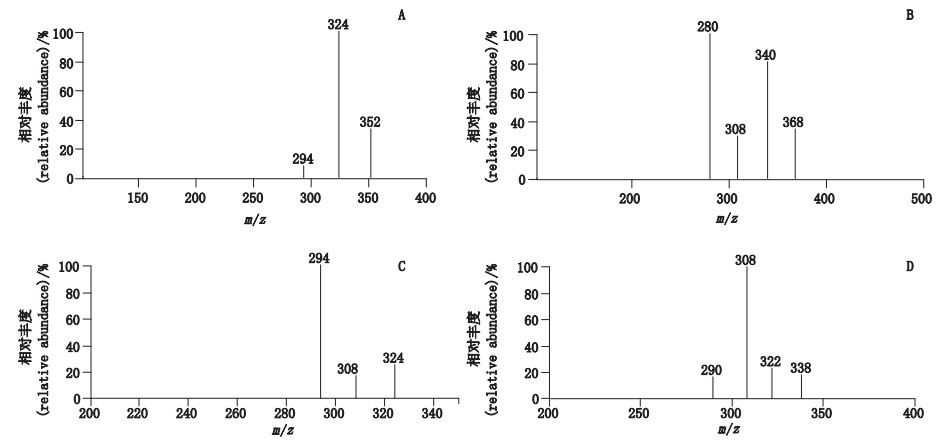
|
A.他扎罗汀(tazarotene,m/z 352)B.有关物质2(related substance 2,m/z 368)C.有关物质5(related substance 5,m/z 324)D.有关物质6(related substance 6,m/z 338) 图 5 他扎罗汀及其已知有关物质的二级质谱图 Fig.5 MS/MS spectra of tazarotene and its known related substances |
|
图 6 他扎罗汀及其已知有关物质的裂解途径 Fig.6 MS/MS fragmentation pathways of tazarotene and its known related substances |
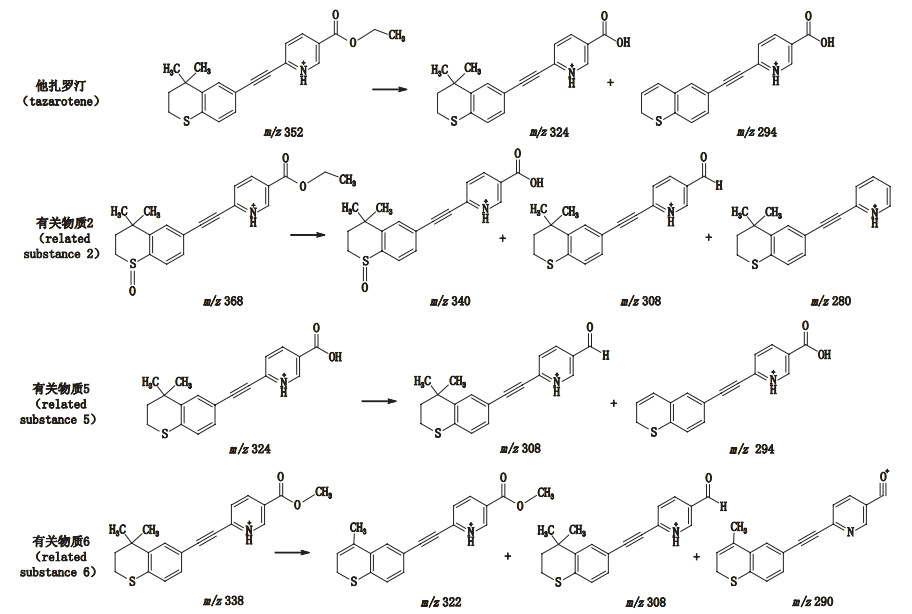
他扎罗汀及其已知有关物质裂解规律如下:
① 他扎罗汀及有关物质2的母离子中,3-吡啶羧酸乙酯脱去乙基,生成质量数少28的特征碎片离子。
② 他扎罗汀及有关物质5的母离子中,苯并噻喃环上的甲基脱落,生成m/z 294特征碎片离子;有关物质6同样裂解规律下形成m/z 322特征碎片离子。
③ 有关物质5和6的母离子中,3-吡啶羧酸酯处的酯键断裂,生成m/z 308特征碎片离子。
④ 有关物质2的母离子3-吡啶羧酸乙酯处的酯键断裂,同时苯并噻喃环上的甲基脱落形成m/z 308特征碎片离子;有关物质6同样裂解规律下生成m/z 290特征碎片离子。
3.2.2 未知有关物质的确证通过有关物质HPLC定位及质谱特征,结合他扎罗汀及已知有关物质的裂解规律,对各未知有关物质进行综合分析并鉴定其结构。
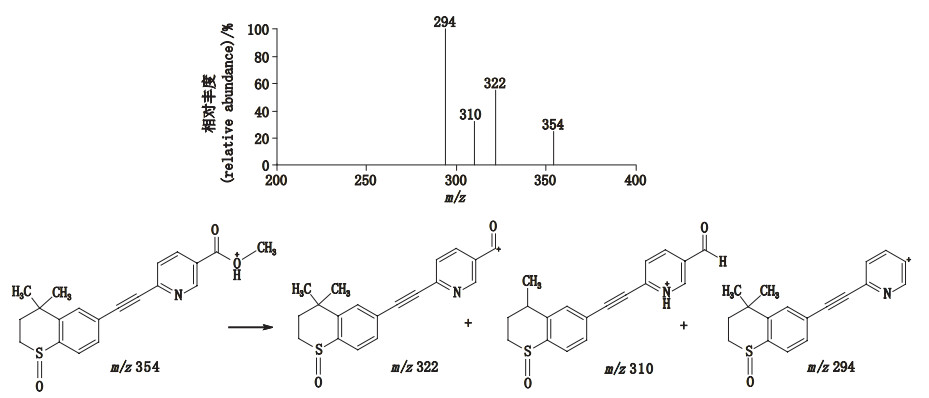
有关物质1:采用ESI+-TOF/MS测得有关物质1 [M+H]+的准确质量为354.116 3,与离子式C20H20NO3S+相应,与已知有关物质2(他扎罗汀亚砜)相比,其质量数少14,离子式少CH2,对应1个亚甲基,推测其为他扎罗汀亚砜与甲醇发生酯交换的产物。MS/MS主要特征碎片离子为m/z 322、310、294,其中m/z 294比已知有关物质2的m/z 308碎片离子质量数少14,有关物质1吡啶羧酸甲酯的酯键断裂形成m/z 322的碎片离子,再脱甲基形成m/z 310的碎片离子。质谱裂解(图 7)均得到合理归属。
|
图 7 有关物质1[M+H]+离子的二级质谱图及其裂解途径 Fig.7 MS/MS spectrum and fragmentation pathways of [M+H]+ ions of related substance 1 |
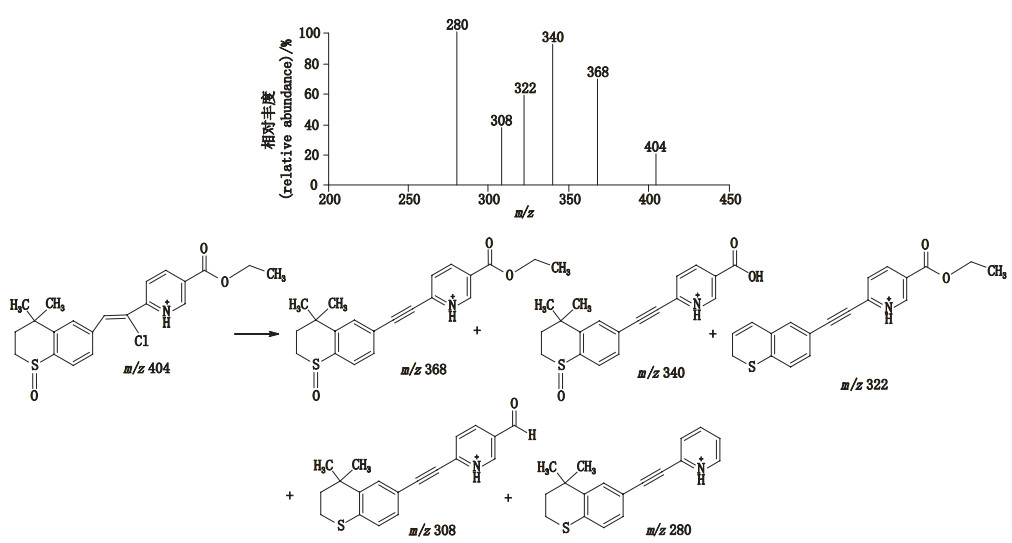
有关物质3:采用ESI+-TOF/MS测得有关物质3 [M+H]+的准确质量为404.108 7,与离子式C21H23ClNO3S+相应,与已知有关物质2(他扎罗汀亚砜)相比,其质量数多36,离子式多HCl,推测其为他扎罗汀亚砜与盐酸反应的产物。MS/MS主要特征碎片离子为m/z 368、340、322、308、280,其中m/z 340、308、280与已知有关物质2的碎片离子一致,而m/z 368则与有关物质2的母离子一致,说明有关物质3应为他扎罗汀亚砜的炔键与盐酸发生加成反应的产物,质谱裂解(图 8)均得到合理归属。
|
图 8 有关物质3[M+H]+离子的二级质谱图及其裂解途径 Fig.8 MS/MS spectrum and fragmentation pathways of [M+H]+ ions of related substance 3 |
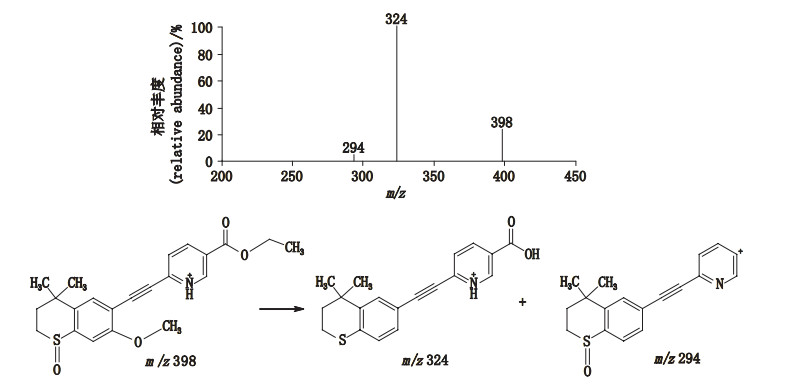
有关物质4:采用ESI+-TOF/MS测得有关物质4[M+H]+的准确质量为398.142 3,与离子式C22H24NO4S+相应,与已知有关物质2(他扎罗汀亚砜)相比,其质量数多30,离子式多CH2O,推测其为他扎罗汀亚砜与甲醇反应的产物。MS/MS主要特征碎片离子为m/z 324、294,m/z 324与主成分他扎罗汀的碎片离子一致,m/z 324是由苯并噻喃环脱甲基和亚砜后环合形成的碎片离子,质谱裂解(图 9)均得到合理归属。
|
图 9 有关物质4[M+H]+离子的二级质谱图及其裂解途径 Fig.9 MS/MS spectrum and fragmentation pathways of [M+H]+ ions of related substance 4 |
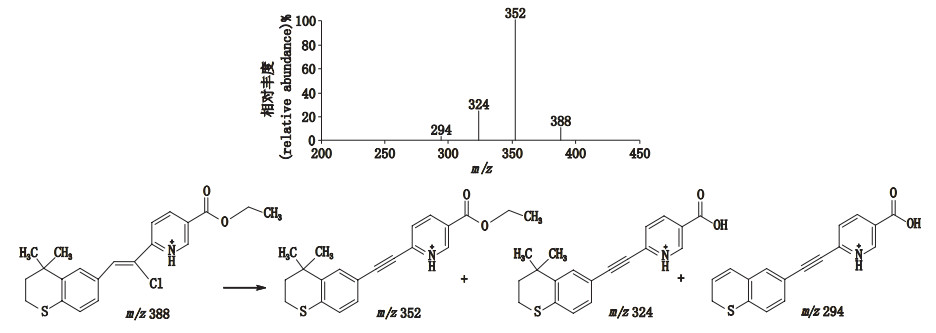
有关物质7:采用ESI+-TOF/MS测得有关物质7[M+H]+的准确质量为388.112 1,与离子式C21H23ClNO2S+相应,与他扎罗汀相比,其质量数多36,离子式多HCl,推测其为他扎罗汀与盐酸反应的产物。MS/MS主要特征碎片离子为m/z 352、324、294,其中m/z 324、294与他扎罗汀的碎片离子一致,而m/z 352则与他扎罗汀的母离子一致,说明有关物质7应为他扎罗汀的炔键与盐酸发生加成反应的产物,质谱裂解(图 10)均得到合理归属。
|
图 10 有关物质7[M+H]+离子的二级质谱图及其裂解途径 Fig.10 MS/MS spectrum and fragmentation pathways of [M+H]+ ions of related substance 7 |
丙酸氯倍他索的有关物质个数较少,含量较低,根据有关物质8和11的二级碎片离子特征,并结合丙酸氯倍他索及已知有关物质9、12的裂解规律,解析出有关物质8和11分别为欧洲药典记载的有关物质A(倍他米松17-丙酸酯)和K(倍他米松21-丙酸酯)[10],并首次鉴定出未知有关物质10的结构,其碎片均经合理途径产生。
4 讨论由于他扎罗汀与丙酸氯倍他索各自有关物质的最大吸收波长分别为325 nm和240 nm,故建立了双波长的液相色谱检测方法。在建立的挥发性流动相色谱-质谱联用鉴定条件下,他扎罗汀和丙酸氯倍他索与各有关物质均得到有效的分离,共检测到12个有关物质;其中1~7为他扎罗汀的有关物质[16],8~12为丙酸氯倍他索的有关物质,而已知有关物质共7个,分别为2、5、6、8、9、11和12;未知有关物质共5个,分别为1、3、4、7和10,5个未知有关物质均为本文首次鉴定。由于没有对照品比对,有关物质结构鉴定仍存在不确定性,本文的推断结果仅供参考和学习。
强制降解试验结果表明,他扎他索软膏中的主成分他扎罗汀在酸、碱、氧化、高温及光照条件下均不稳定,其中强酸条件下产生的有关物质个数最多,包括有关物质1~7,有关物质2、5和6分别为已知有关物质他扎罗汀亚砜、他扎罗汀酸和他扎罗汀酸甲酯,有关物质1和4均为他扎罗汀或他扎罗汀亚砜与甲醇反应的产物,有关物质3和7分别为他扎罗汀亚砜和他扎罗汀与盐酸反应的产物,二者均为酸破坏条件下的特定有关物质。他扎他索软膏中的主成分丙酸氯倍他索在各个强制降解条件下均较稳定,产生的有关物质个数较少,含量较低,其中有关物质8和11仅在碱性条件下产生,有关物质9和12在碱及高温条件下产生。因此,他扎他索软膏应避光、阴凉暗处密闭存储。
通过色谱-质谱联用技术对他扎他索软膏有关物质进行分析研究,对其降解途径进行了探讨,为其存储条件和质量研究提供了参考依据。
| [1] |
DANDO TM, WELLINGTON K. Topical tazarotene-A review of its use in the treatment of plaque psoriasis[J]. Am J Clin Dermatol, 2005, 6(4): 255. DOI:10.2165/00128071-200506040-00006 |
| [2] |
由蕾, 严煜林. 维甲酸类化合物及其受体与银屑病研究进展[J]. 医学综述, 2007, 13(6): 466. YOU L, YAN YL. Study progress of psoriasis with retinoids and their receptor[J]. Med Recapit, 2007, 13(6): 466. DOI:10.3969/j.issn.1006-2084.2007.06.029 |
| [3] |
孙联文, 郑家润. 他扎罗汀的临床前药理及临床药理研究[J]. 国外医学皮肤性病学分册, 1999, 25(6): 342. SUN LW, ZHENG JR. Preclinical and clinical pharmacology of tazarotene[J]. Foreign Med Sci(Sect Dermatol Venereol), 1999, 25(6): 342. |
| [4] |
FELDMAN SR, YENTZER BA. Topical clobetasol propionate in the treatment of psoriasis:a review of newer formulations[J]. Am J Clin Dermatol, 2009, 10(6): 397. DOI:10.2165/11311020-000000000-00000 |
| [5] |
SCHLEICHER SM. Psoriasis:pathogenesis, assessment, and therapeutic update[J]. Clin Podiatr Med Surg, 2016, 33(3): 355. DOI:10.1016/j.cpm.2016.02.004 |
| [6] |
石娴, 石年, 黄朝卫, 等. 丙酸氯倍他索联合他扎罗汀乳膏治疗寻常型银屑病的疗效与安全性分析[J]. 医学理论与实践, 2018, 31(11): 1640. SHI X, SHI N, HUANG CW, et al. Efficacy and safety of clobetasol propionate combined with tazarotene cream in the treatment of psoriasis vulgaris[J]. J Med Theory Pract, 2018, 31(11): 1640. |
| [7] |
李琳琳. 复方丙酸氯倍他索软膏联合NB-UVB治疗寻常型银屑病疗效观察[J]. 皮肤病与性病, 2018, 40(4): 555. LI LL. Therapeutic effect of compound clobetasol propionate ointment combined with NB-UVB on psoriasis vulgaris[J]. J Dermatol Venereol, 2018, 40(4): 555. DOI:10.3969/j.issn.1002-1310.2018.04.053 |
| [8] |
顾军, 陈洁, 陈棋枫. 复方丙酸氯倍他索软膏治疗寻常性银屑病临床疗效观察[J]. 中国皮肤性病学杂志, 2003, 17(1): 35. GU J, CHEN J, CHEN QF. The efficacy and safety of clobetasol propionate compound ointment in patients with psoriasis vulgaris[J]. Chin J Dermatovenereol, 2003, 17(1): 35. DOI:10.3969/j.issn.1001-7089.2003.01.013 |
| [9] |
中国医学科学院皮肤病研究所.治疗银屑病的复方外用药物: 中国, CN 1528313A[P].2004-09-15 Institute of Dermatology, Chinese Academy of Medical Sciences.Compound Topical Medicine for Treating Psoriasis: China, CN 1528313A[P].2004-09-15 |
| [10] |
EP 9.0[S].2017: 2116
|
| [11] |
中华人民共和国药典2015版.二部[S].2015: 148, 232 ChP 2015.Vol Ⅱ[S].2015: 148, 232 |
| [12] |
PATHARE DB, JADHAV AS, SHINGARE MS. A validated stability indicating RPLC method for tazarotene[J]. Chromatographia, 2007, 66(3-4): 247. DOI:10.1365/s10337-007-0265-z |
| [13] |
ROY C, CHAKRABARTY J. Development and validation of a stability-indicating rp-hplc method for simultaneous determination of phenoxyethanol, methylparaben, propylparaben, mometasone furoate, and tazarotene in topical pharmaceutical dosage formulation[J]. Sci Pharm, 2013, 81(4): 951. DOI:10.3797/scipharm.1303-22 |
| [14] |
MARIKA K, KATHERINE F, JIANMIN L, et al. A sensitive high-throughput HPLC assay for simultaneous determination of everolimus and clobetasol propionate[J]. J Chromatogr Sci, 2008, 46(1): 23. DOI:10.1093/chromsci/46.1.23 |
| [15] |
FAUZEE AFB, WALKER RB. Forced degradation studies of clobetasol 17-propionate in methanol, propylene glycol, as bulk drug and cream formulations by RP-HPLC[J]. J Sep Sci, 2013, 36(5): 849. DOI:10.1002/jssc.201200969 |
| [16] |
NAGULAKONDA NNM, ANANTHULA RS, KRISHNAMURTHY T, et al. Quantification and in silico toxicity assessment of tazarotene and its impurities for a quality and safe drug product development[J]. J Chromatogr Sci, 2019, 57(7): 625. DOI:10.1093/chromsci/bmz037 |
 2019, Vol. 39
2019, Vol. 39 
