2. 苏州市药品检验检测研究中心, 苏州 215104
2. Suzhou Institute for Drug Control, Suzhou 215104, China
穿山甲来源于鲮鲤科动物中华穿山甲(Manis pentadactyla)的鳞甲,味咸,性微寒,入肝、胃经,具有通经下乳,活血消癥,消肿排脓,搜风通络的功效[1]。
炮山甲主要含有胆固醇、二十三酸丁胺、脂肪族酰胺等脂溶性成分以及氨基酸、蛋白等亲水性组分[2]。L-丝-L-酪环二肽、D-丝-L-酪环二肽是穿山甲中已知的2种环二肽[3],L-甘-L-酪氨酸环二肽存在于美洲大蠊等药材中[4]。值得注意的是,中华穿山甲、马来穿山甲、印度穿山甲、树穿山甲经砂炒炮制后均产生大量丝-酪环二肽类成分,但在生品中含量却很低[5]。研究表明,环二肽类成分表现出了抗炎、抗肿瘤、抗凝、神经保护、免疫调节等多种显著的生物活性[6-7]。穿山甲中的L-丝-L-酪氨酸环二肽不仅能够提高小白鼠常压缺氧的耐受能力[2],还具有活血化瘀的活性[8]。目前对穿山甲炮制后化学组成的研究大多集中于氨基酸组分、无机元素、溶出度等方面[9],而关于其炮制后肽类成分的含量却鲜有报道[10],仅有学者对穿山甲中L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽这2个成分的含量进行了测定[11],但对其他环二肽类成分未作研究,另外前处理较为烦琐,易导致操作误差。2015年版《中华人民共和国药典》未收载穿山甲含量测定方法,为提高穿山甲质量标准,本文在前期对炮山甲化学成分提取、分离、鉴定的研究基础上,对炮山甲中含量较高的L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽以及首次从炮山甲中分离得到的L-甘-L-酪氨酸环二肽进行了含量测定研究,建立反相高效液相色谱同时3个成分的方法,方法经验证简便可行。同时考察了40批炮山甲饮片中3个成分的含量范围,为炮山甲的质量控制及应用提供了科学依据。
1 仪器与试药 1.1 仪器赛默飞DGLC-3600 UltiMate® 3000高效液相色谱仪,DAD检测器,赛分Sepax Bio-C18色谱柱(4.6 mm×250 mm,5 μm;填料为十八烷基硅烷键合硅胶);梅特勒Mettler Toledo XS105DC电子天平(十万分之一),METTLER AE240电子天平(万分之一),赛默飞BIOFUGE primoR高速离心机;超纯水机水(Mill-pore)。
1.2 试药对照品L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽、L-甘-L-酪氨酸环二肽为本课题组自制,通过1H-NMR、13C-NMR、MS等手段确证其结构,HPLC法检测纯度 > 99%(面积归一法)。乙腈为色谱纯(Fisher公司),三氟乙酸(TFA)为色谱纯(格里斯公司),水为超纯水。经作者鉴定,样品9为印度穿山甲(Manis crassicaudata),样品10、14、16、25、29为树穿山甲(Manis tricuspis),其余样品为中华穿山甲(Manis pentadactyla Linnaeus)[5],样品16、40为非法增重品[12],见图 1。

|
图 1 40批炮山甲样品图 Fig.1 40 samples of stir-baked pangolin scales |
精密称取L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽、L-甘-L-酪氨酸环二肽的对照品适量,加流动相配制得质量浓度分别为0.1122、0.1226、0.1174 mg·mL-1的混合溶液,即得。
2.1.2 供试品溶液取炮山甲样品粉末(过6号筛)约2 g,精密称定,置于锥形瓶中,加10倍量水回流提取30 min,放冷至室温,称量后用水补足减失的量,摇匀,滤过,取续滤液用微孔滤膜滤过,即得。
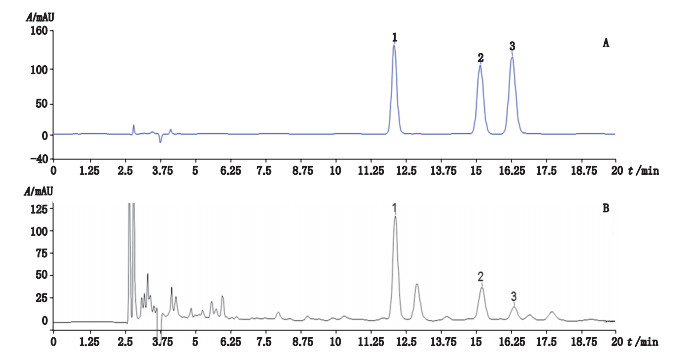
2.2 色谱条件采用赛分C18色谱柱(250 mm×4.6 mm,5 μm),柱温30 ℃,以0.1%TFA乙腈-0.1%TFA水(2:98)为流动相,流速1.0 mL·min-1,检测波长210 nm,进样量10 μL。取“2.1”项下制得的溶液在上述色谱条件下测得的色谱图见图 2。
|
1. L-丝-L-酪氨酸环二肽(cyclo-(L-Ser-L-Tyr))2. D-丝-L-酪氨酸环二肽(cyclo-D-Ser-L-Tyr)3. L-甘-L-酪氨酸环二肽(cyclo-(L-gly-L-Tyr)) 图 2 混合对照品(A)、1号样品(B)HPLC色谱图 Fig.2 HPLC chromatograms of mixed reference substances(A)and sample No.1(B) |
精密吸取“2.1.1”项下混合对照品溶液0.5、1、2、5、10、15、20 μL,分别注入液相色谱仪进行测定,以峰面积Y对进样量X(μg)进行线性回归计算,回归方程、相关系数和线性范围结果见表 1。另取“2.1.1”项下混合对照品溶液逐级稀释,进样测定,当信噪比10:1时测得定量下限(LOQ),信噪比3:1时测得检测下限(LOD)。结果见表 1。
|
|
表 1 3个成分的回归方程、线性范围、相关系数和检出下限、定量下限 Tab.1 Regression regressions, linear ranges, r, LODs and LOQs of 3 components |
精密吸取“2.1.1”项下混合对照品溶液,按“2.2”项下色谱条件连续进样6次,记录峰面积,L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽、L-甘-L-酪氨酸环二肽峰面积RSD分别为0.55%、0.21%、0.44%。表明仪器精密度良好。
2.3.3 稳定性试验取炮山甲粉末,按“2.1.2”项下方法制备供试品溶液,按“2.2”项下色谱条件分别于0、2、4、8、12、24 h进样分析,L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽、L-甘-L-酪氨酸环二肽峰面积RSD分别为0.61%、1.3%、0.53%,表明供试品溶液在24 h内稳定性良好。
2.3.4 重复性试验取同一批次的炮山甲粉末,按“2.1.2”项下方法平行制备6份供试品溶液,按“2.2”项下色谱条件进样分析,记录峰面积,计算L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽、L-甘-L-酪氨酸环二肽的平均含量分别为2.285、0.853 2、0.354 8 mg·g-1,RSD分别为0.92%、0.93%,2.3%。
2.3.5 加样回收试验精密称取已知含量的同一批炮山甲粉末6份,每份1 g,加入约与样品中待测成分含量等量的对照品,按“2.1.2”项下方法制备供试溶液,按“2.2”项下色谱条件进样分析,计算回收率。结果L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽、L-甘-L-酪氨酸环二肽平均回收率分别101.8%、98.1%、95.7%,RSD分别为0.76%、2.2%、2.8%。
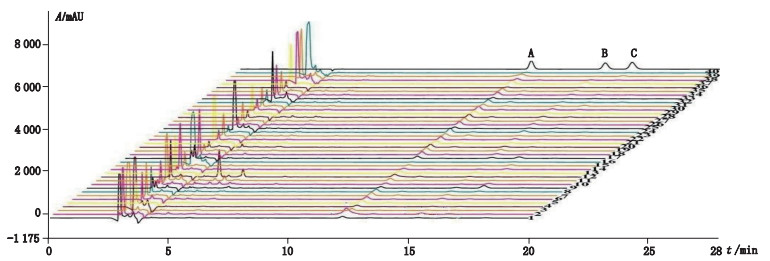
2.4 样品含量测定按“2.1.2”项下方法制备40批炮山甲样品的供试品溶液,按“2.2”项下色谱条件进行测定,外标法计算3个成分的含量,每个样品平行3份,结果见表 2。L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽、L-甘-L-酪氨酸环二肽平均含量分别为0.13%、0.06%、0.04%,40批样品色谱图见图 3。
|
|
表 2 40批炮山甲样品含量测定结果 Tab.2 Results of content determination of 40 samples |
|
A. L-丝-L-酪氨酸环二肽(cyclo-(L-Ser-L-Tyr))B. D-丝-L-酪氨酸环二肽(cyclo-(D-Ser-L-Tyr))C. L-甘-L-酪氨酸环二肽(cyclo-(L-Gly-L-Tyr)) 图 3 40批穿山甲炮制品HPLC图谱 Fig.3 HPLC chromatograms of 40 batches of stir-baked pangolin scales |
使用SPSS 22.0软件对40批不同炮山甲样品的3个环二肽成分的含量进了系统聚类分析,采用组间连接法,采用Euclidean距离法进行计算[13],结果见图 2。40批样品共为两大类,其中样品9为第2大类,其余39个样品为第1大类。随着阈值的减少,第1大类随着阈值的减小继续分为A、B两大类,三部分能够明显区分开,结果见图 4。

|
图 4 环二肽类成分聚类分析 Fig.4 Cluster analysis of cyclic dipeptides |
应用DAD检测器在190~400 nm范围内对L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽、L-甘-L-酪氨酸环二肽进行光谱扫描,结果表明,在204 nm波长附近3个成分吸收系数均最大,干扰少且稳定,故选择210 nm作为检测波长,由于210 nm波长处甲醇会造成干扰,故本实验选择含0.1%TFA的水和乙腈作为流动相。
3.2 供试品溶液制备方法的考察考察了超声提取法和回流提取法对L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽、L-甘-L-酪氨酸环二肽含量测定的影响。结果显示,回流提取法提取更完全。提取溶剂考察了水、甲醇溶液(25%甲醇水溶液、50%甲醇水溶液、75%甲醇水溶液、甲醇),乙醇溶液(25%乙醇水溶液、50%乙醇水溶液、75%乙醇水溶液、乙醇)。结果显示,采用水溶液提取时,L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽、L-甘-L-酪氨酸环二肽含量均较高,且L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽、L-甘-L-酪氨酸环二肽不易溶于甲醇、乙醇。考察了提取时间为0.5、1、2 h时的提取效果。结果含量相近,因此选择0.5 h作为提取时间。
4 结论本实验对40批炮山甲样品中L-丝-L-酪氨酸环二肽、D-丝-L-酪氨酸环二肽、L-甘-L-酪氨酸环二肽成分的含量进行测定,通过含量测定及聚类分析结果可以看出,不同批次的炮山甲均含有上述3个成分,但各样品含量差异较大。多数样品中L-丝-L-酪氨酸环二肽的含量最高,少数样品如9号(印度穿山甲)、10号(树穿山甲)、14号(树穿山甲)、39号(中华穿山甲)的L-甘-L-酪氨酸环二肽含量最高;样品中环二肽含量的差异与不同来源穿山甲的相关性不明显。但是,盐类增重的16号及40号样品被分在1组,且环二肽含量较低,说明盐类增重对炮山甲中的环二肽含量影响较大,会影响环二肽的稳定性。炮山甲中环二肽含量可能与来源、加工、环境等因素有一定的联系,都可能在一定程度上影响环二肽的含量,本研究可为穿山甲相关成分的进一步研究提供参考依据。
| [1] |
中华人民共和国药典2015年版.一部[S]. 2015: 268 ChP 2015. Vol Ⅰ[S]. 2015: 268 |
| [2] |
马雪梅, 秦永祺. 穿山甲化学成分的研究[J]. 药学学报, 1988, 23(8): 588. MA XM, QIN YQ. Studies of chemical constituents of manis pentadctyla[J]. Acta Pharm Sin, 1988, 23(8): 588. |
| [3] |
吕扬, 郑启泰, 王树春, 等. 穿山甲中两对差向异构二肽化合物的X衍射分析[J]. 中国药物化学杂志, 1998, 9(2): 49. LÜ Y, ZHENG QT, WANG SC, et al. X ray diffraction analysis of two epimer dipeptide compounds from Squama Manis[J]. Chin J Med Chem, 1998, 9(2): 49. |
| [4] |
王心龙, 向斌, 李亚美, 等. 虫药美洲大蠊水溶性成分及其促血管生成活性[J]. 天然产物研究与开发, 2017, 29(12): 2004. WANG XL, XIANG B, LI YM, et al. Water soluble compounds from Periplaneta American and their angiogenesis activity[J]. Nat Prod Res Dev, 2017, 29(12): 2004. |
| [5] |
刘逊, 张华峰, 刘雪梅, 等. 4种不同基原穿山甲炮制品的鉴定[J]. 中药材, 2017, 40(3): 585. LIU X, ZHANG HF, LIU XM, et al. The identification of four manis pentadactyla stir fried with sand[J]. J Chin Med Mater, 2017, 40(3): 585. |
| [6] |
李文利, 夏娟. 二酮哌嗪类化合物生物合成研究进展[J]. 微生物学报, 2014, 41(1): 111. LI WL, XIA J. Recent advances in diketopiperazines biosynthesis[J]. Microbiol China, 2014, 41(1): 111. |
| [7] |
Martins MBC. Diketopiperazines:biological activity and synthesis[J]. Tetrahedron, 2007, 63(40): 9923. DOI:10.1016/j.tet.2007.04.105 |
| [8] |
马雪梅, 秦永祺, 郭启栋. 穿山甲活性成分丝-酪环二肽的合成[J]. 中草药, 1993, 24(3): 162. MA XM, QIN YQ, GUO QD. Synthesis of pangolin active constituents cyclo(L-Ser-L-Tyr)[J]. Chin Tradit Herb Drugs, 1993, 24(3): 162. |
| [9] |
谢汉凤, 张清民. 穿山甲生品及醋制品超微粉的制备工艺[J]. 今日药学, 2018, 28(1): 23. XIE HF, ZHANG QM. Study on the preparation process of ultrafine powder of the crude and vinegar products of pangolin[J]. Pharm Today, 2018, 28(1): 23. |
| [10] |
马雪梅, 王强, 秦永祺. 炮制前后穿山甲中环二肽成分的HPLC定量分析[J]. 中草药, 1990, 21(9): 19. MA XM, WANG Q, QIN YQ. HPLC quantitative analysis of dipeptide components in pangolin before and after processing[J]. Chin Tradit Herb Drugs, 1990, 21(9): 19. DOI:10.3321/j.issn:0253-2670.1990.09.003 |
| [11] |
刘潇潇, 李雪, 张丽丹, 等. 离子色谱法检测穿山甲饮片中非法掺加硫酸盐或盐酸盐增重[J]. 药学研究, 2018, 37(1): 27. LIU XX, LI X, ZHANG LD, et al. Determination of sulphate or chloride adulterated in illegal processed pangolin by ion chromatography[J]. J Pharm Res, 2018, 37(1): 27. |
| [12] |
张丽, 王薇, 李玉泽, 等. HPLC法同时测定桃儿七中8个成分的含量[J]. 药物分析杂志, 2017, 37(8): 1461. ZHANG L, WANG W, LI YZ, et al. Simultaneous determination of eight compounds in Sinopodophylli Radix et Rhzoma by HPLC[J]. Chin J Pharm Anal, 2017, 37(8): 1461. |
 2019, Vol. 39
2019, Vol. 39 
