一测多评法同时测定五味子中12个木脂素类成分的含量
刘移兰
1
,
蔡卫华
2

,
窦志华
2

,
曹瑞
3,
倪丽丽
3,
张琳
2
1. 泰州市姜堰中医院, 泰州 225500;
2. 南通大学附属南通第三医院, 南通 226006;
3. 南京中医药大学, 南京 210023
收稿日期:2018-06-22
基金项目:南通市关键技术研究项目(MS22015086);江苏省药学会Shire生物药学基金课题(S201608);南通市科技计划项目(YYZ16017);南通市卫生计生委青年医学人才科研基金项目(WQ2016017)
摘要:目的:建立可用于测定五味子中12个木脂素类成分的一测多评法(QAMS法)。方法:采用高效液相色谱法,色谱柱为Symmetry C18(4.6 mm×250 mm,5 μm),以乙腈(A)-0.1%磷酸水(B)为流动相进行梯度洗脱(0~25 min,45% A→50% A;25~26 min,50% A→60% A;26~36 min,60% A→55% A;36~50 min,55% A→50% A;50~55 min,50% A→65% A;55~70 min,65% A;70~75 min,65% A→70% A;75~85 min,70% A),流速1.0 mL·min-1,柱温30℃,检测波长217 nm。以五味子醇甲为内参物,采用多点校正法,分别建立戈米辛D、戈米辛J、五味子醇乙、当归酰戈米辛H、戈米辛G、五味子酯甲、五味子酯乙、五味子酚、五味子甲素、五味子乙素、五味子丙素11个待测成分与五味子醇甲的相对校正因子,计算待测成分与五味子醇甲色谱峰的相对保留值。采用相对校正因子计算14批五味子样品中11个待测成分的含量,并以差异百分比(PD)为参数,与外标法(ESM)测定结果进行比较,验证QAMS的准确性。另取9批五味子样品,使用3根色谱柱分别在2个实验室的3台仪器采用所建立的方法进行五味子醇甲的含量测定和11个待测成分的含量计算,比较测定和计算结果的相对标准偏差(RSD),验证所建立方法的实用性。结果:上述11个待测成分的RCF分别为1.127、0.883、0.679、0.772、0.712、0.483、0.736、0.451、0.404、0.767和0.754,相对保留值分别为1.179、1.263、1.342、1.810、2.025、2.230、2.280、2.448、3.529、3.996和4.303,QAMS法计算的11个待测木脂素类成分含量与ESM测定结果之间的PD均小于5%。另外9批样品的五味子醇甲含量测定结果和11个待测成分含量计算结果的RSD也均小于5%。23批五味子中上述11个待测成分及五味子醇甲的含量范围分别为0.173~0.395、0.197~0.438、0.571~1.124、0.518~1.016、0.105~0.214、0.076~0.715、0.399~0.812、0.061~0.135、0.349~1.250、1.308~2.376、0.126~0.444和3.571~6.764 mg·g-1。结论:建立的QAMS法可实际应用于五味子中12个木脂素类成分含量测定。
关键词:五味子 木脂素 相对校正因子 一测多评法 外标法 高效液相色谱法
Simultaneous determination of 12 lignans in Schisandrae Chinensis Fructus by quantitative analysis of multi-components with single marker
LIU Yi-lan1
,
CAI Wei-hua2

,
DOU Zhi-hua2

,
CAO Rui3,
NI Li-li3,
ZHANG Lin2
1. Jiangyan Hospital of Traditional Chinese Medicine of Taizhou, Taizhou 225500, China;
2. Nantong Third Affiliated Hospital of Nantong University, Nantong 226006, China;
3. Nanjing University of Chinese Medicine, Nanjing 210023, China
Abstract: Objective: To establish a quantitative analysis of multi-components by single marker(QAMS)method for the determination of 12 lignans in Schisandrae Chinensis Fructus.Methods: A high-performance liquid chromatography(HPLC)method was developed on a Symmetry C18(4.6 mm×250 mm, 5 μm)column with acetonitrile(A)-0.1% phosphoric acid(B)as mobile phase with gradient elution(0-25 min, 45%A→50%A; 25-26 min, 50%A→60%A; 26-36 min, 60%A→55%A; 36-50 min, 55%A→50%A; 50-55 min, 50%A→65%A; 55-70 min, 65%A; 70-75 min, 65%A→70%A; 75-85 min, 70%A).The flow rate was set at 1.0 mL·min-1, the temperature maintained at 30℃, and the detection wavelength was set at 217 nm.Schisandrol A was chosen as the internal reference substance, the relative correction factors of 11 components were determined by multi-point correction method, including gomisin D, gomisin J, schisandrol B, angeloylgomisin H, gomisin G, schisantherin A, schisantherin B, schisanhenol, deoxyschisandrin, schisandrin B and schisandrin C.And the relative retention values of the chromatographic peaks of the components to schisandrol A were calculated, respectively.The contents of 11 components in 14 batches of Schisandrae Chinensis Fructus were determined by relative correction factors, and the percentage difference(PD)was used as a parameter to compare the results with that of external standard method(ESM)to verify the accuracy of QAMS.Three chromatographic columns and three instruments were used in two laboratories to determine the content of schisandrol A, and to calculate the contents of 11 components in another nine batches of samples.And the feasibility of the established method was verified by the relative standard deviation(RSD)of the measured and calculated results.Results: The relative correction factors of 11 components were 1.127, 0.883, 0.679, 0.772, 0.712, 0.483, 0.736, 0.451, 0.404, 0.767 and 0.754, respectively and the relative retention values were 1.179, 1.263, 1.342, 1.810, 2.025, 2.230, 2.280, 2.448, 3.529, 3.996, and 4.303, respectively.The PDs of the contents of 11 lignans calculated by QAMS and determined by ESM were less than 5%.The RSDs of the measured content of schisandrol A and the calculated contents of 11 components in other nine batches of Schisandrae Chinensis Fructus were also less than 5%.The contents of 11 components and schisandrol A in 23 batches of Schisandrae Chinensis Fructus ranged from 0.173 to 0.395, 0.197 to 0.438, 0.571 to 1.124, 0.518 to 1.016, 0.105 to 0.214, 0.076 to 0.715, 0.399 to 0.812, 0.061 to 0.135, 0.349 to 1.250, 1.308 to 2.376, 0.126 to 0.444 and 3.571 to 6.764 mg·g-1, respectively.Conclusion: The established QAMS method can be applied in the determination of 12 lignans in Schisandrae Chinensis Fructus.
Keywords:
Schisandrae Chinensis Fructus lignans relative correction factor quantitative analysis of multi-components with single marker external standard method high-performance liquid chromatography
由于中药成分的复杂性,过去单个成分测定的质量控制方法逐渐被多指标测定替代[1],但是由于后者需要的多个对照品有时难以获得且成本较高,使得多指标的质量控制方法面临挑战[2]。一定线性范围内,成分的量(质量或浓度)和检测器响应值呈正比,根据此原理,一测多评法(QAMS法)选择1个对照品价廉易得的成分为内参物,建立该成分与其他成分之间的相对校正因子,通过相对校正因子计算其他成分的含量,在没有多个对照品的情况下实现多指标质量控制,被包括美国药典、欧洲药典在内的世界各地官方药典广泛采用[3],也是2015年版《中华人民共和国药典》(以下简称《中国药典》)的重点推广方法之一[4]。近年来QAMS应用于中药多成分定量的研究报道逐渐增多[2],但几乎均未进行所建立方法的实用性验证。
五味子为木兰科植物五味子Schisandra chinensis(Turcz.)Baill.的干燥成熟果实,所含有的木脂素为其主要活性成分[5],迄今为止从五味子中分离得到木脂素类成分约50个[6]。本课题组前期建立了QAMS测定五味子中6个木脂素类成分含量的方法[7],也见有采用该方法测定五味子中6个[8]和8个[9]木脂素类成分含量的报道。为了提高五味子质量控制水平,本实验建立了QAMS测定其五味子醇甲、戈米辛D、戈米辛J、五味子醇乙、当归酰戈米辛H、戈米辛G、五味子酯甲、五味子酯乙、五味子酚、五味子甲素、五味子乙素和五味子丙素12个木脂素类成分含量的方法,并对该方法进行了实际应用价值验证。
1 仪器与试药
Waters Alliance高效液相色谱系统(包括e2695分离单元、2998二极管阵列检测器和Empower色谱工作站,Waters公司),SK5200H超声波清洗器(上海科导超声仪器有限公司),Sartorius BT 25S型电子天平(赛多利斯公司)。
对照品五味子醇甲(批号110857-201211,纯度99.9%)、五味子酯甲(批号111529-200604,纯度≥98%)、五味子甲素(批号110764-201111,纯度99.5%)、五味子乙素(批号1100765-200710,纯度≥98%),购自中国食品药品检定研究院;五味子醇乙(批号20120517,纯度≥98%),购自鼎瑞化工(上海)有限公司;五味子酯乙(批号151031020,纯度≥98%)、戈米辛D(批号151031005,纯度≥98%)、戈米辛J(批号151031011,纯度≥98%)、戈米辛G(批号151031020,纯度≥98%)、当归酰戈米辛H(批号151031013,纯度≥98%)、五味子酚(批号151031004,纯度≥98%),购自上海将来生物科技有限公司。甲醇(色谱纯,国药集团化学试剂有限公司),乙腈(色谱纯,TEDIA公司),哇哈哈饮用纯净水(杭州娃哈哈集团有限公司)。
9批(S1~S9)五味子饮片(醋制)购自国内9家医院,4批(S10~S13)五味子药材购自4家饮片公司,1批标准药材(S14)购自中国食品药品检定研究院。经南通市食品药品监督检验中心龚旭东主任中药师鉴定,S1~S13的基源均为木兰科植物五味子Schisandra chinensis(Turcz.)Baill.。方法实用性验证试验用9批五味子样品由南京中医药大学陆兔林教授馈赠并鉴定。
2 方法与结果
2.1 HPLC定量方法的建立
2.1.1 供试品溶液制备
样品粉碎,过3号筛,取粉末约0.15 g,精密称定,置10 mL量瓶中,加甲醇约9.5 mL,超声(功率250 W,频率20 kHz)提取30 min,补充甲醇至刻度,摇匀,滤过,取续滤液过0.45 μm滤膜,即得。
2.1.2 混合对照品溶液制备
精密称取12个对照品适量,以甲醇配成五味子醇甲、戈米辛D、戈米辛J、五味子醇乙、当归酰戈米辛H、戈米辛G、五味子酯甲、五味子酯乙、五味子酚、五味子甲素、五味子乙素和五味子丙素质量浓度分别为2 080.00、54.50、41.60、105.60、560.00、45.00、249.20、454.00、65.40、208.00、1 072.00和89.60 μg·mL-1的12个对照品储备液,再精密量取各对照品储备液适量,以甲醇配成以上12个成分质量浓度分别为104.00、5.42、4.16、21.12、28.00、4.50、12.46、22.70、3.27、20.80、53.60和4.48 μg·mL-1的混合溶液,摇匀,滤过,取续滤液过0.45 μm滤膜,即得。
2.1.3 色谱条件
采用Symmetry C18色谱柱(4.6 mm×250 mm,5 μm),流动相为乙腈(A)-0.1%磷酸水(B),梯度洗脱(0~25 min,45%A→50%A;25~26 min,50%A→60%A;26~36 min,60%A→55%A;36~50 min,55%A→50%A;50~55 min,50%A→65%A;55~70 min,65%A;70~75 min,65%A→70%A;75~85 min,70%A),流速1.0 mL·min-1,柱温30 ℃,检测波长217 nm。以上色谱条件下的样品及混合对照品色谱图见图 1。
2.1.4 线性关系考察
分别精密吸取混合对照品溶液1、2、5、10、15、20、30 μL,按“2.1.3”项下色谱条件进样测定,记录12个成分峰面积值,以峰面积Y对进样量X(μg)进行回归处理,得各成分的回归方程及线性范围。见表 1。
表 1
Tab.1
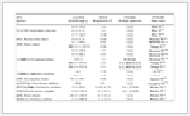
表 1 12个成分回归方程及线性范围
Tab.1 Regression equations and linear ranges of 12 constituents
成分
(component) |
回归方程
(regression equation) |
r |
线性范围
(linear range)/ng |
| 五味子醇甲(schisandrol A) |
Y=6.33×106 X-8.77×104 |
0.999 9 |
104~3 120 |
| 戈米辛D(gomisin D) |
Y=5.67×106 X-5.46×103 |
0.999 9 |
5.42~162.6 |
| 戈米辛J(gomisin J) |
Y=7.25×106 X-5.06×103 |
0.999 9 |
4.16~124.8 |
| 五味子醇乙(schisandrol B) |
Y=9.36×106 X-2.91×104 |
0.999 9 |
21.12~633.6 |
| 当归酰戈米辛H(angeloylgomisin H) |
Y=8.24×106 X-3.46×104 |
0.999 9 |
28~840 |
| 戈米辛G(gomisin G) |
Y=8.94×106 X-7.15×103 |
0.999 9 |
4.5~135 |
| 五味子酯甲(schisantherin A) |
Y=1.32×107 X-2.98×104 |
0.999 9 |
12.46~373.8 |
| 五味子酯乙(schisantherin B) |
Y=8.36×106 X-2.94×104 |
0.999 9 |
22.7~681 |
| 五味子酚(schisanhenol) |
Y=1.44×107 X-1.11×104 |
0.999 9 |
3.27~98.1 |
| 五味子甲素(deoxyschisandrin) |
Y=1.58×107 X-5.22×104 |
0.999 9 |
20.8~624 |
| 五味子乙素(schisandrin B) |
Y=8.24×106 X-4.95×104 |
0.999 9 |
53.6~1608 |
| 五味子丙素(schisandrin C) |
Y=8.52×106 X-6.40×103 |
0.999 9 |
4.48~134.4 |
|
表 1 12个成分回归方程及线性范围
Tab.1 Regression equations and linear ranges of 12 constituents |
2.1.5 精密度试验
精密吸取混合对照品溶液10 μL,连续进样6次,进行日内精密度试验;每天进样2次,连续3 d,进行日间精密度试验。记录五味子醇甲、戈米辛D、戈米辛J、五味子醇乙、当归酰戈米辛H、戈米辛G、五味子酯甲、五味子酯乙、五味子酚、五味子甲素、五味子乙素和五味子丙素的峰面积积分值,计算RSD。结果日内精密度试验,上述成分峰面积积分值的RSD分别为2.2%、2.4%、2.2%、2.2%、1.6%、2.4%、2.5%、2.6%、1.7%、2.9%、2.5%和2.7%;日间精密度试验,上述12个成分峰面积积分值的RSD分别为2.3%、2.1%、2.0%、2.3%、1.7%、2.3%、2.8%、2.7%、2.4%、3.1%、2.4%和2.2%。表明仪器精密度良好。
2.1.6 稳定性试验
精密吸取样品S13的供试品溶液10 μL,分别于制备后的0、3、6、9、12、24、36和48 h进样测定,记录五味子醇甲、戈米辛D、戈米辛J、五味子醇乙、当归酰戈米辛H、戈米辛G、五味子酯甲、五味子酯乙、五味子酚、五味子甲素、五味子乙素和五味子丙素12个成分的峰面积积分值,计算RSD,结果分别为2.0%、4.3%、2.0%、2.1%、2.8%、2.4%、1.9%、2.6%、3.8%、2.0%、2.1%和3.5%,表明该供试品溶液在48 h内稳定。
2.1.7 重复性试验
精密称定样品S13的粉末6份,每份约0.15 g,分别按“2.1.1”项下方法制备供试品溶液,分别精密吸取10 μL进样测定,计算五味子醇甲、戈米辛D、戈米辛J、五味子醇乙、当归酰戈米辛H、戈米辛G、五味子酯甲、五味子酯乙、五味子酚、五味子甲素、五味子乙素和五味子丙素12个成分的平均含量及其RSD。结果平均含量分别为5.007、0.312、0.280、0.845、0.743、0.146、0.139、0.553、0.054、0.458、1.688和0.137 mg·g-1,RSD分别为2.4%、2.5%、2.2%、2.0%、2.1%、2.2%、2.7%、1.9%、4.0%、2.9%、2.5%和1.8%,表明该方法的重复性较好。
2.1.8 回收率试验
精密称定样品S13的粉末6份,每份约0.075 g,分别精密添加五味子醇甲、戈米辛D、戈米辛J、五味子醇乙、当归酰戈米辛H、戈米辛G、五味子酯甲、五味子酯乙、五味子酚、五味子甲素、五味子乙素和五味子丙素对照品储备液0.20、0.50、0.50、0.60、0.10、0.30、0.10、0.10、0.10、0.20、0.10和0.15 mL,按“2.1.1”项下方法制成供试溶液,分别精密吸取10 μL进样测定并计算以上12个成分的加样回收率及其RSD。结果平均回收率分别为96.3%、97.7%、101.6%、101.5%、98.7%、96.3%、96.3%、96.4%、98.1%、97.9%、102.8%和97.8%,RSD分别为2.7%、3.1%、1.3%、0.9%、1.4%、3.1%、2.0%、0.8%、1.5%、2.4%、4.1%和3.0%。
2.2 相对校正因子的计算
相对校正因子计算公式:fi/s=fi/fs=(Wi/Ai)/(Ws/As)=(Wi×As)/(Ws×Ai),其中fi/s、fi、fs分别为待测成分与内参物的相对校正因子、待测成分及内参物的绝对校正因子,Ai、As分别为待测成分及内参物的峰面积,Wi、Ws分别为待测成分及内参物的量。
以五味子醇甲为内参物,取混合对照品溶液1、2、5、10、15、20、30 μL 7个进样体积折合成进样量(质量),计算待测成分戈米辛D(B)、戈米辛J(C)、五味子醇乙(D)、当归酰戈米辛H(E)、戈米辛G(F)、五味子酯甲(G)、五味子酯乙(H)、五味子酚(I)、五味子甲素(J)、五味子乙素(K)、五味子丙素(L)与内参物五味子醇甲(A)的相对校正因子(fi/s),取平均值作为定量用相对校正因子,并考察了7个质量点计算的相对校正因子的RSD,结果11个待测成分与内参物的相对校正因子的RSD均小于5%,见表 2。
表 2
Tab.2

表 2 11个待测成分与五味子醇甲的相对校正因子(fi/s)
Tab.2 Relative correction factors of(fi/s)11 components to schizandrol A
进样体积
(injection volume)/μL |
fB/A |
fC/A |
fD/A |
fE/A |
fF/A |
fG/A |
fH/A |
fI/A |
fJ/A |
fK/A |
fL/A |
| 1 |
1.134 |
0.903 |
0.684 |
0.771 |
0.694 |
0.491 |
0.772 |
0.475 |
0.414 |
0.771 |
0.753 |
| 2 |
1.131 |
0.897 |
0.680 |
0.781 |
0.730 |
0.490 |
0.771 |
0.444 |
0.404 |
0.768 |
0.792 |
| 5 |
1.139 |
0.881 |
0.679 |
0.773 |
0.718 |
0.480 |
0.761 |
0.456 |
0.401 |
0.762 |
0.769 |
| 10 |
1.127 |
0.875 |
0.678 |
0.770 |
0.713 |
0.483 |
0.758 |
0.447 |
0.403 |
0.764 |
0.739 |
| 15 |
1.116 |
0.874 |
0.677 |
0.768 |
0.713 |
0.480 |
0.758 |
0.446 |
0.402 |
0.767 |
0.740 |
| 20 |
1.121 |
0.876 |
0.677 |
0.770 |
0.710 |
0.480 |
0.759 |
0.444 |
0.402 |
0.767 |
0.738 |
| 30 |
1.118 |
0.874 |
0.677 |
0.769 |
0.709 |
0.478 |
0.758 |
0.441 |
0.401 |
0.768 |
0.748 |
| 平均值(mean) |
1.127 |
0.883 |
0.679 |
0.772 |
0.712 |
0.483 |
0.763 |
0.451 |
0.404 |
0.767 |
0.754 |
| RSD/% |
0.7 |
1.4 |
0.4 |
0.6 |
1.5 |
1.1 |
0.8 |
2.6 |
1.1 |
0.4 |
2.7 |
|
表 2 11个待测成分与五味子醇甲的相对校正因子(fi/s)
Tab.2 Relative correction factors of(fi/s)11 components to schizandrol A |
2.3 相对校正因子的重现性考察
精密吸取混合对照品溶液10 μL,分别在2个实验室考察了Waters 2695和Agilent 1200 2种高效液相色谱系统及Symmetry C18(4.6 mm×250 mm,5 μm)和Welchrom C18(4.6 mm×250 mm,5 μm)2种色谱柱对相对校正因子的影响,并计算RSD,结果均小于5%,表明建立的相对校正因子在不同实验室、色谱系统和色谱柱重现性良好。结果见表 3。
表 3
Tab.3

表 3 不同仪器和色谱柱测定的11个待测成分与五味子醇甲的相对校正因子(fi/s)
Tab.3 Relative correction factors(fi/s)of 11 components to schizandrol A determined by different instruments and different columns
仪器
(instrument) |
色谱柱
(column) |
fB/A |
fC/A |
fD/A |
fE/A |
fF/A |
fG/A |
fH/A |
fI/A |
fJ/A |
fK/A |
fL/A |
| Waters 2695 |
Symmetry C18 |
1.116 |
0.874 |
0.677 |
0.768 |
0.713 |
0.480 |
0.758 |
0.446 |
0.402 |
0.767 |
0.740 |
|
Welchrom C18 |
1.127 |
0.889 |
0.682 |
0.806 |
0.735 |
0.473 |
0.768 |
0.445 |
0.395 |
0.752 |
0.719 |
| Agilent 1200 |
Symmetry C18 |
1.090 |
0.864 |
0.667 |
0.810 |
0.713 |
0.498 |
0.785 |
0.452 |
0.416 |
0.787 |
0.755 |
|
Welchrom C18 |
1.120 |
0.878 |
0.669 |
0.799 |
0.737 |
0.510 |
0.734 |
0.434 |
0.420 |
0.799 |
0.770 |
|
平均值(mean) |
1.113 |
0.876 |
0.674 |
0.796 |
0.725 |
0.490 |
0.761 |
0.444 |
0.408 |
0.776 |
0.746 |
|
RSD/% |
1.5 |
1.2 |
1.1 |
2.4 |
1.8 |
3.4 |
2.8 |
1.7 |
2.9 |
2.7 |
2.9 |
|
表 3 不同仪器和色谱柱测定的11个待测成分与五味子醇甲的相对校正因子(fi/s)
Tab.3 Relative correction factors(fi/s)of 11 components to schizandrol A determined by different instruments and different columns |
2.4 待测成分色谱峰的定位
根据“2.3”项中得到的保留时间计算待测成分与内参物的相对保留值(ri/s=tRi/tRs,其中tRi、tRs分别为待测成分、内参物的保留时间)及其RSD,结果各待测成分相对保留值的RSD均小于5%,表明相对保留值数值稳定,可用于待测成分色谱峰的定位。结果见表 4。
表 4
Tab.4

表 4 不同仪器和色谱柱测定的11个待测成分与五味子醇甲相对保留值(ri/s)
Tab.4 The relative retention value s(ri/s) of 11 components to schizandrol A determined by different instruments and different columns
仪器
(instrument) |
色谱柱
(column) |
rB/A |
rC/A |
rD/A |
rE/A |
rF/A |
rG/A |
rH/A |
rI/A |
rJ/A |
rK/A |
rL/A |
| Waters2695 |
Symmetry C18 |
1.215 |
1.292 |
1.372 |
1.798 |
1.987 |
2.225 |
2.289 |
2.473 |
3.457 |
3.914 |
4.236 |
|
Welchrom C18 |
1.214 |
1.299 |
1.379 |
1.793 |
1.985 |
2.224 |
2.265 |
2.443 |
3.441 |
3.878 |
4.196 |
| Agilent1200 |
Symmetry C18 |
1.148 |
1.233 |
1.311 |
1.867 |
2.105 |
2.303 |
2.358 |
2.510 |
3.726 |
4.248 |
4.555 |
|
Welchrom C18 |
1.137 |
1.227 |
1.305 |
1.781 |
2.025 |
2.167 |
2.207 |
2.368 |
3.493 |
3.944 |
4.226 |
|
平均值(mean) |
1.179 |
1.263 |
1.342 |
1.810 |
2.025 |
2.230 |
2.280 |
2.448 |
3.529 |
3.996 |
4.303 |
|
RSD/% |
3.5 |
3.0 |
2.9 |
2.2 |
2.8 |
2.5 |
2.7 |
2.5 |
3.8 |
4.3 |
3.9 |
|
表 4 不同仪器和色谱柱测定的11个待测成分与五味子醇甲相对保留值(ri/s)
Tab.4 The relative retention value s(ri/s) of 11 components to schizandrol A determined by different instruments and different columns |
2.5 QAMS法与外标法测定结果的比较
分别精密吸取样品S1~S14的供试品溶液10 μL,注入高效液相色谱仪测定。采用外标法(external standard method,ESM)测定12个成分的含量,再用建立的QAMS法进行含量计算(Wi=fi/s×Ws×Ai/As),并以差异百分比(percent difference,PD=|QAMS-ESM|/[(QAMS+ESM)/2]×100%)为参数,对2种方法所得结果进行比较[10],结果表明,PD均小于5%,提示建立的方法具有较好的可信度。见表 5。
表 5
Tab.5

表 5 QAMS与ESM测得的五味子中12个木脂素类成分含量(mg·g-1)
Tab.5 Contents of 12 lignans in Schisandrae Chinensis Fructus measured by ESM and QAMS
样品
(sample) |
含量/差异百分比(content/PD) |
方法
(method) |
五味子醇甲
(schisandrol A) |
戈米辛D
(gomisin D) |
戈米辛J
(gomisin J) |
五味子醇乙
(schisandrol B) |
当归酰戈米辛H
(angeloylgomisin H) |
戈米辛G
(gomisin G) |
五味子酯甲
(schisantherin A) |
五味子酯乙
(schisantherin B) |
五味子酚
(schisanhenol) |
五味子甲素
(deoxyschisandrin) |
五味子乙素
(schisandrin B) |
五味子丙素
(schisandrin C) |
| S1 |
含量(content)/(mg·g-1) |
ESM |
6.371 |
0.298 |
0.354 |
1.124 |
0.997 |
0.135 |
0.715 |
0.637 |
0.066 |
0.548 |
2.328 |
0.245 |
|
QAMS |
|
0.298 |
0.359 |
1.124 |
0.987 |
0.132 |
0.718 |
0.626 |
0.063 |
0.538 |
2.317 |
0.247 |
|
PD/% |
|
|
0.1 |
1.2 |
0.0 |
1.0 |
2.0 |
0.4 |
1.6 |
4.4 |
1.9 |
0.4 |
0.9 |
| S2 |
含量(content)/(mg·g-1) |
ESM |
5.444 |
0.349 |
0.299 |
0.880 |
0.820 |
0.142 |
0.301 |
0.682 |
0.069 |
0.675 |
1.863 |
0.125 |
|
QAMS |
|
0.352 |
0.303 |
0.878 |
0.809 |
0.140 |
0.294 |
0.675 |
0.066 |
0.670 |
1.851 |
0.124 |
|
PD/% |
|
|
0.7 |
1.2 |
0.3 |
1.4 |
1.6 |
2.3 |
1.1 |
3.9 |
0.9 |
0.6 |
0.8 |
| S3 |
含量(content)/(mg·g-1) |
ESM |
5.497 |
0.305 |
0.366 |
0.883 |
0.864 |
0.138 |
0.207 |
0.399 |
0.063 |
0.588 |
2.328 |
0.319 |
|
QAMS |
|
0.306 |
0.372 |
0.880 |
0.854 |
0.136 |
0.197 |
0.385 |
0.060 |
0.580 |
2.323 |
0.324 |
|
PD/% |
|
|
0.4 |
1.5 |
0.3 |
1.2 |
1.7 |
4.8 |
3.7 |
4.6 |
1.4 |
0.2 |
1.6 |
| S4 |
含量(content)/(mg·g-1) |
ESM |
5.494 |
0.254 |
0.304 |
0.859 |
0.798 |
0.134 |
0.296 |
0.641 |
0.086 |
0.715 |
2.076 |
0.164 |
|
QAMS |
|
0.254 |
0.308 |
0.855 |
0.786 |
0.131 |
0.289 |
0.632 |
0.084 |
0.710 |
2.067 |
0.165 |
|
PD/% |
|
|
0.0 |
1.3 |
0.4 |
1.5 |
1.8 |
2.4 |
1.4 |
2.3 |
0.7 |
0.4 |
0.1 |
| S5 |
含量(content)/(mg·g-1) |
ESM |
5.290 |
0.263 |
0.357 |
1.012 |
0.832 |
0.137 |
0.219 |
0.448 |
0.061 |
0.492 |
2.165 |
0.257 |
|
QAMS |
|
0.263 |
0.363 |
1.012 |
0.822 |
0.135 |
0.210 |
0.435 |
0.058 |
0.482 |
2.159 |
0.260 |
|
PD/% |
|
|
0.1 |
1.5 |
0.0 |
1.3 |
1.7 |
4.3 |
2.9 |
4.9 |
2.1 |
0.3 |
1.3 |
| S6 |
含量(content)/(mg·g-1) |
ESM |
3.693 |
0.211 |
0.213 |
0.571 |
0.558 |
0.116 |
0.460 |
0.563 |
0.086 |
1.250 |
1.308 |
0.132 |
|
QAMS |
|
0.211 |
0.216 |
0.564 |
0.540 |
0.113 |
0.460 |
0.553 |
0.083 |
1.273 |
1.295 |
0.132 |
|
PD/% |
|
|
0.1 |
1.6 |
1.3 |
3.4 |
2.6 |
0.1 |
1.8 |
3.1 |
1.8 |
1.0 |
0.4 |
| S7 |
含量(content)/(mg·g-1) |
ESM |
4.802 |
0.280 |
0.254 |
0.781 |
0.716 |
0.120 |
0.199 |
0.507 |
0.062 |
0.554 |
1.599 |
0.142 |
|
QAMS |
|
0.281 |
0.257 |
0.778 |
0.704 |
0.117 |
0.189 |
0.496 |
0.060 |
0.546 |
1.587 |
0.142 |
|
PD/% |
|
|
0.5 |
1.2 |
0.4 |
1.6 |
2.0 |
4.8 |
2.1 |
4.5 |
1.4 |
0.8 |
0.1 |
| S8 |
含量(content)/(mg·g-1) |
ESM |
5.467 |
0.247 |
0.368 |
1.038 |
0.823 |
0.144 |
0.242 |
0.518 |
0.064 |
0.526 |
2.180 |
0.227 |
|
QAMS |
|
0.247 |
0.374 |
1.039 |
0.812 |
0.142 |
0.234 |
0.506 |
0.061 |
0.516 |
2.173 |
0.229 |
|
PD/% |
|
|
0.1 |
1.5 |
0.0 |
1.4 |
1.5 |
3.6 |
2.3 |
4.5 |
1.8 |
0.3 |
1.0 |
| S9 |
含量(content)/(mg·g-1) |
ESM |
5.444 |
0.278 |
0.321 |
0.856 |
0.800 |
0.130 |
0.277 |
0.590 |
0.064 |
0.556 |
1.875 |
0.150 |
|
QAMS |
|
0.279 |
0.325 |
0.852 |
0.789 |
0.127 |
0.270 |
0.580 |
0.061 |
0.547 |
1.863 |
0.150 |
|
PD/% |
|
|
0.2 |
1.3 |
0.4 |
1.5 |
1.9 |
2.8 |
1.7 |
4.5 |
1.6 |
0.6 |
0.2 |
| S10 |
含量(content)/(mg·g-1) |
ESM |
6.301 |
0.308 |
0.314 |
0.984 |
0.936 |
0.159 |
0.254 |
0.670 |
0.071 |
0.638 |
2.245 |
0.193 |
|
QAMS |
|
0.309 |
0.317 |
0.981 |
0.926 |
0.157 |
0.245 |
0.660 |
0.068 |
0.630 |
2.234 |
0.194 |
|
PD/% |
|
|
0.2 |
1.1 |
0.3 |
1.2 |
1.4 |
3.6 |
1.4 |
3.9 |
1.3 |
0.5 |
0.4 |
| S11 |
含量(content)/(mg·g-1) |
ESM |
5.794 |
0.301 |
0.321 |
1.052 |
0.896 |
0.149 |
0.274 |
0.617 |
0.062 |
0.580 |
2.114 |
0.188 |
|
QAMS |
|
0.302 |
0.325 |
1.052 |
0.885 |
0.147 |
0.266 |
0.607 |
0.059 |
0.571 |
2.104 |
0.188 |
|
PD/% |
|
|
0.3 |
1.2 |
0.0 |
1.2 |
1.5 |
3.0 |
1.6 |
4.9 |
1.6 |
0.5 |
0.4 |
| S12 |
含量(content)/(mg·g-1) |
ESM |
6.511 |
0.312 |
0.363 |
1.082 |
1.016 |
0.182 |
0.308 |
0.810 |
0.074 |
0.663 |
2.376 |
0.170 |
|
QAMS |
|
0.313 |
0.367 |
1.080 |
1.006 |
0.180 |
0.300 |
0.803 |
0.072 |
0.655 |
2.366 |
0.170 |
|
PD/% |
|
|
0.2 |
1.2 |
0.2 |
1.0 |
1.0 |
2.5 |
0.8 |
3.6 |
1.2 |
0.4 |
0.0 |
| S13 |
含量(content)/(mg·g-1) |
ESM |
5.109 |
0.308 |
0.285 |
0.858 |
0.749 |
0.150 |
0.224 |
0.561 |
0.062 |
0.470 |
1.711 |
0.141 |
|
QAMS |
|
0.310 |
0.288 |
0.856 |
0.737 |
0.148 |
0.215 |
0.551 |
0.059 |
0.460 |
1.699 |
0.140 |
|
PD/% |
|
|
0.6 |
1.3 |
0.3 |
1.6 |
1.3 |
4.1 |
1.8 |
4.7 |
2.2 |
0.7 |
0.3 |
| S14 |
含量(content)/(mg·g-1) |
ESM |
4.305 |
0.257 |
0.341 |
0.927 |
0.648 |
0.141 |
0.192 |
0.461 |
0.062 |
0.349 |
1.601 |
0.186 |
|
QAMS |
|
0.258 |
0.347 |
0.930 |
0.636 |
0.140 |
0.182 |
0.450 |
0.060 |
0.337 |
1.593 |
0.188 |
|
PD/% |
|
|
0.5 |
1.9 |
0.3 |
1.9 |
1.1 |
4.9 |
2.4 |
4.4 |
3.6 |
0.5 |
1.0 |
|
表 5 QAMS与ESM测得的五味子中12个木脂素类成分含量(mg·g-1)
Tab.5 Contents of 12 lignans in Schisandrae Chinensis Fructus measured by ESM and QAMS |
2.6 建立的QAMS法的实用性验证试验
另取9批五味子样品,按“2.1.1”项下方法制备供试品溶液;精密称取五味子醇甲10.33 mg,置100 mL量瓶中,加甲醇溶解并稀释至刻度,制得对照品溶液。使用Symmetry C18(4.6 mm×250 mm,5 μm)、Agilent ZORBAX SB-C18(4.6 mm×250 mm,5 μm)和SHISEIDO C18(4.6 mm×250 mm,5 μm)3根色谱柱,分别用2个实验室的Waters Alliance e2695、岛津LC-20A和DIONEX ULtiMate 3000 3台仪器高效液相色谱仪,按“2.1.3”项色谱条件进样测定,建立五味子醇甲的回归方程,并对9批样品进行测定,ESM计算五味子醇甲的含量,按“2.4”项下所得相对保留值,定位戈米辛D、戈米辛J、五味子醇乙、当归酰戈米辛H、戈米辛G、五味子酯甲、五味子酯乙、五味子酚、五味子甲素、五味子乙素、五味子丙素色谱峰,记录峰面积,按“2.2”项下所得相对校正因子和“2.5”项下公式计算含量,9批样品中12个成分的9组测定和计算的结果见表 6。计算并比较测定和计算的结果的相对标准偏差(RSD,计算公式为表 6中标准差s/均数x×100%),结果RSD均小于5%,证明所建立的QAMS法具有实用价值。
表 6
Tab.6

表 6 使用3根色谱柱和3台高效液相色谱仪测定的9批五味子中五味子醇甲含量及QAMS法计算的另外11个木脂素类成分含量(x±s,n=9)
Tab.6 Contents of schisandrol A determined by 3 chromatographic columns and 3 HPLC instruments and the contents of 11 other lignans calculated by QAMS method in 9 batches of Schisandrae Chinensis Fructus
样品
(sample) |
含量(content)/(mg·g-1) |
含量(content)/(mg·g-1) |
五味子醇甲
(schisandrol A) |
戈米辛D
(gomisin D) |
戈米辛J
(gomisin J) |
五味子醇乙
(schisandrol B) |
当归酰戈米辛H
(angeloylgomisin H) |
戈米辛G
(gomisin G) |
五味子酯甲
(schisantherin A) |
五味子酯乙
(schisantherin B) |
五味子酚
(schisanhenol) |
五味子甲素
(deoxyschisandrin) |
五味子乙素
(schisandrin B) |
五味子丙素
(schisandrin C) |
| 1 |
3.571±0.099 |
0.173±0.006 |
0.197±0.009 |
0.633±0.026 |
0.518±0.025 |
0.105±0.004 |
0.076±0.003 |
0.449±0.021 |
0.069±0.004 |
0.446±0.021 |
1.364±0.057 |
0.141±0.006 |
| 2 |
6.162±0.082 |
0.331±0.013 |
0.409±0.019 |
1.137±0.045 |
0.938±0.041 |
0.214±0.010 |
0.138±0.007 |
0.671±0.012 |
0.112±0.005 |
0.662±0.023 |
2.206±0.059 |
0.297±0.014 |
| 3 |
5.545±0.188 |
0.296±0.008 |
0.321±0.016 |
0.689±0.031 |
0.755±0.036 |
0.165±0.008 |
0.144±0.007 |
0.724±0.036 |
0.123±0.004 |
0.791±0.033 |
1.674±0.056 |
0.138±0.006 |
| 4 |
6.764±0.193 |
0.355±0.013 |
0.326±0.015 |
1.062±0.051 |
0.931±0.038 |
0.184±0.009 |
0.169±0.006 |
0.812±0.025 |
0.135±0.003 |
0.743±0.033 |
2.190±0.084 |
0.235±0.009 |
| 5 |
5.299±0.194 |
0.270±0.012 |
0.322±0.015 |
0.924±0.046 |
0.759±0.019 |
0.162±0.006 |
0.123±0.004 |
0.566±0.014 |
0.112±0.005 |
0.556±0.021 |
1.980±0.091 |
0.440±0.011 |
| 6 |
5.297±0.144 |
0.328±0.014 |
0.309±0.011 |
0.932±0.046 |
0.775±0.037 |
0.163±0.005 |
0.124±0.003 |
0.645±0.029 |
0.086±0.002 |
0.426±0.018 |
1.963±0.080 |
0.227±0.006 |
| 7 |
4.872±0.151 |
0.240±0.009 |
0.316±0.015 |
0.928±0.039 |
0.739±0.035 |
0.151±0.006 |
0.106±0.005 |
0.564±0.027 |
0.097±0.003 |
0.500±0.024 |
1.875±0.073 |
0.338±0.006 |
| 8 |
5.912±0.184 |
0.277±0.008 |
0.347±0.015 |
0.954±0.041 |
0.834±0.041 |
0.155±0.007 |
0.110±0.005 |
0.707±0.014 |
0.114±0.004 |
0.564±0.026 |
2.184±0.106 |
0.201±0.009 |
| 9 |
5.171±0.169 |
0.395±0.013 |
0.438±0.021 |
1.087±0.049 |
0.804±0.040 |
0.209±0.008 |
0.097±0.004 |
0.423±0.012 |
0.085±0.003 |
0.442±0.020 |
2.169±0.093 |
0.372±0.016 |
|
表 6 使用3根色谱柱和3台高效液相色谱仪测定的9批五味子中五味子醇甲含量及QAMS法计算的另外11个木脂素类成分含量(x±s,n=9)
Tab.6 Contents of schisandrol A determined by 3 chromatographic columns and 3 HPLC instruments and the contents of 11 other lignans calculated by QAMS method in 9 batches of Schisandrae Chinensis Fructus |
3 讨论
校正因子有绝对校正因子和相对校正因子之分。对色谱法而言,《中国药典》[11]将绝对校正因子定义为单位面积的色谱峰代表的待测物质的量,将相对校正因子定义为测定物质与所选定的参照物质的绝对校正因子之比。前者用公式表示为f=W/A,其中f、A、W分别为某成分的绝对校正因子、色谱峰峰面积和色谱峰峰面积对应的物质的量;后者的公式见“2.2”项。要注意的是,关于相对校正因子的表述有2种:(1)待测成分与内参物间的相对校正因子,即“fi/s”,也就是《中国药典》所定义的相对校正因子;(2)内参物与待测成分间的相对校正因子[12],其公式为fs/i=fs/fi=(Ws/As)/(Wi/Ai)=(Ws×Ai)/(Wi×As)。“fi/s”和“fs/i”之间是倒数关系,两者都可以用来计算待测成分的量,但计算公式不同,前者计算公式已在“2.5”项中表述,后者则为Wi=(Ws×Ai)/(fs/i×As)。分别采用“fi/s”和“fs/i”计算11个待测成分的含量,结果一样。但是,检索文献发现,目前对相对校正因子的表述不一致,有些甚至是错误的。
相对校正因子计算方法主要有2种,一种是本研究中所采用的多点校正法,另一种为标准曲线斜率校正法[13],实验过程中采用斜率校正法对11个待测成分的含量进行QAMS计算,并以PD为参数与ESM测得结果进行了比较,结果发现,部分批次五味子酯甲和五味子酚的PD大于5%,提示斜率校正法不适用于五味子的QAMS计算。
待测成分色谱峰的快速、准确定位是QAMS法的关键[2],文献普遍采用相对保留时间(即“2.4”项中的相对保留值ri/s)或保留时间差(△ti/s=tRi-tRs)定位法[13]。实验过程中计算了“2.3”项采用2种高效液相色谱系统及2种色谱柱测定所得11个待测成分色谱峰与内参物色谱峰的保留时间差及其RSD,结果发现2个成分保留时间差的RSD大于20%,1个成分大于10%,3个成分大于5%,提示保留时间差不适用于五味子QAMS法的待测成分色谱峰定位。
近年来,QAMS应用于中药多成分定量的研究报道逐渐增多[2],但几乎均只有所报道的样品QAMS计算结果与ESM测定结果的比较,没有采用其他样品在其他实验室、仪器、色谱柱验证所建立方法的实际应用价值。本研究中另取9批五味子样品,在2个实验室使用3台仪器3根色谱柱对所建立的方法进行了实用性验证,结果证明所建立的方法可实际应用于五味子中12个木脂素类成分含量测定,进而进行质量评价。
参考文献
| [1] |
ZHU C, LI X, ZHANG B, et al. Quantitative analysis of multi-components by single marker—a rational method for the internal quality of Chinese herbal medicine[J]. Integr Med Res, 2017, 6(1): 1. |
| [2] |
秦昆明, 杨冰, 胡静, 等. 一测多评法在中药多组分质量控制中的应用现状与思考[J]. 中草药, 2018, 49(3): 725. QIN KM, YANG B, HU J, et al. Application status and thinking of quantitative analysis of multi-components by single marker in quality control of multi-components traditional Chinese medicine[J]. Chin Tradit Herb Drugs, 2018, 49(3): 725. |
| [3] |
DONG Y, GUO Q, LIU J, et al. Simultaneous determination of seven phenylethanoid glycosides in Cistanches Herba by a single marker using a new calculation of relative correction factor[J]. J Sep Sci, 2018, 41(9): 1913. DOI:10.1002/jssc.v41.9 |
| [4] |
杨洋, 黄良永, 朱美玲, 等. 一测多评法在中国药典2015年版中的应用[J]. 中南药学, 2017, 15(2): 1738. YANG Y, HUANG LY, ZHU ML, et al. Quantitative analysis of multi-components with single-marker in China Pharmacopoeia(2015 edition)[J]. Cent South Pharm, 2017, 15(2): 1738. |
| [5] |
陈舒妤, 石婧婧, 邹立思, 等. UFLC-Q-TRAP-MS/MS同时测定五味子中木脂素及有机酸类成分[J]. 中国中药杂志, 2018, 43(10): 2104. CHEN SY, SHI JJ, ZOU LS, et al. Simultaneous determination of lignans and organic acids in Schisandrae Chinensis Fructus by UFLC-Q-TRAP-MS/MS[J]. China J Chin Mater Med, 2018, 43(10): 2104. |
| [6] | |
| [7] |
窦志华, 安莉萍, 陈敏, 等. 一测多评法同时测定五味子中6种木脂素类成分含量[J]. 中国药学杂志, 2014, 49(2): 147. DOU ZH, AN LP, CHEN M, et al. Simultaneous determination of six lignanoids in Schisandra chinensis by quantitative analysis of multi-components by single marker[J]. Chin Pharm J, 2014, 49(2): 147. DOI:10.11669/cpj.2014.02.017 |
| [8] |
贺凤成, 李守信, 赵志全, 等. 一测多评法测定五味子中4种木脂素类成分的含量[J]. 药学学报, 2012, 47(7): 930. HE FC, LI SX, ZHAO ZQ, et al. Simultaneous quantitative analysis of four lignanoids in Schisandra chinensis by quantitative analysis of multi-components by single marker[J]. Acta Pharm Sin, 2012, 47(7): 930. |
| [9] |
汪丽君, 刘淑敏, 毛春芹, 等. 一测多评法同时测定五味子中8个木脂素类成分的含量[J]. 药物分析杂志, 2015, 35(7): 1191. WANG LJ, LIU SM, MAO CQ, et al. Simultaneous determination of 8 lignans in Schisandra chinensis by quantitative analysis of multi-components by single marker[J]. Chin J Pharm Anal, 2015, 35(7): 1191. |
| [10] |
ZHANG Y, CHEN Z, XU X, et al. Rapid separation and simultaneous quantitative determination of 13 constituents in Psoraleae Fructus by a single marker using high-performance liquid chromatography with diode array detection[J]. J Sep Sci, 2018, 40(21): 4191. |
| [11] |
中华人民共和国药典2015年版.四部[S].2015: 375
ChP 2015.Vol Ⅳ[S].2015: 375
|
| [12] |
王智民, 钱忠直, 张启伟, 等. 一测多评法建立的技术指南[J]. 中国中药杂志, 2011, 36(6): 657. WANG ZM, QIAN ZZ, ZHANG QW, et al. The guidelines for establishment of QAMS[J]. China J Chin Mater Med, 2011, 36(6): 657. |
| [13] |
何兵, 杨世艳, 张燕. 一测多评中待测成分校正和定位的新方法研究[J]. 药学学报, 2012, 47(12): 1653. HE B, YANG SY, ZHANG Y, et al. A new method of calibration and positioning in quantitative analysis of multicomponents by single marker[J]. Acta Pharm Sin, 2012, 47(12): 1653. |

 2019, Vol. 39
2019, Vol. 39 
