2. 大连民族大学生物技术与资源利用教育部重点实验室, 大连 116600;
3. 大连理工大学生命科学与技术学院, 大连 116024
2. Key Laboratory of Biotechnology and Bioresources Utilization, Ministry of Education, Dalian Minzu University, Ministry of Education, Dalian 116600, China;
3. School of Life Science and Technology, Dalian University of Technology, Dalian 116024, China
复方木鸡颗粒为满药现代制剂,由云芝提取物、核桃楸皮、山豆根和菟丝子4味药制成,其来源于满族民间验方“木鸡汤”,收载于《中药成方制剂》第十六册。复方木鸡颗粒疗效确切,具有扶正清热解毒功效,能抑制甲胎蛋白升高和调节免疫功能,临床上用于治疗原发性肝癌、肝硬化、肝炎等肝脏疾病。作为最具有代表性的满药,复方木鸡颗粒临床疗效显著,且为目前国内肝癌前期阻断治疗药物,具有较大的开发研究价值[1-4]。
目前,国内外针对复方木鸡颗粒的研究尚不多见,主要集中在临床疗效观察、药理作用等内容[1-7],其药效物质基础未见有研究报道。为了明确其活性成分并阐述该复方的物质基础和作用机制,其化学成分的全面快速鉴定成为亟待解决的问题。本实验采用液相色谱-离子阱静电场轨道阱质谱(HPLC-LTQ-Orbitrap/MS)技术对复方木鸡颗粒提取物中化学成分进行分析,根据化学成分质谱信息及与对照品、相关文献数据[8-17]比对,鉴定复方木鸡颗粒中的甲醇提取物成分,对其进行归纳总结,并对典型化合物的质谱裂解规律进行研究,旨在为其质量控制提供准确、快速鉴定方法,为后期复方木鸡颗粒的深入研究提供依据。
1 仪器与材料 1.1 仪器LTQ Orbitrap XL液相色谱-高分辨质谱联用仪配有电喷雾离子化(ESI)源、Accela 1250四元梯度泵、Accela AS自动进样系统、Accela光电二极管阵列(PDA)检测器和Thermo Xcalibur 2.1数据处理系统(Thermo Fisher公司);KQ 2200E型超声波清洗器(昆山市超声仪器有限公司);ME104万分之一电子精密天平[梅特勒-托利多仪器(上海)有限公司]。
1.2 试药色谱级乙腈(Merck公司);色谱纯甲醇和甲酸(天津科密欧化学试剂有限公司);娃哈哈纯净水。
对照品没食子酸(批号110780-201508)购于中国食品药品检定研究院,金丝桃苷(批号16032113)、苦参碱(批号16031411)、柚皮素(批号16032406)、金雀花碱(批号16031516)、芒柄花黄素(批号16031005)购于北京世纪奥科生物技术有限公司,丁香酸(批号C10079561),槲皮苷(批号C10053026)购于上海麦克林生化科技有限公司,槐果碱(批号612A022),杨梅苷(批号1109A022)购于北京索来宝科技有限公司。各对照品质量分数均大于98%。
复方木鸡颗粒(批号160601,丹东药业集团)购于大连益春堂药店。
2 方法 2.1 供试品溶液的制备称取复方木鸡颗粒适量,研磨成粉末,精密称取1 g,置于具磨口塞的三角瓶中,加入30%甲醇20 mL,盖塞,超声提取(40 kHz,100 W)30 min 2次,合并提取液,室温放置,滤过,取续滤液,用0.22 μm微孔滤膜滤过,即得。
2.2 对照品溶液的制备分别精密称取对照品没食子酸、金丝桃苷、苦参碱、柚皮素、绿原酸、杨梅苷、槲皮苷、丁香酸、槐果碱、芒柄花黄素适量,用甲醇溶液配制成质量浓度均为8 μg·mL-1的溶液,即得。
2.3 色谱条件采用Waters Xselect T3 C18色谱柱(250 mm×4.6 mm,5 μm),流动相A为0.1%甲酸-水溶液,流动相B为乙腈溶液,洗脱梯度(0~5 min,5% B;5~30 min,5%B→10%B;30~50 min,10%B→18%B;50~80 min,18%B→30%B;80~100 min,30%B→60%B;100~110 min,60%B→100%B),流速0.5 mL·min-1,柱温30 ℃,进样量5 μL。
采用ESI源,源喷射电压为4.0 kV,鞘气流速为15 L·min-1,辅助气流速为5.0 L·min-1,加热毛细管温度为275 ℃。正负离子模式检测,扫描方式为一级及二级全扫描,扫描范围为m/z 120~1 000,分辨率为30 000,最大允许偏差为5×10-6,碰撞能量35 eV。
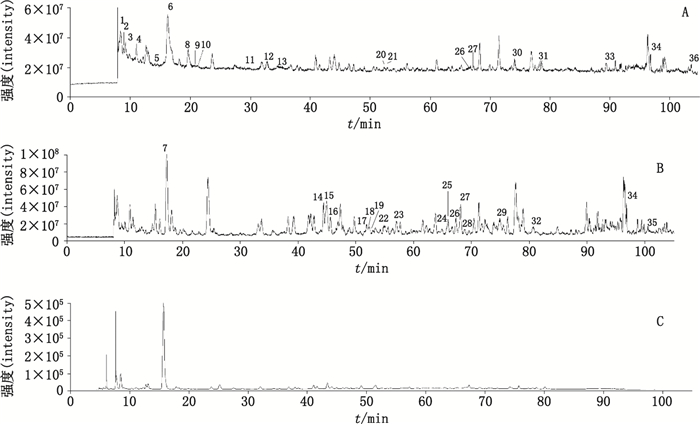
3 结果 3.1 化学成分分析经过色谱条件和质谱条件的优化,应用LC-LTQ-Orbitrap/MS对复方木鸡颗粒供试品溶液和对照品溶液进行分析,图 1为正负离子模式下测定复方木鸡颗粒的总离子流(TIC)图,以及在260 nm下的液相色谱图。
|
图 1 复方木鸡颗粒甲醇提取物在正(A)、负(B)离子模式下和260 nm(C)下的色谱图 Fig.1 Chromatograms of methanol extract of compound Muji granules under ESI+ mode(A), ESI- mode(B)and 260 nm(C) |
通过LC-LTQ-Orbitrap/MS检测得到复方木鸡颗粒中各化学成分的保留时间(tR)和质谱信息,结合对照品及相关文献[8-17]数据的对比进行化学成分确认,ESI-MS模式下检测到的化合物结果见表 1。鉴定或推断了复方木鸡颗粒中36个化合物的结构,包括13个生物碱类化合物,13个黄酮类化合物,3个萘醌类化合物,5个有机酸类化合物和2个其他类化合物,并基于裂解碎片的精确质荷比对典型化合物的裂解规律进行了推测,对应的碎片信息见表 2。
|
|
表 1 复方木鸡颗粒化学成分分析 Tab.1 Chemical composition analysis of compound Muji granules |
|
|
表 2 典型化合物的特征二级碎片及裂解途径 Tab.2 Characteristic ions and proposed main fragmentation pathways of compound 8, 17, 18, 22 and 32 |
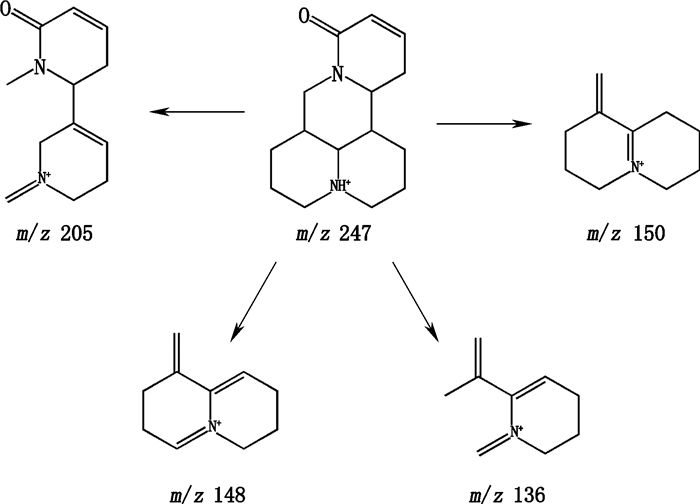
生物碱类化合物是复方木鸡颗粒中山豆根的主要成分,也是其主要的活性成分,所含的生物碱多属于喹诺里西啶类生物碱。根据对照品比对和文献中苦参生物碱类化合物裂解碎片的总结,苦参类生物碱二级质谱具有相同的裂解方式,即各环逐步裂解产生碎片。经与对照品比对,并结合精确相对分子质量,确定化合物1、6和8分别为金雀花碱、苦参碱和槐果碱。槐果碱(化合物8)其一、二级质谱图和推断的裂解途径分别见图 2~3。具有较高丰度的m/z 148、m/z 150以及[M+H-H2O]+离子是苦参型生物碱典型的质谱碎片[13-14],羟基氧化物的[2M+H]+离子丰度相对较低,但具有丰度较高的脱水峰。据此可推断化合物2~6及8~13均为苦参型生物碱。化合物3、4、12、13和14的一级质谱具有高丰度的[M+H]+离子265,但[2M+H]+离子丰度较低或几乎没有,推定为羟基生物碱。结合文献[9-10]及保留时间规律,推定化合物13为槐醇,3、4、12为14或13或9位羟基化苦参碱。经比较精确相对分子质量、保留时间以及碎片离子,并结合文献数据[11-12],推测化合物2为槐果碱的氧化物,化合物5为苦参碱的双氧化物,和苦参碱的氧化,化合物9和10为苦参碱的乙酰化物,化合物11为去氢苦参碱。

|
图 2 化合物8一级(A)和二级(B)全扫描质谱图 Fig.2 Full scan MS(A) and MS/MS(B) spectra for compound 8 |
|
图 3 化合物8主要裂解途径 Fig.3 Proposed main fragmentation pathway of compound 8 |
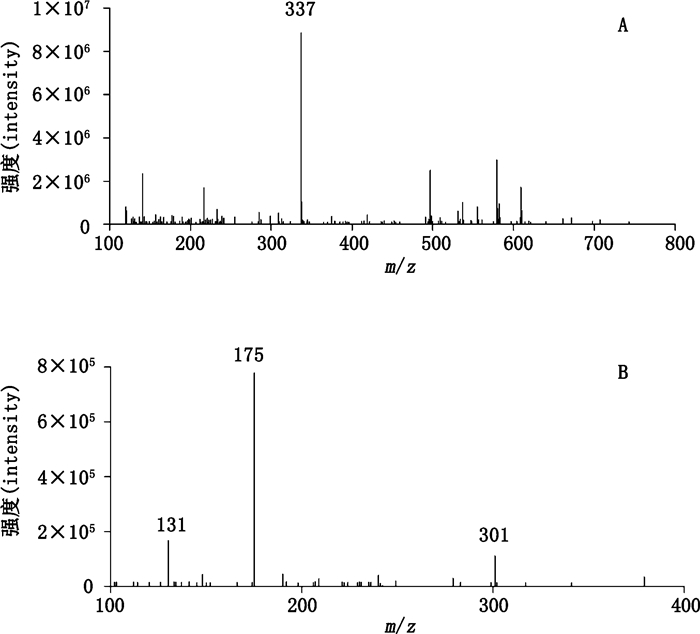
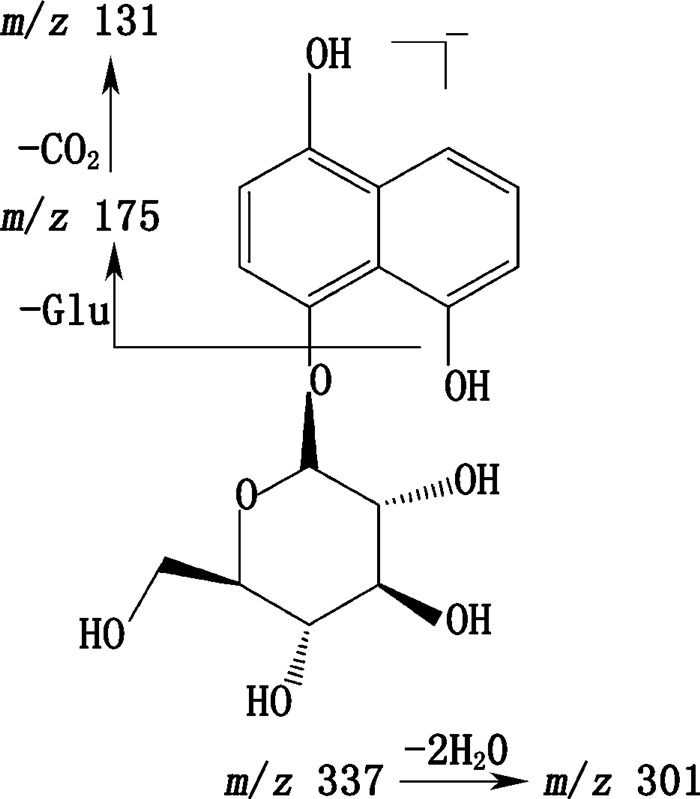
萘醌类化合物是核桃属植物中主要的抗肿瘤活性物质,在复方木鸡颗粒中检测到3个(化合物22、23和31)萘醌类化合物,推测其来源于核桃楸皮。化合物22其准分子离子峰为m/z 337[M-H]-,丰度比较高,其糖苷键易断裂,脱去葡萄糖基形成丰度较高的m/z 175[M-H-C6H10O5]-,失去2个水分子形成m/z 301[M-H-2H2O]-,结合文献推断化合物22为1,4,8-三羟基萘-1-O-β-D-吡喃葡萄糖苷。化合物22一、二级质谱图和推断的裂解途径分别见图 4、5。化合物23其准分子离子峰为m/z 469[M-H]-,其糖苷键断裂形成丰度较高的m/z 175[M-H-C11H18O9]-,结合文献[14]推断化合物23为1,4,8-三羟基萘-1-O-β-D-吡喃葡萄糖苷-(1→6)-β-D-木吡喃糖苷。化合物31其准分子离子峰为m/z 489[M+H]+,其糖苷键断裂形成丰度较高的m/z 327[M+H-C6H10O5]+,结合文献[15-17]推断化合物31为1,8,9,10-四羟基-6H-萘-[1,2-b]-苯[d]-吡喃-6-酮-12-O-β-D-葡萄糖苷。
|
图 4 化合物22一级(A)和二级(B)全扫描质谱图 Fig.4 Full scan MS(A)and MS/MS(B)spectra for compound 22 |
|
图 5 化合物22主要裂解途径 Fig.5 Proposed main fragmentation pathway of compound 22 |
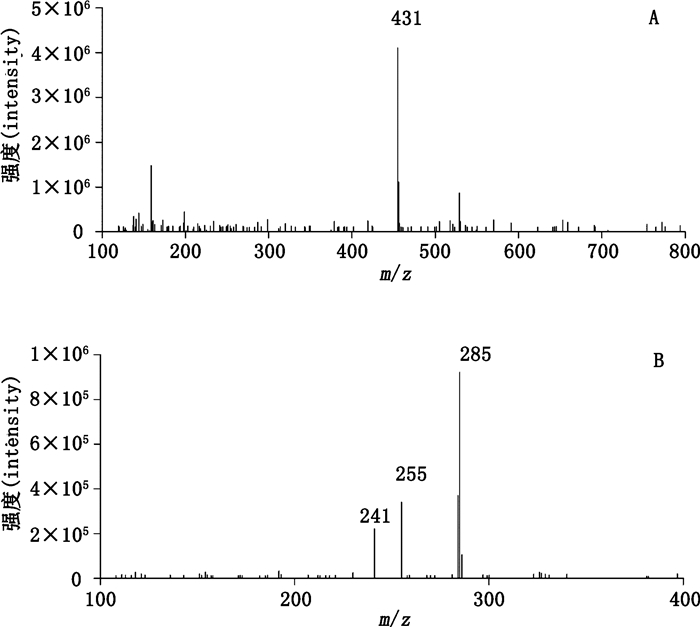
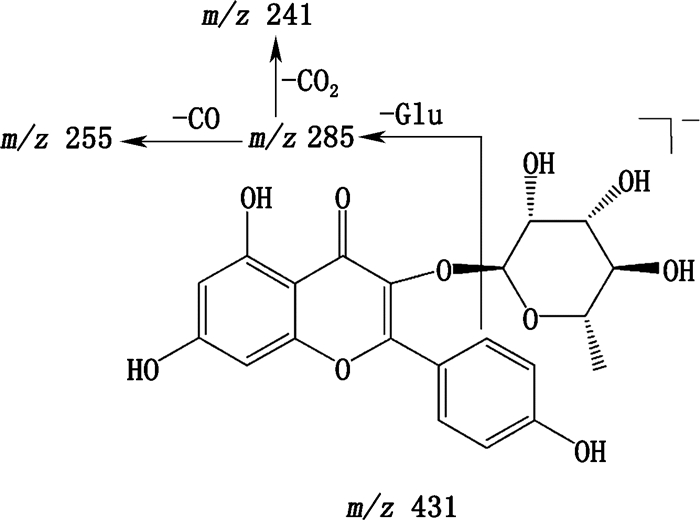
黄酮类成分是广泛存在于自然界的一大类化合物,多个黄酮类化合物都具有明显的抗肿瘤和逆转肿瘤细胞多药耐药作用。复方木鸡颗粒提取物中黄酮类化合物较多,但含量甚微。黄酮类化合物质谱裂解规律的研究较多,以化合物32为例,其负离子模式下,准分子离子m/z 431[M-H]-丰度较高,其失去黄酮C环上的取代基形成丰度较高的m/z 285[M-H-C6H10O4]-,由于黄酮C环的收缩和断裂,此离子继续丢失CO和2H,形成丰度较低的m/z 255[M-H-C7H12O5]-,离子285[M-H-C6H10O4]-失去CO2,形成碎片m/z 241,经比较精确相对分子质量、保留时间以及碎片离子,并结合文献序号数据,推断化合物32为阿福豆苷,其一、二级质谱图和推断的裂解途径分别见图 6和图 7。
|
图 6 化合物32一级(A)和二级(B)全扫描质谱图 Fig.6 Full scan MS(A)and MS/MS(B)spectra for compound 32 |
|
图 7 化合物32主要裂解途径 Fig.7 Proposed main fragmentation pathway of compound 32 |
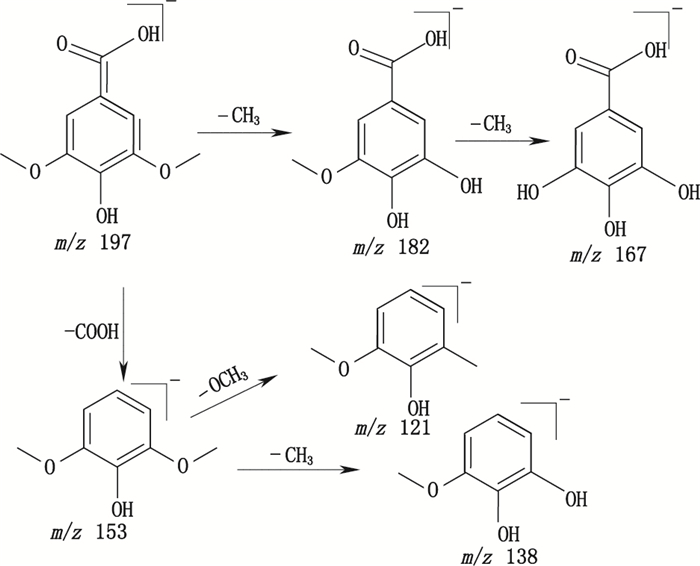
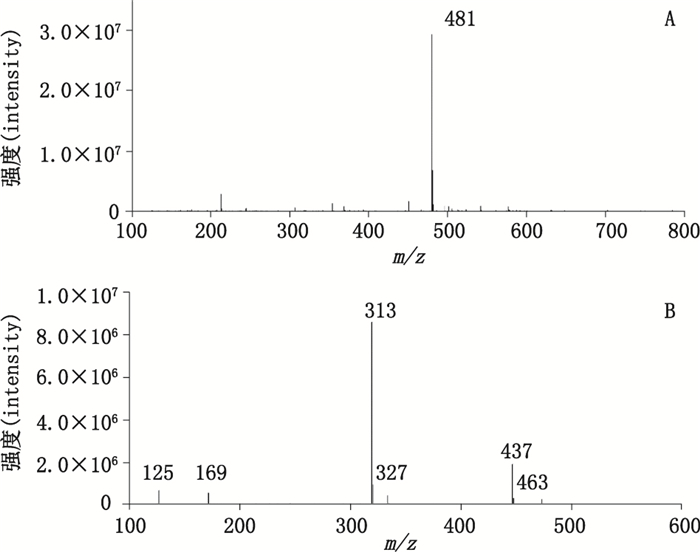
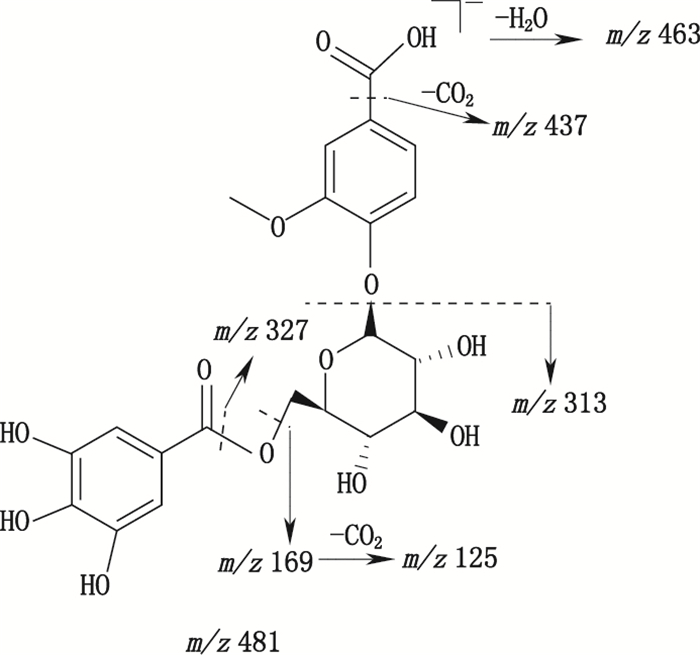
很多中药含有丰富的酚酸类成分,其药理作用广泛,如抗炎症反应,抑制血小板聚集,抗血栓,抗氧化,诱导肿瘤细胞凋亡等。从复方木鸡颗粒提取物中检测到生理活性较强的绿原酸、没食子酸、丁香酸、鞣花酸、对香豆酸和咖啡酸。酚酸类是具有1个苯核和羧基(-COOH)的酸性化合物,结构简单,其在负离子模式下丰度较高,多形成脱去羟基等活性基团的碎片离子,以丁香酸(化合物18)为例,其在负离子模式下形成准分子离子峰197[M-H]-,脱甲基形成m/z 182[M-H-CH3]-和167 m/z [M-H-2CH3]-,脱去羧基形成m/z 153[M-H-COO]-,进而分别脱去一甲基和甲氧基形成m/z 138[M-H-CH3-COO]-和121 m/z [M-H-OCH3-COOH]-,其一、二级质谱图和推断的裂解途径分别见图 8、9。此外,复方木鸡颗粒提取物中亦检测到2种葡萄糖苷,化合物14和化合物17,以化合物17香草酸-4-O-β-D-[6′-O-(3″,4″,5″-三羟基苯甲酰)]吡喃葡萄糖苷为例,其在负离子模式下形成准分子离子峰m/z 481[M-H]-,脱水形成碎片离子m/z 463[M-H-H2O],脱羧得到碎片离子m/z 437[M-H-CO2],其糖苷键断裂形成丰度较高的m/z 313[M-H-C8H8O4]-,准分子离子脱去三羟基苯甲酰形成碎片离子m/z 327[M-H-C7H6O4],糖基6′-O键断裂,形成碎片离子m/z 169[M-H-C14H16O8]-,该离子脱羧生成碎片离子m/z 125[M-H-C15H16O10]-。其一、二级质谱图和推断的裂解途径分别见图 10、图 11。

|
图 8 化合物18一级(A)和二级(B)全扫描质谱图 Fig.8 Full scan MS(A)and MS/MS(B)spectra for compound 18 |
|
图 9 化合物18主要裂解途径 Fig.9 Proposed main fragmentation pathway of compound 18 |
|
图 10 化合物17一级和二级全扫描质谱图 Fig.10 Full scan MS and MS/MS spectra for compound 17 |
|
图 11 化合物17主要裂解途径 Fig.11 Proposed main fragmentation pathway of compound 17 |
复方木鸡颗粒提取物中成分复杂,本实验首先考察了不同比例的甲醇和乙醇为提取溶剂,以及超声和回流提取方法对方剂的提取效率,结果表明30%甲醇超声提取2次的提取效果最佳。同时考察了甲醇-水、乙腈-水2种溶剂系统,以及流动相中加入不同比例的甲酸、乙酸、醋酸铵、三乙胺的分离效果,结果乙腈-0.1%甲酸的洗脱效果最佳。
本研究采用LC-LTQ-Orbitrap/MS联用技术,对满药复方木鸡颗粒的化学成分进行了研究,鉴定或推断了复方木鸡颗粒中的36个主要化学成分,其中12个生物碱类和13个黄酮类化合物是其主要的化学物质组成,推测生物碱类主要来源于复方中的山豆根,而黄酮类化合物主要来源于复方中的山豆根、核桃楸皮和菟丝子。本研究实现了对复方木鸡颗粒中化学成分的快速分类及鉴定,为复方木鸡颗粒药效物质基础和质量控制研究提供了实验基础。
| [1] |
金黎明, 胡文忠, 侯梦阳. 满药复方木鸡颗粒防治肝病的研究进展[J]. 广州中医药大学学报, 2017, 35(2): 292. JIN LM, HU WZ, HOU MY. The research progress on compound Muji granules preventing and treating liver disease[J]. J Guangzhou Univ Tradit Chin Med, 2017, 35(2): 292. |
| [2] |
宋玉荣, 姜春霞. 满药复方木鸡颗粒研究新进展[J]. 中国医药导报, 2013, 10(1): 4. SONG YR, JIANG CX. New study progress of compound muji granule of Manchu medicine[J]. China Med Her, 2013, 10(1): 4. DOI:10.3969/j.issn.1673-7210.2013.01.002 |
| [3] |
时晓亚, 李志浩, 李鹏. HPLC法测定复方木鸡颗粒中金丝桃苷的含量[J]. 中国医药导报, 2015, 21(20): 28. SHI XY, LI ZH, LI P. Determination of hyperoside in Fufang Muji granules by HPLC[J]. China Med Her, 2015, 21(20): 28. |
| [4] |
郑阳阳, 王帅, 孟宪生, 等. 复方木鸡颗粒对小鼠慢性肝损伤的影响[J]. 亚太传统医药, 2016, 12(5): 13. ZHENG YY, WANG S, MENG XS, et al. The influence of compound muji granules on chronic liver in injury in mice[J]. Asia-Pacific Tradit Med, 2016, 12(5): 13. |
| [5] |
黄海燕, 鲁静. 复方木鸡颗粒检测方法研究[J]. 药物分析杂志, 2007, 27(8): 1190. HUANG HY, LU J. Study on the quality control method of compound Muji granules[J]. Chin J Pharm Anal, 2007, 27(8): 1190. |
| [6] |
王颖, 王帅, 包永睿, 等. 复方木鸡颗粒对CCl4诱导大鼠肝硬化的防治作用[J]. 中成药, 2017, 39(3): 597. WANG Y, WANG S, BAO YR, et al. The compound Muji granules on prevention and treatment of liver cirrhosis in rats induced by CCl4[J]. Chin Tradit Pat Med, 2017, 39(3): 597. |
| [7] |
孙俊艳.雄激素受体信号通路对神经母细胞瘤的调节作用及复方木鸡颗粒对神经母细胞瘤治疗作用的初步观察[D].大连: 大连医科大学, 2017 SUN JY.Androgen Receptor Signaling Regulates the Growth of Neuroblastoma Cells In Vitro and In Vivo and Initial Observation of the Effect of Fufangmujikeli on Neuroblastoma[D].Dalian: Dalian Medical University, 2017 http://cdmd.cnki.com.cn/Article/CDMD-10161-1017131859.htm |
| [8] |
程钱.山豆根指纹图谱、含量测定及成分分析研究[D].北京: 北京中医药大学, 2017 CHENG Q.Studies on Fingerprint, Determination of the Content and Composition Analysis of Sophorae tonkinensis[D].Beijing: Beijing university of Chinese Medicine, 2017 http://cdmd.cnki.com.cn/Article/CDMD-10026-1017184013.htm |
| [9] |
郭智.基于UPLC-ESI-QTof的山豆根、苦参化学成分比较及柴胡不同提取方法柴胡皂苷a、d变化的研究[D].北京: 北京协和医学院, 2013 GUO Z.Studies on Chemical Constituents of S.tonkinensis and S.flavescens and Transformation of Saikosaponin a, d in Different Extracting Method by Using UPLC-ESI-Qtof[D].Beijing: Peking Union Medical College, 2013 http://cdmd.cnki.com.cn/article/cdmd-10023-1014352385.htm |
| [10] |
曾祖平, 郭智, 彭冰, 等. 山豆根和苦参碱类成分UPLC/Q-TOF MSE比较研究[J]. 天然产物研究与开发, 2015, 27(5): 804. ZENG ZP, GUO Z, PENG B, et al. Comparative analysis of alkaloids in Radix Sophorae Tonkinensis and Radix Sophorae Flavescentis using UPLC/Q-TOF MSE[J]. Nat Prod Res Dev, 2015, 27(5): 804. |
| [11] |
王增绘, 王冬梅, 刘艾琳, 等. 山豆根抑制丁酰胆碱酯酶活性及活性部位UPLC-Q-TOF-MS分析[J]. 中国现代中药, 2015, 17(9): 912. WANG ZH, WANG DM, LIU AL, et al. Analysis of chemical constituents of effective part of anti-butyrylcholinesterase of Sophora tonkinensis by UPLC-Q-TOF-MS[J]. Mod Chin Med, 2015, 17(9): 912. |
| [12] |
陈怀侠, 韩凤梅, 杜鹏, 等. 苦参生物碱电喷雾质谱分析[J]. 分析化学, 2006, 34(2): 205. CHEN HX, HAN FM, DU P, et al. Electrospray ionization mass spectrometry for analyses of alkaloids in Sophora flavescens Ait[J]. Chin J Anal Chem, 2006, 34(2): 205. DOI:10.3321/j.issn:0253-3820.2006.02.014 |
| [13] |
ZOU DX, WANG JF, ZHANG B, et al. Analysis of chemical constituents in Wuzi-Yanzong-Wan by UPLC-ESI-LTQ-Orbitrap-MS[J]. Molecules, 2015, 20(12): 21373. DOI:10.3390/molecules201219765 |
| [14] |
孙国东, 霍金海, 王改丽, 等. 基于UPLC-Q-TOF/MS技术的核桃楸皮成分分析[J]. 中草药, 2017, 48(4): 657. SUN GD, HUO JH, WANG GL, et al. Identification and characterization of chemical constituents in Cortex Juglandis Mandshuricae based on UPLC-Q-TOF/MS[J]. Chin Tradit Herb Drugs, 2017, 48(4): 657. |
| [15] |
何常明.苦参和山豆根黄酮类成分及其生物活性的比较研究[D].上海: 复旦大学, 2010 HE CM.Comparative Studies on Flavonoids and Their Bioactivities of Sophora flavescens and S.tokinensis[D].Shanghai: Fudan University, 2010 http://cdmd.cnki.com.cn/Article/CDMD-10246-1015570306.htm |
| [16] |
AHMADA A, TANDONA S, XUAN TD, et al. A review on phytoconstituents and biological activities of Cuscutaspecies[J]. Biomed Pharmacother, 2017, 92: 772. DOI:10.1016/j.biopha.2017.05.124 |
| [17] |
李文兰, 丁晶鑫, 藏宝珊, 等. 基于HPLC-Q TOF-MS/MS技术分析纯化后菟丝子拟雌激素活性成分[J]. 中国药学杂志, 2014, 49(20): 1791. LI WL, DING JX, ZANG BS, et al. Analysis of purified active ingredients of estrogen mimic effect in Cuscuta chinensis by HPLC-Q TOF-MS/MS[J]. Chin Pharm J, 2014, 49(20): 1791. |
 2019, Vol. 39
2019, Vol. 39 
