2. 浙江省食品药品检验研究院, 杭州 310052
2. Zhejiang Institute for, Food and Drug Control, Hangzhou 310004, China
头孢菌素类药物(cephalosporin)属于β-内酰胺类抗生素,具有适应证多,毒副作用小,抗菌谱广,效果显著等优势,使其在临床上得到广泛应用[1-2]。但该类药物稳定性差,降解杂质多,存在严重的过敏反应和安全隐患。而导致过敏反应的原因是其中含有的高分子过敏杂质和降解产物[3-4]。此外,随着抗生素在畜牧业生产中的非法应用,动物体内抗生素残留量增加,长期食用含有β-内酰胺类抗生素的食品会对人体健康带来不同程度的危害[5-6]。因此,通过总结头孢菌素类药物质谱裂解规律,可为食品中类药物监控、检测以及未知杂质结构的推导提供实验依据。
液相色谱-质谱联用仪具有检测下限低,定性定量准确,结构信息丰富等诸多优势,成为了药物分析领域的研究热点之一[7]。电喷雾质谱(ESI-MS)作为一种软电离技术,既可测定化合物的相对分子质量,又能获得较为丰富的结构信息,在医药领域的应用较为广泛,尤其适用于研究头孢菌素类药物在质谱中的裂解规律[8-10]。由于大部分头孢菌素类药物(C-2位酯化的除外)结构中同时含有羧基和氨基,使得其在电喷雾正负离子模式下都具有响应。关于头孢菌素类药物在正离子模式下的质谱裂解规律的研究报道较多。胡昌勤等采用电喷雾质谱法对头孢菌素类药物在正离子模式下的裂解规律进行研究[11]。该研究可为药物快速鉴别及头孢菌素类药物中杂质结构鉴定提供依据。但王建等采用二维液相色谱-离子肼-飞行时间质谱在正负离子模式下对头孢匹胺及其杂质结构进行研究时[12],发现头孢匹胺及其降解杂质在正离子模式得到的碎片离子都是相同的,而在负离子模式下能得到更为丰富的结构碎片,因此无法直接通过在正离子模式下得到的裂解规律对杂质结构进行判断,需要借助负离子模式下头孢匹胺的裂解规律。本文采用LC-IT-TOF/MS方法对16个头孢菌素类药物进行[M-H+]的碎片结构分析,归纳其在负离子模式下电喷雾质谱裂解规律,为头孢菌素类药物的质谱裂解提供补充,并为其的快速检测以及杂质结构鉴定提供新的依据。
1 仪器与试剂 1.1 仪器岛津Nexera-XR高效液相色谱系统(包括在线真空脱气机,双元泵(LC-30AD),自动进样器(SIL-30AC),柱温箱(CTO-20A),UV检测器(SPD-M20A));岛津公司液相色谱-离子阱-飞行时间串联质谱仪,数据采集由岛津公司的Lab-solution软件完成。
1.2 试药头孢曲松原料药(批号130480-200903)、头孢羟氨苄原料药(批号130431-201203)、头孢呋辛原料药(批号130493-201105)、头孢拉定原料药(批号130427-201107)、头孢丙烯原料药(批号20060224)、头孢唑肟原料药(批号130504-200702)、头孢呋辛酯原料药(批号130492-200402)、头孢替安原料药(批号130565-200902)、头孢噻肟原料药(批号060401)、头孢克洛原料药(批号130481-201205),由中国食品药品检定研究院提供。头孢尼西钠原料药(批号060401)、头孢米诺钠原料药(批号060401)、头孢地嗪原料药(批号060401)、头孢地尼原料药(批号110107),由浙江惠迪森医药有限公司提供。头孢匹胺原料药(批号20060224)、头孢孟多酯原料药(批号130533-201202)、头孢匹胺原料药(批号20060224),由杭州永邦医药有限公司提供。甲醇(色谱纯,Merck公司);甲酸铵(色谱纯,Sigma-Aldrich公司);Milli-Q纯化水(Merck公司)。
2 方法与结果 2.1 色谱条件流动相为10 mmol·L-1甲酸铵水溶液-甲醇(80:20),洗脱条件为0~3 min时80%A,流速0.8 mL·min-1,柱温30 ℃,检测波长254 nm,进样量1 μL。
2.2 质谱条件ESI源;负离子检测;喷雾气(nebulizer gas):1.5 L·min-1 (氮气);碰撞能:50%;碰撞气体:氩气;CDL温度:200 ℃;检测器电压:1.56 V;扫描范围:m/z 100~1200;MSn模式:自动。
2.3 供试品溶液的配制取头孢菌素原料药约1 mg,置10 mL量瓶中,加水溶解并稀释至刻度,摇匀,即得。
2.4 质谱结果IT-TOF/MS高分辨质谱在负离子模式下获得的的头孢曲松、头孢羟氨苄、头孢呋辛和头孢拉定等16个头孢菌素类药物的一级质谱数据见表 1;在负离子模式下获得的头孢曲松、头孢羟氨苄、头孢呋辛和头孢拉定等16个头孢菌素类药物的多级质谱碎片离子见表 2。
|
|
表 1 16个头孢菌素类药物在负离子模式下的一级质谱数据。 Tab.1 MS data of sixteen cephalosporins in the negative ion mode |
|
|
表 2 16个头孢菌素类药物在负离子模式下的多级质谱数据 Tab.2 MSn data of sixteen cephalosporins in the negative ion mode. |
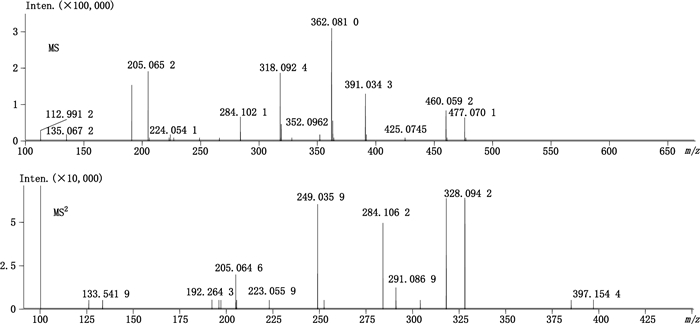
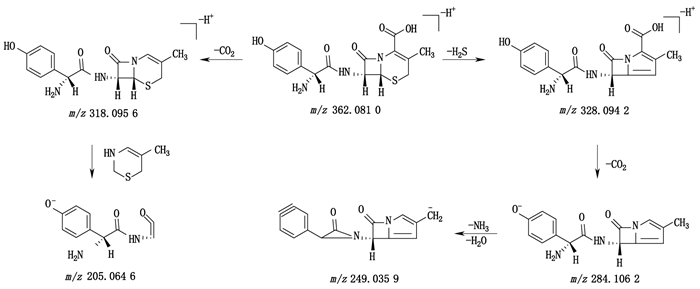
头孢羟氨苄的一级质谱图中m/z 362.081 0为[M-H+]离子,二级质谱显示[M-H+]离子的氢化噻嗪环碎裂丢失一分子中性分子H2S形成碎片离子m/z 328.094 2,接着C-2位丢失一分子CO2形成碎片离子m/z 284.106 2。碎片离子m/z 284.106 2可进一步丢失一分子NH3和H2O形成碎片离子m/z 249.035 9。碎片离子m/z 318.095 6可由母离子在C-2位丢失一分子CO2形成的,进一步发生β-内酰胺环的断裂并丢失一分子中性分子C5H9NS形成碎片离子m/z 205.064 6。头孢羟氨苄的多级质谱图、结构式及裂解途径见图 1、2。
|
图 1 头孢羟氨苄在负离子模式下的多级质谱图 Fig.1 The MS and MS2 spectra of cefadroxil in the negative ion mode |
|
图 2 头孢羟氨苄负离子模式下裂解途径 Fig.2 Proposed fragmentation pathways of cefadroxil in the negative ion mode |
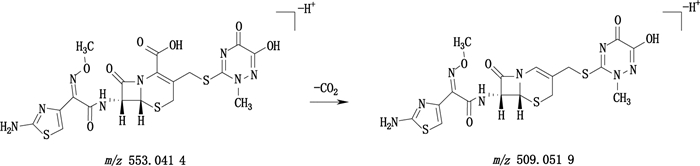
头孢曲松的一级质谱图中m/z 553.041 4为[M-H+]离子,二级质谱显示[M-H+]离子在C-2位丢失一分子CO2形成二级碎片离子m/z 509.051 9。头孢曲松的裂解途径见图 3。
|
图 3 头孢曲松负离子模式下裂解途径 Fig.3 Proposed fragmentation pathway of ceftriaxone in the negative ion mode |
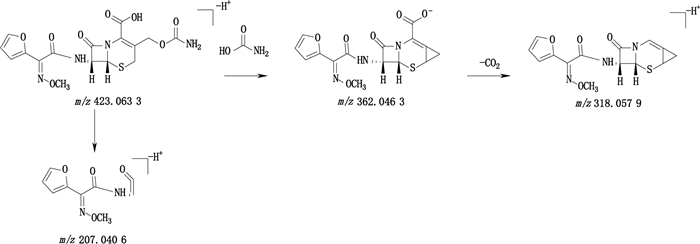
头孢呋辛的一级质谱图中m/z 423.0633为[M-H+]离子,二级质谱显示[M-H+]离子在C-3位上侧链发生醚键的断裂并丢失一分子中性分子CH3NO2形成碎片离子m/z 362.046 3,进一步在C-2位丢失一分子CO2形成碎片离子m/z 318.057 9。碎片离子m/z 207.040 6可由母离子发生β-内酰胺环的断裂形成的。头孢呋辛的结构式及裂解途径见图 4。
|
图 4 头孢呋辛负离子模式下裂解途径 Fig.4 Proposed fragmentation pathways of cefuroxim in the negative ion mode |
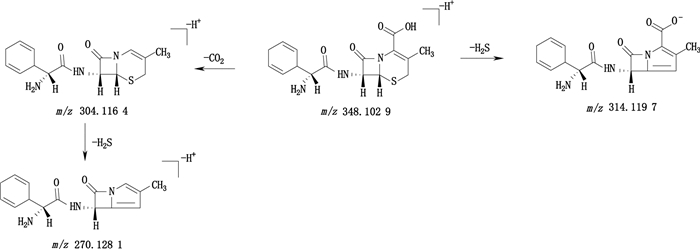
头孢拉定的一级质谱图中m/z 348.1029为[M-H+]离子,二级质谱显示[M-H+]离子在C-2位丢失一分子CO2形成碎片离子m/z 304.116 4,进一步发生氢化噻嗪环碎裂丢失一分子H2S形成碎片离子m/z 270.128 1。[M-H+]离子的另一条裂解途径是直接发生氢化噻嗪环碎裂丢失一分子H2S形成碎片离子m/z 314.119 7。头孢拉定的结构式及裂解途径见图 5。
|
图 5 头孢拉定负离子模式下裂解途径 Fig.5 Proposed fragmentation pathways of cefradine in the negative ion mode |
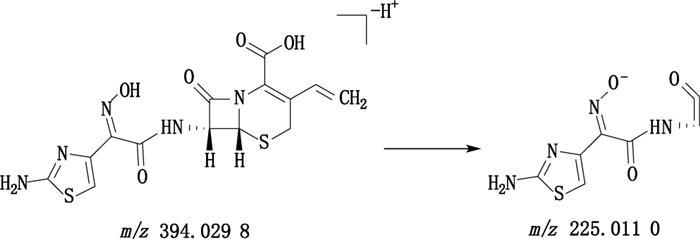
头孢地尼的一级质谱图中m/z 394.0298为[M-H+]离子,二级质谱显示[M-H+]离子发生β-内酰胺环的断裂生成碎片离子m/z 225.011 0。头孢地尼的结构式及裂解途径见图 6。
|
图 6 头孢地尼负离子模式下裂解途径 Fig.6 Proposed fragmentation pathway of cefdinir in the negative ion mode |
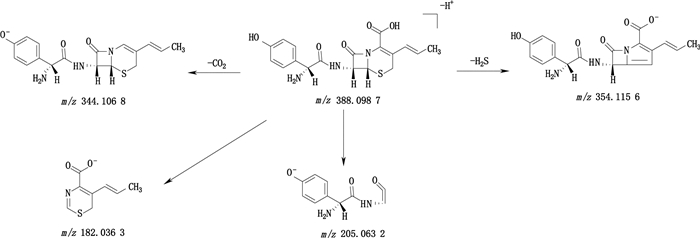
头孢丙烯的一级质谱图中m/z 388.098 7为[M-H+]离子,二级质谱显示[M-H+]离子发生β-内酰胺环的断裂形成碎片离子m/z 205.063 2和m/z 182.036 3。母离子可分别在C-2位丢失一分子CO2和氢化噻嗪环发生碎裂丢失一分子H2S形成碎片离子m/z 344.106 8和m/z 354.063 2。头孢丙烯的结构式及裂解途径见图 7。
|
图 7 头孢丙烯负离子模式下裂解途径 Fig.7 Proposed fragmentation pathways of cefprozil in the negative ion mode |
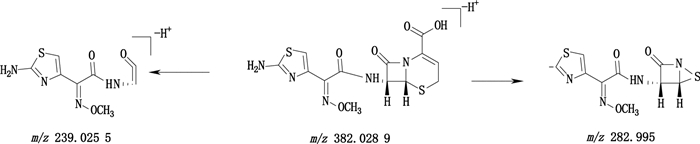
头孢唑肟的一级质谱图中m/z 382.028 9为[M-H+]离子,二级质谱显示[M-H+]离子发生β-内酰胺环的断裂生成碎片离子m/z 239.025 5。碎片离子m/z 282.995 0可由母离子发生氢化噻嗪环断裂形成的。头孢唑肟的结构式及裂解途径见图 8。
|
图 8 头孢唑肟负离子模式下裂解途径 Fig.8 Proposed fragmentation pathways of ceftizoxime in the negative ion mode |
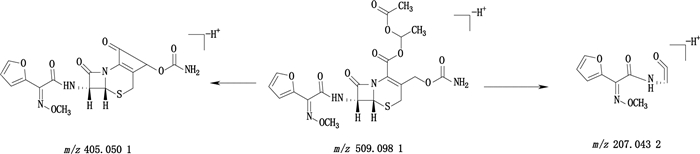
头孢呋辛酯的一级质谱图中m/z 509.098 1为[M-H+]离子,二级质谱显示[M-H+]离子发生β-内酰胺环的断裂形成碎片离子m/z 207.043 2。碎片离子m/z 405.050 1可由母离子在C-2位发生酯键的断裂与C-3位上侧链形成四元环并丢失一分子中性分子C4H8O3形成的。头孢唑肟的结构式及裂解途径见图 9。
|
图 9 头孢呋辛酯负离子模式下裂解途径 Fig.9 Proposed fragmentation pathways of cefuroxime axetil in the negative ion mode |
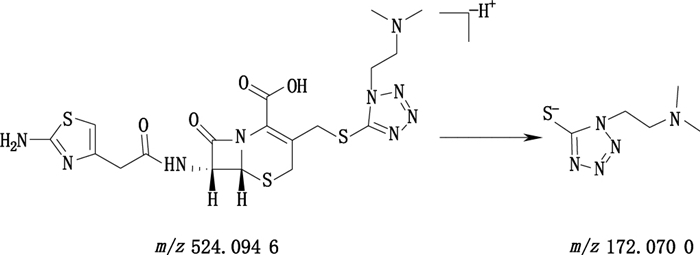
头孢替安的一级质谱图中m/z 524.094 6为[M-H+]离子,二级质谱显示[M-H+]离子在C-3位上发生醚键的断裂形成碎片离子m/z 172.070 0。头孢替安的结构式及裂解途径见图 10。
|
图 10 头孢替安负离子模式下裂解途径 Fig.10 Proposed fragmentation pathway of cefotiam in the negative ion mode |
头孢噻肟的一级质谱图中m/z 454.047 2为[M-H+]离子,二级质谱显示[M-H+]离子在C-3位侧链发生醚键的断裂并丢失一分子CH3COOH形成碎片离子m/z 394.027 2,进一步在C-2位上丢失一分子CO2形成碎片离子m/z 350.036 3。碎片离子m/z 394.027 2可分别在β-内酰胺环和氢化噻嗪环的断裂形成碎片离子m/z 239.024 7和m/z 283.014 6。头孢噻肟的结构式及裂解途径见图 11。

|
图 11 头孢噻肟负离子模式下裂解途径 Fig.11 Proposed fragmentation pathways of cefotaxime in the negative ion mode |
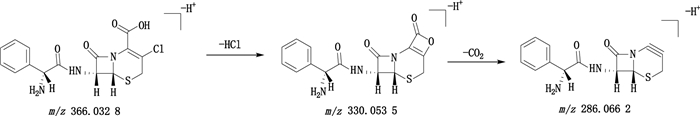
头孢克洛的一级质谱图中m/z 366.032 8为[M-H+]离子,二级质谱显示[M-H+]离子丢失一分子氯化氢并与C-2位的羧基形成四元内酯环得到碎片离子m/z 330.053 5,进一步丢失一分子CO2形成碎片离子m/z 286.066 2。头孢克洛的结构式及裂解途径见图 12。
|
图 12 头孢克洛负离子模式下裂解途径 Fig.12 Proposed fragmentation pathway of cefaclor in the negative ion mode |
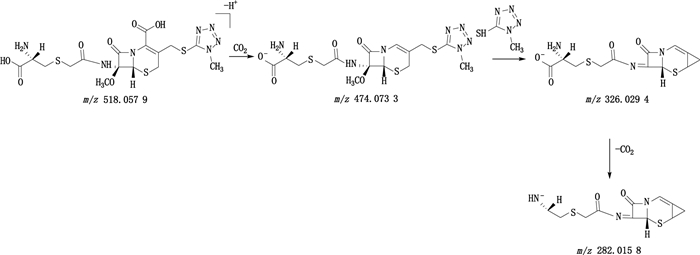
头孢米诺的一级质谱图中m/z 518.057 9为[M-H+]离子,二级质谱显示[M-H+]离子在C-2位丢失一分子CO2形成碎片离子m/z 474.073 3,接着C-3位上侧链发生醚键的断裂并丢失一分子5-巯基-1-甲基四唑形成碎片离子m/z 326.029 4。碎片离子m/z 282.015 8可由碎片离子m/z 326.029 4丢失一分子CO2形成的。头孢米诺的结构式及裂解途径见图 13。
|
图 13 头孢米诺负离子模式下裂解途径 Fig.13 Proposed fragmentation pathway of cefminox in the negative ion mode |
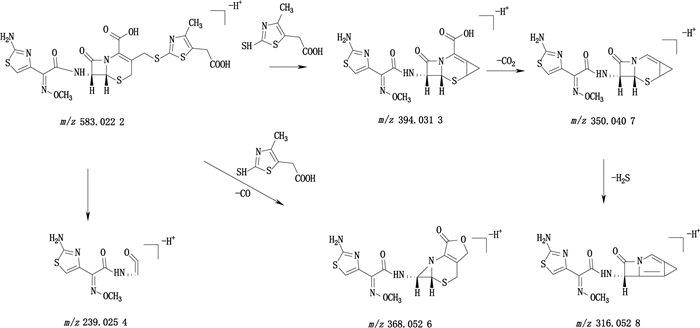
头孢地嗪的一级质谱图中m/z 583.022 2为[M-H+]离子,二级质谱显示[M-H+]离子的C-3位上侧链发生断裂并丢失一分子4-甲基-2巯基-5-羧基噻唑形成碎片离子m/z 394.031 3,进一步在C-2位丢失一分子CO2形成碎片离子m/z 350.040 7。碎片离子m/z 350.040 7发生氢化噻嗪环碎裂丢失一分子H2S形成碎片离子m/z 316.052 8。碎片离子m/z 239.025 4可由母离子发生β-内酰胺环断裂形成的。母离子可丢失一分子4-甲基-2巯基-5-羧基噻唑和一分子CO形成碎片离子m/z 368.052 6。头孢地嗪的结构式及裂解途径见图 14。
|
图 14 头孢地嗪负离子模式下裂解途径 Fig.14 Proposed fragmentation pathways of cefodizime in the negative ion mode |
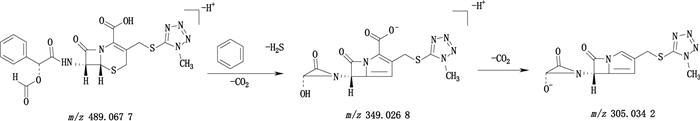
头孢孟多的一级质谱图中m/z 489.067 7为[M-H+]离子,二级质谱显示[M-H+]离子丢失一分子苯、H2S和CO2形成碎片离子m/z 349.026 8,进一步丢失一分子CO2形成碎片离子m/z 305.034 2。头孢孟多的结构式及裂解途径见图 15。
|
图 15 头孢孟多负离子模式下裂解途径 Fig.15 Proposed fragmentation pathway of cefamandole in the negative ion mode |
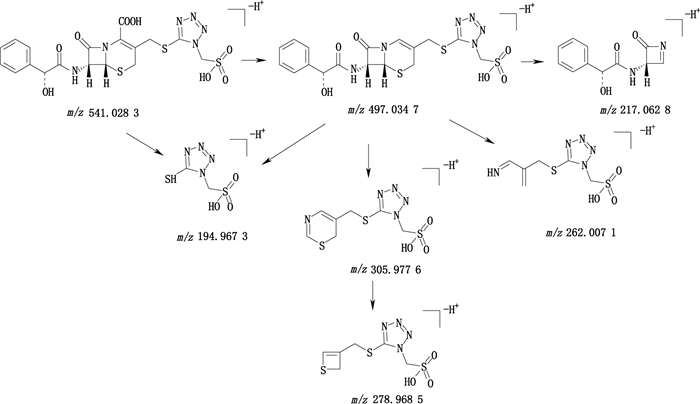
头孢尼西的一级质谱图中m/z 541.028 3为[M-H+]离子,m/z 541.0283为[M-H+]离子在C-2位上丢失一分子CO2形成碎片离子m/z 497.034 7,接着发生β-内酰胺环的断裂形成碎片离子m/z 305.978 2,进一步丢失一分子CHN形成碎片离子m/z 278.968 5。碎片离子m/z 497.034 7的另一条裂解途径是氢化噻嗪环断裂形成碎片离子m/z 217.062 8和m/z 262.006 5。碎片离子m/z 194.967 3的形成可由母离子m/z 541.028 3和碎片离子m/z 497.034 7在C-3位上的侧链发生断裂并丢失一分子5-巯基-1-磺酸甲基四唑形成的。头孢尼西的结构式及裂解途径见图 16。
|
图 16 头孢尼西负离子模式下裂解途径 Fig.16 Proposed fragmentation pathways of cefonicid in the negative ion mode |
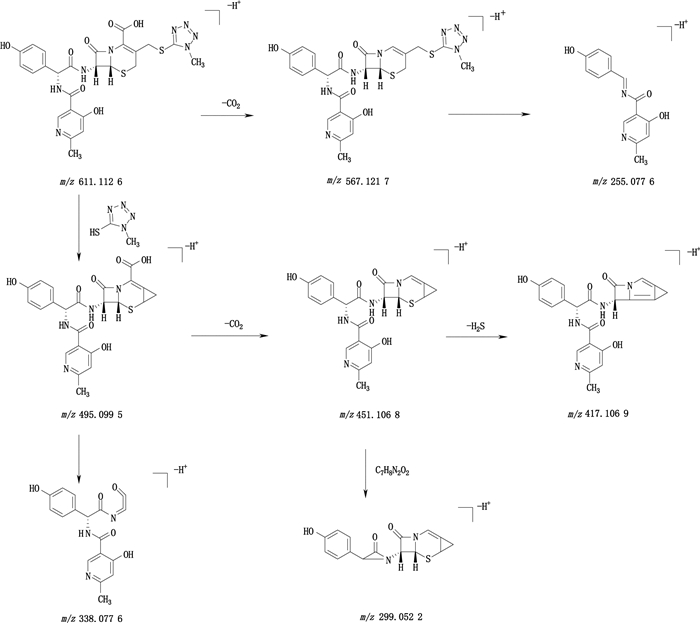
头孢匹胺的一级质谱图中m/z 611.112 6为[M-H+]离子。在负离子模式下,m/z 611.112 6为[M-H+]离子经裂解丢失一分子CO2形成碎片离子m/z 567.121 7离子,接着通过C-10和C-11键的断裂形成碎片离子m/z 255.077 6。[M-H+]离子的另一条裂解途径是丢失一分子5-巯基-1-甲基四唑形成碎片离子m/z 495.099 5,进一步在C-2位丢失一分子CO2和氢化噻嗪环发生碎裂丢失一分子H2S分别形成碎片离子m/z 451.106 8和m/z 417.106 9。碎片离子m/z 495.099 5经β-内酰胺环的断裂形成碎片离子m/z 338.077 6。碎片离子m/z 299.052 2是由碎片离子m/z 451.106 8丢失一分子C7H8N2O2形成的。头孢匹胺的结构式及裂解途径见图 17。
|
图 17 头孢匹胺负离子模式下裂解途径 Fig.17 Proposed fragmentation pathways of cefpiramide in the negative ion mode |
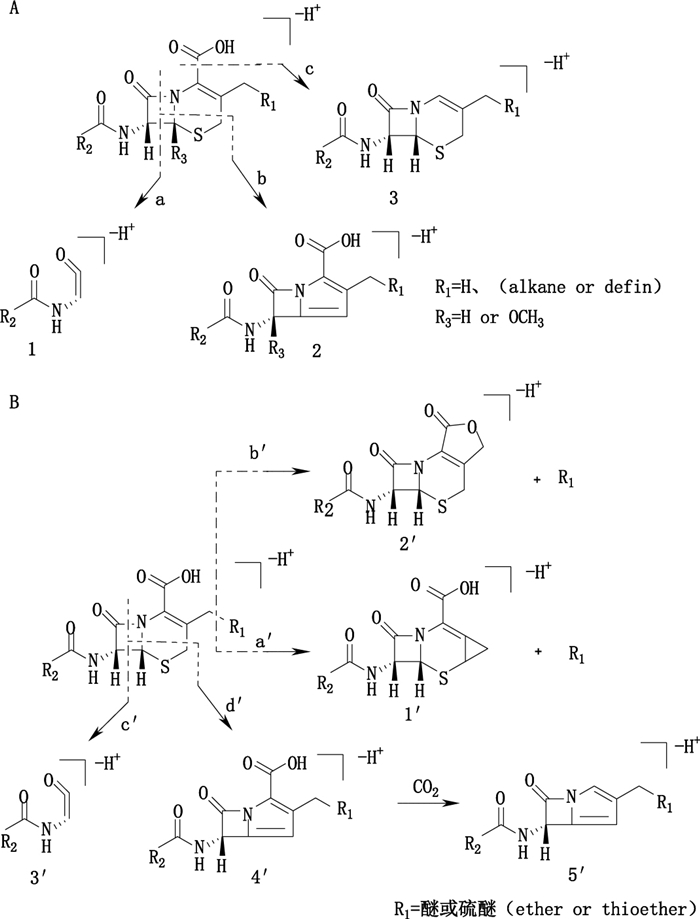
根据质谱分析,图 18显示了头孢菌素在负离子下的质谱裂解规律。此类抗生素可发生的裂解途径2类,如图 18-A所示,当头孢菌素类药物的C-3位上的侧链为烷烃或烯烃时的裂解途径,途径(a):当头孢菌素类药物在C-3位上的侧链为烷烃或烯烃的时候,C-3位上的侧链不易断裂。而β-内酰胺环的断裂成为主要的裂解途径,易于形成碎片离子1,这是因为由于β-内酰胺环和四元环具有较大的键角张力而很不稳定,所以裂解首先发生在此处;途径(b):头孢菌素类药物在负离子模式下,氢化噻嗪环容易发生碎裂并丢失一分子H2S形成碎片离子2;途径(c):头孢菌素类药物在负离子模式下,在C-2位易丢失一分子CO2形成碎片离子3。
|
图 18 头孢类抗生素的电喷雾负离子裂解规律 Fig.18 Diagrammatic sketch for electrospray MS fragmentation regularity of impurities in cephalosporins in negative ion mode |
图 18-B显示了头孢菌素类药物的C-3位上的侧链为醚或硫醚时的特征裂解途径,途径(a’):首先C-3位上侧链发生断裂,与C-5形成三元环形成碎片离子1’和R1;或发生途径(b’):C-3位上侧链发生断裂后进攻C-2位上的羧基形成五元内酯环生成碎片离子2’和R1。当C-3侧链上的碳原子与醚、硫醚等相连时,由于氧原子和硫原子含有孤对电子,使得杂化碳原子的电负性越大,不仅与之相连的氢原子越容易离去,同时生成的碳负离子也越稳定。此外,头孢菌素C-2位连有强的吸电基-COOH,由于它的吸电的共轭效应(主要)和诱导效应(次要)影响的结果,能更好地分散C-3位侧链上的负电荷,使碳负离子中间体更稳定,反应更容易进行[14]。同时,当C-3位上的侧链为醚或硫醚的时候也容易发生β-内酰胺环的断裂,氢化噻嗪环碎裂丢失一分子H2S和C-2位上丢失一分子CO2,分别形成碎片离子3’、4’和5’。
2.6.2 仪器原理不同会造成负离子结果与实验结果有差异因为质谱裂解规律与仪器本身有一定的关系,化合物在质谱仪中发生裂解,除了和设定裂解条件有关,也和仪器设计构造相关,如离子源、离子光学系统、离子阱等。因此,仪器原理不同会造成负离子结果与文献报道的实验结果有差异。
2.6.3 小结由上可见,通过16个头孢菌类药物在负离子模式下碎片离子断裂途径推断出头孢菌素类药物的特征断裂主要为β-内酰胺环断裂及氢化噻嗪环发生碎裂失去一分子H2S。当C-3侧链结构为烷烃或烯烃时,C-3位上的侧链不易断裂。而当C-3位上的侧链为醚或硫醚时易发生C-3位上的侧链断裂并与C-5形成三元环或与C-2位上的羧基形成五元内酯环或与C-2位的羧基形成五元内酯环的特征裂解。并且通过对16个头孢菌素类药物在负离子模式下的碎片结构分析,揭示了头孢菌素类药物在负离子模式下电喷雾质谱裂解规律,发现其与文献报道的正离子模式下的裂解规律有所不同,该结果可以作为头孢菌素类药物的质谱裂解提供补充,并为杂质结构解析和头孢菌素类药物的快速测定提供新的依据。
| [1] |
吴建国. 头孢菌素类抗菌药物临床应用分析[J]. 世界最新医学信息文摘, 2018, 18(44): 21. WU JG. Clinical application analysis of cephalosporins[J]. World Latest Med Inf, 2018, 18(44): 21. |
| [2] |
薛雨, 陈宇瑛. 头孢菌素类抗生素的最新研究进展[J]. 中国抗生素杂志, 2011, 36(2): 86. XUE Y, CHEN YY. New development of cephalosporin antibiotics[J]. Chin J Antibiolt, 2011, 36(2): 86. |
| [3] |
朱培曦, 贾飞, 陈悦, 等. 两对头孢菌素类抗生素异构体的质谱识别研究[J]. 质谱学报, 2015, 36(4): 350. ZHU PX, JIA F, CHEN Y, et al. Differentiation of two pairs of cephalosporins isomers by mass spectrometry[J]. J Chin Mass Spectrom Soc, 2015, 36(4): 350. |
| [4] |
金少鸿, 经洁, 郑昌亮. 头孢噻肟中高分子杂质和过敏反应关系的研究Ⅱ头孢噻肟中高分子过敏性杂质的本质探讨[J]. 中国抗生素杂质, 1986, 11(6): 463. JIN SH, JING J, ZHENG CL. Study on the relation between the high molecular weight impurities in cefotaxime and the allergic reaction Ⅱ characterization of the high molecular weight impurities in cefotaxime[J]. Chin J Antibiot, 1986, 11(6): 463. |
| [5] |
陈号, 马文静, 田晋红, 等. 牛奶中非法添加β-内酰胺酶的检测方法及研究现状[J]. 畜牧与饲料科学, 2010, 31(1): 67. CHEN H, MA WJ, TIAN JH, et al. Detecting methods for the illegal addition of β-lactamases in milk[J]. Anim Husb Feed Sci, 2010, 31(1): 67. DOI:10.3969/j.issn.1672-5190.2010.01.033 |
| [6] |
BECKER M, ZITTLAU E, PETZ M. Residue analysis of 15 penicillins and cephalosporins in bovine muscle, kidney and milk by liquid chromatography-tandem mass spectrometry[J]. Anal Chim Acta, 2004, 520(1): 19. |
| [7] |
王高升, 张宏森, 苏军, 等. 头孢替安串接质谱裂解规律的研究[J]. 黑龙江医药, 2010, 23(2): 195. WANG GS, ZHANG HS, SU J, et al. Study on fragmentation pathways of cefotiam by mean of electrospray ionization tandem mass spectrometry[J]. Heilongjiang Med J, 2010, 23(2): 195. DOI:10.3969/j.issn.1006-2882.2010.02.024 |
| [8] |
王晓雪, 赫军, 崔刚, 等. 碳青霉烯类抗生素的电喷雾质谱裂解规律分析[J]. 中国药房, 2014, 25(45): 4294. WANG XX, HE J, CUI G, et al. Analysis of electrospray mass spectrum fragmentation regularity of carbapenem antibiotics[J]. China Pharm, 2014, 25(45): 4294. DOI:10.6039/j.issn.1001-0408.2014.45.22 |
| [9] |
HORIMOTO S, MAYUMI T, AOE K, et al. Analysis of β-lactam antibiotics by high performance liquid chromatography-atmospheric pressure chemical ionization mass spectrometry using bromoform[J]. J Pharm Biomed, 2002, 30(4): 1093. DOI:10.1016/S0731-7085(02)00402-8 |
| [10] |
郭泽琴, 霍佳丽, 王建华, 等. β-内酰胺类抗生素质谱裂解机理研究[J]. 质谱学报, 2014, 35(1): 45. GUO ZQ, HUO JL, WANG JH, et al. Study on the cleavage rule of β-lactam antibiotic by electrospray quadrupole time-of-flight tandem mass spectrometry[J]. J Chin Mass Spectrom Soc, 2014, 35(1): 45. |
| [11] |
CHONG XM, HU CQ. Compilation of an ESI-MS library of β-lactam antibiotics for rapid identification of drugs[J]. Chromatographia, 2008, 68(9): 759. |
| [12] |
WNAG J, XU Y, ZHANG YF, et al. Separation and characterization of unknown impurities in cefonicid sodium by trap-free two-dimensional liquid chromatography combined with ion trap time-of-flight mass spectrometry[J]. Rapid Commun Mass Spectrom, 2017, 31(18): 1541. DOI:10.1002/rcm.7934 |
| [13] |
WANG J, XU Y, WEN CC, et al. Application of a trap-free two-dimensional liquid chromatography combined with ion trap/time-of-flight mass spectrometry for separation and characterization of impurities and isomers in cefpiramide[J]. Anal Chim Acta, 2017, 992(1). |
| [14] |
姚鸿宾. 有机化学[M]. 第4版. 北京: 高等教育出版社, 2005: 279. YAO HB. Organic Chemistry[M]. 4th Ed. Beijing: Higher Education Press, 2005: 279. |
 2019, Vol. 39
2019, Vol. 39 
