二妙丸源由《丹溪心法》,原为二妙散一方,《医学纲目》中记载,由黄柏、苍术等份,炼蜜为丸[1]。现收载于《中华人民共和国药典》2015年版,由炒黄柏、炒苍术2味中药组成,将炒黄柏、炒苍术粉碎成细粉,过筛,混匀,用水泛丸,干燥,即得。具有燥湿清热的功能,主要用于治疗湿热下注,足膝红肿热痛,下肢丹毒,白带,阴囊湿痒等病症[2]。方中黄柏为君药,来源于芸香科植物黄皮树Phellodendron chinense Schneid.的干燥树皮,行使清热燥湿之功效,以生物碱类为主要活性成分,主要包括盐酸小檗碱、盐酸巴马汀、药根碱和盐酸黄柏碱等[3-4];苍术为臣药,为菊科植物茅苍术Atractylodes lancea (Thunb.)DC.或北苍术Atractylodes chinensis (DC.)Koidz.的干燥根茎,辅助以加强燥湿健脾的功效,主要活性成分为苍术素和苍术素醇等聚乙炔类化合物[5-6]。但目前质量标准中仅以测定盐酸小檗碱的含量来作为评价二妙丸的指标,并不能反映出二妙丸的真实质量。
为保证中成药治疗的安全性和有效性,避免在其加工和储藏过程中受到各种微生物的污染,必须采取灭菌措施。目前中药灭菌的常用方法有高压灭菌、微波灭菌和60Co-γ射线辐照灭菌等[7-8],其中高压灭菌和微波灭菌均具有热特性,会破坏中成药中的不耐热成分,从而降低有效成分的含量;而60Co-γ射线辐照灭菌法可以在常温下进行,能有效保护中成药中的有效成分,因此使用越发广泛[9-10]。
本研究采用60Co-γ射线辐照对二妙丸进行消毒灭菌,并建立同时测定二妙丸中6个有效成分苍术素、苍术素醇、盐酸小檗碱、盐酸药根碱、盐酸黄柏碱和盐酸巴马汀的含量检测方法,分别考察2、5、8 kGy 3种辐照剂量对有效成分含量的影响,比较辐照前后含量变化,并确定最佳有效辐照强度条件,为二妙丸的生产灭菌提供参考依据。
1 仪器和材料 1.1 仪器Agilent 1260高效液相色谱仪(安捷伦科技有限公司,包括G1311A四元梯度泵,G1329A自动进样器,G1314B-DAD检测器,G1316A柱温箱,Agilent-Chemistation数据处理系统);AUW-220D岛津电子天平(精度0.01 mg);辐照源为60Co-γ射线辐照设备(深圳市金鹏源辐照技术有限公司);KQ-250DB型数控超声波清洗器(昆山超声波仪器有限公司,功率500 W,频率40 kHz);LRH-150B型生化培养箱(广东省医疗器械厂);YJ-875型医用净化工作台(苏州净化设备厂)。
1.2 材料对照品苍术素(atractylodin,批号111924-201605,含量99.8%)、盐酸小檗碱(berberine hydrochloride,批号110713-201613,含量86.8%)、盐酸药根碱(jatrorrhizine hydrochloride,批号110733-201609,含量89.5%)、盐酸黄柏碱(phellodendrine hydrochloride,批号111895-201504,含量94.9%)和盐酸巴马汀(palmatine hydrochloride,批号110732-201611,含量86.8%)均购自中国食品药品检定研究院,供含量测定用;苍术素醇(atractyoldinol,批号17-201715,含量98%,上海瓦兰生物科技有限公司);沙氏琼脂培养基(批号170213),胰酪胨大豆琼脂培养基(批号170322),pH 7.0无菌氯化钠-蛋白胨缓冲液(批号170307)均由北京三药科技开发公司生产;甲醇、乙腈为色谱纯,水为超纯水,其余试剂均为分析纯。
二妙丸(批号170211、170423、170506、170718、171012、171125、180109),规格:6克×20袋·盒-1,湖南天济草堂制药股份有限公司生产。
1.3 统计方法以SPSS 19.0软件包进行统计学处理,辐照前与辐照后两样本均数用配对t检验进行处理。
2 方法 2.1 灭菌效果检查取已辐照的二妙丸粉末(过4号筛)10 g作辐照后供试品,未经辐照的二妙丸10 g作辐照前对照品,分别加pH 7.0无菌氯化钠-蛋白胨缓冲液至100 mL,浸泡分散,充分振摇,制成1:10的供试液,取1:10的供试液1 mL均匀分至5个平皿(0.2 mL·皿-1),按10倍培养基稀释法制得1:100和1:1 000的供试液。取制备好的供试液1 mL,置直径90 mm的无菌平皿中,注入15~20 mL温度不超过45 ℃熔化的胰酪大豆胨琼脂培养基或沙氏葡萄糖琼脂培养基,混匀,凝固,倒置培养,除另有规定外,胰酪胨大豆琼脂培养基平板在30~35 ℃培养35 d,沙氏葡萄糖琼脂培养基平板在20~25 ℃培养57 d,观察菌落生长情况,点计辐照前后平板上生长的所有需氧菌总数、霉菌和酵母菌菌落数。结果见表 1。从表 1可以看出,随着辐照剂量增加,二妙丸的含菌量显著降低,可见60Co-γ辐照能有效除去二妙丸中微生物。
|
|
表 1 辐照前后含菌量测定结果 Tab.1 Results of bacteria level before and after irradiation |
分别称取苍术素、苍术素醇、盐酸小檗碱、盐酸药根碱、盐酸黄柏碱和盐酸巴马汀的对照品适量,用甲醇超声溶解并稀释制成每1 mL含苍术素0.090 1 mg、苍术素醇0.128 9 mg、盐酸小檗碱0.246 5 mg、盐酸药根碱0.076 8 mg、盐酸黄柏碱0.120 3 mg及盐酸巴马汀0.051 2 mg的混合对照品溶液,冰箱避光保存。
2.2.2 供试品溶液取本品适量,研细,混匀,取约1 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,称量,密塞,超声处理(功率500 W,频率40 kHz)40 min,放冷,再称量,用甲醇补足减失的量,置冰箱中(2~10 ℃)浸渍过夜,摇匀,滤液经0.45 μm微孔滤膜过滤,取续滤液,即得。避光操作。
2.3 色谱条件[11-13]色谱柱为Agilent Zorbax-C18柱(4.6 mm×250 mm,5 μm);流动相为乙腈(A)-0.5%磷酸水溶液(B)(每100 mL加十二烷基硫酸钠0.2 g),按表 2进行梯度洗脱;流速1.0 mL·min-1;检测波长见表 2;柱温30 ℃。分别取混合对照品溶液与供试品溶液各10 μL注入色谱仪,结果如图 1,表明各成分在此色谱条件下达到较好分离。
|
|
表 2 梯度洗脱程序及检测波长 Tab.2 Gradient elution program and wavelength |
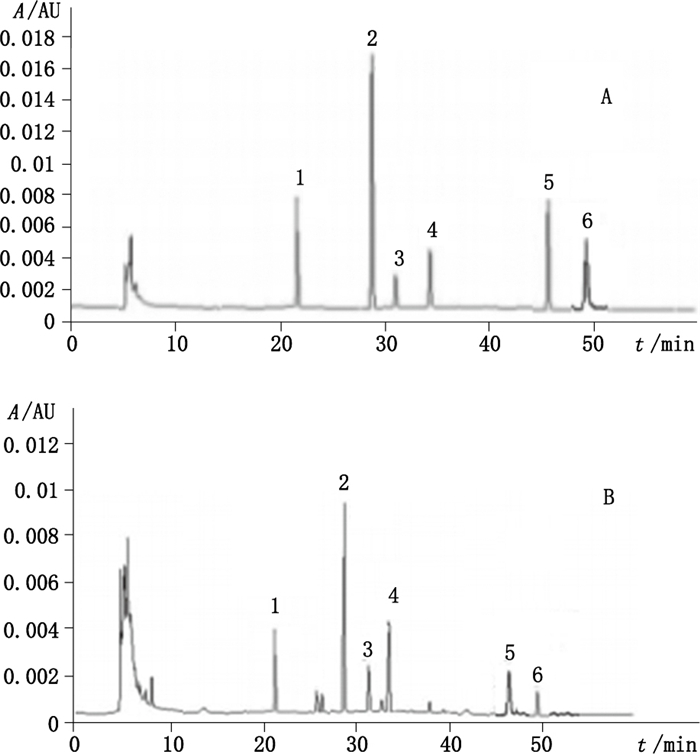
|
1.黄柏碱(phellodendrine) 2.小檗碱(berberine) 3.巴马汀(palma-tine) 4.药根碱(jatrorrhizine) 5.苍术素醇(atractyoldinol) 6.苍术素(atractylodin) 图 1 混合对照品(A)和二妙丸供试品(B)HPLC图 Fig.1 HPLC chromatograms of mixed reference substances (A) and Ermiao pills (B) |
精密吸取混合对照品溶液0.1、0.2、0.5、1.0、1.5、2.0、2.5 mL,分别置100.0 mL棕色量瓶中,用甲醇稀释至刻度,制成系列混合对照品溶液。按照“2.3”项的色谱条件进行测定,记录色谱图,以峰面积Y为纵坐标,以各对照品进样量(X,μg)为横坐标,分别绘制各组分标准曲线并进行回归计算,结果各组分线性关系良好。取混合对照溶液,用甲醇逐步稀释,吸取10 μL进行测定,取峰面积的信噪比为10倍(S/N=10)时的对照品浓度为定量下限(LOQ),回归方程及定量下限见表 3。
|
|
表 3 线性关系和定量下限 Tab.3 Linear relation and LOQ |
取“2.2.1”项下的混合对照品溶液10 μL,按“2.3”项下色谱条件连续进样6次,记录色谱图,以峰面积计,苍术素、苍术素醇、小檗碱、药根碱、黄柏碱和巴马汀的RSD(n=6)分别为0.80%、1.2%、0.90%、1.1%、0.70%及1.0%,说明仪器精密度良好。
2.4.3 重复性试验取同一批二妙丸(批号171014),按“2.2.2”项下方法平行制备6份供试品溶液,按“2.3”项下色谱条件进行分析,记录色谱图。结果苍术素、苍术素醇、盐酸小檗碱、盐酸药根碱、盐酸黄柏碱和盐酸巴马汀6个成分平均含量(n=6)分别为0.495、0.786、3.934、2.100、2.098、0.848 mg·g-1;RSD分别为0.90%、1.0%、1.1%、0.80%、1.2%和0.70%,表明重复性良好。
2.4.4 稳定性试验取同一批供试品溶液(批号171014),分别于0、4、8、12、16、20、24 h进样10 μL,记录色谱图,计算苍术素、苍术素醇、小檗碱、药根碱、黄柏碱和巴马汀峰面积的RSD(n=7)分别为1.2%、0.80%、1.0%、1.1%、0.70%和0.90%,表明供试品溶液在24 h内稳定。
2.4.5 加样回收率试验取同一批二妙丸(批号171014)6份,每份约0.5 g,精密称定,分别精密加入0.167 1 mg·mL–1苍术素对照品储备液、0.267 2 mg·mL–1苍术素醇对照品储备液、1.336 6 mg·mL–1盐酸小檗碱对照品储备液、0.549 7 mg·mL–1盐酸药根碱对照品储备液、0.702 3 mg·mL–1盐酸黄柏碱对照品储备液和0.285 7 mg·mL–1盐酸巴马汀对照品储备液各1.5 mL,按“2.2.2”项下方法制备供试溶液,按“2.3”项下色谱条件进行分析,记录色谱图,计算各成分回收率,结果见表 4。
|
|
表 4 加样回收试验结果(n=6) Tab.4 Analytical results of recoveries |
取辐照前后二妙丸7批(批号170211、170423、170506、170718、171014、171125、180109),按“2.2.2”项下方法制备供试品溶液,按“2.3”项下色谱条件进行分析,记录色谱图,分别计算苍术素、苍术素醇及盐酸小檗碱、盐酸药根碱、盐酸黄柏碱和盐酸巴马汀6个成分的含量,结果见表 5。
|
|
表 5 样品的测定结果(mg·g-1,n=7) Tab.5 The determination results of the samples |
经成组t 检验,盐酸小檗碱、盐酸药根碱、盐酸黄柏碱和盐酸巴马汀4个生物碱的含量辐照前后之间差异无统计学意义(p > 0.05),而当剂量增加到8 kGy时,苍术素、苍术素醇的含量存在显著性差异(p < 0.05)。可以认为辐照前后盐酸小檗碱、盐酸药根碱、盐酸黄柏碱和盐酸巴马汀的含量变化不大,而苍术素、苍术素醇的含量变化较大。
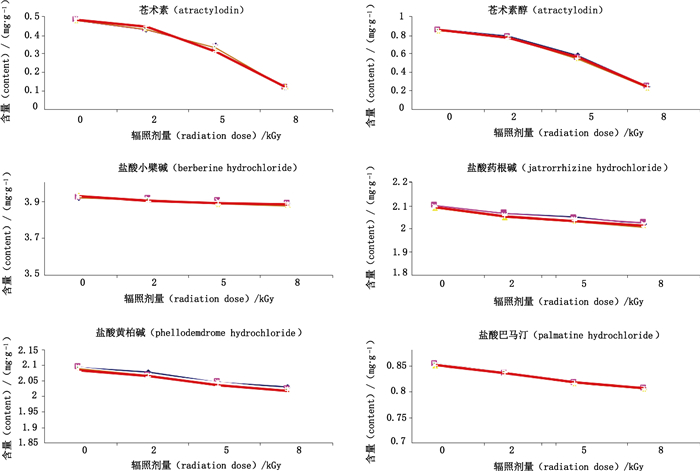
2.6 辐照剂量选择分别取辐照前后7批二妙丸(批号170211、170423、170506、170718、171014、171125、180109),分别以剂量0、2、5、8 kGy辐照处理后,按“2.2.2”项下制备供试品溶液,按“2.3”项下色谱条件进行测定,分别计算苍术素、苍术素醇、盐酸小檗碱、盐酸药根碱、盐酸黄柏碱和盐酸巴马汀的含量,并绘制含量随剂量变化折线图,结果见图 2。
|
图 2 不同剂量钴60辐照对二妙丸各成分含量的影响 Fig.2 Effect of irradiation at different doses on contents of effective ingredients in Ermiao pills |
从图 2可直观看出,盐酸小檗碱、盐酸药根碱、盐酸黄柏碱和盐酸巴马汀4个生物碱含量在辐照剂量不高于8 kGy时含量变化不大,基本上在一条直线,含量较辐照前基本变化不大,而苍术素及苍术素醇受辐照强度的影响较大,当剂量增加到2 kGy时,含量降低不明显,在5 kGy剂量处出现明显向下趋势,表示这与“2.5”项下对含量数据进行的成组t检验结果一致,故建议为防止苍术素及苍术素醇降解过度,影响二妙丸的质量,建议60Co-γ射线辐照不宜高于5 kGy。
4 讨论苍术素和苍术素醇作为苍术中的特征性成分,其结构极其相似,苍术素醇在其C-9上连有1个羟基,从而两者的极性相差很大。这2个成分均属于聚乙烯炔类化合物,带有呋喃环不饱和体系结构,性质不稳定,在光照和加热条件下易发生空间构型变化[14],降低其含量。
分别取供试品溶液及各对照品溶液,用紫外分光光度计进行扫描测定,结果显示小檗碱、药根碱、黄柏碱和巴马汀在280 nm处有最大吸收,苍术素和苍术素醇在340 nm处有最大吸收,且色谱图中各峰的峰形较好,故采用检测波长切换的方法,在0~40 min采用280 nm波长检测4个生物碱成分,40 min后切换成340 nm波长检测苍术素和苍术素醇。
在流动相的选择中,分别尝试了乙腈-水、甲醇-水、乙腈-0.5%冰醋酸水溶液、乙腈(1:1)-0.5%三乙胺-0.2%磷酸水、乙腈-0.5%磷酸水溶液(每100 mL加十二烷基硫酸钠0.1g)5种不同的流动相体系。最后发现以乙腈-0.5%磷酸水溶液(每100 mL加十二烷基硫酸钠0.2 g)为流动相进行梯度洗脱时,各成分分离良好且峰形对称。提取方法考察了回流提取、超声提取,考虑到加热对二妙丸有效成分的影响,故选用超声提取法,并通过比较不同提取溶剂体积及不同提取时间下超声提取法对6个成分的提取率,最终确定为用甲醇作溶剂超声提取40 min。
对不同品牌色谱柱[Agilent Zorbax-C18(4.6 mm × 250 mm,5μm)、Thermo Hypersil-C18(4.6 mm × 250 mm,5μm)、Shim-pack VP-ODS(4.6 mm × 250 mm,5μm)]进行了考察,结果色谱柱具有较好的耐受性。
本实验通过考察60Co-γ射线辐照对二妙丸中6个活性成分含量的影响,发现辐照剂量控制在5 kGy时,能有效地对二妙丸消毒灭菌,同时不影响制剂质量,可为今后该类药物采用60Co-γ射线辐照灭菌提供参考。
| [1] |
元·朱震亨.丹溪心法[M].大连: 辽宁科学技术出版社, 1997: 72 Yuan·ZHU ZH.Dan Xi Xin Fa[M]. Dalian: Liaoning Science and Technology Press, 1997: 72 |
| [2] |
中华人民共和国药典2015年版.一部[S]. 2015: 438 ChP 2015.Vol Ⅰ[S]. 2015: 438 |
| [3] |
吴珊珊, 胡麟, 龚晓猛, 等. HPLC法同时测定不同等级黄柏饮片中多指标成分的含量[J]. 中国药房, 2016, 27(15): 2135. WU SS, HU L, GONG XM, et al. Simultaneous determination of multi index components in different grades of Cortex Phellodendri by HPLC[J]. China Pharm, 2016, 27(15): 2135. DOI:10.6039/j.issn.1001-0408.2016.15.40 |
| [4] |
沈娟, 尹莲, 段金廒. HPLC法测定黄柏生物碱成分含量及在二妙丸类方中的比较研究[J]. 中国实验方剂学杂志, 2010, 16(13): 31. SHEN J, YIN L, DUAN JA. Determination of alkaloids in Cortex Phellodendri by HPLC and comparative study in two Miao pills[J]. Chin J Exp Tradit Med Form, 2010, 16(13): 31. DOI:10.3969/j.issn.1005-9903.2010.13.009 |
| [5] |
赵森淼, 王瑞, 侴桂新, 等. 苍术的定性定量分析方法研究[J]. 药物分析杂志, 2010, 30(5): 954. ZHAO SM, WANG R, RU GX, et al. Study on qualitative and quantitative analysis of Atractylodes[J]. Chin J Pharm Anal, 2010, 30(5): 954. |
| [6] |
陈炎明, 陈静, 侴桂新. 苍术化学成分和药理活性研究进展[J]. 上海中医药大学学学报, 2006, 20(4): 95. CHEN YM, CHEN J, RU GX. Advances in the chemical composition and pharmacological activity of Atractylodes rhizome[J]. J Shanghai Univ Tradit Chin Med, 2006, 20(4): 95. |
| [7] |
雷曦, 申鸿. 60Co-γ射线辐照贮藏中药材对其主要成分的影响[J]. 中国药房, 2002, 13(2): 119. LEI X, SHEN H. 60Co- gamma ray irradiation, the influence of Chinese herbal medicine on its main components[J]. China Pharm, 2002, 13(2): 119. DOI:10.3969/j.issn.1001-0408.2002.02.031 |
| [8] |
孙建宇. 60Co-γ射线辐照灭菌在中药及制剂中的应用研究[J]. 中国药师, 2006, 9(5): 464. SUN JY. Application of 60Co- ray irradiation sterilization in Chinese medicine and preparation[J]. China Pharm, 2006, 9(5): 464. DOI:10.3969/j.issn.1008-049X.2006.05.040 |
| [9] |
张世才, 李奉勤. 辐照灭菌在中药方面的应用研究进展[J]. 中国药业, 2009, 18(20): 76. ZHANG SC, LI FQ. Research progress in application of radiation sterilization in Chinese medicine[J]. China Pharm, 2009, 18(20): 76. DOI:10.3969/j.issn.1006-4931.2009.20.058 |
| [10] |
冯少俊, 伍振锋, 王雅琪, 等. 中药灭菌工艺研究现状及问题分析[J]. 中草药, 2015, 46(18): 2667. FENG SJ, WU ZF, WANG YQ, et al. Research status and problem analysis of Chinese medicine sterilization technology[J]. China Tradit Herb Drugs, 2015, 46(18): 2667. DOI:10.7501/j.issn.0253-2670.2015.18.001 |
| [11] |
潘超, 张莉, 王玉. HPLC法同时测定二妙丸中黄柏碱、木兰花碱、药根碱、盐酸巴马汀和盐酸小檗碱的含量[J]. 中国生化药物杂志, 2012, 33(4): 361. PAN C, ZHANG L, WANG Y. Simultaneous determination of phellodendrine, magnoflorin, jatrorrhiine, palmatine hydrochloride and berberine hydrochloride in Ermiao pillsby HPLC[J]. Chin J Biochem Pharm, 2012, 33(4): 361. |
| [12] |
郭晓, 张伟, 贾晓益, 等. HPLC双波长切换法测定二妙丸中盐酸小檗碱、苍术素含量[J]. 贵阳中医学院学报, 2017, 39(5): 31. GUO X, ZHANG W, JIA XY, et al. Determination of berberine hydrochloride and atractylodes hydrochloride in Er Miao pills by HPLC dual wavelength switching method[J]. J Guiyang Coll Tradit Chin Med, 2017, 39(5): 31. |
| [13] |
雷蓉, 周亚楠, 刘亚兰, 等. 二妙丸HPLC指纹图谱及UPLC-LTQ-Orbitrap成分分析[J]. 中草药, 2017, 48(17): 3511. LEI R, ZHOU YN, LIU YL, et al. HPLC fingerprint and UPLC-LTQ-Orbitrap analysis of Er Miao pills[J]. China Tradit Herb Drugs, 2017, 48(17): 3511. DOI:10.7501/j.issn.0253-2670.2017.17.010 |
| [14] |
黄琦, 陈炎明, 侴桂新, 等. 苍术化学指纹图谱建立及其稳定性研究[J]. 上海中医药杂志, 2012, 46(10): 76. HUANG Q, CHEN YM, RU GX, et al. Establishment and stability of chemical fingerprint of Atractylodes rhizome[J]. Shanghai J Tradit Chin Med, 2012, 46(10): 76. |
 2019, Vol. 39
2019, Vol. 39 
