四物汤是中医补血调经之经典基础方剂,始见于晚唐蔺道人所著的《仙授理伤续断秘方》,至宋代收载于我国第1部官方制剂规范《太平惠民和剂局方》,主要用于治疗月经不调、崩中漏下、恶露不止等妇人诸证,被誉为“妇女之圣药”、“妇科第一方”[1-2]。全方4味,熟地黄为君药,可滋阴养血,补髓填精;辅以当归补血养肝、活血调经;佐以白芍和营养肝;使以川芎活血行滞,四药合用,调益荣卫、滋养气血[2-3]。四物汤现已开发为膏剂、合剂、颗粒剂、片剂、胶囊剂5种剂型,并广泛应用于临床,其中四物合剂于2000年开始收载于《中华人民共和国药典》,四物颗粒也已载入《中华人民共和国药典》2015年版[4]。
目前,四物汤质量控制研究较多,但测定的指标只有单个或少数几个成分[5-7]。中药复方化学成分复杂,其单一或较少的评价指标无法科学指导复方制备工艺参数的优选和制剂成品的质量控制,测定多种成分能更好地控制复方的质量[8-10]。课题组前期在四物汤血清药物化学研究中初步辨识了四物汤中的有效成分,包括原型成分洋川芎内酯A、洋川芎内酯P、天狮酸、川芎嗪、5-羟甲基糠醛、芍药苷亚硫酸酯,以及体内有代谢的成分川芎嗪、绿原酸、儿茶素、咖啡酸、梓醇、芍药苷。结合其体内药代动力学特征、成分含量及可测性等因素,筛选出文中所测的阿魏酸、芍药苷、毛蕊花糖苷、5-羟甲基糠醛、绿原酸、咖啡酸、洋川芎内酯A、藁本内酯8个成分作为四物汤的质量控制指标。该8个成分涉及方中4味药,且都具有确切的药理活性,能协同叠加发挥四物汤补血调经的作用[11-15]。本实验采用HPLC波长切换法同时测定该8个有效成分的含量,为四物汤的质量控制与评价提供科学依据。同时,因四物合剂一直采用水提醇沉工艺制备,故实验以四物合剂水提醇沉工艺为切入点,以四物汤传统汤剂样品为对照,考察了四物汤在水提醇沉过程中产生的水煎液、醇沉上清液、醇沉沉淀中有效成分的含量变化,以明确在该工艺过程中四物汤中有效成分的传递情况。
1 仪器与试药 1.1 仪器Agilent 1260高效液相色谱仪(配置四元泵、DAD检测器、Open LAB工作站,安捷伦科技有限公司);METTLERAE240分析天平(梅特勒-托利多仪器有限公司);TGL-16G高速台式离心机(上海安亭科学仪器厂);BT 40A超声波清洗器(成都雅源科技有限公司)。
1.2 试药5-羟甲基糠醛(批号1121A022,纯度≥98.0%),洋川芎内酯A(批号P20N8F48643,纯度≥98%)均购自上海源叶生物科技有限公司;绿原酸(批号L-007-160504,纯度 > 98%)、咖啡酸(批号K-003-161216,纯度 > 98%)、芍药苷(批号S-010-170214,纯度≥98%)、毛蕊花糖苷(批号M-011-170629,纯度 > 98%)、藁本内酯(批号G-010-160719,纯度 > 98%)均购自成都瑞芬思生物科技有限公司;阿魏酸(批号MUST-16021902,纯度99.32%)购自成都曼斯特生物科技有限公司。乙腈、甲醇,色谱纯(Fisher公司);磷酸,色谱纯(成都市科龙化工试剂厂);95%乙醇,分析纯(成都市科隆化学品有限公司);水为超纯水。
熟地黄饮片(批号G02717J01)、当归饮片(批号G02617M01)、白芍饮片(批号G01217P01)、川芎饮片(批号G02217H01),均购于四川中庸药业有限公司。饮片经成都中医药大学蒋桂华教授鉴定,依次是玄参科植物地黄Rehmannia glutinosa Libosch.的干燥块根炮制品;伞形科植物当归Angelica sinensis (Oliv.)Diels. 的干燥根;毛莨科植物芍药Paeonia lactiflora Pall. 的干燥根;伞形科植物川芎Ligusticum chuanxiong Hort. 的干燥根茎。
2 方法与结果 2.1 溶液的制备 2.1.1 混合对照品溶液分别精密称取对照品5-羟甲基糠醛、绿原酸、咖啡酸、芍药苷、阿魏酸、毛蕊花糖苷、洋川芎内酯A、藁本内酯适量,加甲醇制成质量浓度分别为0.150、0.360、0.392、0.442、0.416、0.846、0.239、0.339 mg·mL-1的单一成分对照品储备液。分别精密量取上述对照品储备液适量,置同一量瓶中,用甲醇制成质量浓度分别为19.50、31.80、5.88、332.00、29.10、8.46、47.80、22.60 μg·mL-1的混合对照品溶液。
2.1.2 供试溶液四物汤传统汤剂:取当归、川芎、白芍、熟地黄各25 g,第1次加7倍量水浸泡0.5 h,煎煮1 h,第2、3次各加6倍量水煎煮1.5 h,合并煎液,滤过,浓缩并定容至200 mL,备用。
四物汤水煎液:取当归、川芎各25 g,加7倍量水,冷浸0.5 h,水蒸气蒸馏法收集蒸馏液25 mL,水煎液另器保存;药渣与白芍、熟地黄各25 g,第1次加7倍量水煎煮1 h,第2、3次各加6倍量水煎煮1.5 h,合并煎液,滤过,滤液与上述水煎液、蒸馏液合并,浓缩并定容至200 mL,备用。
四物汤醇沉上清液:取上述水煎液100 mL,加乙醇至含醇量达55%,静置24 h,离心(3 500 r·min-1,5 min),上清液回收乙醇,加水定容至100 mL,备用。
四物汤醇沉淀物:离心后所得醇沉淀物,加水涡旋混溶,定容至100 mL,备用。
分别精密量取上述4种备用液1 mL,加水定容至10 mL,离心(12 000 r·min-1,5 min),过0.22 μm微孔滤膜,即得四物汤传统汤剂供试溶液、四物汤水煎液样品、四物汤醇沉上清液供试溶液、四物汤醇沉淀物供试溶液。
2.1.3 阴性样品溶液按照“2.1.2”项下四物汤水煎液样品的制备方法分别制备缺川芎、当归、白芍、熟地黄的阴性样品。
2.2 色谱条件色谱柱:Agilent HC-C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.5%磷酸水溶液(C),梯度洗脱(0~10 min,5%A→13%A;10~35 min,13%A→21%A;35~40 min,21%A→65%A;40~47 min,65%A→80%A;47~50 min,80%A);流速:1.0 mL·min-1;柱温:23 ℃;进样量:10 μL;检测波长:280 nm(0~10 min、检测5-羟甲基糠醛45~46 min检测洋川芎内酯A)、327 nm(10~20 min检测绿原酸、咖啡酸)、230 nm(20~25 min检测芍药苷)、316 nm(25~29 min检测阿魏酸)、334 nm(29~45 min检测毛蕊花糖苷)、324 nm(46~50 min检测藁本内酯)。
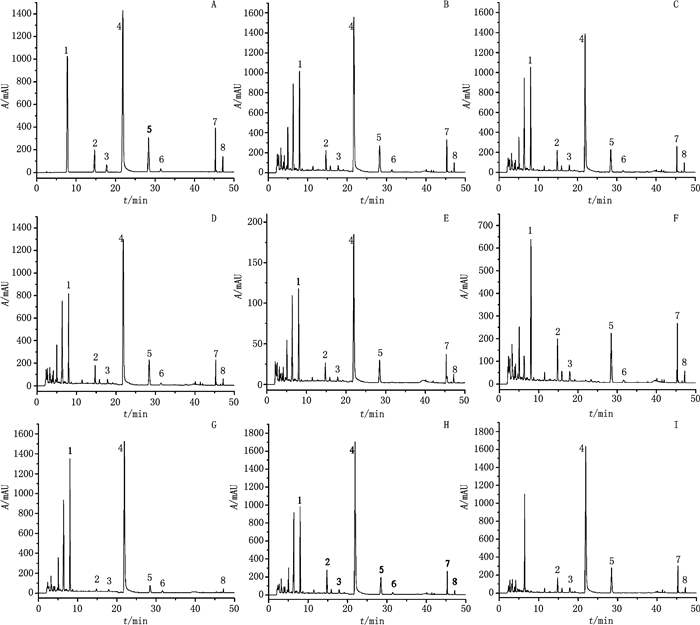
2.3 专属性试验取混合对照品溶液、供试品溶液和阴性样品溶液,按“2.2”项下色谱条件进行测定。结果供试品溶液中5-羟甲基糠醛、绿原酸、咖啡酸、芍药苷、阿魏酸、毛蕊花糖苷、洋川芎内酯A、藁本内酯与其他峰分离度良好,阴性样品色谱图中,在所测成分的相应位置处无干扰,表明该方法专属性良好,色谱图见图 1。
|
1. 5-羟甲基糠醛(5-hydroxymethylfurfural)2.绿原酸(chlorogenic acid)3.咖啡酸(caffeic acid)4.芍药苷(paeoniflorin)5.阿魏酸(ferulic acid)6.毛蕊花糖苷(acteoside)7.洋川芎内酯A(senkyunolide A)8.藁本内酯(ligustilide) 图 1 混合对照品(A)、四物汤水煎液样品(B)、四物汤传统汤剂样品(C)、四物汤醇沉上清液样品(D)、四物汤醇沉淀物样品(E)及缺白芍(F)、缺川芎(G)、缺当归(H)、缺熟地黄(I)阴性样品的HPLC色谱图 Fig.1 HPLC chromatograms of mixed reference substance (A), Siwu decoction sample (B), Siwu traditional decoction sample (C), Siwu ethanol supernatant sample (D), Siwu ethanol sediment sample (E), negative sample without Paeoniae Alba Radix (F), negative sample without Chuanxiong Rhizoma (G), negative sample without Angelicae Sinensis Radix (G) and negative sample without Rehmanniae Radix Praeparata (I) |
取“2.1.1”项下混合对照品溶液适量,按2倍稀释法分别用甲醇将其稀释1/2、1/4、1/8、1/16、1/32倍,制得系列质量浓度的混合对照品溶液,按“2.2”项下色谱条件进行测定。以色谱峰峰面积(Y)对质量浓度(X)进行线性回归,得各成分的线性回归方程,结果见表 1,表明各成分在测定范围内线性关系良好。
|
|
表 1 线性关系考察结果 Tab.1 Results of linear relationship |
取混合对照品溶液,按“2.2”项下色谱条件连续进样6次,计算各成分峰面积的RSD。结果5-羟甲基糠醛、绿原酸、咖啡酸、芍药苷、阿魏酸、毛蕊花糖苷、洋川芎内酯A和藁本内酯峰面积的RSD分别为0.70%、0.60%、0.60%、1.1%、0.60%、0.60%、0.10%、0.60%,表明该仪器精密度良好。
2.6 重复性试验平行制备四物汤水煎液的供试溶液6份,按“2.2”项下色谱条件进行测定,计算各成分的含量。结果5-羟甲基糠醛、绿原酸、咖啡酸、芍药苷、阿魏酸、毛蕊花糖苷、洋川芎内酯A和藁本内酯的平均含量分别为0.169、0.195、0.039、3.114、0.246、0.023、0.404、0.164 mg·g-1,RSD分别为2.0%、1.9%、2.8%、1.9%、2.3%、2.6%、1.3%、2.6%,表明该方法重复性良好。
2.7 稳定性试验取同一四物汤水煎液的供试溶液,室温放置,按“2.2”项下色谱条件分别于0、2、4、8、12、24 h进样,计算各成分峰面积的RSD。结果5-羟甲基糠醛、绿原酸、咖啡酸、芍药苷、阿魏酸、毛蕊花糖苷、洋川芎内酯A和藁本内酯峰面积的RSD分别为0.70%、1.1%、1.0%、0.90%、0.40%、1.70%、0.70%、0.50%,表明该供试品溶液在室温条件下24 h内稳定性良好。
2.8 加样回收率试验精密吸取6份已知各成分量的四物汤水煎液的供试溶液10 mL,分别精密加入混合对照品溶液(5-羟甲基糠醛1.63 mg·mL-1、绿原酸1.91 mg·mL-1、咖啡酸0.36 mg·mL-1、阿魏酸2.51 mg·mL-1、毛蕊花糖苷0.28 mg·mL-1、洋川芎内酯A 4.10 mg·mL-1、藁本内酯1.65mg·mL-1)0.1 mL,再分别精密加入芍药苷对照品3.11 mg,按照“2.2”项下色谱条件进行测定。结果见表 2。该方法回收率良好。
|
|
表 2 加样回收率试验结果 Tab.2 The results of recovery rate test |
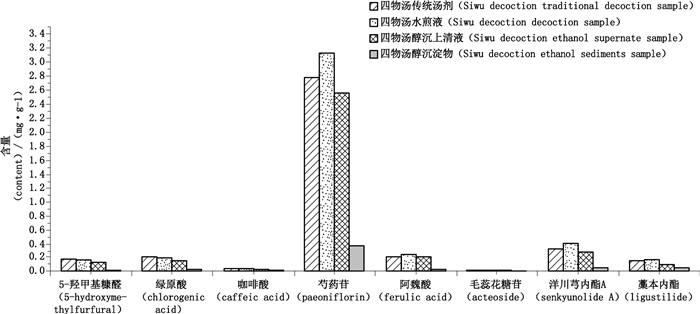
取6份饮片,按“2.1.2”项下方法平行制备4种供试溶液,按“2.2”项下色谱条件进行测定,根据标准曲线计算各成分的含量,结果见表 3、图 2。
|
|
表 3 四物汤中8个有效成分的含量测定结果(mg·g-1,n=6) Tab.3 Determination results of eight active components in Siwu decoction |
|
图 2 四物汤中8个有效成分的测定结果(n=6) Fig.2 Determination of eight active components in Siwu decoction |
在处理样品时,考虑到溶剂对成分的影响,实验中分别考察了25%甲醇水、50%甲醇水、75%甲醇水、纯甲醇和纯水作为溶剂。综合考虑待测成分的色谱峰峰形及分离度,最终选择以纯水作为样品溶剂。
3.2 流动相的选择实验中分别对甲醇-水、乙腈-水流动相体系进行了考察,结果乙腈-水在色谱峰峰形、分离度及出峰数量等方面均优于甲醇-水,但该体系存在部分待测成分的分离效果不佳,峰形拖尾现象。在此基础上,分别考察了乙腈-0.1%磷酸水溶液、乙腈-0.5%磷酸水溶液,结果乙腈-0.5%磷酸水溶液能有效地提高待测成分的分离度以及改善峰形,故最终选择以乙腈-0.5%磷酸水溶液作为流动相。
3.3 检测波长的选择本文8个待测成分的最大紫外吸收波长各不相同,为了使待测成分处于各自的最大吸收并且避免极性相似但检测波长不一致成分的干扰,课题组采用波长切换法对各成分进行检测[16-17]。实验前采用二极管阵列检测器(DAD检测器)对各成分进行全波长扫描,通过分析三维图谱,考虑待测成分的最大吸收及其他成分的干扰,最终将各成分的检测波长选定为5-羟甲基糠醛、洋川芎内酯A(280 nm)、绿原酸、咖啡酸(327 nm)、芍药苷(230 nm)、阿魏酸(316 nm)、毛蕊花糖苷(334 nm)、藁本内酯(324 nm)。
3.4 实验结果分析本实验建立了采用HPLC波长切换法同时测定四物汤中8个有效成分(5-羟甲基糠醛、绿原酸、咖啡酸、芍药苷、阿魏酸、毛蕊花糖苷、洋川芎内酯A、藁本内酯)的含量测定方法,该方法合理可行,重复性好,能准确反映四物汤复方的内在质量,为该方的质量控制及评价提供了科学有效的方法。
测定结果显示,从8个成分的总体含量变化来看,先提取蒸馏液再煎煮的现代提取工艺较传统煎煮工艺更为科学。与水煎液相比,醇沉上清液的供试溶液中5-羟甲基糠醛、绿原酸、咖啡酸、芍药苷、阿魏酸、毛蕊花糖苷的损失比例为15%~20%,洋川芎内酯A、蒿本内酯的损失比例分别为31%、41%,醇沉沉淀中残留了少量有效成分。说明该水提醇沉工艺在达到提取精制及减少服用量的同时,有效成分有一定的损失,对当归、川芎中内酯类成分影响较大。为提高四物汤用药的有效性,应进一步完善四物汤质量控制与评价体系,对醇沉时间、醇沉浓度等工艺参数进行进一步优化,以提高四物汤生产质量控制水平。
| [1] |
李泓涛, 李胜涛. 四物汤药理作用及其应用研究[J]. 光明中医, 2016, 31(6): 897. LI HT, LI ST. Study on the pharmacological effects and application of Siwu Tang[J]. Guangming Tradit Chin Med, 2016, 31(6): 897. DOI:10.3969/j.issn.1003-8914.2016.06.074 |
| [2] |
唐昆, 吴希. 四物汤的现代药理作用和临床应用[J]. 中国中医急症, 2006, 15(12): 1397. TANG K, WU X. Modern pharmacological effects and clinical application of Siwu Tang[J]. J Emerg Tradit Chin Med, 2006, 15(12): 1397. DOI:10.3969/j.issn.1004-745X.2006.12.054 |
| [3] |
胡琦, 郭平. 四物汤补血机制研究进展[J]. 山东中医杂志, 2017, 36(9): 819. HU Q, GUO P. Research progress on enriching blood mechanism of Siwu decoction[J]. Shandong J Tradit Chin Med, 2017, 36(9): 819. |
| [4] |
中华人民共和国药典2015年版.一部[S]. 2015: 786 ChP 2015.Vol Ⅰ[S]. 2015: 786 |
| [5] |
刘婷婷, 何瑶, 王丽娟, 等. HPLC法同时测定四物汤中6种成分的含量[J]. 中药材, 2016, 39(7): 1602. LIU TT, HE Y, WANG LJ, et al. Simultaneous determination of six components in Siwu decoction by HPLC[J]. J Chin Med Mater, 2016, 39(7): 1602. |
| [6] |
李思漫, 林灿城, 陈文青, 等. 高效液相色谱法测定四物汤中阿魏酸的含量[J]. 广东化工, 2015, 42(15): 221. LI SM, LIN CC, CHEN WQ, et al. Determination of ferulic acid in Siwu Tang by HPLC[J]. Guangdong Chem Ind, 2015, 42(15): 221. DOI:10.3969/j.issn.1007-1865.2015.15.109 |
| [7] |
黄月纯, 刘翠玲, 张琼丹, 等. 四物汤中四种成分的含量测定研究[J]. 现代中药研究与实践, 2010, 24(4): 64. HUANG YC, LIU CL, ZHANG QD, et al. Study on the content determination of four components in Siwu decoction[J]. Res Pract Chin Med, 2010, 24(4): 64. |
| [8] |
郝乘仪, 郭淑英, 朱鹤云, 等. HPLC法同时测定牛黄清感胶囊中6个成分的含量[J]. 药物分析杂志, 2017, 37(3): 422. HAO CY, GUO SY, ZHU HY, et al. Simultaneous determination of six compounds in Niuhuang Qinggan capsules by HPLC[J]. Chin J Pharm Anal, 2017, 37(3): 422. |
| [9] |
CUI HR, XU GH, WU MQ, et al. Simultaneous determination of eight active components in Liuwei Wuling tablet using HPLC[J]. Chin Herb Med, 2016, 8(4): 331. DOI:10.1016/S1674-6384(16)60059-X |
| [10] |
袁强华, 呼梅, 宋英, 等. HPLC-DAD波长切换法同时测定化扁汤中10种有效成分的含量[J]. 中国医院药学杂志, 2017, 37(1): 30. YUAN QH, HU M, SONG Y, et al. Simultaneous determination of ten active components in Huabian decoction by HPLC-DAD wavelength switching method[J]. Chin J Hosp Pharm, 2017, 37(1): 30. |
| [11] |
何瑶, 王丽娟, 刘婷婷, 等. 基于代谢组学技术分析四物汤治疗原发性痛经证的作用机制[J]. 中国实验方剂学杂志, 2017, 23(12): 82. HE Y, WANG LJ, LIU TT, et al. Analysis of therapeutic mechanism of Siwu Tang in primary dysmenorrhea syndrome based on metabolomics technique[J]. China J Exp Tradit Med Form, 2017, 23(12): 82. |
| [12] |
曾柳庭, 刘慧萍, 杨凯麟, 等. 四物汤有效成分的关联性分析[J]. 中成药, 2017, 39(3): 576. ZENG LT, LIU HP, YANG KL, et al. Correlation analysis of active components in Siwu Tang[J]. Chin Tradit Pat Med, 2017, 39(3): 576. |
| [13] |
ZHAO L, CHEN J, SU J, et al. In vitro antioxidant and antiproliferative activities of 5-hydroxymethylfurfural[J]. J Agric Food Chem, 2013, 61(44): 10604. DOI:10.1021/jf403098y |
| [14] |
唐于平, 黄美艳, 张彦华, 等. 四物汤类方与组方药材及其所含主要芳香酸体外抗氧化活性比较与量效关系研究[J]. 中国中西医结合杂志, 2012, 32(1): 64. TANG YP, HUANG MY, ZHANG YH, et al. Comparison of in vitro anti-oxidative activities among Siwu decoction Serial Recipes, their composed crude herbs, and main aromatic acids, as well as their dose-effect correlation[J]. Chin J Integr Tradit West Med, 2012, 32(1): 64. |
| [15] |
张海鸣, 闫寒, 彭娟, 等. 脂质体平衡透析-液质联用色谱法筛选四物汤药效物质的研究[J]. 药物分析杂志, 2014, 34(12): 2107. ZHANG HM, YAN H, PENG J, et al. Study on screening of effective substances of Siwu decoction by liposome equilibrium dialysis and LC-MS method[J]. Chin J Pharm Anal, 2014, 34(12): 2107. |
| [16] |
高森, 白雪, 文柳静, 等. HPLC-DVD变波长法同时测定跌打止痛散中6种指标成分[J]. 中草药, 2016, 47(16): 2863. GAO S, BAI X, WEN LJ, et al. Determination of six kinds of index components in Dieda Zhitong San by HPLC-DVD variable wavelength method[J]. Chin Tradit Herb Drugs, 2016, 47(16): 2863. DOI:10.7501/j.issn.0253-2670.2016.16.014 |
| [17] |
张梅, 任爱农, 杨玉兰, 等. HPLC波长切换法同时测定清清颗粒中9个成分的含量[J]. 药物分析杂志, 2015, 35(1): 29. ZHANG M, REN AN, YANG YL, et al. Simultaneous determination of contents of nine components in Qingqing granules by HPLC wavelength switching method[J]. Chin J Pharm Anal, 2015, 35(1): 29. |
 2019, Vol. 39
2019, Vol. 39 
