龟甲及龟甲胶中25种金属及有害元素含量测定及初步风险评估
龙小艳
1,2
,
陈莹
1,2,
费毅琴
2,
肖凌
2

,
聂晶
2

,
黄志军
1
1. 武汉理工大学, 武汉 430070;
2. 湖北省药品监督检验研究院, 武汉 430075
收稿日期:2018-05-06
基金项目:国家药典委员会药品医疗器械审评审批制度改革子课题(ZG2016-1);湖北省食品药品监督管理局科研项目"基于特征肽及模式识别技术的龟甲药材及饮片真伪鉴定研究"(201601+01);国家药典委员会《中国药典》药品标准提高项目2016年33号"龟甲胶质量标准提高研究"
摘要:目的:分析研究龟甲及龟甲胶中25种金属及有害元素的含量,对其进行风险评估,为质量保证提供依据。方法:采用电感耦合等离子体质谱(ICP-MS)法测定20种微量元素含量,射频功率1 200 W,雾化气流速1.04 L·min-1,辅助气流速1.3 L·min-1,等离子体气流速15 L·min-1,蠕动泵20.0 r·min-1,重复次数3次,扫描次数10次;采用火焰原子吸收光谱(FAAS)法测定5种常量元素含量,锌(Zn)、镁(Mg)、铁(Fe)、锶(Sr)、钙(Ca)的波长分别是213.8、279.6、248.3、460.7、422.7 nm,Zn、Mg、Fe、Ca的灯电流为5.0 mA,Sr的为3.0 mA,光谱通带均为0.2 nm;分析各元素间相关性。根据风险评估要求,对龟甲及龟甲胶中金属及有害元素安全性进行评估。结果:镉(Cd)、铍(Be)、银(Ag)、汞(Hg)、钛(Ti)、镝(Dy)、钯(Pd)、硒(Se)8种元素在龟甲中未检出。龟甲制成龟甲胶后金属及有害元素含量大幅降低。23批龟甲中有3批的砷(As)、铅(Pb)实际测定值(含量范围分别为0.3~1.5和1.1~1.3 mg·kg-1)大于最大残留限量值,15批龟甲胶中的Pb、As、Hg、Cd、铜(Cu)实际测定值(含量范围分别为0~0.23、0~0.18、0~0.005、0~0.01和0~0.59 mg·kg-1)均远小于最大残留限量值。结论:龟甲中As、Pb存在一定风险,龟甲胶中的金属及有害元素安全风险较低。
关键词:金属及有害元素 龟甲 龟甲胶 相关性分析 风险评估 电感耦合等离子体质谱(ICP-MS) 火焰原子吸收光谱(FAAS)
Determination and risk evaluation of 25 metals and harmful elements in Testudinis Carapax et Plastrum and Testudinis Carapax et Plastri Colla
LONG Xiao-yan1,2
,
CHEN Ying1,2,
FEI Yi-qin2,
XIAO Ling2

,
NIE Jing2

,
HUANG Zhi-jun1
1. Wuhan University of Technology, Wuhan 430070, China;
2. Hubei Institute for Drug Control, Wuhan 430075, China
Abstract: Objective: To analyze the contents of 25 metals and harmful elements in Testudinis Carapax et Plastrum and Testudinis Carapax et Plastri Colla, and to perform the risk evaluation in order to provide reference for quality assurance.Methods: The contents of 20 trace elements were determined by inductively coupled plasma mass spectrometry (ICP-MS) and the parameters of the instrument were as follows:radio frequency power:1 200 W, atomizing gas flow rate:1.04 L·min-1, auxiliary gas flow rate:1.3 L·min-1, plasma gas flow:15.0 L·min-1, peristaltic pump:20.0 r·min-1, repeat times:3 times, and scanning times:10 times.The contents of 5 macro elements were determined by flame atomic absorption spectroscopy (FAAS) with wavelengths of Zn, Mg, Fe, Sr, Ca at 213.8 nm, 279.6 nm, 248.3 nm, 460.7 nm and 422.7 nm, respectively.The lamp currents of Zn, Mg, Fe, and Ca were 5.0 mA, and that of Sr was 3.0 mA.The spectral passband was 0.2 nm.The correlations between elements were analyzed.According to the risk assessment requirements, the safety of metals and harmful elements in Ttestudinis Carapax et Plastrum and Testudinis Carapax et Plastri Colla was evaluated.Results: Cd, Be, Ag, Hg, Ti, Dy, Pd and Se were not detected in Testudinis Carapax et Plastrum.The contents of metals and harmful elements were greatly reduced in Testudinis Carapax et Plastri Colla.The contents of As and Pb in 3 batches of Testudinis Carapax et Plastrum exceeded the maximum residue limits with contents range of 0.3-1.5 mg·kg-1 and 1.1-1.3 mg·kg-1, respectively.The contents of Pb, As, Hg, Cd and Cu in 15 batches of Testudinis Carapax et Plastri Colla were all far below the maximum residue limits with content ranges of 0-0.23 mg·kg-1, 0-0.18 mg·kg-1, 0-0.005 mg·kg-1, 0-0.01 mg·kg-1 and 0-0.59 mg·kg-11, respectively.Conclusion: Risks of As and Pb residues are existed in Testudinis Carapax et Plastrum, and there are no risks of metals and harmful elements residues in Testudinis Carapax et Plastri Colla.
Keywords:
metals and harmful elements Testudinis Carapax et Plastrum Testudinis Carapax et Plastri Colla correlation analysis risk evaluation inductively coupled plasma mass spectrometry (ICP-MS) flame atomic absorption spectroscopy(FAAS)
龟甲药用始载于汉代《神农本草经》[1],列为上品。《中华人民共和国药典》(简称《中国药典》)2015年版规定龟甲为龟科动物乌龟Chinemys reevesii(Gray)的背甲及腹甲;其味咸、甘,性微寒,归肝、肾、心经,具有滋阴潜阳,益肾强骨,固经止血,补心安神等功能;多分布于山东、安徽、陕西、湖北、四川、云南、广东、广西、海南等湖泊水域地[2]。龟甲经水煎煮,加黄酒等辅料浓缩制成的胶剂即为龟甲胶。有文献报道[3]龟甲胶中砷、铅、铬、镉、铜、汞6种金属及有害元素的含量,但目前还未见龟甲及龟甲胶中金属及有害元素含量测定分析的全面报道。本文采用简便、准确、灵敏度高的ICP-MS法和FAAS法测定了23批龟甲及15批龟甲胶中25种元素的含量;基于25种元素的含量进一步分析元素之间的相关性;依据《中国药典》、联合国粮农组织(Food and Agriculture Oganization,FAO)和世界卫生组织(WHO)下的食品添加剂联合专家委员会(Joint FAO/WHO Expert Committee on Food Additives,JECFA)中药材标准等金属及有害元素限量标准,对龟甲及龟甲胶中砷、铅、铬、铜、汞5种金属及有害元素进行初步风险评估,探讨龟甲及龟甲胶中金属及有害元素的安全性,为制订龟甲及龟甲胶质量标准提供依据。
1 仪器及试药
Scientific X Series2 ICP-MS仪(Thermo Fisher公司),AAnaiyst 800原子吸收分光光度计(Perkin Elmer公司),Multiwave型微波消解仪(Anton Paar公司),Millipore Mill-Q超纯水机(Millipor公司)。硝酸、30%过氧化氢溶液均为超纯级,超纯水自制。内标单元素标准溶液:锗(Ge,批号GSB04-1723)、铟(Y,批号GSB04-1731)、铋(Bi,批号GSB04-1719)均购自中国计量科学研究院,质量浓度为100 mg·L-1。铅(Pb)、镉(Cd)、砷(As)、汞(Hg)、铜(Cu)、铝(Al)、铬(Cr)、锰(Mn)、钯(Pd)、钡(Ba)、钨(W)、镍(Ni)、钼(Mo)、硒(Se)、镝(Dy)、铊(Tl)、银(Ag)、锡(Sn)、铍(Be)、锑(Sb)、锶(Sr)、钙(Ca)、锌(Zn)、镁(Mg)、铁(Fe)、金(Au)26种单元素标准溶液,除Dy和Mg质量浓度为100 mg·L-1外,其余质量浓度均为1 000 mg·L-1,均购自国家钢铁材料测试中心。
23批龟甲样品均由湖北省药品监督检验研究院肖凌副主任药师鉴定为龟科动物乌龟Chinemys reevesii(Gray)的背甲及腹甲。15批龟甲胶来源为生产企业收集样品。
2 方法与结果
2.1 试验条件
2.1.1 微波消解条件
设置功率模式消解程序,第一阶段10 min升至1 100 W,保持10 min;第二阶段15 min升至1 400 W,保持20 min。
2.1.2 ICP-MS条件
射频功率1 200 W,雾化气流速1.04 L·min-1,辅助气流速1.3 L·min-1,等离子体气流速15 L·min-1,蠕动泵转速20.0 r·min-1,重复次数为3次,扫描次数为10次。
2.1.3 FAAS法条件
Zn、Mg、Fe、Sr、Ca的波长分别为213.8、279.6、248.3、460.7、422.7 nm;Zn、Mg、Fe、Ca的灯电流为5.0 mA,Sr的为3.0 mA;光谱通带均为0.2 nm。
2.2 溶液制备
2.2.1 标准储备工作溶液
分别精密量取单元素标准溶液适量,用5%硝酸溶液稀释制成每1 mL分别含Pb、As、Pd、W、Cr、Mn、Ni 5 μg,含Al、Ba、Cu、Zn、Mg、Ca 50 μg,含Cd、Mo、Se 2.5 μg,含Hg、Dy、Tl、Ag、Sn、Be、Sb、Sr 0.5 μg,含Fe 1.5 μg的溶液,即得。
2.2.2 标准工作溶液
精密量取上述标准储备工作溶液适量,用5%硝酸溶液稀释制成每1 mL含Pb、As、Pd、W、Cr、Mn、Ni均分别为0、1、5、10、20、50 ng,含Al、Ba、Cu、Zn、Mg、Ca均分别为0、10、50、100、200、500 ng,含Cd、Mo、Se均分别为0、0.5、2.5、5、10、25 ng,含Hg、Dy、Tl、Ag、Sn、Be、Sb、Sr均分别为0、0.1、0.5、1、2、5 ng,含Fe分别为0、40、60、80、100、120 ng的混合溶液,即得。
2.2.3 内标溶液
精密量取Ge、Y、Bi内标单元素标准溶液适量,用水稀释制成1 μg·mL-1的混合溶液,即得。
2.2.4 供试品溶液
称取中药材龟甲粉末(过50目筛)样品0.1 g(龟甲胶0.25 g),精密称定,置于高压消解罐中,加入过氧化氢溶液2 mL和硝酸5 mL,放置12 h,旋紧罐盖,按照微波消解仪的标准操作步骤进行消解。冷却后取出,缓慢打开罐盖排气,将高压消解罐放入控温电热板上,于135 ℃赶酸。消解罐取出放冷,将消化液转移至50 mL量瓶中,用10 mL水分次洗涤消解罐,洗液合并于量瓶中,加入Au单元素标准工作溶液(用5%硝酸稀释制成1 mg·L-1的溶液)200 μL,加水稀释至刻度,摇匀,即得供试品溶液;除不加样品及Au单元素标准溶液外,其余同法制备试剂空白溶液。用ICP-MS法测定Pb、Cd、As、Hg、Cu、Al、Cr、Mn、Pd、Ba、W、Ni、Mo、Se、Dy、Tl、Ag、Sn、Be、Sb共20种元素含量;用FAAS法测定Sr、Ca、Zn、Fe、Mg元素含量。
2.3 线性关系考察及检测下限测定
将上述25种元素标准工作溶液依法测定,绘制标准曲线,求得回归方程及相关系数(r),取11次试剂空白溶液测定值计算标准偏差s,本方法检测下限L = 3s/f(其中f为标准曲线斜率),结果见表 1。
表 1
Tab.1
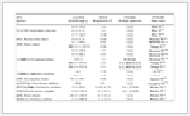
表 1 ICP-MS法和FAAS法测定中药材龟甲及龟甲胶中25种元素方法学验证(n = 6)
Tab.1 The method validation of determination of 25 elements in Testudinis Carapax et Plastrum and Testudinis Carapax et Plastri Colla by ICP-MS and FAAS
方法
(method) |
元素
(element) |
回归方程
(regression equation) |
r |
线性范围
(linear range)/(ng·mL-1) |
平均回收率
(mean recovery)/% |
RSD/% |
检测下限
(detection limit)/(μg·L-1) |
| ICP-MS |
Pb |
Y=8.080×103X-75.50 |
1.000 |
0~50 |
93.9 |
2.6 |
0.06 |
|
Cd |
Y=1.875×103X-3.944×102 |
0.999 9 |
0~25 |
99.7 |
2.5 |
0.01 |
|
As |
Y=1.498×103X-3.901×102 |
0.999 8 |
0~50 |
104.7 |
8.7 |
0.04 |
|
Hg |
Y=1.096×104X+3.488×102 |
0.999 4 |
0~5 |
76.8 |
7.3 |
0.04 |
|
Cu |
Y=5.335×103X+1.793×103 |
0.999 9 |
0~500 |
96.3 |
8.0 |
0.14 |
|
Cr |
Y=6.672×103X+8.915×102 |
1.000 |
0~50 |
96.1 |
8.1 |
0.30 |
|
Mn |
Y=9.689×103X-4.502×102 |
1.000 |
0~50 |
109.6 |
1.9 |
0.03 |
|
Pd |
Y=3.457×103X+2.12 |
1.000 |
0~50 |
116.2 |
9.5 |
0.03 |
|
Ba |
Y=1.503×104X+1.426×103 |
0.999 9 |
0~500 |
106.5 |
7.4 |
0.08 |
|
W |
Y=2.649×103X+5.301×102 |
1.000 |
0~50 |
121.4 |
2.1 |
0.08 |
|
Be |
Y=2.130×102X-5.95 |
0.999 8 |
0~5 |
86.8 |
6.6 |
0.05 |
|
Al |
Y=4.116×103X+24.831×103 |
0.999 7 |
0~500 |
98.9 |
2.4 |
0.73 |
|
Ni |
Y=2.196×103X-24.37 |
1.000 |
0~50 |
97.2 |
7.6 |
0.07 |
|
Se |
Y=1.739×102X-1.439×102 |
0.999 9 |
0~25 |
107.9 |
3.8 |
4.19 |
|
Mo |
Y=4.602×103X-41.33 |
1.000 |
0~25 |
106.2 |
2.4 |
0.02 |
|
Ag |
Y=9.004×103X+3.060×102 |
1.000 |
0~5 |
82.8 |
1.9 |
0.02 |
|
Sn |
Y=2.757×103X-2.341×102 |
1.000 |
0~5 |
99.6 |
1.5 |
0.09 |
|
Sb |
Y=2.406×103X+1.541×102 |
0.999 2 |
0~5 |
74.6 |
6.6 |
0.16 |
|
Dy |
Y=6.023×103X+2.063×103 |
0.999 5 |
0~5 |
107.7 |
2.5 |
0.002 |
|
Tl |
Y=1.176×104X+8.188×102 |
0.999 9 |
0~5 |
94.4 |
2.1 |
0.01 |
| FAAS |
Zn |
Y=10.44X+1.400×10-3 |
0.999 9 |
0~500 |
99.8 |
0.81 |
0.43 |
|
Mg |
Y=2.855×10-1X+1.710×10-2 |
0.998 9 |
0~500 |
99.1 |
1.3 |
0.29 |
|
Fe |
Y=1.010×10-1X+2.46×10-2 |
0.999 4 |
40~120 |
102.2 |
1.7 |
42.27 |
|
Sr |
Y=1.572×106X-1.048×105 |
0.999 5 |
0~5 |
105.6 |
2.2 |
0.05 |
|
Ca |
Y=1.856×104X+3.976×103 |
0.999 0 |
1~500 |
106.6 |
2.1 |
1.63 |
|
表 1 ICP-MS法和FAAS法测定中药材龟甲及龟甲胶中25种元素方法学验证(n = 6)
Tab.1 The method validation of determination of 25 elements in Testudinis Carapax et Plastrum and Testudinis Carapax et Plastri Colla by ICP-MS and FAAS |
2.4 加样回收率试验
称取已测知含量的1号龟甲样品4份,每份0.1 g,分别加入Pb、As、Pd、W、Cr、Mn、Ni 250 ng,Cd、Mo、Se 125 ng,Sb、Sn、Dy、Tl、Be、Ag、Hg 25 ng,Al、Ba、Cu 2 500 ng,Sr 50 μg,Ca 0.01 g,Mg 0.4 mg,Zn 0.01 mg,Fe 20 μg,依法制成50 mL的供试品溶液,进样测定。元素回收率测定结果均在74.6%~116.2%,RSD在0.81%~9.50%,表明该方法回收率良好。
2.5 样品含量测定
取23批龟甲及15批龟甲胶,按“2.2.4”项下方法制备供试溶液,按“2.1”项下条件对样品中的25种元素含量进行测定,结果见表 2、3。
表 2
Tab.2

表 2 龟甲中金属及有害元素含量测定结果
Tab.2 Contents of metals and harmful elements in Testudinis Carapax et Plastrum
| 样品号(sample No.) |
采集地
(collection location) |
Pb |
Ni |
Cu |
As |
Cd |
Be |
Al |
Cr |
Mn |
Se |
Sn |
Ba |
Mo |
Ag |
Hg |
Tl |
Dy |
Sb |
W |
Pd |
Ca |
Mg |
Sr |
Zn |
Fe |
| 1 |
湖北省荆州市(Jingzhou City,Hubei Province) |
0.4 |
4.9 |
0.5 |
0.2 |
/ |
/ |
11 |
2 |
9.1 |
/ |
/ |
42.7 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
184 |
3.70 |
0.45 |
0.14 |
0.08 |
| 2 |
湖北省荆门市京山县钱场镇荆条村(Jingtiao Village,Qianchang Town,Jingshan County,Jingmen City,Hubei Province) |
0.4 |
5.6 |
0.3 |
0.2 |
/ |
/ |
48 |
1.9 |
8.1 |
/ |
0.1 |
40.5 |
0.1 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
196 |
4.21 |
0.35 |
0.14 |
0.07 |
| 3 |
湖北省荆门市京山县钱场镇荆条村(Jingtiao Village,Qianchang Town,Jingshan County,Jingmen City,Hubei Province) |
0.3 |
5.6 |
0.2 |
0.1 |
/ |
/ |
7 |
2.3 |
4.7 |
/ |
/ |
46.3 |
0.1 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
194 |
3.43 |
0.39 |
0.14 |
0.12 |
| 4 |
湖北省荆州市(Jingzhou City,Hubei Province) |
0.1 |
5.6 |
0.4 |
0.1 |
/ |
/ |
5 |
2.5 |
4 |
/ |
0.1 |
36.5 |
0.1 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
208 |
3.69 |
0.7 |
0.12 |
0.08 |
| 5 |
湖北省荆门市沙洋县(Shayang County,Jingmen City,Hubei Province) |
0.7 |
5.8 |
0.4 |
0.1 |
/ |
/ |
34 |
4.5 |
4.4 |
/ |
0.2 |
17.5 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
210 |
3.61 |
0.36 |
0.12 |
0.15 |
| 6 |
广东省佛山市顺德区(Shunde District,Foshan City,Guangdong Province) |
0.2 |
9.6 |
1 |
0.1 |
/ |
/ |
8 |
2.1 |
3.4 |
/ |
0.3 |
49.2 |
0.1 |
/ |
/ |
/ |
/ |
0.1 |
/ |
/ |
201 |
4.19 |
0.29 |
0.11 |
0.15 |
| 7 |
广东省惠州市博罗县横河镇芦屋村(Luwu Village,Henghe Town,Boluo County,Huizhou City,Guangdong Province) |
1.1 |
9.3 |
0.7 |
0.1 |
/ |
/ |
5 |
2 |
4.8 |
/ |
0.1 |
46.6 |
0.1 |
/ |
/ |
/ |
/ |
0.1 |
/ |
/ |
187 |
4.19 |
0.32 |
0.12 |
0.16 |
| 8 |
广东省珠海市白蕉镇六乡螺州工业园区(Luozhou Industrial Park,Liuxiang Town,Baijiao Town,Zhuhai City,Guangdong Province) |
0.1 |
5.4 |
0.5 |
0.1 |
/ |
/ |
39 |
3.6 |
4.7 |
/ |
0.2 |
29.7 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
178 |
3.79 |
0.35 |
0.12 |
0.45 |
| 9 |
广东省佛山市顺德区(Shunde District,Foshan City,Guangdong Province) |
1.3 |
9.6 |
1.1 |
1.5 |
/ |
/ |
43 |
4.4 |
14.2 |
/ |
0.2 |
62.4 |
0.1 |
/ |
/ |
/ |
/ |
/ |
0.1 |
/ |
207 |
3.20 |
0.45 |
0.12 |
0.09 |
| 10 |
广东省东莞市(Dongguan City,Guangdong Province) |
0.2 |
6.3 |
1.1 |
0.3 |
/ |
/ |
27 |
5.7 |
5.2 |
/ |
/ |
25.7 |
0.2 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
187 |
3.98 |
0.44 |
0.10 |
0.08 |
| 11 |
浙江省嘉兴市桐乡市(Tongxiang City,Jiaxing City,Zhejiang Province) |
/ |
4.2 |
0.3 |
0.1 |
/ |
/ |
21 |
1.5 |
3.6 |
/ |
/ |
19.1 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
198 |
3.42 |
0.66 |
0.15 |
0.19 |
| 12 |
浙江省湖州市(Huzhou City,Zhejiang Province) |
0.4 |
5.1 |
0.5 |
0.2 |
/ |
/ |
32 |
1.7 |
4.7 |
/ |
2.9 |
30 |
0.1 |
/ |
/ |
/ |
/ |
/ |
0.1 |
/ |
150 |
3.58 |
0.31 |
0.14 |
0.38 |
| 13 |
浙江省杭州余杭区临平镇(Linping Town,Yuhang District,Hangzhou,Zhejiang) |
0.4 |
6.5 |
0.5 |
0.2 |
/ |
/ |
205 |
4.9 |
11.1 |
/ |
0.2 |
56.5 |
0.1 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
206 |
4.10 |
0.23 |
0.16 |
0.13 |
| 14 |
浙江省杭州市桐庐县瑶琳镇(Yaolin Town,Tonglu County,Hangzhou,Zhejiang) |
0.3 |
6.1 |
0.3 |
0.1 |
/ |
/ |
42 |
4.2 |
6.5 |
/ |
/ |
33.5 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
190 |
3.13 |
0.38 |
0.14 |
0.08 |
| 15 |
安徽省芜湖市无为县(Wuwei County,Wuhu City,Anhui Province) |
0.1 |
4.7 |
0.3 |
/ |
/ |
/ |
35 |
2.2 |
2.6 |
/ |
/ |
31.4 |
0.1 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
231 |
3.60 |
0.33 |
0.14 |
0.11 |
| 16 |
安徽省芜湖市南陵县许镇马仁村(Maren Village,Xu Town,Nanling County,Wuhu City,Anhui Province) |
/ |
3.2 |
0.2 |
/ |
/ |
/ |
61 |
0.9 |
2.1 |
/ |
/ |
29.3 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
229 |
4.33 |
0.46 |
0.14 |
0.14 |
| 17 |
湖南省常德市汉寿县(Hanshou County,Changde City,Hunan Province) |
0.2 |
6.4 |
0.3 |
0.1 |
/ |
/ |
24 |
2.9 |
3.7 |
/ |
0.1 |
24.7 |
0.2 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
192 |
3.80 |
0.51 |
0.11 |
0.15 |
| 18 |
湖南省常德市汉寿县(Hanshou County,Changde City,Hunan Province) |
0.2 |
5.2 |
0.3 |
0.6 |
/ |
/ |
46 |
2.2 |
9.9 |
/ |
/ |
41.2 |
0.1 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
215 |
3.51 |
0.57 |
0.15 |
0.11 |
| 19 |
江苏省苏州市吴江区八都镇(Badu Town,Wujiang District,Suzhou City,Jiangsu Province) |
0.1 |
4.9 |
0.2 |
0.1 |
/ |
/ |
17 |
1.4 |
4.4 |
/ |
/ |
31 |
0.1 |
/ |
/ |
/ |
/ |
/ |
0.1 |
/ |
191 |
4.20 |
0.75 |
0.12 |
0.43 |
| 20 |
江苏省常州市武进区前黄镇灵台村(Lingtai Village,Qianhuang Town,Wujin District,Changzhou City,Jiangsu Province) |
0.2 |
5.8 |
0.4 |
0.2 |
/ |
/ |
21 |
3.3 |
4 |
/ |
/ |
30.1 |
0.1 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
158 |
3.21 |
0.63 |
0.11 |
0.28 |
| 21 |
江西省芜州市南丰县太和镇(Taihe Town,Nanfeng County,Cangzhou City,Jiangxi Province) |
0.5 |
7.7 |
0.6 |
0.2 |
/ |
/ |
70 |
6.7 |
23.7 |
/ |
0.2 |
36.7 |
/ |
/ |
/ |
/ |
/ |
/ |
0.1 |
/ |
201 |
3.83 |
0.92 |
0.10 |
0.19 |
| 22 |
四川省南充市南部县寒坡乡彭家垭村(Pengjiatun Village,Hanpo Township,Southern County,Nanchong City,Sichuan Province) |
0.6 |
9.2 |
0.4 |
0.1 |
/ |
/ |
18 |
4.3 |
24.8 |
/ |
0.5 |
147.6 |
0.2 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
195 |
3.72 |
0.58 |
0.13 |
0.10 |
| 23 |
河北省保定市安新县白洋淀(Baiyangdian,Anxin County,Baoding City,Hebei Province) |
0.3 |
6.7 |
0.9 |
0.1 |
/ |
/ |
31 |
3.1 |
3.7 |
/ |
0.3 |
14.7 |
0.1 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
165 |
4.08 |
0.55 |
0.09 |
0.11 |
| 注(note):“/”表示未检出(“/” means not detected);Ca、Sr、Mg、Fe、Zn单位为g·kg-1,其余元素单位均为mg·kg-1(the units of Ca,Sr,Mg,Fe and Zn are g·kg-1,and the remaining element units are mg·kg-1);Cu、As、Cd、Hg、Pb的检出限分别为1×10-4、4×10-5、1×10-5、4×10-5和6×10-5 mg·kg-1(the detection limits of Cu,As,Cd,Hg and Pb were 1×10-4,4×10-5,1×10-5,4×10-5 and 6×10-5 mg·kg-1,respectively) |
|
表 2 龟甲中金属及有害元素含量测定结果
Tab.2 Contents of metals and harmful elements in Testudinis Carapax et Plastrum |
表 3
Tab.3

表 3 龟甲胶中金属及有害元素含量测定结果
Tab.3 Contents of metal and harmful elements in Testudinis Carapax et Plastri Colla
| 样品号(sample No.) |
生产企业(manufacturer) |
批号(lot No.) |
Be |
Al |
Cr |
Mn |
Ni |
Cu |
As |
Se |
Sr |
Mo |
Pd |
Ag |
Cd |
Sn |
Sb |
Ba |
Dy |
W |
Hg |
Tl |
Pb |
Mg |
Zn |
Ca |
Fe |
| 1 |
河南A公司(Henan A Company) |
20160402 |
0.000 |
2.942 |
0.125 |
0.284 |
0.519 |
0.110 |
0.151 |
/ |
32.206 |
0.009 |
0.074 |
/ |
0.008 |
/ |
0.012 |
3.375 |
/ |
0.009 |
0.002 |
/ |
/ |
0.147 |
0.147 |
0.364 |
0.021 |
| 2 |
河南B公司(Henan B Company) |
161002 |
/ |
/ |
/ |
/ |
/ |
/ |
0.010 |
/ |
0.062 |
/ |
/ |
0.002 |
/ |
/ |
/ |
/ |
/ |
/ |
0.002 |
/ |
/ |
0.434 |
0.434 |
0.456 |
0.004 |
| 3 |
河北A公司(Hebei A Company) |
150301 |
/ |
/ |
/ |
/ |
0.006 |
/ |
0.054 |
/ |
/ |
/ |
0.029 |
0.036 |
0.000 |
/ |
0.004 |
/ |
/ |
/ |
0.000 |
0.000 |
0.018 |
0.401 |
0.401 |
0.677 |
0.063 |
| 4 |
河北B公司(Hebei B Company) |
14071002 |
/ |
4.644 |
0.115 |
0.305 |
0.546 |
0.095 |
0.176 |
0.269 |
34.355 |
/ |
0.048 |
/ |
0.010 |
/ |
1.023 |
3.559 |
0.000 |
0.003 |
0.001 |
0.008 |
0.075 |
0.367 |
0.367 |
0.215 |
0.014 |
| 5 |
河北C公司(Hebei C Company) |
161108 |
0.000 |
/ |
/ |
/ |
/ |
/ |
0.008 |
/ |
0.033 |
/ |
/ |
0.009 |
/ |
/ |
/ |
/ |
/ |
0.000 |
/ |
/ |
/ |
0.326 |
0.326 |
0.898 |
0.122 |
| 6 |
山东A公司(Shandong A Company) |
20150511 |
/ |
/ |
/ |
0.007 |
0.020 |
/ |
0.029 |
0.012 |
0.069 |
/ |
0.105 |
0.022 |
0.000 |
/ |
0.003 |
0.025 |
/ |
0.001 |
0.000 |
0.001 |
0.026 |
0.622 |
0.622 |
0.961 |
0.084 |
| 7 |
山东B公司(Shandong B Company) |
2016030801 |
0.000 |
/ |
/ |
/ |
0.008 |
/ |
0.024 |
/ |
/ |
/ |
/ |
0.020 |
/ |
/ |
0.005 |
/ |
/ |
0.001 |
/ |
0.001 |
0.014 |
0.049 |
0.049 |
0.150 |
0.021 |
| 8 |
山东C公司(Shandong C Company) |
16041501 |
/ |
9.386 |
0.326 |
0.406 |
0.169 |
0.587 |
0.123 |
0.234 |
3.314 |
0.017 |
/ |
/ |
0.003 |
0.136 |
0.011 |
/ |
0.001 |
0.015 |
0.005 |
0.002 |
0.231 |
0.552 |
0.552 |
0.261 |
0.025 |
| 9 |
山东D公司(Shandong D Company) |
20150505 |
0.001 |
0.453 |
0.044 |
0.093 |
0.015 |
0.016 |
0.051 |
/ |
0.148 |
0.001 |
0.151 |
0.007 |
0.001 |
/ |
0.005 |
0.046 |
/ |
0.002 |
/ |
0.001 |
0.062 |
0.044 |
0.044 |
0.693 |
0.010 |
| 10 |
湖南A公司(Hunan A Company) |
1509002 |
0.000 |
2.942 |
0.125 |
0.284 |
0.519 |
0.110 |
0.151 |
0.214 |
32.206 |
0.009 |
0.074 |
/ |
0.008 |
/ |
0.012 |
3.375 |
0.001 |
0.009 |
0.001 |
0.008 |
0.092 |
0.760 |
0.760 |
0.607 |
0.034 |
| 11 |
湖南B公司(Hunan B Company) |
20151008 |
/ |
/ |
/ |
0.011 |
0.008 |
0.102 |
0.048 |
/ |
0.012 |
/ |
/ |
0.018 |
/ |
/ |
0.004 |
0.022 |
/ |
0.001 |
/ |
0.001 |
0.027 |
0.115 |
0.115 |
0.477 |
0.014 |
| 12 |
湖北A公司(Hubei A Company) |
1507211 |
/ |
0.049 |
0.007 |
0.002 |
0.010 |
0.017 |
0.010 |
/ |
/ |
0.001 |
/ |
0.010 |
/ |
0.002 |
0.000 |
0.000 |
/ |
0.001 |
/ |
/ |
0.003 |
0.314 |
0.314 |
0.091 |
0.065 |
| 13 |
湖北B公司(Hubei B Company) |
160501 |
0.000 |
/ |
/ |
/ |
0.014 |
0.000 |
0.031 |
/ |
0.072 |
/ |
0.046 |
0.015 |
0.000 |
/ |
0.004 |
/ |
/ |
0.002 |
0.000 |
0.001 |
0.029 |
0.575 |
0.575 |
0.295 |
0.045 |
| 14 |
山西A公司(Shanxi A Company) |
20150306 |
/ |
/ |
/ |
/ |
0.004 |
/ |
0.026 |
/ |
/ |
/ |
/ |
0.026 |
0.000 |
/ |
0.005 |
0.023 |
/ |
0.001 |
0.000 |
0.001 |
0.022 |
0.125 |
0.125 |
0.179 |
0.011 |
| 15 |
甘肃A公司(Gansu A Company) |
160603 |
/ |
0.048 |
/ |
/ |
/ |
/ |
/ |
/ |
/ |
0.001 |
/ |
/ |
0.000 |
/ |
/ |
/ |
0.001 |
0.061 |
0.002 |
/ |
/ |
0.246 |
0.246 |
0.412 |
0.007 |
| 注(note):“/”表示未检出(means no detection);Ca、Mg、Fe、Zn含量单位为g·kg-1,其余元素含量单位均为mg·kg-1(the units of Ca,Sr,Mg,Fe and Zn are g·kg-1,and the remaining element units are mg·kg-1);Cu、As、Cd、Hg、Pb的检测下限分别为4.3×10-5、2.2×10-3、2.2×10-3、2.1×10-5和1.0×10-5 mg·kg-1(the detection limit of Cu,As,Cd,Hg and Pb were 4.3×10-5,2.2×10-3,2.2×10-3,2.1×10-5 and 1.0×10-5 mg·kg-1) |
|
表 3 龟甲胶中金属及有害元素含量测定结果
Tab.3 Contents of metal and harmful elements in Testudinis Carapax et Plastri Colla |
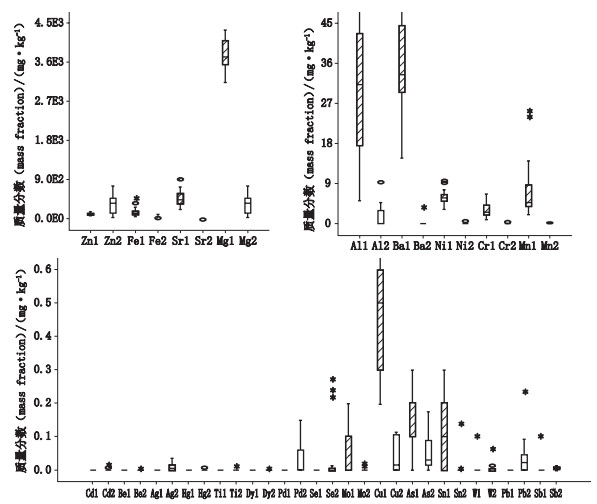
其中Cd、Be、Ag、Hg、Ti、Dy、Pd、Se在龟甲中未检出,龟甲胶中的金属元素及有害元素含量较龟甲大幅降低,其中Ca元素含量降幅达5个数量级,Se、Pb、Ag、Hg元素含量稍有增加,结果见图 1。
3 讨论
3.1 常量金属元素
5种常量元素在龟甲中含量从大到小依次为Ca、Mg、Sr、Fe、Zn,在龟甲胶中含量从大到小依次为Ca、Mg、Zn、Fe、Sr。龟甲和龟甲胶中5种常量元素平均含量分别为194.5 g·kg-1和0.45 g·kg-1;Sr元素在龟甲胶中有明显减少,在龟甲和龟甲胶中的平均含量分别为0.48 g·kg-1和6.83 mg·kg-1;龟甲和龟甲胶中Mg元素平均含量分别为3.8 g·kg-1和0.34 g·kg-1,Zn元素平均含量分别为0.13 g·kg-1和0.34 g·kg-1,Fe元素平均含量分别为0.17 g·kg-1和0.036 g·kg-1。龟甲的主要成分为碳酸钙及磷酸钙,Ca元素含量占龟甲量近20%;Sr是人体必需的微量元素之一,Sr与骨生成关系较为密切,体内外研究均表明Sr具有促进成骨细胞生长和抑制破骨细胞形成的双重功效[4-6]。Ca和Sr元素在龟甲中含量较高,与文献报道[7]吻合。Mg元素几乎参与人体的所有新陈代谢过程,Fe和Zn元素作为人体必需的微量元素,对人的生长发育有着重要作用。在龟甲和龟甲胶中,上述5种常量元素可能与滋阴潜阳,健骨功效有一定联系,其相关性有待进一步研究。
3.2 部分微量金属元素
Cd是农业环境中最危险的重金属元素之一,被WHO确定为优先研究的食品污染物。江晨洁等[8]对全国6省市甲壳类水产品中Pb和Cd污染情况调查与分析发现,被检样品中Pb和Cd的检出率均为100%。而在所测龟甲及龟甲胶样品中均未测出Cd含量,这有利于龟甲的进一步开发利用。
W元素经胃肠吸收量极微,W盐含量相等于2%时,经胃肠吸收的量足以引起死亡[9]。龟甲中W元素含量均≤0.1 mg·kg-1,龟甲胶中W元素含量均 < 0.061 mg·kg-1。W元素在龟甲及龟甲胶中较为安全。
Al元素与人体健康有着密切关系,摄入过量的Al元素,将影响中枢神经系统,增加老年痴呆症的发生几率,我国每日允许摄入Al的量为60 mg·d-1[10]。龟甲中Al的含量范围为5.0~205.0 mg·kg-1,龟甲胶中Al的含量范围为0~9.39 mg·kg-1,按服用量,龟甲及龟甲胶中Al相对安全。
Ni元素是人体必需元素,Ni具有许多独特的生理功能,缺少Ni也会引起各种疾病,如糖尿病、贫血、肝硬化、尿毒症、肾衰和肝脂质及磷脂质代谢异常等[11]。Ni的含量范围为3.2~6.9 mg·kg-1,龟甲胶中Al为0~0.546 mg·kg-1。人体对Ni的日需要量约为0.3 mg[12],按服用量,龟甲及龟甲胶能适当为机体提供Ni元素,Ni相对安全。
Mn元素摄入量国家科学院确定成年男女分别为2.3 mg·d-1和1.8 mg·d-1,日常饮食是摄入Mn的主要来源[13]。Mn的含量范围,龟甲为2.1~24.8 mg·kg-1,龟甲胶为未检出~0.406 mg·kg-1,按服用量,龟甲及龟甲胶中Mn相对安全。
3.3 龟甲中各元素相关性分析
Cd、Be、Ag、Hg、Ti、Dy、Pd、Se这8种元素在龟甲中未检出,进行其他17种元素相关性分析(SPSS 21.0),结果见表 4。结果表明,Pb与Ni、As之间,Ni与Cu、Ba、Sb之间,Cr与Mn之间,Mn与Ba、Sn之间存在显著正相关(P < 0.01)。有研究[14]表明,Cr能提高周围组织对葡萄糖的利用,Mn2+可作为柠檬酸脱氢酶的辅助因子,参与糖的有氧氧化,两者具有协同作用。Zn与Ni、Cu、Sr之间,Sn与Ca之间存在显著负相关(P < 0.05),说明龟甲中这些元素在被吸收时可能相互抑制;其中,Zn元素的含量会影响Cu的吸收,研究表明金属硫蛋白对Cu具有更高的亲和力,Zn含量增加时,可以通过金属硫蛋白抑制Cu的吸收[14]。生物体内金属元素之间,金属元素与成分之间会形成各种形态或配位化合物,通过协同或拮抗作用改变药物的生理活性[15]。深入研究元素、成分之间的相关性,将有助于揭示中药材治病机理。
表 4
Tab.4

表 4 17种元素相关性分析
Tab.4 The correlation analysis of 17 kinds of metal elements
| 元素(element) |
Pb |
Ni |
Cu |
As |
Al |
Cr |
Mn |
Sn |
Ba |
Mo |
Sb |
W |
Ca |
Sr |
Mg |
Zn |
Ca |
| Pb |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Ni |
0.701** |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Cu |
0.454* |
0.657** |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| As |
0.598** |
0.381 |
0.477* |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
| Al |
0.031 |
-0.055 |
-0.026 |
0.093 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
| Cr |
0.332 |
0.435* |
0.423* |
0.248 |
0.383 |
1 |
|
|
|
|
|
|
|
|
|
|
|
| Mn |
0.439* |
0.499* |
0.13 |
0.323 |
0.258 |
0.595** |
1 |
|
|
|
|
|
|
|
|
|
|
| Sn |
0.115 |
0.013 |
0.091 |
0.008 |
0.001 |
-0.108 |
0.032 |
1 |
|
|
|
|
|
|
|
|
|
| Ba |
0.374 |
0.552** |
0.044 |
0.172 |
0.048 |
0.192 |
0.716** |
0.054 |
1 |
|
|
|
|
|
|
|
|
| Mo |
0.088 |
0.381 |
0.245 |
0.122 |
-0.105 |
0.081 |
0.1 |
0.11 |
0.399 |
1 |
|
|
|
|
|
|
|
| Sb |
0.291 |
0.580** |
0.399 |
-0.112 |
-0.237 |
-0.212 |
-0.164 |
-0.018 |
0.093 |
0.084 |
1 |
|
|
|
|
|
|
| W |
0.323 |
0.158 |
0.175 |
0.447* |
0.041 |
0.155 |
0.343 |
0.465* |
-0.002 |
-0.055 |
-0.142 |
1 |
|
|
|
|
|
| Ca |
-0.039 |
-0.086 |
-0.214 |
0.091 |
0.233 |
-0.027 |
0.093 |
-0.502* |
0.113 |
-0.136 |
-0.008 |
-0.173 |
1 |
|
|
|
|
| Sr |
-0.195 |
-0.077 |
-0.156 |
0.017 |
-0.223 |
0.156 |
0.363 |
-0.218 |
-0.011 |
-0.058 |
-0.319 |
0.358 |
-0.012 |
1 |
|
|
|
| Mg |
-0.131 |
0.042 |
0.129 |
-0.38 |
0.191 |
-0.196 |
-0.11 |
-0.062 |
-0.032 |
0.142 |
0.382 |
-0.079 |
0.132 |
-0.112 |
1 |
|
|
| Zn |
-0.211 |
-.505* |
-0.617** |
-0.061 |
0.384 |
-0.382 |
-0.063 |
0.038 |
0.087 |
-0.313 |
-0.246 |
-0.205 |
0.388* |
-0.326** |
-0.175 |
1 |
|
| Ca |
-0.374 |
-0.335 |
-0.472* |
-0.348 |
0.318 |
-0.253 |
-0.203 |
0.3 |
-0.041 |
0.063 |
-0.074 |
0.058 |
0.177 |
-0.192* |
0.168 |
0.352 |
1 |
| Fe |
-0.222 |
-0.221 |
-0.169 |
-0.168 |
-0.063 |
-0.175 |
-0.188 |
0.399 |
-0.223 |
-0.17 |
-0.033 |
0.452 |
-0.473 |
0.133 |
0.066 |
-0.104 |
0.185 |
|
*P < 0.05,**P < 0.01
|
|
表 4 17种元素相关性分析
Tab.4 The correlation analysis of 17 kinds of metal elements |
3.4 龟甲及龟甲胶风险评估
JECFA发布《食品添加剂和污染物评估报告》中设定,每千克体质量每周可耐受摄入量(PTWI) = 7 d×每日可接受摄入量(ADI),每千克体质量每月可耐受摄入量(PTMI) = 30 d×ADI。2010年Cd的PTMI设定为25 μg·kg-1[16];Pb的PTWI为25 μg·kg-1,As的PTWI为15 μg·kg-1,无机Hg的PTWI为4 μg·kg-1[17];JECFA推荐人群Cu的暂定每日最大耐受摄入量(PMTDI)为0.05~0.5 mg·kg-1,本文采用0.5 mg·kg-1[18]。
以每日由膳食补充剂中摄取的金属及有害元素的量不大于日总暴露量的10%折算最大残留限量L(mg·kg-1),L = W×C×10%/F,其中F为中药材(饮片)的最大日摄入量(kg);C为ADI(mg·kg-1);W为某个体的体质量(60 kg)。
参照欧洲食品安全局(EFSA)于2009年推出的累积风险评估工作范例[19]中的评价方式,依据JECFA的规定,按成人龟甲最大服用量0.024 kg·d-1(《中国药典》2015年版一部规定龟甲的服用量为9~24 g·d-1)换算最大限量(表 5)。进一步通过比较最大残留限量与样品实际测定值来评估23批龟甲样品。样品10、19的As超限,超限率为8.7%;样品8、10的Pb超限,超限率为8.7%。龟甲中As、Pb存在一定风险。同理,对龟甲胶进行评估,公式仍为L = W×C×10%/F,但F为龟甲胶最大服用量0.009 kg·d-1,比较最大残留限量值与样品实际测定值来评估值评估15批龟甲胶样品。结果见表 5。
表 5
Tab.5

表 5 龟甲及龟甲胶中金属及有害元素最大残留限量值
Tab.5 Maximum residue limit of metal and harmful elements in Testudinis Carapax et Plastrum and Testudinis Carapax et Plastri Colla
| 元素(element) |
ADI |
最大残留量(maximum residue limit)/(mg·kg-1) |
| 龟甲(Testudinis Carapax et Plastrum) |
龟甲胶(Testudinis Carapax et Plastri Colla) |
| Pb |
0.003 6 |
0.90 |
2.4 |
| Cd |
0.000 83 |
0.21 |
0.6 |
| As |
0.002 1 |
0.53 |
1.4 |
| Hg |
0.000 57 |
0.14 |
0.38 |
| Cu |
0.5 |
125 |
333 |
|
表 5 龟甲及龟甲胶中金属及有害元素最大残留限量值
Tab.5 Maximum residue limit of metal and harmful elements in Testudinis Carapax et Plastrum and Testudinis Carapax et Plastri Colla |
结果显示,龟甲胶中Pb、As、Hg、Cd、Cu的实际测定值均远小于最大残留限量,可认为龟甲胶中金属及有害元素的风险较小。
参考文献
| [1] |
王素燕, 朱凡, 梁小翠. 长沙市4种蔬菜中As和Hg的污染分析与评价[J]. 食品与机械, 2013, 29(4): 166. WANG SY, ZHU F, LIANG XC. Analysis and evaluation of arsenic and mercury contamination in four kinds of vegetables from Changsha[J]. Food Machin, 2013, 29(4): 166. DOI:10.3969/j.issn.1003-5788.2013.04.042 |
| [2] |
顾观光, 杨鹏举. 神农本草经[M]. 北京: 学苑出版社, 1998: 106.
GU GG, YANG PJ. Shennong Materia Medica[M]. Beijing: Xueyuan Press, 1998: 106.
|
| [3] |
蒋受军, 王瑾, 朱斌, 等. ICP-MS法测定注射用丹参(冻干)中15种微量元素[J]. 药物分析杂志, 2008, 28(8): 1297. JIANG SJ, WANG J, ZHU B, et al. ICP-MS determination of fifteen microelements in freeze-dried Danshen injection[J]. Chin J Pharm Anal, 2008, 28(8): 1297. |
| [4] |
苗健, 高琦, 许思来, 等. 微量元素与相关疾[M]. 郑州: 河南医科大学出社, 1997: 150.
MIAO J, GAO Q, XU SL, et al. Trace Elements and Related Diseases[M]. Zhengzhou: Henan Medical University, 1997: 150.
|
| [5] |
黄祎雯, 傅远飞, 张保卫. 锶对骨代谢影响的研究进展[J]. 中国口腔种植学杂志, 2010, 15(3): 153. HUANG YW, FU YF, ZHANG BW. Research progress in the effect of strontium on bone metabolism[J]. Chin J Oral Implantol, 2010, 15(3): 153. DOI:10.3969/j.issn.1007-3957.2010.03.026 |
| [6] | |
| [7] |
南京中医药大学. 中药大辞典(上)[M]. 第2版. 上海: 上海科学技术出版社, 2006: 1607.
Nanjing University of Chinese Medicine. Traditional Chinese Medicine Dictionary(Ⅰ)[M]. 2nd Ed. Shanghai: Shanghai Scientific and Technical Publishers, 2006: 1607.
|
| [8] |
江晨洁, 吴光红, 张美琴, 等. 全国6省市甲壳类水产品中Pb和Cd污染情况调查与分析[J]. 食品安全质量检测学报, 2015, 21(8): 3237.
JIANG CJ, WU GH, ZHANG MQ, et al. Investigation and analysis of Pb and Cd pollution in 6 Provinces and municipalities in the crustacea[J]. J Food Safety Qual, 2015, 21(8): 3237. |
| [9] |
贾如宝. 钨(W)对人体健康的双向影响[J]. 金属世界, 1995(4): 27. JIA RB. The two-way effect of tungsten(W) on human health[J]. Metal World, 1995(4): 27. |
| [10] |
张磊. 中国与一些发达国家膳食有害元素摄入状况比较[J]. 卫生研究, 2003, 32(3): 268. ZHANG L. Comparison on intake status of harmful elements between China and some developed countries[J]. J Hyg Res, 2003, 32(3): 268. DOI:10.3969/j.issn.1000-8020.2003.03.029 |
| [11] |
李青仁, 苏斌, 李胜钏. 微量元素钴、镍与人体健康[J]. 广东微量元素科学, 2008, 15(1): 66. LI QR, SU B, LI SC. Trace elements cobalt, nickel and human health[J]. Guangdong Trace Elem Sci, 2008, 15(1): 66. DOI:10.3969/j.issn.1006-446X.2008.01.013 |
| [12] |
李志, 杨明杰, 黄俊明, 等. 氯化镍染毒对小鼠外周血网织红细胞微核形成的影响[J]. 环境与健康杂志, 2006, 23(2): 134. LI Z, YANG MJ, HUANG JM, et al. Analysis of micronuclei induced by nickel chloride in peripheral blood reticulocytes in mice using flow cytometry[J]. J Environ Health, 2006, 23(2): 134. DOI:10.3969/j.issn.1001-5914.2006.02.012 |
| [13] | |
| [14] | |
| [15] |
秦双双, 黄静雯, 袁媛, 等. 中药材重金属元素及其与指标性成分相关性分析[J]. 中国实验方剂学杂志, 2018, 24(6): 66. QIN SS, HUANG JW, YUAN Y, et al. Correlation analysis of heavy metals and index components in traditional Chinese medicinal materials[J]. Chin J Exp Tradit Med Form, 2018, 24(6): 66. |
| [16] | |
| [17] | |
| [18] | |
| [19] |
左甜甜, 张磊, 金红宇, 等. 中药材提取前后重金属及有害元素转移率和分级别风险评估的研究[J]. 药物分析杂志, 2017, 37(8): 1398. ZUO TT, ZHANG L, JIN HY, et al. Research of transfer rates of heavy metals and harmful elements in tradition Chinese medicines before and after extraction and tiered risk assessment[J]. Chin J Pharm Anal, 2017, 37(8): 1398. |
 2019, Vol. 39
2019, Vol. 39 
