2. 河南省精准临床药学重点实验室, 郑州 450052;
3. 郑州大学第一附属医院超声科, 郑州 450052;
4. 郑州大学生理学与神经生物学系, 郑州 450001;
5. 郑州大学化学与分子工程学院, 郑州 450000
2. Henan Key Laboratory of Precision Clinical Pharmacy, Zhengzhou 450052, China;
3. Ultrasonic Department, The First Affiliated Hospital of Zhengzhou University, Zhengzhou 450052, China;
4. Department of Physiology and Neurobiology, Zhengzhou University, Zhengzhou 450001, China;
5. Chemistry and Molecular Engineering College of Zhengzhou University, Zhengzhou 450000, China
复方血栓通胶囊是在传统中医药理论的指导下,由三七、丹参、黄芪、玄参4味中药材组成的中药复方制剂[1],具有活血化瘀、益气养阴之功效,临床上主要用于治疗血瘀兼气阴两虚证的视网膜静脉阻塞或稳定性劳累型心绞痛,症如视力下降、眼底淤血、口干咽干、心悸、心慌、胸闷痛等[2-3]。
中药的药效作用是药物中所有活性化学成分群的综合体现,具有多成分、多靶点和整体调节的物质属性。方剂中各味药材之间依照“君、臣、佐、使”的组方原则进行配伍,不同成分之间相互协同,从而发挥增效减毒的药理作用[4]。然而中药化学成分复杂多样,有效成分谱较为模糊,药效物质基础尚不明确,难以保证其临床使用的安全有效,同时也严重限制了对其作用机制和质量控制的进一步深入研究,并已成为制约中药现代化进程的重要因素[5]。因此,明确中药化学成分,阐明药效物质对于中药更加安全、合理、科学地进行临床应用具有至关重要的作用。
复方血栓通疗效确切,临床应用广泛,查阅相关资料发现,目前尚未有对其化学成分进行系统研究的相关报道。中药化学成分复杂,依靠传统的液相色谱及低分辨质谱已经不能实现对药物中复杂成分进行准确定性的目的,本实验采用先进的UHPLC-Q-Orbitrap HRMS技术,对复方血栓通胶囊中主要化学成分进行快速识别,该技术同时具有高分辨率和高质量精度的强大优势,其首先利用四极杆对待测离子进行预分离,然后通过敏感性极高的Orbitrap检测器对待测离子的精确质量数进行检测。该检测器具有极高的分辨率(最高为140 000 FWHM),使得离子的质量数检测结果高度精准,可精确至小数点后5位,完全能够满足对中药活性成分进行快速、准确定性的需要。该研究在明确复方血栓通胶囊中主要化学成分谱的同时,可为其进一步的药效物质基础、质量控制及临床合理应用等研究奠定科学的前期基础。
1 仪器与试剂 1.1 仪器UHPLC-Q-Orbitrap液相色谱-质谱联用系统:Ultimate 3000超高效液相色谱仪(Dionex公司)串联Q Exactive型高分辨质谱(Thermo Fisher Scientific公司);ACQUITY UPLC® HSS T3色谱柱(100 mm×2.1 mm,1.8 μm,Waters公司);Master-E型超纯水机(上海和泰仪器有限公司);New Classic MS型十万分之一分析天平(瑞士Mettler Toledo上海有限公司);MDS-6G型多通量微波消解/萃取系统(上海新仪微波化学科技有限公司)。
1.2 试剂复方血栓通胶囊(批号160417,广东众生药业股份有限公司)。对照品信息见表 1,其中,除大黄素和二氢丹参酮Ⅰ购于四川维克奇生物科技有限公司外,其余对照品均购于成都曼思特生物科技有限公司,所有对照品经峰面积归一化法测得纯度均大于99%。甲酸、甲醇及乙腈为色谱纯,美国Fisher公司;水为超纯水;其他试剂均为分析纯。
|
|
表 1 对照品信息 Tab.1 The information of the reference substances |
色谱柱为Waters ACQUITY UPLC® BEH C18(2.1 mm×50 mm,1.7 µm);以乙腈(A)-0.1%甲酸水溶液(B)为流动相,梯度洗脱(0.0~1.0 min,5%A;1.0~2.0 min,5%A→35%A;2.0~8.0 min,35% A→45%A;8.0~12.0 min,45%A→85%A;12.0~15.0 min,85%A→100%A;15.0~18.0 min,100%A);流速0.2 mL·min-1;进样量5 µL;柱温40 ℃。
2.1.2 质谱条件UHPLC-Q Exactive液质联用仪:离子源采用HESI源(heated ESI),辅助气流速10 μL·min-1,辅助气温度300 ℃,离子传输管温度320 ℃;正离子模式下鞘气流速40 μL·min-1,喷雾电压3.50 kV;负离子模式下鞘气流速38 μL·min-1,喷雾电压2.80 kV。扫描方式:正、负离子Full MS/dd-MS2模式,其中包括1次一级全扫描(分辨率为70 000 FWHM)和1次数据依赖的二级扫描(分辨率为17 500 FWHM)2个事件,质荷比窗口宽度设置为2,碰撞能梯度为20、50、100 eV,扫描范围:m/z 80~1 200。
2.2 供试品溶液和混合对照品溶液制备取本品3粒,去壳后,取内容物约1.0 g,精密称定,置量瓶中,精密加入纯甲醇50 mL,微波萃取(功率600 W)15 min,摇匀,滤过,后经0.22 μm微孔滤膜滤过,即得供试品溶液。
取各对照品约1.0 mg,精密称定,分别置10 mL量瓶中,加入纯甲醇溶解并稀释至刻度,摇匀,最终制备成质量浓度为0.1 mg·mL-1的单一对照品储备液;分别精密量取上述单一对照品储备液适量,将其混合后加入纯甲醇稀释,最终制备成各对照品质量浓度均为1 μg·mL-1的混合对照品溶液。
2.3 化合物结构分析依照“2.1”项下优化后的色谱-质谱条件进样,根据高分辨质谱提供的准分子离子和加荷离子等信息推测并得到各成分的精确相对分子质量,经Xcalibar 2.0软件拟合分子式,并与数据库进行比对,以对各色谱峰进行初步推测,再依据对照品或参考文献、Mass Bank、Chemical Book等数据库提供的保留时间及高能碰撞下产生的多级碎片离子信息,进一步准确识别化学成分。
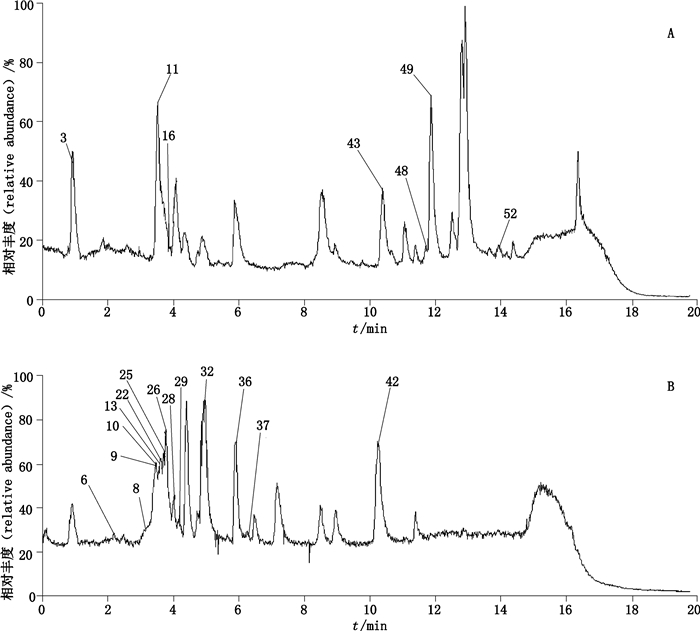
3 结果图 1、2分别为复方血栓通胶囊及混合对照品在UHPLC-Q-Orbitrap HRMS条件下采集得到的总离子流图。根据“2.3”项下的化合物结构分析方法,共鉴定得到52个化学成分,其中21个经对照品比对确证;并同时通过Traditional Chinese Medicine Systems Pharmacology Database and Analysis Platform数据库对所有成分进行药材归属,结果见表 2。

|
1~52.同表 2(same as Tab. 2) A.正离子模式(positive ion mode) B.负离子模式(negative ion mode) 图 1 复方血栓通胶囊总离子流图 Fig.1 TIC of Compound Xueshuantong |
|
|
表 2 复方血栓通胶囊化学成分鉴定表 Tab.2 The chemical composition identified in Compound Xueshuantong Capsule |
|
峰号同表 2(the peek numbers were same as Tab. 2) A.正离子模式(positive ion mode) B.负离子模式(negative ion mode) 图 2 混合对照品总离子流图 Fig.2 TIC of mixed reference substances |
酚酸类成分是植物体内的重要次生代谢产物,广泛分布于自然界的多种药用植物中。该类化合物在质谱条件下主要以[M-H]-的准分子离子峰形式存在,高能碰撞下易产生[M-H-CO2]-或[M-H-H2O]-的碎片离子。此外,当化合物结构中含丹参素时,易出现丹参素的丢失[M-H-gallicacid]-而产生丹参素残基碎片离子;结构中含咖啡酸时,易产生咖啡酰基的丢失[M-H-caffeoyl]-而产生咖啡酸碎片离子[32]。本研究从复方血栓通胶囊中共鉴定出酚酸类化合物共13个,分别为丹酚酸B、丹参素、咖啡酸、原儿茶醛、鞣花酸、原儿茶酸、丹酚酸D、迷迭香酸、丹酚酸H、丹酚酸A、丹酚酸C、紫草酸和阿魏酸。
|
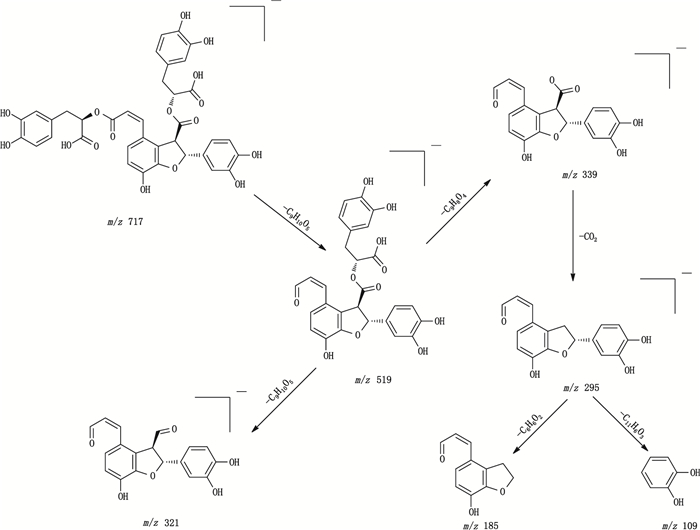
图 3 丹酚酸B的质谱裂解途径 Fig.3 The MS fragmentation pathways of salvianolic acid B |
|
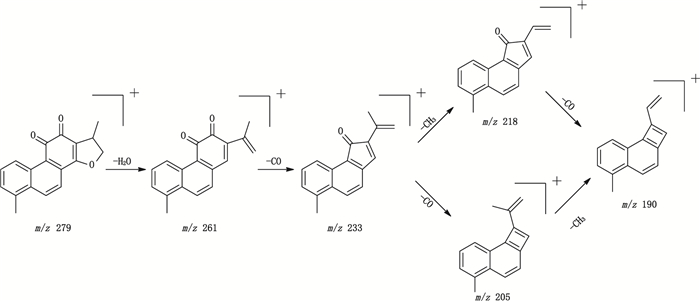
图 4 二氢丹参酮Ⅰ的质谱裂解途径 Fig.4 The MS fragmentation pathways of dihydrotanshinone Ⅰ |
|
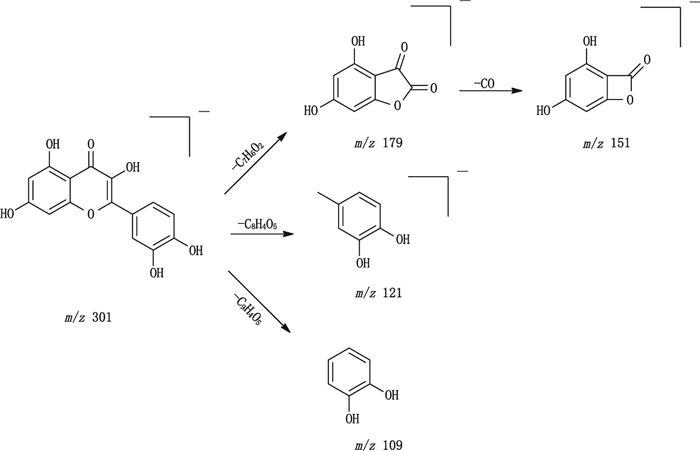
图 5 槲皮素的质谱裂解途径 Fig.5 The MS fragmentation pathways of quercetin |
以丹酚酸B为例,质谱条件下该化合物的负离子模式响应较好,其在样品色谱图中的保留时间为4.27 min,在混合对照品色谱图中的保留时间为4.33 min,经Xcalibar软件拟合分子离子峰[M-H]-的分子式为C36H30O16,高能碰撞下得到的多级碎片离子信息主要有m/z 519.092 96[M-H-tanshinol]-、339.051 03[M-H-tanshinol-C9H8O4]-、321.040 68[M-H-tanshinol-tanshinol]-、295.061 28[M-H-tanshinol-C9H8O4-CO2]-、293.045 81[M-H-tanshinol-tanshinol-CO]-、185.023 71[M-H-tanshinol-tanshinol-C7H4O3]-、109.023 71[M-H-tanshinol-tanshinol-C12H4O4]-。推测该化合物符合酚酸类裂解规律,并与相关对照品进行比对后,最终确定27号峰为丹酚酸B,其质谱裂解途径见图 3。
3.2 醌类醌类化合物是一类具有醌式结构的活性化学成分,主要分为苯醌、萘醌、菲醌和蒽醌4种类型,在中药中以蒽醌及其衍生物形式存在,尤为重要。大多数该类化合物在正离子模式下的响应明显好于负离子,蒽醌类化合物(芦荟大黄素除外)的特征裂解规律主要为逐级失去CO中性碎片,并伴随CO2的中性丢失;萘醌类化合物在准分子离子阶段连续失去H2O和CO是其典型的断裂方式;菲醌类主要通过丢失CH3、H2O及CO等中性小分子而发生裂解。本研究从复方血栓通胶囊中共鉴定出11个醌类化合物,分别为:丹参酮ⅡB、羟基丹参酮ⅡA、丹参新醌A、大黄素、二氢丹参酮Ⅰ、丹参新醌B、丹参酮Ⅴ、丹参酮Ⅰ、隐丹参酮、表丹参隐螺内酯和丹参新酮。
以二氢丹参酮Ⅰ为例,质谱条件下该化合物的正离子模式响应较好,其在样品色谱图中的保留时间为10.39 min,在混合对照品色谱图中的保留时间为10.39 min,经Xcalibar软件拟合分子离子峰[M+H]+的分子式为C18H14O3,高能碰撞下的二级碎片离子主要有m/z 261.09[M+H-H2O]+、233.10[M+H-H2O-CO]+、218.01[M+H-H2O-CO-CH3]+、205.10[M+H-H2O-CO-CO]+、190.08[M+H-H2O-CO-CO-CH3]+,发现其符合醌类化合物的裂解规律,并与相关对照品进行比对后,最终确定44号峰为二氢丹参酮Ⅰ,其质谱裂解途径见图 4。
3.3 黄酮类黄酮类化合物是指广泛存在于自然界中的,具有2-苯基色原酮结构的一类活性成分,现泛指由2个苯环(A环和B环)通过三碳链相互连接而成的一系列化合物。黄酮类化合物在质谱条件下的断裂方式主要有CO、CO2、C2H2O、H2O等中性粒子的丢失和RDA裂解以及糖基的断裂[33]。本品共鉴定出9个黄酮类化合物,分别为槲皮素、毛蕊异黄酮苷、异鼠李素、芒柄花苷、木犀草素、毛蕊异黄酮、山柰酚、芒柄花黄素和金丝桃苷。
以槲皮素为例,质谱条件下该化合物的负离子模式响应较好,其在样品色谱图中的保留时间为4.41 min,在混合对照品色谱图中的保留时间为4.42 min,经Xcalibar软件拟合分子离子峰[M-H]-的分子式为C15H10O7,高能碰撞下的二级碎片离子主要有m/z 179.00、121.03和109.03分别为母离子丢失一分子C7H6O2、C8H4O5和C9H4O5形成的,其中m/z 151.00为m/z 179.00继续丢失一分子CO形成的碎片离子。推测该化合物为黄酮类化合物,并与相关对照品进行比对后,最终确定30号峰为槲皮素,其质谱裂解途径见图 5。
3.4 氨基酸类氨基酸是植物生长所必须的营养物质,该类化合物在正离子模式下的离子峰强度显著高于负离子。质谱条件下,大多数氨基酸(除精氨酸外)极易失去NH3、COOH或OH等基团而产生碎片离子[6]。本品共鉴定出3个氨基酸类化合物,分别为苏氨酸、脯氨酸和亮氨酸。
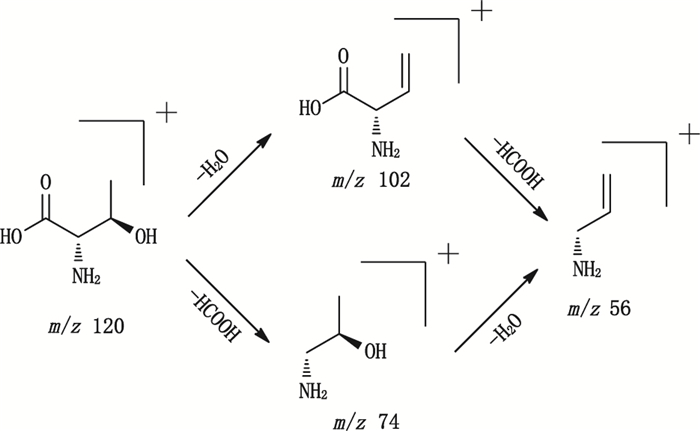
以苏氨酸为例,其在样品色谱图中的保留时间为0.90 min,根据其一级质谱提供的精准m/z 120.065 48信息,经Xcalibar软件拟合其分子离子峰[M+H]+的分子式为C4H9NO3,并根据其二级质谱碎片离子m/z 102.06 [M+H-H2O]+,74.06[M+H-HCOOH]+和56.05[M+H-HCOOH-H2O]+,推测该化合物可能为苏氨酸,最后与文献[6]进行对比后,确定1号峰为苏氨酸,苏氨酸的质谱裂解途径见图 6。
|
图 6 苏氨酸的质谱裂解途径 Fig.6 The MS fragmentation pathways of threonine |
此外,本研究还从复方血栓通胶囊中鉴定出其他类化合物,主要包括甜菜碱、哈帕苷、类叶升麻苷、三七皂苷R1、人参皂苷Rg1、人参皂苷Rf、人参皂苷Rb1、人参皂苷F3、三七皂苷R2、人参皂苷F5、人参皂苷Re、20(S)-人参皂苷Rg2、齐墩果酸、花侧柏烯、阿魏酸乙酯和腺苷。
4 讨论 4.1 提取方法的优化本实验前期分别对提取溶剂(体积分数为50%乙醇水、50%甲醇水、70%甲醇水及纯甲醇)、溶剂体积(20、30、50 mL)及提取方法(微波萃取、超声处理及索氏提取)进行了单变量考察,以选择最佳的提取方法。结果表明,采用50 mL纯甲醇结合微波萃取处理时,各分析物响应最好,提取率最高,提取效果最优。
4.2 色谱、质谱条件的优化优化色谱条件时,本研究重点比较了甲醇-水、乙腈-水和乙腈-0.1%甲酸水分别作为流动相时的色谱行为,结果表明乙腈-水的色谱分离效果明显优于甲醇-水,主要表现为色谱出峰较多且分离较好;当在水相中加入0.1%的甲酸溶液时,可见各色谱峰的峰形更佳,质谱响应更好。因此,本实验最终选择乙腈-0.1%甲酸水作为流动相系统进行梯度洗脱。优化质谱条件时,本实验采用了一级定量Full-MS结合正、负离子同时扫描的模式对各化合物的质谱响应进行了初步考察,结果表明各成分在正、负离子模式下的响应强度具有明显的差异。因此,本实验按照各成分的理化性质结合其在不同扫描模式下的质谱响应优劣,最终选择了响应最佳时的离子模式作为检测条件,使各待测物均具有较好的响应值和峰形,并能够满足快速、准确的定性要求。
本实验在正、负离子同时扫描的模式下,对复方血栓通胶囊中的主要活性化学成分进行快速识别,共鉴定出52种物质,其中黄酮类化合物13种,醌类11种,氨基酸类3种,酚酸类9种和其他类化合物16种。在以上成分中,黄酮类化合物具有抗氧化,抗肿瘤,抗心血管病以及抗炎症等药理作用,本品中的黄硐类化合物如基柄花茸、槲皮素主要来自于黄芪和丹参[34];醌类化合物具有抗肿瘤,抗病原微生物,抗炎,抗氧化,保护心血管等功效,本品中的醌类化合物如丹参酮ⅡA、隐丹参酮、丹参酮Ⅰ主要来自于丹参[35];酚酸类化合物是一类具有酚羟基母核结构的单/多酚酸聚合物超家族,具有抗炎,抗氧化,降血脂等药理作用,本品中的酚酸类成分如丹酚酸A、紫草酸等主要来自于丹参[36];氨基酸类化合物是具有维持生理、生化、免疫机能以及生长发育、新陈代谢等生命活动的重要功能,本品中的氨基酸类化合物如苏氨酸,主要来自于丹参和黄芪;此外,本研究还鉴定出的其他类化合物如三七皂苷Re,类叶升麻苷及人参皂苷Rb1等主要来自于三七和玄参。以上不同类别、不同来源的药物活性成分可通过协同或互补等作用,实现多成分、多靶点、多通路的治疗效果,最终使复方血栓通胶囊发挥活血化瘀、益气养阴之功效的显著功效。
研究结果表明,本实验建立的基于UHPLC-Q-Orbitrap的化学成分研究方法可全面、系统、准确地对复方血栓通胶囊中的主要活性成分进行快速识别。本研究首次从整体层面上对复方血栓通胶囊的有效成分化学谱进行深入探索,为深入挖掘分析其药效物质奠定了坚实的基础,同时也为该药今后质量控制的提高和进一步的临床研究奠定了科学的理论基础。
| [1] |
孙志, 胡玉荣, 左莉华, 等. UPLC-MS/MS法同时测定复方血栓通胶囊中9种成分的含量[J]. 中国药房, 2017, 28(21): 2959. SUN Z, HU YR, ZUO LH, et al. Simultaneous determination of 9 components in compound Xueshuantong capsules by UPLC-MS/MS[J]. China Pharm, 2017, 28(21): 2959. DOI:10.6039/j.issn.1001-0408.2017.21.22 |
| [2] |
龙克立. 复方血栓通胶囊在眼底疾病治疗中的应用价值[J]. 中外医疗, 2016, 35(8): 105. LONG KL. Application value of compound Xueshuantong capsule in treatment of fundus oculi disease[J]. China Foreign Med Treat, 2016, 35(8): 105. |
| [3] |
吴华锋, 蔡雪桃, 孔肖樱, 等. 复方血栓通胶囊治疗稳定型心绞痛的临床观察[J]. 亚太传统医药, 2012, 8(3): 79. WU HF, CAI XT, KONG XY, et al. Clinical observation on the treatment of stable angina pectoris by compound Xueshuantong capsule[J]. Asia Pac Tradit Med, 2012, 8(3): 79. DOI:10.3969/j.issn.1673-2197.2012.03.043 |
| [4] |
陈旭, 周立新, 田晓娟, 等. 工艺变更对中药制剂质量的影响[J]. 首都食品与医药, 2015, 22(14): 5. CHEN X, ZHOU LX, TIAN XJ, et al. Influence of the quality for Chinese medicine preparation changed by process[J]. Cap Food Med, 2015, 22(14): 5. |
| [5] |
刘俊, 朱宝平, 孙志, 等. 基于超高效液相色谱-四极杆/静电场轨道阱高分辨质谱的妇可靖胶囊中11种成分定量研究[J]. 中草药, 2018, 49(2): 353. LIU J, ZHU BP, SUN Z, et al. Quantitative research of multiple active components in Fukejing capsule based on ultra performance liquid chromatography-quadrupole/orbitrap high resolution mass spectrometry[J]. Chin Tradit Herb Drugs, 2018, 49(2): 353. |
| [6] |
渠琛玲, 张寒琦, 张华蓉, 等. 电喷雾质谱法研究氨基酸的质谱碎裂及其与人参皂苷Rb3的相互作用[J]. 高等学校化学学报, 2008, 29(9): 1721. QU CL, ZHANG HQ, ZHANG HR, et al. Studies on fragmentation pathways of amino acidsand their interactions with ginsenoside Rb3 by pectrospray ionization mass spectrometry[J]. Chem J Chin Univ, 2008, 29(9): 1721. DOI:10.3321/j.issn:0251-0790.2008.09.004 |
| [7] |
张玉, 董文婷, 霍金海, 等. 基于UPLC-Q-TOF-MS技术的广地龙化学成分分析[J]. 中草药, 2017, 48(2): 252. ZHANG Y, DONG WT, HUO JH, et al. Analysis on chemical constituents of Pheretima aspergillum by UPLC-Q-TOF-MS[J]. Chin Tradit Herb Drugs, 2017, 48(2): 252. |
| [8] |
秦伟瀚, 刘飞, 刘翔, 等. 基于UPLC-Q-TOF-MS法分析江西虫草化学成分[J]. 中药材, 2017, 40(6): 1339. QIN WH, LIU F, LIU X, et al. Study on chemical compositions in Cordyceps jiangxiensis by UPLC-Q-TOF-MS[J]. J Chin Med Mater, 2017, 40(6): 1339. |
| [9] |
National Center for Biotechnology Information.D-tert-leucine[EB/OL].USA, Bethesda: 2006[2018-03-17]. https: //pubchem.ncbi.nlm.nih.gov/compound/6950340#section=Top
|
| [10] |
王静哲, 徐风, 刘震, 等. 玄参化学成分HPLC-ESI-IT-TOF-MS分析[J]. 中国中药杂志, 2016, 41(7): 1257. WANG JZ, XU F, LIU Z, et al. Identification of chemical constituents in Scrophulariae Radix by HPLC-IT-TOF-MS[J]. China J Chin Mater Med, 2016, 41(7): 1257. |
| [11] |
陶益, 蒋妍慧, 唐克建, 等. 地黄炮制前后化学成分的UHPLC-Q-TOF/MS比较研究[J]. 中药新药与临床药理, 2016, 27(1): 102. TAO Y, JIANG YH, TANG KJ, et al. Comparison of chemical constituents of crude and processed products of Rehmannia glutinosa by using UHPLC-Q-TOF/MS[J]. Tradit Chin Drug Res Clin Pharmacol, 2016, 27(1): 102. |
| [12] |
束艳, 宿树兰, 钱大玮, 等. 柔肝胶囊化学成分的UPLC-ESI-QTOF/MS分析[J]. 中成药, 2011, 33(1): 73. SHU Y, SU SL, QIAN DW, et al. Chemical composition of Rougan capsule by UPLC-ESI-QTOF/MS[J]. Chin Tradit Pat Med, 2011, 33(1): 73. DOI:10.3969/j.issn.1001-1528.2011.01.019 |
| [13] |
夏玮, 古丽加玛丽·阿比斯, 潘晨, 等. 腊梅花中黄酮类化合物的UHPLC/QTOF-MS分析[J]. 中成药, 2014, 36(11): 2345. XIA W, GULIJIAMALI·A, PAN C, et al. Identification of flavonoids from Chimonanthus praecox(L.)Link by UHPLC /QTOF-MS[J]. Chin Tradit Pat Med, 2014, 36(11): 2345. DOI:10.3969/j.issn.1001-1528.2014.11.027 |
| [14] |
陈平, 路通, 吴伯英, 等. 应用液相色谱-质谱联用技术检测血浆样品中丹参酚酸类成分的浓度[J]. 中国临床药理学与治疗学, 2007, 12(7): 748. CHEN P, LU T, WU BY, et al. LC-MS/MS-based measurement of danshen phenolic acids in plasma[J]. Chin J Clin Pharmacol Ther, 2007, 12(7): 748. DOI:10.3969/j.issn.1009-2501.2007.07.006 |
| [15] |
万建波, 黎畅明, 李绍平, 等. 加压溶剂提取与液相色谱-电喷雾质谱联用技术分析三七中皂苷类成分[J]. 中药材, 2005, 28(10): 26. WAN JB, LI CM, LI SP, et al. Analysis of saponins from Panax notoginseng using pressurized solvent extraction coupled with liquid chromatography-electrospray mass spectrum[J]. J Chin Med Mater, 2005, 28(10): 26. |
| [16] |
徐文, 丘小惠, 张靖, 等. 超高压液相/电喷雾-LTQ-Orbitrap质谱联用技术分析三七根中皂苷类成分[J]. 药学学报, 2012, 47(6): 773. XU W, QIU XH, ZHANG J, et al. Analysis of saponins in Panax notoginseng by UP LC-LT Q-Orbitrap MS/MS[J]. Acta Pharm Sin, 2012, 47(6): 773. |
| [17] |
黄永松, 傅家谟, 盛国英, 等. 高蜡原油及其生油岩中新生物标志物-α雪松烯和花侧柏烯[J]. 地球化学, 1991, 20(3): 276. HUANG YS, FU JM, SHENG GY, et al. Identification and confirmation of α-cedrene and cuparene in high-vax oils and related Source rocks[J]. Geochimica, 1991, 20(3): 276. DOI:10.3321/j.issn:0379-1726.1991.03.009 |
| [18] |
刘炎.中药黄芪炮制及复方配伍的化学研究[D].长春: 长春中医药大学, 2007 LIU Y.Study on Chemical Constituents of Processed Radix Astragali and Combination of Radix Astragali and Radix Angelicae Sinensis[D].Changchun: Changchun University of Chinese Medicine, 2007 |
| [19] |
董昕, 徐立, 娄子洋. 丹参药材中水溶性及脂溶性成分的电喷雾离子阱质谱研究[J]. 中国药学杂志, 2010, 45(14): 1048. DONG X, XU L, LOU ZY. Determination of chemical components from Salvia miltiorrhiza Bunge by electrospray ion-trap mass spectrometry[J]. Chin Pharm J, 2010, 45(14): 1048. |
| [20] |
毛艳, 张瑞萍, 贺金华, 等. 高效液相色谱-四极杆/静电场轨道阱高分辨质谱分析紫草中酚酸类化合物[J]. 药物分析杂志, 2016, 36(7): 1199. MAO Y, ZHANG RP, HE JH, et al. Determination of phenolic acids compounds in Arnebia euchroma(Royle)Johnstn.by Q exactive hybrid quadrupole-orbitrap mass spectrometer[J]. Chin J Pharm Anal, 2016, 36(7): 1199. |
| [21] |
张靖, 丘小惠, 徐文, 等. 基于液质联用技术的复方三芪口服液化学成分特征图谱研究[J]. 中华中医药杂志, 2013, 28(5): 1572. ZHANG J, QIU XH, XU W, et al. Characteristic spectrum analysis of chemical components in Sanqi oral liquid by UPLC-MS/MS[J]. Chin J Tradit Chin Med Pharm, 2013, 28(5): 1572. |
| [22] |
孔海宁.三七茎叶提取物中皂甙成分定性及三七皂甙Fa的制备[D].天津: 天津大学, 2006 KONG HN.The Identification of the Notoginseng Folium Saponins and the Purification of Notoginsenoside Fa[D].Tianjing: Tianjin University, 2006 |
| [23] |
朱慧明.基于液质联用技术的芪苈强心胶囊中多组分分析与药代动力学研究[D].石家庄: 河北医科大学, 2014 ZHU HM.Multicomponent Analysis and Pharmacokinetic Studies by UPLC/Q-TOF-MS/MS in Qiliqiangxin Capsules[D].Shijiazhuang: Hebei Medical University, 2014 |
| [24] |
National Center for Biotechnology Information.Ginsenoside Re[EB/OL].USA, Bethesda: 2005[2018-03-17]. https://pubchem.ncbi.nlm.nih.gov/compound/441921
|
| [25] |
刘劼, 杨黄浩, 黎先春, 等. 高效液相色谱-电喷雾飞行时间质谱分析丹参中的丹参酮类化合物[J]. 质谱学报, 2008, 29(5): 261. LIU J, YANG HH, LI XC, et al. Analysis of diterpene quinones in Danshen(Salvia miltiorrhiza Bunge)by HPLC-ESI/TOF MS[J]. J Chin Mass Spectrom Soc, 2008, 29(5): 261. |
| [26] |
The Human Metabolome Database.Hydroxytanshinone(HMDB0036635)[EB/OL].Canada, Edmonton: 2012[2018-03-12].http://www.hmdb.ca/metabolites/HMDB36635
|
| [27] |
闫海全.三七中主要皂苷类化合物的液相色谱分析与制备鉴定[D].成都: 成都理工大学, 2009 YAN HQ.The Analysis by HPLC, Isolation and Identification of Main Saponin Compounds in Panax notoginseng[D].Chengdu: Chengdu University of Technology, 2009 |
| [28] |
National Center for Biotechnology Information.Przewalskin[EB/OL].USA, Bethesda: 2007[2018-03-17].https://pubchem.ncbi.nlm.nih.gov/compound/14139389#section=Top
|
| [29] |
National Center for Biotechnology Information.Danshenxinkun B[EB/OL].USA, Bethesda: 2006[2018-03-17].https://pubchem.ncbi.nlm.nih.gov/compound/5320113#section=Top
|
| [30] |
National Center for Biotechnology Information.Neocryptotanshinone[EB/OL].USA, Bethesda: 2005[2018-03-17].https://pubchem.ncbi.nlm.nih.gov/compound/184103#section=Top
|
| [31] |
孔德云, 刘星堦, 滕脉坤, 等. 丹参中丹参螺旋缩酮内酯的结构[J]. 药学学报, 1985, 20(10): 747. KONG DY, LIU XJ, TENG MK, et al. The structure of Dan-Shen epiroketallactone of Dan-Shen(Salvia miltiorrhiza Bunge)[J]. Acta Pharm Sin, 1985, 20(10): 747. |
| [32] |
王红蕾, 齐崴, 吴小东, 等. 丹参水溶性多酚酸的多级串联电喷雾离子阱质谱断裂机理解析[J]. 质谱学报, 2008, 29(3): 129. WANG HL, QI W, WU XD, et al. Fragmentation mechanisms of phenolic acids from Danshen in an ion trap by electrospray ionization multi-stage tandem mass spectrometry[J]. J Chin Mass Spectrom Soc, 2008, 29(3): 129. |
| [33] |
李想.黄酮醇类化合物ESI-ITMSn质谱裂解规律的量子化学研究[D].佳木斯: 佳木斯大学, 2015 LI X.Quantum Chemistry Study on ESI-ITMSn Cleavage Regularity of Flavonol Compounds[D].Heilongjiang: Jiamusi University, 2015 |
| [34] |
张丹萍, 丁丁. 黄酮类化合物药理作用的研究[J]. 北方药学, 2015, 12(8): 150. ZHANG DP, DING D. Study on the pharmacological action of flavonoids[J]. J North Pharm, 2015, 12(8): 150. |
| [35] |
魏蕾. 醌类化合物的分布和药理作用[J]. 现代中药研究与实践, 2013, 27(1): 34. WEI L. Distribution and pharmacology of quinones[J]. Res Pract Chin Med, 2013, 27(1): 34. |
| [36] |
斯日古楞, 刘洪涛. 中药酚酸的体内代谢研究进展[J]. 亚太传统医药, 2008, 4(6): 49. SIRIGULENG, LIU HT. Research on the metabolism of phenolic acids in Chinese medicine[J]. Asia Pac Tradit Med, 2008, 4(6): 49. |
 2019, Vol. 39
2019, Vol. 39 
