中药防风始载于《神农本草经》,被列为上品,为伞形科植物防风Saposhnikovia divaricata(Turcz.)Schisck的干燥根;其味辛甘,性温,能解表祛风,胜湿,止痉[1]。野生防风主要分布于我国东北、内蒙古、河北、山东、河南、陕西、甘肃等部分地区,根据产地不同,可分为关防风、口防风、西防风和山防风等,其中以关防风质量最佳[2]。
防风主要含有香豆素和色原酮两大类化学成分,现代药理学表明[3],升麻素苷和5-O-甲基维斯阿米醇苷均具有明显的解热、镇痛、消炎及抗血小板凝聚作用。据文献报道[4],防风在血浆中含量最高的成分是升麻素、升麻素苷和5-O-甲基维斯阿米醇苷等苷类物质必须在肠道内转化为升麻素苷后才能被吸收。亥茅酚苷是具有消炎和抗免疫作用[5]的一种色原酮类化合物,研究发现,升麻苷和亥茅酚苷在人源肠Caco-2细胞单层吸收模型具有中等程度的吸收性,提示它们可以进入血液循环发挥生物学活性[6];所以,色原酮类化合物升麻素、升麻素苷、亥茅酚苷和5-O-甲基维斯阿米醇苷可作为防风质量考察的重要指标。由于防风有栽培和野生2种生长方式,栽培繁殖方式也不尽相同,质量悬殊较大,用同一种质量评价方式考察野生和栽培防风的质量难免有所缺陷。
中药指纹图谱[7]能较为全面地反映中药及其制剂中所含化学成分的种类与数量,进而对药品质量进行整体描述和评价,在中药质量控制领域已被广泛运用[8-10]。一测多评法(quantitative analysis of multi-components by single marker,QAMS)只需测定1个成分(对照品易得)即可实现多个成分同时测定[11],可以有效解决质量分析过程中由于对照品短缺带来的困难。本课题收集来自10个不同地区的野生关防风和2个栽培品种进行研究,将指纹图谱法和一测多评法相结合,利用HPLC建立关防风HPLC指纹图谱,并建立升麻素、升麻素苷、亥茅酚苷和5-O-甲基维斯阿米醇苷一测多评定量分析法,通过定性和定量2种方法考察关防风质量,为防风质量评价提供参考依据。
1 仪器和材料Waters 2695-2996型高效液相色谱仪;ES520A电子分析天平(0.1 mg,普利赛斯公司);KQ5200超声波清洗仪(昆山市超声仪器有限公司;功率250 W,频率40 kHz);Milli-Q Integral 5超纯水机(德国默克密理博公司);FW100中草药粉碎机(天津市泰斯特仪器有限公司)。
12批防风药材购自黑龙江哈尔滨三棵树中药材专业市场(见表 1),经吉林农业大学中药材学院张连学教授鉴定为伞形科植物Saposhnikovia divaricata(Tucrz.)Schischk的干燥根。取干燥根适量,置45 ℃烘干至恒重,粉碎过筛(4号筛),备用。
|
|
表 1 关防风药品来源 Tab.1 The origins of Radix Saposhnikoviae from northeast |
对照品升麻素苷(批号111522-201310,含量95%)、5-O-甲基维斯阿米醇苷(批号111523-201208,含量96.4%)、亥茅酚苷(批号111714-200501,含量≥98.0%)、升麻素(批号111710-200602,含量≥98.0%)、汉黄芩苷(批号112002-201702,含量98.5%)、欧前胡素(批号110826-201616,含量99.6%)均来源于中国食品药品检定研究院,香柑内酯对照品(批号36706,含量≥98.0%)由上海晶纯实业有限公司提供;甲醇为色谱纯,水为超纯水,其余试剂均为分析纯。
2 方法与结果 2.1 溶液的制备 2.1.1 混合对照品溶液精密称取升麻素苷、升麻素、5-O-甲基维斯阿米醇苷及亥茅酚苷、汉黄芩苷、欧前胡素及香柑内酯的对照品各适量,加色谱甲醇制得含升麻素苷0.148 mg·mL-1、升麻素0.018 mg·mL-1、5-O-甲基维斯阿米醇苷0.117 mg·mL-1、亥茅酚苷0.024 mg·mL-1、汉黄芩苷0.026 mg·mL-1、欧前胡素0.056 mg·mL-1及香柑内酯0.028 mg·mL-1的混合溶液,滤过(0.22 μm微孔滤膜),取续滤液,即得。
2.1.2 供试品溶液取防风粉末约5 g,精密称定,置具塞锥形瓶中,精密加入甲醇100 mL,称量,水浴回流2 h,放冷,再称量,用甲醇补足减失的量,摇匀,滤过(0.22 μm微孔滤膜),取续滤液,即得。
2.2 色谱条件[12]色谱柱为Agilent ZORBAX Eclipse XDB C18(2)(250 mm×4.6 mm,5 μm);流动相A为甲醇,B为水,梯度洗脱(见表 2);流速为1.0 mL·min-1;检测波长为254 nm;柱温为30 ℃;进样量为10 μL。
|
|
表 2 梯度洗脱程序 Tab.2 Gradient elution |
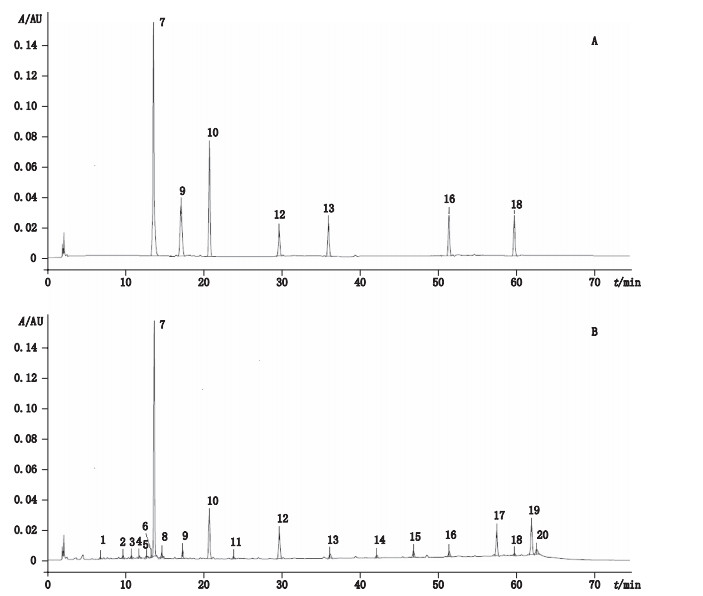
分别取空白溶剂、混合对照品溶液及防风供试品溶液各10 μL,按上述色谱条件进行分析,结果空白溶剂无干扰,样品中各峰分离完全,升麻素苷、升麻素、5-O-甲基维斯阿米醇苷及亥茅酚苷峰理论板数均大于5 000,色谱图见图 1。
|
7.升麻素苷(prim-O-glucosylcimifugin)9.升麻素(cimifugin)10.5-O-甲基维斯阿米醇苷(4′-O-β-D-glucosyl-5-O-methylvisamminol)12.亥茅酚苷(sec-O-glucosylhamaudol)13.香柑内酯(bergapten)16.汉黄芩苷(wogonoside)18.欧前胡素(imperatorin) 图 1 关防风混合对照品(A)和供试品(B)HPLC图 Fig.1 HPLC chromatograms of mixed reference substances(A)and sample(B)in Radix Saposhnikoviae from northeast |
取来源于辽宁省义县的防风供试品溶液(样品编号S1),按“2.2”项色谱条件,连续进样6次,记录色谱图,以5-O-甲基维斯阿米醇苷为参比峰,计算各共有峰相对保留时间的RSD均小于0.2%,相对峰面积的RSD均小于2.5%,表明仪器精密度良好。
2.3.2 稳定性试验取供试品溶液(样品编号S1),按“2.2”项色谱条件,分别在0、4、8、12、24、36、48 h进样,记录色谱图,以5-O-甲基维斯阿米醇苷为参比峰,计算各共有峰相对保留时间的RSD均小于0.2%,相对峰面积的RSD均小于3.0%,结果表明供试品溶液在48 h内稳定。
2.3.3 重复性试验取样品(编号S1)细粉6份,按“2.1.2”项下方法制备供试品溶液,分别精密吸取10 μL,按“2.2”项色谱条件分析,记录色谱图,以5-O-甲基维斯阿米醇苷为参比峰,计算各共有峰相对保留时间的RSD均小于0.1%,相对峰面积的RSD均小于3.0%,结果表明方法重复性良好。
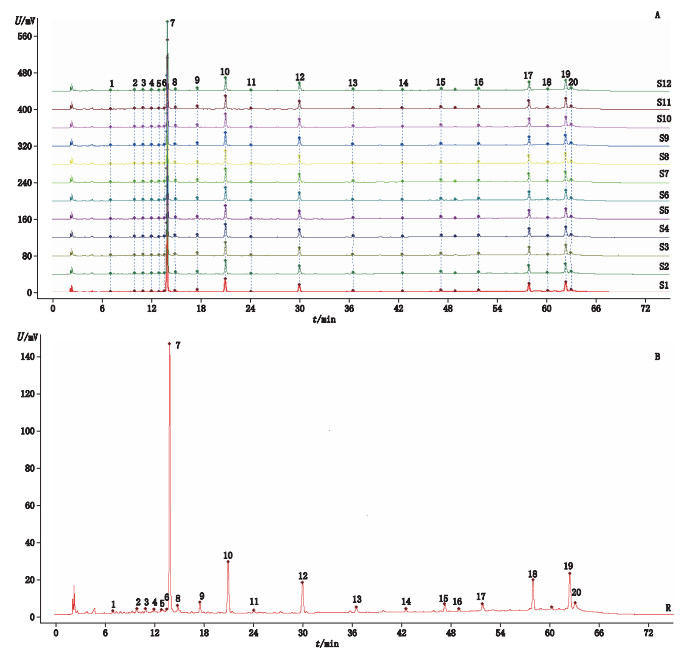
2.3.4 指纹图谱的建立及部分共有峰指认将来源自12个不同产区防风药材HPLC色谱图导入《中药色谱指纹图谱相似度评价系统》(2012年版)软件进行分析,以S1号图谱为参考,时间窗宽度设为0.1 min,采用多点校正全谱峰匹配,建立各自指纹图谱并生成指纹图谱共有模式,其中标定了共有峰20个,指纹图谱见图 2。通过与混合对照品保留时间进行比对,指认出20个共有峰当中的7个,分别为7号峰(升麻素苷)、9号峰(升麻素)、10号峰(5-O-甲基维斯阿米醇苷)、12号峰(亥茅酚苷)、13号峰(香柑内酯)、16号峰(汉黄芩苷)、18号峰(欧前胡素)。在20个共有峰中,以10号峰(5-O-甲基维斯阿米醇苷)的峰形最佳,位置适中,以其为参照峰(S),计算各共有峰的相对峰面积及相对保留时间进行方法学考察,相对峰面积见表 3。
|
图 2 12批关防风HPLC指纹图谱(A)和对照指纹图谱(B) Fig.2 Fingerprints(A)of 12 batches of Radix Saposhnikoviae from northeast and reference fingerprint(B) |
|
|
表 3 12批样品(S1~S12)共有峰相对峰面积 Tab.3 Common relative peak areas of 12 samples(S1-S12) |
以共有模式作为对照指纹图谱,采用国家药典委员会推荐的《中药色谱指纹图谱相似度评价系统》(2012年版)软件对12批防风样品指纹图谱进行相似度评价。结果,S1~S12号样品与对照图谱的相似度分别为0.939、0.936、0.986、0.959、0.978、0.992、0.985、0.956、0.965、0.968、0.959、0.963、0.972,相似度均大于0.90,说明不同来源12批关防风所含化学成分基本一致,符合指纹图谱相关要求。
2.4 一测多评法测定关防风中4个指标性成分含量 2.4.1 溶液制备及色谱条件依“2.1”和“2.2”项下方法同法处理。
2.4.2 线性关系考察分别精密吸取混合对照品溶液2、4、8、12、24、40 μL,按“2.2”项色谱条件测定,记录色谱图,以各组分峰面积(Y)对进样量(X,μg)进行回归处理,得各组分回归方程及线性范围,见表 4。
|
|
表 4 4个化合物的回归方程及线性范围 Tab.4 Regression equations and linear ranges of 4 compounds |
取已知含量关防风(编号S1)细粉约2.5 g,精密称定,置具塞锥形瓶中,精密加入对照品混合溶液(含升麻素苷3.518 mg·mL-1、升麻素0.643 mg·mL-1、5-O-甲基维斯阿米醇苷2.201 mg·mL-1及亥茅酚苷0.650 mg·mL-1)1 mL,按“2.1.2”项下方法制备供试溶液,按“2.2”项色谱条件测定,记录色谱图,计算回收率,结果见表 5。
|
|
表 5 关防风中4个成分的加样回收率结果(n=6) Tab.5 Recoveries of 4 components in Radix Saposhnikoviae from northeast |
一测多评法是利用在一定线性范围成分的量(质量或浓度)与检测器响应成正比的原理,本研究采用多点校正法计算相对校正因子,公式为fks=fk/fs=(Ck×As)/(Cs×Ak)(式中As为内参物s峰面积,Cs为内参物s的浓度,Ak为某待测成分k峰面积,Ck为某待测成分对照品k的浓度)。
取“2.1.1”项下混合对照品溶液,按“2.2”项下色谱条件,分别进样2、5、10、15、20、30 μL,测定。以10号峰(5-O-甲基维斯阿米醇苷)为内参物s,根据公式分别计算待测组分升麻素苷(a)、升麻素(b)、亥茅酚苷(c)的相对校正因子,结果见表 6。
|
|
表 6 4个成分相对校正因子 Tab.6 The relative correction factors of four components |
精密量取混合对照品溶液10 μL,按“2.2”项色谱条件测定,分别考察Waters 2695、Agilent 1260、日立Chromaster3种高效液相色谱仪和Agilent ZORBAX Eclipse XDB C18(2)(250 mm×4.6 mm,5 μm)、Shim-pack GIST C18(250 mm×4.6 mm,5 μm)、Thermo ODS C18(250 mm×4.6 mm,5 μm)3种色谱柱对相对校正因子的影响,结果见表 7。结果RSD均小于5%,表明不同色谱仪及色谱柱对相对校正因子无显著影响。
|
|
表 7 不同高效液相色谱仪及色谱柱的相对校正因子 Tab.7 Relative correction factors in different high performance liquid chromatographs and columns |
一测多评法峰定位主要分为相对保留值法和保留时间差法2种,而相对保留值法在实际应用中较多,本研究采用此法,并采用不同色谱仪及色谱柱验证方法耐用性,结果见表 8。结果RSD均小于5%,升麻素苷、升麻素、5-O-甲基维斯阿米醇苷、亥茅酚苷的相对保留时间分别为0.66、0.83、1.00和1.43,表明相对保留值的重现性较好。
|
|
表 8 不同仪器和色谱柱相对保留值比较 Tab.8 Relative retention time determined by different instruments and columns |
取S1~S12号关防风样品,按“2.1.2”项下方法制备供试品溶液,按“2.2”项下色谱条件进行分析,分别采用外标法(ESM)和一测多评法(QASM)计算关防风中升麻素苷、升麻素、5-O-甲基维斯阿米醇苷和亥茅酚苷含量,并利用SPSS Statistics 22统计软件对2组检测结果进行成组t检验,考察2种方法显著性差异,结果见表 9。由表可知,2种方法无显著性差异(P > 0.05),表明一测多评法可用于关防风中4个化学成分的含量测定。
|
|
表 9 QAMS法与ESM法测得的关防风中4个化合物的含量(mg·g-1,n=2) Tab.9 Determination results of 4 compounds in Radix Saposhnikoviae by QAMS and ESM |
防风的化学成分质控方法研究较多,本研究对赵博等[12]利用HPLC法同时测定防风中6个主要成分过程中采用的流动相进行调整,最终确定“2.2”项下甲醇-水梯度洗脱系统。
防风中不仅含有香豆素类和色原酮类化合物,还含有丰富的多糖和单宁等,尽管色原酮类化合物在甲醇中溶解性好,但研究发现,超声处理样品所得色谱图不够理想,化合物分离不够完全,无法达到定量分析要求;最终,通过摸索发现,水浴回流2 h,所有目标化合物能提取完全,干扰成分很小,各峰之间分离度良好。
本研究的指纹图谱和一测多评法均经方法学考察,有着较好的重复性和准确性,能有效区分野生和栽培关防风,在节省实验成本(对照品)的同时,还可以将模糊鉴别和精准定量分析有机结合,既可以对药品整体质量做出客观系统评价,又可以利用部分指标性成分对其做出动态监测,为有效控制关防风质量提供检验依据。
| [1] |
中华人民共和国药典2015年版.一部[S]. 2015: 149 ChP 2015. Vol Ⅰ[S]. 2015: 149 |
| [2] |
杨景明, 姜华, 孟祥才. 中药防风质量评价的现状与思考[J]. 中药材, 2016, 39(7): 1678. YANG JM, JIANG H, MENG XC. Status and thoughts on quality assessment of Saposhnikovia divaricata[J]. Chin Med Mater J, 2016, 39(7): 1678. |
| [3] |
薛宝云, 李文, 李丽, 等. 防风色原酮甙类成分的药理活性研究[J]. 中国中药杂志, 2000, 25(5): 41. XUE BY, LI W, LI L, et al. A Pharmacodynamic research on chromone glucosides of Fangfeng[J]. China J Chin Mater Med, 2000, 25(5): 41. |
| [4] |
李悦悦, 王慧, 陈俊, 等. RRLC-TOF/MS鉴别防风血浆、尿液中成分及代谢产物[J]. 第二军医大学学报, 2010, 31(7): 760. LI YY, WANG H, CHEN J, et al. RRLC-TOF/MS in identification of constituents and metabolites of Radix Saposhnikoviae in rat plasma and urine[J]. Acad J Second Mil Med Univ, 2010, 31(7): 760. |
| [5] |
罗超, 沈立, 吕昌. 亥茅酚苷对脂多糖诱导巨噬细胞一氧化氮和白介素6表达的影响[J]. 中国免疫学杂志, 2015, 31(11): 1486. LUO C, SHEN L, LÜ C. Effects of sec-O-glucosylhamaudol on expressions of nitric oxide and interleukin-6 in ipopolysaccharide stimulated murine macrophage[J]. Chin J Immunol, 2015, 31(11): 1486. DOI:10.3969/j.issn.1000-484X.2015.11.009 |
| [6] |
ZHAO B, YANG XB, YANG XW, et al. Intestinal permeability of the constituents of the roots of Saposhnikovia divaricata in the human Caco-2 cell monolayer model[J]. Plant Med, 2011, 77(13): 1531. DOI:10.1055/s-0030-1270741 |
| [7] |
杨妮娜, 杨天梅, 赵应红, 等. HPLC指纹图谱技术在傣药灯台叶资源评价中的应用[J]. 药物分析杂志, 2016, 36(3): 473. YANG NN, YANG TM, ZHAO YH, et al. Application of HPLC fingerprint technology in the resource evaluation of Alstonia scholaris (L.)R. Br.[J]. Chin J Pharm Anal, 2016, 36(3): 473. |
| [8] |
张春泥, 王英姿, 孙欣光, 等. HPLC-CAD结合化学计量学的川楝子饮片指纹图谱研究[J]. 药学学报, 2017, 52(3): 456. ZHANG CN, WANG YZ, SUN XG, et al. Chromatographic fingerprint analysis of Toosendan Fructus by HPLC-CAD coupled with chemometrics methods[J]. Acta Pharm Sin, 2017, 52(3): 456. |
| [9] |
潘伟东, 杜义龙, 赵胜男. 韩信草的高效液相色谱指纹图谱及化学模式识别[J]. 药物分析杂志, 2015, 35(2): 250. PAN WD, DU YL, ZHAO SN, et al. HPLC fingerprint and chemical pattern recognition of Scutellaria indica[J]. Chin J Pharm Anal, 2015, 35(2): 250. |
| [10] |
杨宁, 刘艳妮, 康杰芳. 山茱萸药材HPLC指纹图谱的优化研究[J]. 药物分析杂志, 2014, 34(11): 1989. YANG N, LIU YN, KANG JF. Optimization of the HPLC fingerprint for Cornus officinalis[J]. Chin J Pharm Anal, 2014, 34(11): 1989. |
| [11] |
王智民, 高慧敏, 付雪涛, 等. "一测多评"法中药质量评价模式方法学研究[J]. 中国中药杂志, 2006, 31(23): 1925. WANG ZM, GAO HM, FU XT, et al. Multi-components quantitation by one marker new method for quality evaluation of Chinese herbal medicine[J]. China J Chin Mater Med, 2006, 31(23): 1925. DOI:10.3321/j.issn:1001-5302.2006.23.001 |
| [12] |
赵博, 杨鑫宝, 杨秀伟, 等. HPLC法同时测定防风中6个主要成分的含量[J]. 药物分析杂志, 2013, 33(3): 382. ZHAO B, YANG XB, YANG XW, et al. Simultaneous determination of six major constituents in the roots of Saposhnikovia divaricata by HPLC[J]. Chin J Pharm Anal, 2013, 33(3): 382. |
| [13] |
王晓燕, 霍甜甜, 李振国. 一测多评法同时测定杞菊地黄口服液中4种有效成分的含量[J]. 药物分析杂志, 2017, 37(2): 290. WANG XY, HUO TT, LI ZG. Simultaneous determination of 4 active components in Qijudihuang oral liquid by QAMS method[J]. Chin J Pharm Anal, 2017, 37(2): 290. |
 2019, Vol. 39
2019, Vol. 39 