2. 常州市食品药品监督检验中心, 常州 213003
2. Changzhou Center for Food and Drug Control, Changzhou 213003, China
枯草杆菌二联活菌颗粒商品名为妈咪爱,是用于治疗腹泻病特别是慢性腹泻的微生态制剂,其主要成分为活菌冻干粉,每袋(1 g)含屎肠球菌R-026 1.35×108 CFU、枯草芽孢杆菌R-179 1.5×107 CFU,以及各种维生素、微量元素锌、矿物质钙, 说明书中用法为40 ℃以下温开水或牛奶冲服,也可直接服用。急性腹泻患儿在补充肠道益生菌的同时也要补锌治疗,葡萄糖酸锌口服溶液为常用的补锌制剂。益生菌制剂作用的决定因素是微生物的活力,影响益生菌发挥作用的因素包括益生菌制剂类型、剂量、是否与牛奶或食物共同进食、温度、胃液pH、胆汁、肠道动力以及肠道基础菌群分布等。目前对枯草杆菌二联活菌颗粒的研究主要集中在治疗小儿急性、肺炎继发性和消化不良性腹泻[1-3]、便秘[4]、生理及病理性黄疸[5-6]、过敏和免疫性疾病[7-8]及其安全性评价[9],对给药方式的研究尚未见报道。为寻求一个最佳给药方式,本文模拟了枯草杆菌二联活菌颗粒的4种给药过程,考察了人工胃液、葡萄糖酸锌口服溶液、牛奶等对枯草杆菌二联活菌颗粒中2种益生菌的体外活性的影响。
1 实验仪器与材料含糖胃蛋白酶由甘肃天森药业有限公司生产(批号151001);枯草杆菌二联活菌颗粒由北京韩美药品有限公司生产(批号16110056、17040047、17040059);胰酪大豆胨琼脂培养基(批号150923)和胰酪大豆胨液体培养基(批号151228)由北京陆桥技术有限责任公司生产;牛奶为市售纯牛奶;葡萄糖酸锌口服溶液(批号20170525、20170721、20170905)由本院自制;温开水为灭菌纯化水,由本院自制;牛奶和温开水均为40 ℃以下。人工胃液:取稀盐酸16.4 mL,加入纯化水约800 mL与胃蛋白酶10 g,摇匀后加纯化水稀释成1 000 mL。
净化工作台SW-CJ-1FD(苏净集团安泰公司);DNP-9052电热恒温培养箱(上海精宏实验设备有限公司);DHG-9070A型电热鼓风干燥箱(上海一恒科学仪器有限公司);BCD-188AK冰箱(上海尊贵电器有限公司);LMQ.C型立式灭菌器(山东新华医疗器械股份有限公司)。
2 方法与结果 2.1 枯草杆菌二联活菌颗粒中2种菌的分离鉴定和培养基及其温度的选择取枯草杆菌二联活菌颗粒冻干粉少许,分别置于胰酪大豆胨琼脂培养基平板、血平板、6.5%氯化钠营养琼脂培养基平板上,于37 ℃培养48 h,必要时可分离纯化[10]。3种平板上均可见有2种形态的菌落且生长良好:1种为无芽孢,无鞭毛,圆形或椭圆形,表面光滑凸起,白色或乳白色,周边整齐,单个、成对或呈短链状排列,革兰氏染色为阳性球菌,即为屎肠球菌R-026;另1种为表面色暗,粗糙不透明,污白色或微黄色,无荚膜,周生鞭毛,椭圆到柱状,革兰氏染色为阳性杆菌,即为枯草芽孢杆菌R-179。屎肠球菌R-026和枯草芽孢杆菌R-179在血平板上菌落较大,胰酪大豆胨琼脂培养基上次之,6.5%氯化钠营养琼脂培养基上最小。本文选择胰酪大豆胨琼脂培养基。
取上述分离纯化的屎肠球菌R-026、枯草芽孢杆菌R-179,分别加入至10 mL胰酪大豆胨液体培养基中,37 ℃培养24~48 h,制成屎肠球菌、枯草芽孢杆菌浓菌液并用生理盐水逐级稀释;取稀释液1 mL,分别加入40、45、50 ℃的胰酪大豆胨琼脂培养基,混匀,37 ℃培养24~72 h后,点计菌落数。结果2种菌的相同稀释级在不同温度培养基中菌落数无差异,由于40 ℃时培养基趋于凝固,故本文选择常用的45 ℃的胰酪大豆胨琼脂培养基。
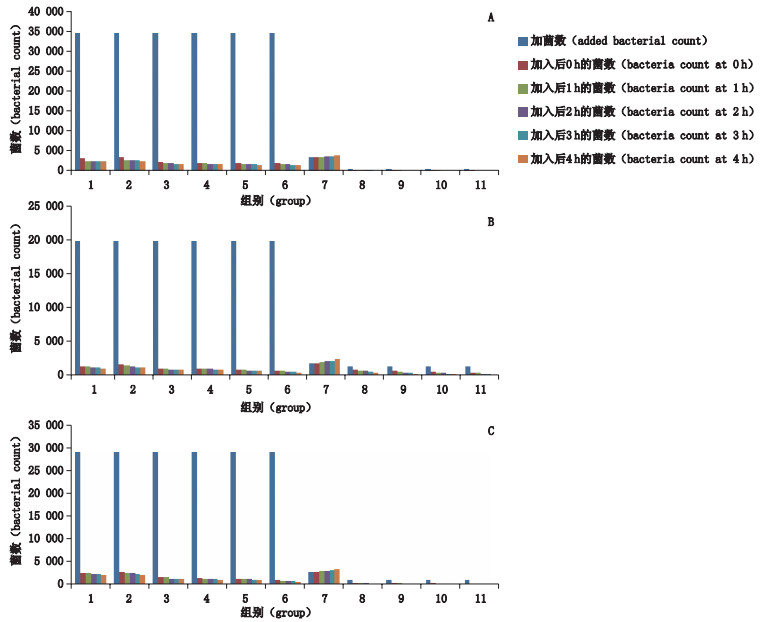
2.2 枯草杆菌二联活菌颗粒在人工胃液、温开水+人工胃液、牛奶+人工胃液和葡萄糖酸锌口服溶液+人工胃液中2种益生菌活性的考察取枯草杆菌二联活菌颗粒10 mg,用生理盐水稀释[11],取适量分别加入至无菌的空瓶、10 mL温开水、10 mL牛奶和6.67、10.00、13.33、20.00 mL葡萄糖酸锌口服溶液中,混匀,各组分别加入37 ℃人工胃液10 mL,混匀,分别于37 ℃培养0、1、2、3、4 h,混匀。取上述各组培养物适量于培养皿中,加入45 ℃胰酪大豆胨琼脂培养基,混匀,37 ℃培养72~120 h,点计菌落数并折算成原溶液所含的总菌数。取3个批号的枯草杆菌二联活菌颗粒平行操作3次,结果见图 1。
|
1.人工胃液+枯草杆菌二联活菌颗粒组(artificial gastric juice + live combined bacillus subtilis and enterococcus faecium granules with multivitamines group) 2.温开水+人工胃液+枯草杆菌二联活菌颗粒组(warm water + artificial gastric juice + live combined bacillus subtilis and enterococcus faecium granules with multivitamines group) 3.葡萄糖酸锌口服溶液6.67 mL+人工胃液+枯草杆菌二联活菌颗粒组(zinc gluconate oral solution 6.67 mL + artificial gastric juice + live combined bacillus subtilis and enterococcus faecium granules with multivitamins group) 4.葡萄糖酸锌口服溶液10.00 mL+人工胃液+枯草杆菌二联活菌颗粒组(zinc gluconate oral solution 10.00 mL + artificial gastric juice + live combined bacillus subtilis and enterococcus faecium granules with multivitamins group) 5.葡萄糖酸锌口服溶液13.33 mL+人工胃液+枯草杆菌二联活菌颗粒组(zinc gluconate oral solution 13.33 mL + artificial gastric juice + live combined bacillus subtilis and enterococcus faecium granules with multivitamins group) 6.葡萄糖酸锌口服溶液20.00 mL+人工胃液+枯草杆菌二联活菌颗粒组(zinc gluconate oral solution 20.00 mL + artificial gastric juice + live combined bacillus subtilis and enterococcus faecium granules with multivitamins group) 7.牛奶+人工胃液+枯草杆菌二联活菌颗粒组(milk + artificial gastric juice + live combined bacillus subtilis and enterococcus faecium granules with multivitamines group) 8.葡萄糖酸锌口服溶液6.67 mL+屎肠球菌R-026组(zinc gluconate oral solution 6.67 mL + Enterococcus faecium R-026 group) 9.葡萄糖酸锌口服溶液10.00 mL+屎肠球菌R-026组(zinc gluconate oral solution 10.00 mL + Enterococcus faecium R-026 group) 10.葡萄糖酸锌口服溶液13.33 mL+屎肠球菌R-026组(zinc gluconate oral solution 13.33 mL +Enterococcus faecium R-026 group) 11.葡萄糖酸锌口服溶液20.00 mL+屎肠球菌R-026组(zinc gluconate oral solution 20.00 mL + Enterococcus faecium R-026 group) A.批号(lot No.)16110056 B.批号(lot No.)17040047 C.批号(lot No.)17040059 图 1 3个批号的枯草杆菌二联活菌颗粒在人工胃液、温开水+人工胃液、牛奶+人工胃液和葡萄糖酸锌口服溶液+人工胃液中,屎肠球菌R-026在葡萄糖酸锌口服溶液中4 h内的菌落数图 Fig.1 The bacteria count of three batches of Live combined bacillus subtilis and enterococcus faecium granules with multivitamines in artificial gastric juice, warm water + artificial gastric juice, zinc gluconate oral solution + artificial gastric juice, milk + artificial gastric juice, of Enterococcus Faecium R-026 in zinc gluconate oral solution in 4 hours |
将屎肠球菌R-026浓菌液用生理盐水稀释,取适量分别加入至不同剂量的无菌葡萄糖酸锌口服溶液中,分别于37 ℃培养0、1、2、3、4 h,取上述各组培养物适量于培养皿中,加入45 ℃胰酪大豆胨琼脂培养基,混匀,37 ℃培养72~120 h,点计菌落数并折算成原溶液中所含的总菌数。取3个批号的枯草杆菌二联活菌颗粒平行操作3次,结果见图 1。
3 讨论 3.1 枯草杆菌二联活菌颗粒在人工胃液、温开水+人工胃液中2种益生菌的生长情况由实验结果可见,含菌落数为1.99×104~3.46×104 CFU的枯草杆菌二联活菌颗粒在人工胃液、温开水+人工胃液中2种益生菌受到抑制,菌落数明显小于加入量且4 h内渐少,仅见枯草芽孢杆菌R-179菌落生长,屎肠球菌R-026被完全抑制。3个批号的枯草杆菌二联活菌颗粒在人工胃液组4 h内分别减少92.69%、93.70%、92.18%,无明显差异;在温开水+人工胃液组4 h内分别减少92.54%、93.56%、91.99%,无明显差异。人工胃液组的菌落数少于温开水+人工胃液组,表明人工胃液的抑制作用大于温开水+人工胃液,但差异不明显。人工胃液、温开水+人工胃液的pH分别为1.5、2.0,pH越小,抑菌作用越强。这与卢士玲等[12]报道的低pH对屎肠球菌的生长和生物胺的产生均有显著的抑制作用一致。
3.2 枯草杆菌二联活菌颗粒在不同剂量的葡萄糖酸锌口服溶液+人工胃液中及屎肠球菌R-026在不同剂量的葡萄糖酸锌口服溶液中2种益生菌的生长情况由实验结果可见,含菌落数为1.99×104~3.46×104 CFU的枯草杆菌二联活菌颗粒在葡萄糖酸锌口服溶液+人工胃液中2种益生菌受到抑制,仅见枯草芽孢杆菌R-179菌落生长,屎肠球菌R-026被完全抑制。3个批号的枯草杆菌二联活菌颗粒在葡萄糖酸锌口服溶液+人工胃液组从小剂量组到大剂量组4 h内分别减少94.63%、95.06%、95.26%,94.94%、95.20%、95.64%,95.34%、95.88%、96.09%和95.66%、97.10%、97.21%,各组内结果无明显差异。葡萄糖酸锌口服溶液+人工胃液组的菌落数少于人工胃液组,表明葡萄糖酸锌口服溶液对枯草芽孢杆菌R-179有抑制作用。含菌落数为542~1 496 CFU的屎肠球菌R-026在葡萄糖酸锌口服溶液中的菌落数均小于加入量且4 h内渐少,表明葡萄糖酸锌口服溶液对屎肠球菌R-026有抑制作用。3个批号的枯草杆菌二联活菌颗粒在葡萄糖酸锌口服溶液+屎肠球菌R-026组从小剂量组到大剂量组4 h内菌落数分别减少57.38%、59.69%、73.23%,71.96%、71.72%、75.92%,77.49%、74.87%、79.09%和100.00%、90.57%、94.96%,各组内结果无明显差异。葡萄糖酸锌口服溶液对2种益生菌的抑制作用与其剂量呈正相关,这与Sumera等[13]报道的ZnO纳米粒子的抗菌活性与其浓度成正比的结果一致。ZnO纳米粒子的抗菌机制可能是ZnO溶液不稳定,分解产生H2O2的同时释放Zn2+发挥抗菌作用。葡萄糖酸锌口服溶液为锌制剂,其作用机制可能是溶液中的Zn2+对枯草芽孢杆菌R-179及屎肠球菌R-026有抑制作用。常见的益生菌制剂说明书中提及不与抗菌药同服,不与铋剂、鞣酸、药用炭、酊剂等并用[14],本实验提示枯草杆菌二联活菌颗粒不与葡萄糖酸锌口服溶液等含锌制剂同服。
3.3 枯草杆菌二联活菌颗粒在牛奶+人工胃液中2种益生菌的生长情况由实验结果可见,含菌落数为1.99×103~3.46×103 CFU的枯草杆菌二联活菌颗粒在牛奶+人工胃液中2种菌落生长良好,菌落数大于加入量且4 h内渐增。3个批号的枯草杆菌二联活菌颗粒在牛奶+人工胃液组4 h内分别增加15.32%、24.62%、21.32%,结果略有差异。牛奶能增强益生菌在抑菌介质中的活力[15-16],枯草杆菌二联活菌颗粒与牛奶同服是最佳给药方式。
致谢: 本文得到常州市第一人民医院史伟峰教授的悉心指导,在此表示感谢。
| [1] |
黄晓明. 赖氨葡锌、妈咪爱、思密达联合治疗急性腹泻的疗效观察[J]. 吉林医学, 2014, 35(3): 539. HUANG XM. Observation on the effect of combined treatment of compound lysine hydrochloride and zinc gluconate granules, Medilac-vita and smecta for acute diarrhoea[J]. Jilin Med J, 2014, 35(3): 539. |
| [2] |
庞铭兴. 妈咪爱在治疗小儿肺炎继发腹泻中的疗效观察[J]. 临床合理用药杂志, 2013, 6(3): 55. PANG MX. Medilac-vita in treating pediatric pneumonia secondary to the clinical curative effect of diarrhea[J]. Chin J Clin Rat Drug Use, 2013, 6(3): 55. DOI:10.3969/j.issn.1674-3296.2013.03.038 |
| [3] |
郝兰林. 小儿肠胃康颗粒联合妈咪爱治疗小儿消化不良性腹泻60例临床观察[J]. 现代诊断与治疗, 2013, 24(13): 2956. HAO LL. Pediatric gastrointestinal kang granules with Medilac-vita therapy pediatric digestive benign diarrhea in 60 cases of clinical observation[J]. Mod Diagn Treat, 2013, 24(13): 2956. DOI:10.3969/j.issn.1001-8174.2013.13.054 |
| [4] |
贾美云, 刘艳红. 妈咪爱联合腹部抚触治疗早产儿便秘临床疗效观察[J]. 中国医学工程, 2014, 22(3): 140. JIA MY, LIU YH. Medilac-vita combined abdominal touch premature constipation curative effect observation of clinical treatment[J]. China Med Eng, 2014, 22(3): 140. |
| [5] |
杨兴华, 王瑞丹, 焦思萌, 等. 微生态制剂妈咪爱对新生儿生理性黄疸消退效果的Meta分析[J]. 中国妇幼保健, 2016, 31(8): 1789. YANG XH, WANG RD, JIAO SM, et al. Meta analysis of probiotics Medilac-vita to the newborn physiologic jaundice faded effect[J]. Chin J Matern Child Health Care, 2016, 31(8): 1789. |
| [6] |
卢安庭. 黄疸茵陈颗粒联合妈咪爱、思密达治疗新生儿病理性黄疸的疗效观察[J]. 中国医药指南, 2014, 12(1): 177. LU AT. Jaundice wormwood particles with Medilac-vita of therapy curative effect observation of the newborn pathological jaundice[J]. Guide China Med, 2014, 12(1): 177. |
| [7] |
刘瑛, 王馨, 吴婕翎. 妈咪爱联合深度水解蛋白配方奶粉对牛奶蛋白过敏引起的特应性皮炎疗效观察[J]. 中国妇幼保健, 2013, 28(33): 5499. LIU Y, WANG X, WU JL. Medilac-vita joint depth protein hydrolysate formula atopic dermatitis caused by milk protein allergy curative effect observation[J]. Chin J Matern Child Health Care, 2013, 28(33): 5499. DOI:10.7620/zgfybj.j.issn.1001-4411.2013.33.33 |
| [8] |
叶冯, 朱德新, 袁丽. 妈咪爱防治早产儿喂养不耐受的临床观察[J]. 华夏医学, 2013, 26(6): 1074. YE F, ZHU DX, YUAN L. Clinical observation of Medilac-vita in preventing the feeding intolerance of premature infants[J]. Acta Med Sin, 2013, 26(6): 1074. |
| [9] |
TOMPKINS TA, HAGEN KE, WALLACE TD, et al. Asia's two strains of probiotic products safety assessment[J]. Can J Microbiol, 2008, 54(5): 391. DOI:10.1139/W08-022 |
| [10] |
王建超, 赵红梅. 活菌制剂"妈咪爱"中枯草杆菌的分离与应用[J]. 中兽医医药杂志, 2013, 32(4): 30. WANG JC, ZHAO HM. Isolation and identification of Bacillus subtilis in live bacteria preparation Medilac-vita[J]. J Tradit Chin Vet Med, 2013, 32(4): 30. DOI:10.3969/j.issn.1000-6354.2013.04.008 |
| [11] |
中华人民共和国药典2015年版.三部[S]. 2015: 46 ChP 2015. Vol Ⅲ[S]. 2015: 46 |
| [12] |
卢士玲, 李开雄, 徐幸莲, 等. 环境因素对屎肠球菌产苯乙胺和酪胺的影响[J]. 食品与发酵工业, 2012, 38(10): 57. LU SL, LI KX, XU XL, et al. The effects of environmental factors on phenylethylamine and tyramine -production by enterococcus faecium[J]. Food Ferment Ind, 2012, 38(10): 57. |
| [13] |
SIDDIQUE S, HUSSAIN Z, SHAHID S, et al. Preparation, characterization and antibacterial activity of ZnO nanoparticles on broad spectrum of microorganisms[J]. Acta Chim Sloven, 2013, 60(3): 660. |
| [14] |
张海英, 吕欣, 李玉珍. 微生态制剂的安全性及其临床应用[J]. 药物不良反应杂志, 2008, 10(5): 340. ZHANG HY, LÜ X, LI YZ. Safety and clinical use of microecological preparations[J]. Adverse Drug React J, 2008, 10(5): 340. DOI:10.3969/j.issn.1008-5734.2008.05.008 |
| [15] |
王岩, 冯万宇, 刘宇, 等. 保护剂在益生菌保藏过程中的应用[J]. 中国草食动物科学, 2015, 35(3): 52. WANG Y, FENG WY, LIU Y, et al. Application of protector in the preservation of probiotics[J]. China Herbiv Sci, 2015, 35(3): 52. DOI:10.3969/j.issn.2095-3887.2015.03.017 |
| [16] |
张健, 郑义, 朱金锦, 等. 冰淇淋中益生菌冷冻胁迫致菌体损伤机制研究进展[J]. 食品安全质量检测学报, 2015, 6(10): 3885. ZHANG J, ZHENG Y, ZHU JJ, et al. Advances of cell injury mechanism by freezing stress during processing of probiotic ice cream[J]. J Food Saf Qual, 2015, 6(10): 3885. |
 2019, Vol. 39
2019, Vol. 39 
