吸烟与健康研究是公共卫生研究热点, 而科学测量烟草暴露是研究吸烟与健康相关性的基础。尿液样本采集方便, 对受试者无侵害性, 常作为吸烟与健康研究的生物监测样品[1-3], 但志愿者排尿易受到饮食、喝水等差异的影响, 且尿液样本的浓度也会有明显的个体差异。一般来说, 普通志愿者24 h尿肌酐和尿酸排出量相对恒定, 因此, 可用肌酐和尿酸含量来校正不同志愿者尿液中分析物的浓度[4-5]。
尿液样品中肌酐和尿酸的检测方法主要有Jaffe法和酶解分光光度法[6]、HPLC法[7-8]、毛细管电泳法[9-10]、LC-MS/MS法[11]等, 其中HPLC法是最常用的测定方法。常规HPLC法测定尿液样品中的尿酸和肌酐常用反相色谱分离, 由于尿酸和肌酐极性大, 在反相色谱柱上保留时间短, 难以与样品中的杂质充分分离[7-8]。HPLC-MS法虽然可以通过选择离子采集实现高选择性, 但仪器成本和运行费用高, 且基质效应干扰大[11-12]。亲水作用色谱(HILIC)是近年来HPLC领域研究的热点之一, 非常适用于分离普通反相色谱柱上保留差的大极性化合物[13-15]。本文研究用超高效亲水作用色谱分离测定吸烟者尿液样品中的尿酸和肌酐, 在4.0 min内可达到完全分离, 并设计了与超高效液相色谱相适应的快速样品前处理方法, 大大简化了样品前处理操作, 用于实际尿液样品中尿酸和肌酐的测定, 取得了满意结果。
1 仪器与试剂ACQUITY UPLC超高效液相色谱系统(Waters, 包括四元泵、自动进样器、二极管阵列检测器和Empower 3色谱工作站); 电子天平(Mettler, AE200)。
肌酐和尿酸准品品(纯度≥98%), 购于Sigma公司; 其余所用试剂均为色谱纯。
吸烟和非吸烟志愿者尿液样本由昆明医科大学提供。所有志愿者年龄在25~55岁之间, 身体健康, 且在参加试验前均须签署知情同意书。
2 方法与结果 2.1 溶液的制备 2.1.1 混合标准品溶液准确称取肌酐和尿酸标准品各0.1 g, 用适量乙腈溶解并定容至100 mL量瓶中, 得到1.0 mg·mL-1的混合标准品储备液; 使用时分别取该溶液5.0、2.5、1.0、0.5、0.1、0.05、0.025 mL, 置10 mL量瓶中, 用乙腈定容至刻度并摇匀, 得质量浓度分别为500、250、100、50、10、5.0、2.5 μg·mL-1的标准工作液。
2.1.2 供试品溶液每位志愿者统一清晨空腹收集尿液中间部分15~30 mL, 并在采集后立即准确移取1.0 mL于萃取瓶内套管中(图 1-A), 用50%乙腈定容至10 mL。将萃取瓶的内套管卡在外套管的口部(图 1-C)并充分摇匀, 把萃取瓶的内套管向下压, 萃取溶液就通过滤筛板进入到内套管中, 并从内套管中的细弯管流出, 达到样品过滤的效果(图 1-D)。用色谱进样瓶从细弯管口收集萃取液, 弃去最初的2~3 mL, 收集1~1.5 mL, 进行UPLC分析。

|
A.外套管(outer casing)B.内套管(inner casing)C.萃取和过滤(extraction and filtration)D.取样(sampling) 图 1 样品萃取装置 Fig.1 Sample extraction devices |
色谱柱为Waters ACQUITY UPLC BEH HILIC液相色谱柱(50 mm×2.1 mm, 1.7 μm), 流动相为70%乙腈(内含0.1%磷酸二氢氨), 流速0.5 mL·min-1, 检测波长235 nm, 进样体积5.0 μL, 柱温30 ℃。
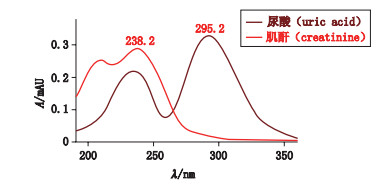
2.3 系统适应性试验尿酸和肌酐的标准品紫外光谱图见图 2。从图 2可以看出, 尿酸和肌酐在235 nm处均有较强的紫外吸收, 在235 nm波长处检测灵敏度能满足实际样品测定的要求, 且基线平稳, 因此本实验中选择在235 nm波长下检测。
|
图 2 尿酸和肌酐紫外光谱图 Fig.2 Ultraviolet spectrum of uric acid and creatinine |
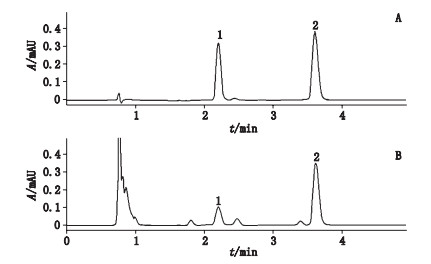
在选定实验条件下, 标准品和样品的色谱图见图 3。从图 3可看出, 实际样品中待测成分和干扰组分得到完全分离, 分离效果与文献[6-7]报道的反相液相色谱法相比有明显的改善, 而且每个样品色谱分离时间只需4.0 min, 与常规液相色谱相比显著缩短。
|
1.尿酸(uric acid)2.肌酐(creatinine) 图 3 标准品(A)和实际尿液样品(B)色谱图 Fig.3 Chromatograms of standard(A)and actual urine sample(B) |
取“2.1.1”项下的混合标准品溶液适量, 按“2.2”项上色谱条件进样分析, 以紫外检测器测得的峰面积(A, mV·S)对尿酸和肌酐的浓度(C, μg·mL-1)进行线性回归, 得到尿酸和肌酐的回归方程:
| $ \begin{array}{l} \mathit{A}{\rm{ = 4}}{\rm{.22}} \times {\rm{1}}{{\rm{0}}^{\rm{4}}}{\rm{ }}\mathit{C}{\rm{ + 162}}{\rm{.3}}\\ \mathit{A}{\rm{ = 3}}{\rm{.18}} \times {\rm{1}}{{\rm{0}}^{\rm{4}}}{\rm{ }}\mathit{C}{\rm{ - 213}}{\rm{.9}} \end{array} $ |
同时以仪器的信噪比S/N=3时测定检测下限(LOD), 尿酸为0.25 μg·mL-1, 肌酐为0.22 μg·mL-1; 以S/N=10时测定定量下限(LOQ), 尿酸为0.85 μg·mL-1, 肌酐为0.72 μg·mL-1。工作曲线相关系数均在0.999 5以上, 尿酸和肌酐的线性范围分别在2.5~500 μg·L-1和5~1 000 μg·L-1, 能满足实际尿液谱中尿酸和肌酐分析的要求。
2.4.2 精密度试验分别取同一批次的供试品溶液, 按“2.2”项下色谱条件连续进样7次, 测得尿酸和肌酐峰面积的RSD(n=7)分别为1.6%和1.8%, 表明仪器精密度良好。
2.4.3 稳定性试验精密量取同一批尿液, 按“2.1.2”项下方法制备供试品溶液。按“2.2”项下色谱条件分别于0、1、2、4、8、12、24 h进样5.0 μL, 测得24 h内尿酸和肌酐峰面积的RSD(n=7)分别为1.7%和1.9%, 表明供试品溶液在24 h内稳定。
2.4.4 重复性试验精密取同一批尿液6份, 按“2.1.2”项下方法制备供试品溶液, 按“2.2”项下色谱条件分别进样5.0 μL测定, 结果尿酸和肌酐的平均含量分别为231.8和965.2 μg·mL-1, RSD分别为1.8%和2.1%, 表明本方法重复性良好。
2.4.5 加样回收率试验依据“2.4.1”的线性范围, 在实际尿液样品中加入已知量的标准品储备液, 加入量设置高(尿酸4.0 mg, 肌酐16.0 mg)、中(尿酸2.0 mg, 肌酐8.0 mg)、低(尿酸1.0 mg, 肌酐4.0 mg)3个浓度水平, 每一浓度分别进样测定7次, 结果尿酸的日内RSD在2.5%~3.0%, 日间RSD在3.0%~3.4%;肌酐的日内RSD在2.3%~2.9%, 日间RSD在2.8%~3.2%, 表明本方法的精密度较好, 见表 1。
|
|
表 1 方法回收率实验 Tab.1 Methods recovery experiments(n=7) |
按建立的方法, 分析9名吸烟志愿者(每天抽吸:重度25~50支、中度15~25支、轻度5~15支)和3名不吸烟志愿者尿液中尿酸和肌酐含量, 并按“YY/T 1207-2013, 尿酸测定试剂盒(尿酸酶过氧化物酶偶联法)”[16]和“YY/T 1231-2014, 肌酐测定试剂(盒)(肌氨酸氧化酶法)”[17]报道的方法对分析结果进行验证, 结果见表 2。从表 2可看出, 本方法和对照方法的测定结果无显著差异(p > 0.05)。
|
|
表 2 样品分析结果(μg·mL-1) Tab.2 Sample analysis results(μg·mL-1) |
本研究针对尿酸和肌酐极性大, 尿液样品复杂, 在反相色谱柱上保留时间短, 样品中的杂质充分分离的难度大, HPLC-MS法仪器成本和运行费用高等现状, 采用自主设计的集萃取和过滤为一体的样品萃取瓶进行前处理、简化了样品前处理操作, 经超高效亲水作用色谱分离测定, 吸烟者尿液样品中的尿酸和肌酐在4.0 min内可完全分离, 缩短了分析检测时间。采用新建方法测定重度吸烟者、中度吸烟者、轻度吸烟者和不吸烟者尿液中的肌酐和尿酸, 测定结果与“YY/T 1207-2013, 尿酸测定试剂盒(尿酸酶过氧化物酶偶联法)”和“YY/T 1231-2014, 肌酐测定试剂(盒)(肌氨酸氧化酶法)”报道方法的测定结果无显著差异(p > 0.05), 为快速、准确测定烟草暴露的关键生物标记物提供了高通量检测方法。
| [1] |
何智慧, 罗嘉, 练文柳. 烟草与尿样中的代谢标记物[J]. 化学研究与应用, 2008, 20(7): 805. HE ZH, LUO J, LIAN WL. Tobacco and the metabolites in urine[J]. Chem Res Appl, 2008, 20(7): 805. DOI:10.3969/j.issn.1004-1656.2008.07.002 |
| [2] |
王珍, 章丽娜, 陈菲菲, 等. 吸烟者尿中致癌物质及其代谢产物的研究进展[J]. 卫生研究, 2008, 37(6): 757. WANG Z, ZHANG LN, CHEN FF, et al. Study advances on carcinogens and their metabolites in urine of smokers[J]. J Hygiene Res, 2008, 37(6): 757. DOI:10.3969/j.issn.1000-8020.2008.06.036 |
| [3] |
YUAN J, BUTLER L, STEPANOV L, et al. Urinary tobacco smokeconstituent biomarkers for assessing risk of lung cancer[J]. Cancer Res, 2014, 74(2): 401. DOI:10.1158/0008-5472.CAN-13-3178 |
| [4] |
程怀民, 吴碧娟. 肌酐和比重校正尿液中苯乙醛酸和苯乙醇酸浓度的探讨[J]. 海峡预防医学杂志, 2002, 8(3): 57. CHENG HM, WU BJ. Study on the concentration of phenylglyoxylic acid and phenylglycolic acid in urine by creatinine and ratio correction[J]. Strait J Prew Med, 2002, 8(3): 57. DOI:10.3969/j.issn.1007-2705.2002.03.028 |
| [5] |
徐紫君, 王丽. 肌酐校正前后尿中汞的含量比较[J]. 中国卫生检验杂志, 2010, 20(5): 1249. XU ZJ, WANG L. Comparison of urinary mercury content before and after creatinine correction[J]. Chin J Health Lab Technol, 2010, 20(5): 1249. |
| [6] |
陈冰, 陈繁. 2种参数设置的Jaffe法与酶法测定血清肌酐结果的比对研究[J]. 国际检验医学杂志, 2014, 35(7): 888. CHEN B, CHEN F. Comparison of Jaffe Kinetic method with two different parameter settings and enzymatic method for serum creatinine determination[J]. Int J Lab Med, 2014, 35(7): 888. DOI:10.3969/j.issn.1673-4130.2014.07.038 |
| [7] |
高新星, 郭娜, 李芳, 等. RP-HPLC法测定尿液中非蛋白氮代谢产物的含量[J]. 沈阳药科大学学报, 2008, 18(9): 724. GAO XX, GUO N, LI F, et al. Determination of non-protein nitrogen metabolites in urine by RP-HPLC[J]. J Shenyang Pharm Univ, 2008, 18(9): 724. |
| [8] |
马晓丽, 冉新建, 孟磊, 等. 反相高效液相色谱法同时测定血清、尿液中尿酸、肌酐的含量[J]. 分析试验室, 2014, 33(6): 638. MA XL, RAN XJ, MENG L, et al. Simultaneous determination of creatinine and uric acid in urine and serum samples by reversedphase high performance liquid chromatographic method[J]. Chin J Anal Lab, 2014, 33(6): 638. |
| [9] |
周小棉, 邹晓, 王毅. 超毛细管电泳同时测定尿中肌酐和尿酸[J]. 第一军医大学学报, 1999, 19(3): 261. ZHOU XM, ZOU X, WANG Y. Simultaneous determination of creatinine and uric acid in human urine by high-performance capillary electrophoresis[J]. Acad J First Med Coll PLA, 1999, 19(3): 261. DOI:10.3321/j.issn:1673-4254.1999.03.025 |
| [10] |
孔宇, 郑凝, 张智超, 等. 高效毛细管电泳测定尿液中非蛋白氮代谢产物[J]. 分析试验室, 2003, 22(6): 53. KONG Y, ZHENG N, ZHANG ZC, et al. Determination of several markers of diabetic nephropathy in human urine with capillary electrophoresis[J]. Chin J Anal Lab, 2003, 22(6): 53. DOI:10.3969/j.issn.1000-0720.2003.06.015 |
| [11] |
马青山, 王茜, 赵凯姝, 等. UPLC-MS/MS法测定高尿酸血症大鼠血清及尿液中的尿酸和肌酐[J]. 高等学校化学学报, 2013, 4(12): 2716. MA QS, WANG Q, ZHAO KZ, et al. UPLC-MS/MS method for determination of uric acid and creatinine in serum and urine of hyperuricemic mice[J]. Chem J Chin Univ, 2013, 4(12): 2716. DOI:10.7503/cjcu20130704 |
| [12] |
霍玉荣. 超高效液相色谱法在药物分析中的应用进展[J]. 首都食品与医药, 2016, 23(10): 25. HUO YR. Progress in the application of ultra performance liquid chromatography in drug analysis[J]. Capital Food Med, 2016, 23(10): 25. |
| [13] |
张禄阳, 田媛, 沈晓航, 等. 亲水作用色谱在体内药物定量分析中的应用进展[J]. 中国药科大学学报, 2012, 43(4): 379. ZHANG LY, TIAN Y, SHEN XH, et al. Hydrophilic interaction chromatography and its application in quantitative bioanalysis[J]. J China Pharm Univ, 2012, 43(4): 379. |
| [14] |
WANG Y, GU HX, LU X, et al. Development of hydrophilic interaction chromatographic hyphenated techniques and their applications[J]. Chin J Chromatogr, 2008, 26(6): 649. |
| [15] |
WENG ND. Bioanalytical liquid chromatography tandem mass spectrometry methods on underivatized silica columns with aqueous/organic mobile phases[J]. J Chroma B Anal Technol Biomed Life Sci, 2003, 796(2): 9. |
| [16] |
YY/T 1207-2013尿酸测定试剂盒(尿酸酶过氧化物酶偶联法)[S]. 2013 YY/T 1207-2013 Uric acid assay kit (Uricase-PAP method)[S]. 2013 |
| [17] |
YY/T 1231-2014肌酐测定试剂(盒)(肌氨酸氧化酶法)[S]. 2014 YY/T 1231-2014 Creatinine test reagent kit(Method of sarcosine oxidase)[S]. 2014 |
 2019, Vol. 39
2019, Vol. 39 
