2. 青岛理工大学, 青岛 266033
2. Qingdao University of Technology, Qingdao 266033, China
理化分析方法广泛应用于药品的检测,对该类方法的验证是确保检测方法科学可靠,并有效评价药品质量的重要手段。
近年来,随着科学技术的发展,对方法验证的统计分析要求将越来越高,特别是在2018年美国药典(USP)收载的“ < 1210 > 方法验证统计工具(statistical tools for procedure validation)”中[1],引入了一些新的理念和统计评价指标,对方法验证的实验设计、方法的变异度、容忍区间、预测区间等方法验证性能指标进行了规范。鉴于各个性能指标均涉及到复杂的统计计算公式,而这些统计公式的引入,使得应用目前简单的计算工具难以实现,成为完成方法验证的“拦路虎”。因此,迫切需要一款专业性强,操作简便,统计分析结果可靠的方法验证统计分析软件。
为解决专业技术人员在方法验证中对数据分析工具的需求,本课题组对近年来方法验证的新统计分析方法进行了广泛研究和比较,并结合自己的科研成果(见本专栏《定量理化分析类方法满足预期用途的判断标准探讨》一文),用Matlab编程语言编写了本款“理化方法验证统计分析软件(PCMV)”,以期满足专业技术人员在方法验证中对数据进行快速简便的统计分析需要。
1 软件设计的理论依据、编写要求和目标 1.1 理论依据“理化方法验证统计分析软件”以USP < 1210 > 和本课题组的研究成果(见本专栏中《定量理化分析方法满足预期用途的判断标准探讨》和《方法验证性能参数的获取和评价新方式探讨》)为基础编写完成。
1.2 软件设计目标既要满足现行版药典[2-3]和其他相关指南[4-5]中所有理化方法(如紫外法、液相色谱法、气相色谱法等)、含量测定类方法和有关物质限度分析方法的验证参数的计算需求,如准确度、精密度、线性、范围、检测下限和定量下限的统计计算;也要满足最新研究提出的要求,如增加方法验证性能指标的统计分析,方法的总变异度及方法使用时的预测区间、容忍区间、方法能力指数(MCI)和方法分级等。
1.3 软件的编写要求目前通用的统计分析软件很多,但进行方法验证的各种计算存在如下问题:(1)必须通过这些软件去实现,无法独立运行;(2)需通过深入编程才能实现这些参数的计算,这对分析专业的技术人员而言操作较困难;(3)通用统计软件占用硬盘空间。
本课题组用Matlab编程语言编写,完成后统一打包形成可独立运行,安装和操作简便,专为理化分析方法验证提供统计计算参数的软件。
2 软件界面设计及其功能为减少或避免对方法验证中参数统计分析的繁杂计算,本软件在编程过程中,将所有的复杂计算均放置在后台运行,仅将运算时需临时设置的参数放置在软件的面板上,以便根据实际需要进行调整。具体如下。
打开软件后,出现图 1的软件初始界面。

|
图 1 软件的初始界面 Fig.1 Initial interface of the software |
界面的左侧是数据调入后,出现的原始数据显示窗口;右侧是软件在应用时需要使用的面板,各图标功能如下:
2.1 数据调入按键完成实验后,将实验结果以文本或Excel方式存储(目前该软件仅支持该2种数据类型),使用本软件时,有2个按键可方便地调入数据:“调入Excel第1页”和“调入Text数据”。
“调入Excel[第1页]”按键:可将以Excel格式存储的数据调入本软件(本软件目前只能识别以Microsoft Excel 97-2003及更低版本存储的数据文件)。将鼠标放置在该按键上后,点击鼠标右键,可以从不同的数据表页中调取文件。
“调入Text”按键:可将以文本文件存储的数据调入本软件。
需要注意的是:数据最好在“英文”输入法状态输入。
2.2 方法验证的目的按键本软件设置2个按键:“检测下限”和“含量测定”,以分别适于含量测定类方法和有关物质定量测定分析方法的结果输出。
当所收集的数据按照所规定的实验设计和排列方式调入后,软件一般会自动识别,并自动在后台进行下一步所需输出参数的运算。但某些特殊情况,需要人工选择。
2.3 统计运算中必需参数及设置Alpha(α):设置显著性水平以计算所需置信水平下的统计区间等,一般α=0.05;当有一定要求时,可在右侧的框中输入相应的值后,按“回车键”。
Beta(β):设置把握度水平(1-β),一般β可设置0.05、0.10或0.20。该参数为计算方法的检测下限(LOD)所用。输入相应的值后,按“回车键”。
样本包含量(P):该值是在计算容忍区间时,对估计总体中拟包含样本量的设定。一般可设置为0.80、0.90或0.95。在方法建立的初期,可选用0.90或0.80。输入相应的值后,按“回车键”。
相对标示量(tau%):是“含量测定”实验中,相对标示含量的值,一般为100%。当原始数据采用正态化转换后,这时的标示量值应选0值。输入相应的值后,按“回车键”。
相对质量标准上下限(USL%、LSL%):为相对质量标准的上下限。当所测产品质量标准为98.0%~102.0%时,应在框中输入“2”和“-2”,当所测产品质量标准为90.0%~110.0%时,应在框中输入“10”和“-10”。需记住的是,每次输入相应的值后,必须按“回车键”。
2.4 结果显示导入数据后,将在显示面板的下方出现2个新的窗口,即“计算结果保留小数点位数”和“原始数据”。如图 2所示。
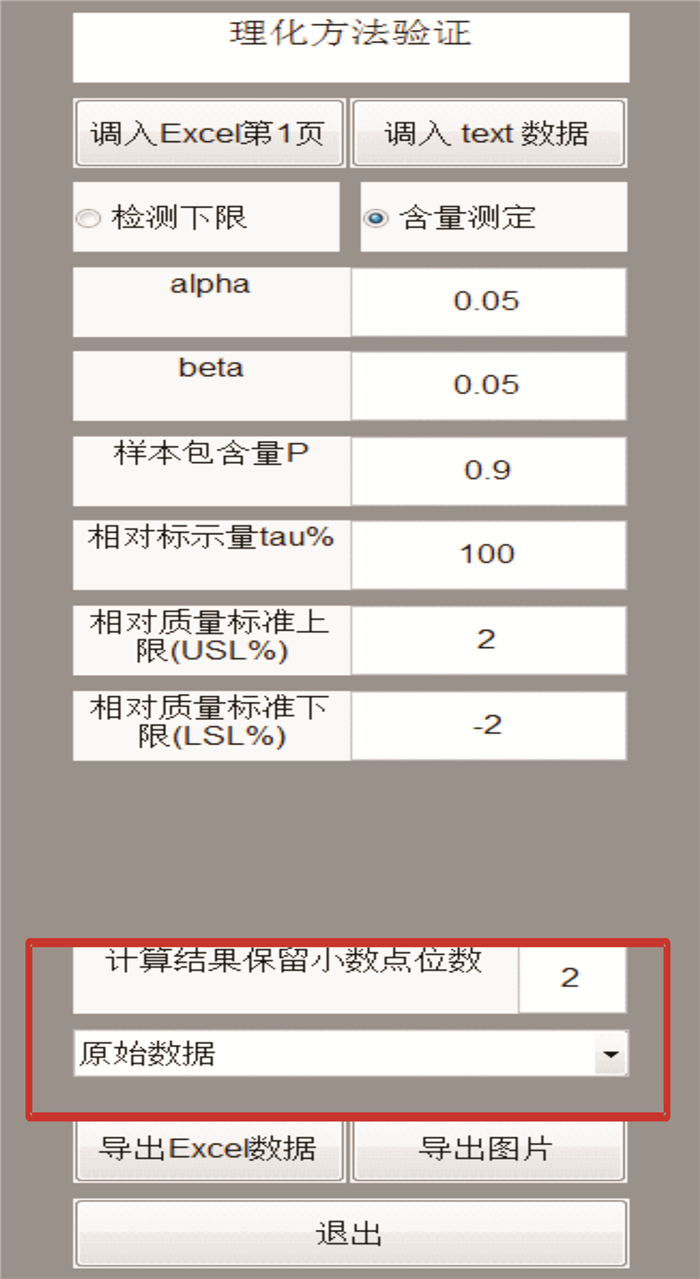
|
图 2 操作面板(红色框内为调入数据后的新增功能窗口) Fig.2 Operating panal(the new function window appeared after data imported is shown in the red area) |
要获得某一方法验证的各项性能参数结果,可点击“原始数据”窗口右侧的下拉箭头;如果输出的结果中需要根据实际调整小数点位数,可在“计算结果保留小数点位数”的右侧输入相应值,并按“回车键”。
2.5 结果导出键验证结果的导出采用面板下方(图 2)的“导出Excel数据”和“导出图片”2个功能键。使用Excel导出的方式,可以对结果进行编辑;使用图片导出的方式,可保证结果的保真性。
2.6 软件退出键面板的最下方是“退出”键,点击即可退出;也可点击软件最右上方的“×”号退出。
3 检测下限模块中验证参数的设计和计算 3.1 参数设计和计算原理线性分析:以USP < 1210 > 的新理念和计算方法为基础进行汇编,给出了除线性函数外的更多参数,如回归线标准误,同时将相关系数用“回归线决定系数(R2)”替代。本软件输出的“直线斜率(a)”、“直线截距(b)”和“回归线标准误(RSME)”3个参数,不仅可给出本次实验更直观的线性描述,同时可对今后长期评价该方法发挥作用,如使用控制图评价不同实验人员的操作误差,采用稳定的实验结果找出该实验中线性回归参数的等效区间等。
范围分析:可根据预期要求,找出满足准确度、精密度和线性需求的范围。
LOD计算:以USP < 1210 > 的计算方式,给出回归线95%预测区间的计算方式。由于进行线性回归实验时,一般每个浓度下有2~3个重复数据,故本软件既给出使用报告值计算的LOD,同时也给出了使用中间精密度求得的LOD结果供参考,可更好地了解LOD的变动范围。
LOQ计算:本软件没有单独LOQ的计算。根据USP < 1210 > ,新LOD的计算引入了统计Ⅰ型错误和Ⅱ型错误的理念,已经具有定量作用,故在实际应用中,LOQ选用不小于本法计算的LOD值即可。
3.2 实验设计和数据的输入格式LOD和线性的计算,需要对验证试验的浓度范围进行合理设计。一般应考虑LOD周围浓度(最低浓度)和方法所对应的产品质量标准限度2个指标。然后在其中设置不少于5个浓度。
实验所获结果应首先将数据的浓度排在左侧一列,然后将不同浓度的测定结果放在右侧一列(每个浓度仅有1个结果)或多列(每个浓度有多个检测结果)。当每个浓度有多个检测结果时,软件将自动计算出各浓度下的报告值。
3.3 实例演示下面以某一理化方法的线性和LOD计算的实例,对软件进行演示。
3.3.1 检测结果的存储将检测数据按照表 1的方式以Excel或文本形式存档。
|
|
表 1 线性回归和LOD计算所需数据存放方式 Tab.1 Data storage format required for linear regression and LOD calculations |
打开软件,根据实验要求对软件右侧控制面板中的Alpha值和Beta值进行设置。这里均选用0.05。
3.3.3 数据调入点击软件的相应数据调入按钮,调入该文件。见图 3。

|
图 3 检测限模块中调入数据的界面 Fig.3 Interface for loaded data in the detection limit module |
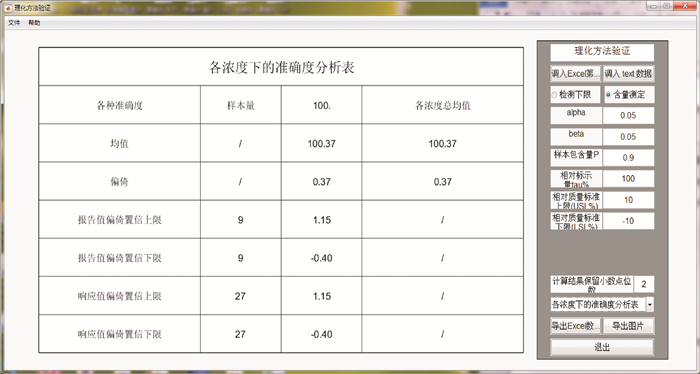
从图 3所示,软件导入数据后,在后台马上进行了各项计算,并首先显示出原始数据。该界面中,还给出了各浓度下的报告值和RSD;可以看到,浓度越低时,检测结果的变异越大,在0.01浓度下,同浓度内RSD达到9.67%。
3.3.4 分析结果的显示点击控制面板中“原始数据”框右侧的下拉箭头,可分别获得该数据结果的“回归线图”(图 4)、“报告值计算的LOD”(图 5)和“中间精密度计算的LOD”(图 6)。
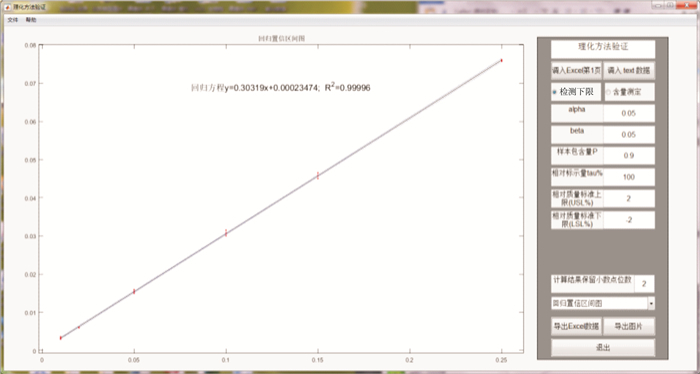
|
图 4 检测限模块中输出的回归线图形 Fig.4 Output of the regression line graph in the LOD module |
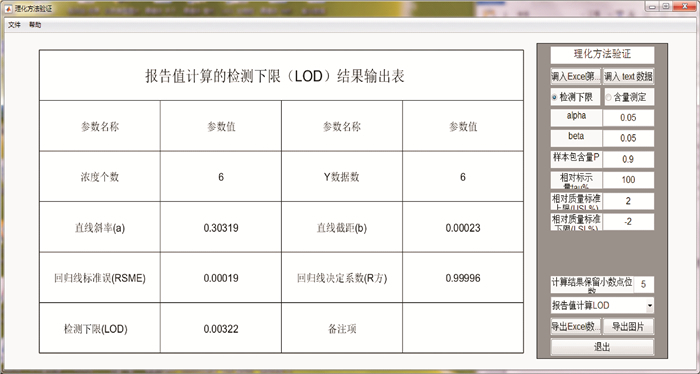
|
图 5 检测限模块中输出的报告值计算回归结果和LOD值 Fig.5 Output of the results of regression and LOD calculated by using the reportable values in the LOD module |

|
图 6 检测限模块中输出的中间精密度计算回归结果和LOD值 Fig.6 Output of the results of regression and LOD calculated by using the intermediate precision value in the LOD module |
点击控制面板上的“导出图片”按键,可将上述结果分别以图片的形式存储(图 3~6)。点击“导出Excel数据”,可将上述结果存储到单独的Excel文件中,见图 7。

|
图 7 使用Excel存贮的验证参数导出文件 Fig.7 Exported files stored by Excel format of the analysis validation parameters |
本模块中对方法验证的“准确度”及“准确度置信区间”、“精密度”(重复性精密度和中间精密度/再现性精密度)及其相应的“置信上限”、方法变异的“容忍区间”和“预测区间”以USP < 1210 > 的新理念和计算方法为基础编写。
对方法验证的“方法总变异度”、“方法能力指数”、“方法能力分级”和该方法能力指数对应的OOS发生概率(方法的误判率),以本专栏中《定量理化分析方法满足预期用途的判断标准探讨》一文为基础编写。
为在输出上更清晰和精准地描述这些验证参数,本软件设置了不同浓度下的准确度结果表、精密度结果表和方法能力评价表;同时也用图形的方式输出不同浓度下容忍区间和预测区间结果汇总图,以便于直观地分析和判断。
关于含量测定类方法的“范围”,只需根据上述输出结果进行判断即可获得。
有关这些输出参数的详细含义,请参考本专栏论文和所附文献。
4.2 实验设计和数据的输入格式要求含量测定类方法的验证,一般选用影响方法的关键因素,如人员和仪器,采用正交析因设计或嵌套设计的方法进行验证设计,此外,也要考虑验证性能参数计算时的样本量(详见本专栏《方法验证性能参数的获取和评价新方式探讨》一文)。
在浓度设置上,一般对质量标准在90.0%~ 110.0%范围的产品,考虑80.0%~120.0%的范围即可;但当该方法用于溶出度/释放度的分析时,应该考虑更广泛的范围,如1.0%或10.0%~120.0%等。关于浓度数量,一般以不少于5个浓度点为宜,便于找出合适的方法适用范围。USP < 1210 > 中的实例使用3个浓度(50.0%、100.0%和150.0%),采用该方式时,若精密度、准确度或线性不能满足要求,无法弥补,需要重新实验。
关于实验数据存储方式,有以下几种情况。
USP < 1210 > 提供的含量测定类实验方法实例,设计了3个浓度(50.0%、100.0%和150.0%),假定选择3个人分别对这3个浓度进行检测,最后以绝对含量的报告值形式给出每次实验的结果,共9个结果。这时,要使用本软件进行计算,需将所有浓度看作1.0或100.0%,然后以表 2方式进行排列。
|
|
表 2 含量测定类方法不同浓度仅1个报告值所需的数据存储方式 Tab.2 Data storage format required for analytical assay with only one reportable value under different concentrations |
若该类实验中,实验者直接给出每个浓度重复3次的数据,且以百分比换算计数,则数据最终以表 3方式存储。
|
|
表 3 含量测定类方法有极少浓度,每个浓度仅3个重复检测结果的存储方式 Tab.3 Data storage format required for analytical assay with only 3 values/concentrations and few sample size |
使用上述2种方式,若方法满足预期要求的准确度和精密度等要求,则证明该方法在50.0%~150.0%的浓度范围是合格的;但若不能满足要求,就需要重新调整浓度范围进行实验。
为了保证方法验证一次成功,最好根据实际需要采用至少5个浓度,并且每个浓度以达到样本量计算需要的设计进行实验。这种实验方案虽然增大了验证的工作量,但具有广泛适应性和结论可靠性。
假定要对1个产品检测方法进行验证,采用了2个检验人员,用2台仪器进行实验,每人在每台仪器上对所设浓度进行2次独立实验,每个独立实验重复3次测量。则所获结果以表 4方式进行记录。
|
|
表 4 含量测定类方法不同浓度下均有8次独立实验,3次重复结果的存储方式 Tab.4 Data storage format required for analytical assay with 8 independent tests and 3 result values/concentrations |
将上述不同检测设计得到的数据以Excel(97-2003文件格式)或文本形式存档,以供分析。
4.3 实例演示 4.3.1 软件启动和设置打开软件,根据实验要求对软件右侧控制面板中相应的参数进行设置:
“Alpha”:一般默认选0.05,也可选择0.10。
“Beta”在含量测定类方法验证的计算中不需要,可不设置(默认0.05)。
“样本包含量”:指在计算容忍区间时,对总体中包含的样本比例的设定,一般0.90;但在方法评价的初期,也可选择0.80。
“相对标示量(tau%)”:一般选择100,当数据进行了正态化转换后,应输入0,但本软件不认可,可输入0.000 01替代0值进行计算。
“相对质量标准上限(USL%)”和“相对质量标准下限(LSL%)”:当质量标准为98.0%~102.0%时,分别输入2和-2;当质量标准为90.0%~110.0%时,分别输入10和-10。
注:如果已经调入了数据,则每次在界面上调整参数后,需按回车键。
4.3.2 数据调入操作同“3.3.3”项。下面演示以调入表 3为例的结果输出。
4.3.3 分析结果的显示点击控制面板中“原始数据”(图 8)框右侧的下拉箭头,可分别获得该数据结果的“各浓度下的精密度分析表”(图 9)、“各浓度下的准确度分析表”(图 10)、“使用报告值计算的方法能力评价表”(图 11)、各浓度下的“容忍区间图”(图 12)和“预测区间图”(图 13)。

|
图 8 含量测定模块中调入数据的界面 Fig.8 The interface of the analytical assay module after data imported |
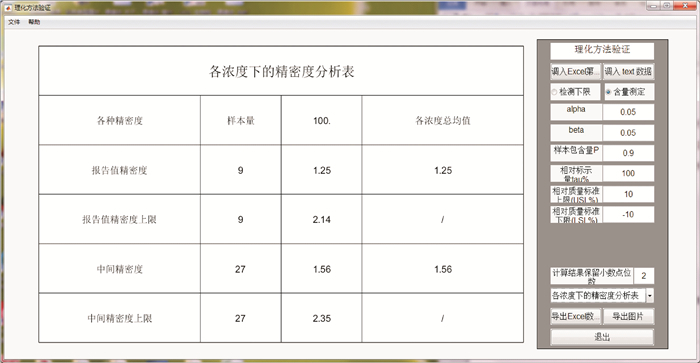
|
图 9 浓度区间内的精密度分析表 Fig.9 Precision analysis table in the experiment concentration interval |
|
图 10 浓度区间下的准确度分析表 Fig.10 Accuracy analysis table in the experiment concentration interval |
|
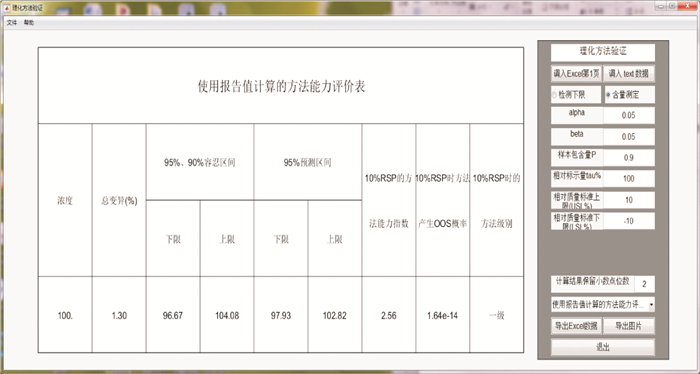
图 11 浓度区间下报告值计算的方法能力评价表 Fig.11 Evalution table for method capability calculated by the reportable value in the experiment concentration interval |
|
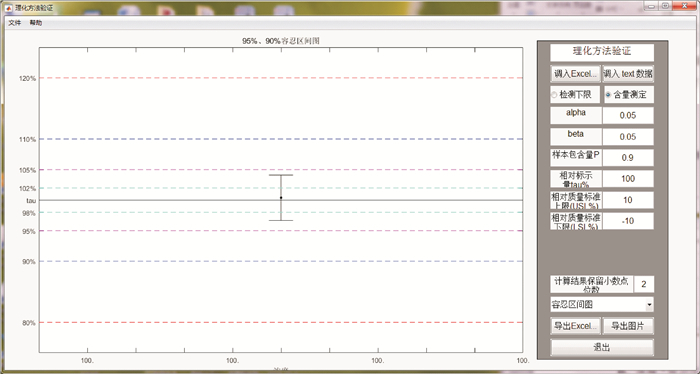
图 12 验证浓度区间下方法的95%/90%变异容忍区间 Fig.12 The 95%95% tolerance interval of the method variability in the experiment concentration interval |
|
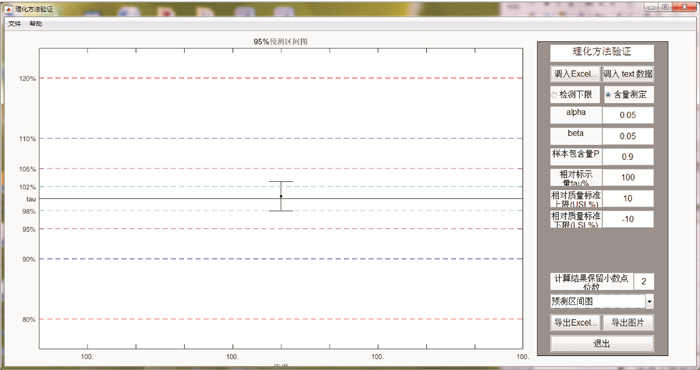
图 13 验证浓度区间下方法的95%变异预测区间 Fig.13 The 95% predictive interval of the method variability in the experiment concentration interval |
同“3.3.5”项。
5 讨论 5.1 关于软件的设计标准及应用范围本软件的开发,完全按照USP < 1210 > 和本专栏《定量理化分析类方法满足预期用途的判断标准探讨》一文中的公式,在Matlab中编辑而成,为国内首款用于方法验证的专业统计分析软件,融合了目前国内外以及本课题组研究的最新成果,在方法验证的实际工作中,为技术人员便捷地提供了比目前药典/指南要求更多、描述更详细的评价指标,如方法准确度(偏倚)的置信区间、方法总变异、方法变异的容忍区间和预测区间、方法能力指数和方法的级别等,对LOD的计算方式也改为回归线95%预测区间计算法。本软件不仅解决了目前方法验证研究人员的数据分析问题,同时也为监管人员判断方法是否满足需求提供了直观的判断依据,不仅适于药品领域的技术人员,同时也适合食品、化妆品和医疗器械等领域。
5.2 软件运算的可靠性本软件利用USP < 1210 > 提供的法定实例数据进行了验证,并与JMP软件的运行结果做了对比,所得结果与USP提供的分析结果完全一致;同时还采用了多个不同实例,用JMP软件与本软件的输出结果进行对比验证,进一步佐证了所编程序的可靠性。
5.3 本软件的优点和不足 5.3.1 优点(1) 操作简单。只需将验证结果按照预定要求,以Excel或文本格式存放。读取后,所有统计运算都在后台运行,并可即时显示出所需参数的结果;(2)统计结果准确可靠。经多种实例验证,并与标准实例的结果进行了比较。(3)独立运行。本软件虽然使用Matlab编程语言开发,但它可以独立运行,不需要其他商业软件支撑。(4)安装简单。只需要Windows7以上64位系统,3G以上自由空间即可。(5)适用范围广。适于从事理化方法验证的技术人员使用,也适于从事软件开发人员的程序验证。
5.3.2 不足(1) 本软件目前仅适用于含量测定类和有关物质的限度分析方法的验证,对于溶出度/释放度(Ⅲ)类方法,还有待后续进行研发;(2)由于专属性指标的特殊性,本软件对此也无法提供支持;(3)本软件的输出格式还有待优化。
| [1] |
USP 41-NF 36[S]. 2018: 7622(<1210> Statistical Tools for Procedure Validation)
|
| [2] |
中华人民共和国药典2015年版.四部[S]. 2015: 374(9101) ChP 2015. Vol Ⅳ[S]. 2015: 374(9101) |
| [3] |
USP 41-NF 36[S]. 2018: 7665(<1225> Validation of compendial Procedures)
|
| [4] |
ICH Q2(R1). Validation of Analytical Procedures Text and Methodology[S]. 2005
|
| [5] |
OMCL Network of the Council of Europe. PA/PH/OMCL(13)822R, Validation_of_analytical_procedures[S].(2015)[2018-12-9]. https://www.edqm.eu/en/quality-management-guidelines-86.html
|
 2019, Vol. 39
2019, Vol. 39 
