2. 沃特世科技有限公司, 上海 201206
2. Waters Corporation, Shanghai 201206, China
目前,农药在中药种植中的应用十分广泛,据报道,我国中药材栽培品种已有400余种[1],所涉及的农药达上百种。农药的使用在防治药用植物病虫害的同时,不可避免地带来了农药残留问题。农药残留是中药材出口检测的重要指标[2],为各国政府监管的重点,其检测技术也成为研究的焦点。
面对中药中上百种农药的广泛使用,建立简便、高效的农药多残留快速筛查方法迫在眉睫;而且,由于农药的非法滥用,适当扩大检测范围也是很有必要的。简单有效的前处理技术和高灵敏度的农药多残留检测技术是农药多残留检测的发展趋势。近年来,发展较快的前处理方法主要有基质固相分散萃取、在线凝胶渗透色谱、QuEChERS法等,其中,QuEChERS法因具有样品通量高、快速、安全、简便及成本低等优点,广泛用于农药检测的前处理[3]。现阶段,常用的农药多残留检测方法主要集中在GC、GC-MS、GC-MS/MS、LC-MS/MS等[4-11],其中GC、GC-MS检出限偏高,定性能力不足;LC-MS/MS由于各仪器供应商离子源以及离子传输等硬件设计上的差异无法形成较统一的农药谱库,而且上述方法都需要对照品随行进样,对于多种农药的筛查需要配制大量农药对照品,建立多个检测方法,样品也需多次测定,耗时费力[11]。总之,上述方法对农药多残留筛查能力有限、检验耗时费力,而近些年发展的高分辨质谱技术因其在质量精度、全质量数据采集、数据可溯源性和数据库检索等方面的优势,越来越多地受到农药多残留检测工作者的青睐[12-16]。本课题组同时利用LC-Qtof和APGC-Qtof结合数据库进行了研究,初步建立了中药中农药多残留快速筛查平台,既能扩大农药筛查的范围,又能使后续定量分析更加有针对性,避免多种农药对照品的购买和测定,既能节省资源,又可提高检验效率和质量。本篇仅介绍采用APGC-QTof初步建立中药材中71种常见农药的快速筛查法。
1 仪器与试药 1.1 仪器分析天平:感量1 mg和0.01 g各1台;气相色谱-高分辨质谱仪:Agilent 7890A气相色谱(安捷伦公司)配置APGC电离源(Waters公司),Xevo G2-XS QTOF-MS高分辨质谱系统(Waters公司);药材粉碎机;离心机(Effendorf公司):转速不低于5 000 r·min-1;数据处理系统为UNIFI科学信息处理软件(Waters公司)。
1.2 试药农药标准物质,纯度大于98%,分别购于国家标准物质研究中心、农业部环境保护监测所、CHEM SERVICE、SIGMA、Ehrenstorfer、Chem service、xStsndard、北京振翔有限公司BePure;Waters DisQuE样品前处理包[内含1.5 g乙酸钠,6 g硫酸镁(Waters部件号为186006812)2 mL净化管:内含150 mg硫酸镁,25 mg PSA,25 mg C18,7 mg GCB(Waters部件号为186008071)]购于Waters公司;乙腈、丙酮均为色谱纯,购于Fisher Chemical。
1.3 药材市售西洋参、金银花、枸杞子、大枣和白花蛇舌草,经课题组前期实验验证残留农药品种较少的样品。
2 实验方法 2.1 溶液的制备 2.1.1 农药单标对照品储备液精密称取表 1中各农药10 mg,置100 mL量瓶中,分别加丙酮溶解并稀释至刻度,作为单标对照品储备溶液(100 μg·mL-1),于-20℃冰箱中保存,有效期一年。
2.1.2 混合对照品储备液分别精密量取2.1.1项中各农药单标对照品储备液1 mL,置100 mL量瓶中,用丙酮稀释至刻度,摇匀,作为混合对照品储备溶液(1 μg·mL-1)。
2.1.3 供试品溶液准确称取样品1 g,置50 mL聚四氟乙烯的离心管中,加水10 mL,涡旋30 s,静置30 min,精密加入1%乙酸乙腈溶液10 mL,加入DisQuE试剂袋(内含1.5 g乙酸钠,6 g硫酸镁),剧烈振摇1 min,离心5 min(离心速度≥4 000 r·min-1),上清液待净化。
精密吸取待净化的上清液1 mL和甲苯溶液0.2 mL,置于2 mL净化小管(内含150 mg硫酸镁,25 mg PSA,25 mg C18,7 mg GCB)中,涡旋30 s使充分混匀,离心5 min(离心速度≥10 000 r·min-1),取上清液置于2 mL进样小瓶,即得。
2.2 实验条件 2.2.1 气相色谱条件设置采用气相系统Agilent 7890 A进行实验,配置大气压气相色谱电离源。色谱柱:DB-5MS UI(30 m×0.25 mm×0.25 μm);载气:He 2 mL·min-1;进样口温度:280 ℃;进样类型:不分流;进样量:1 μL;程序升温:初始为100 ℃,保持1 min,然后以15 ℃·min-1升至220 ℃,再以5 ℃·min-1升至280 ℃,保持10 min;总运行时间:26 min;APGC接口补充气体:N2 300 mL·min-1;传输线温度:300 ℃。
2.2.2 MS条件设置采用Xevo G2 XS QTOF型号的质谱仪器,离子化模式:API+;电晕针电压:2.5 kV;锥孔气流速:200 L·h-1;辅助气流速:200 L·h-1;源温度:150 ℃;采集模式:MSE;低碰撞能量:4 eV;高碰撞能量:10~45 eV;采集质量范围:50~1 200。
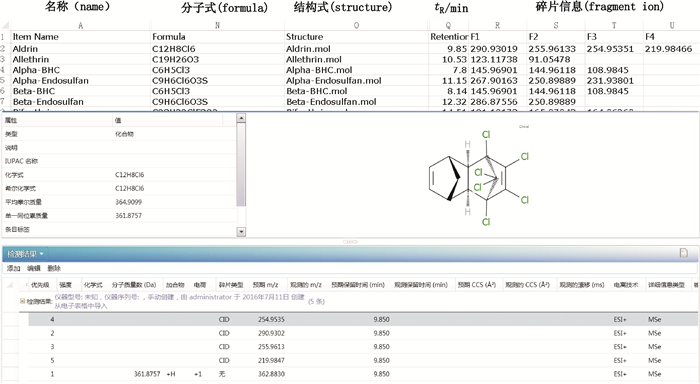
3 实验结果 3.1 数据库建立混合对照品溶液用丙酮稀释至约100 μg·L-1,注入气相色谱APGC/Xevo G2-XS QTof,采集模式为MSE。用UNIFI筛查软件处理数据,并建立筛查数据库,其中包含每个农药的名称、CAS号、化学式、结构式、保留时间、碎片离子的精确质量等信息。详细内容见图 1、表 1。
|
图 1 UNIFI数据库内容 Figure 1 The UNIFI screening database |
|
|
表 1 71种农药化合物的保留时间及碎片离子信息 Table 1 Retention time and fragment ion information of 71 pesticide compounds |
欧盟农药残留分析质量控制程序(SANCO/11945/2015)中规定:应用高分辨质谱进行筛查分析时,要求要有2对离子且质量偏差小于等于5×10-6时才能判定是同一化合物[17]。美国食品药品监督管理局(USFDA)关于残留分析判定的相关文件也有类似的规定,要求保留时间要小于0.2 min,同时有2对离子且一级质谱质量偏差不得大于5×10-6,二级质谱不得大于10×10-6,才能判定是同一化合物[18]。所以参考“欧盟农药残留分析质量控制程序(SANCO/11945/2015)”和“美国食品药品监督管理局(USFDA)”的相关推荐原则,制定筛查结果的判定原则为:①保留时间窗口≤0.2 min;②准分子离子峰的质量偏差≤5×10-6;③至少找到1个碎片离子且碎片离子的质量偏差≤5×10-6 m。
3.3 方法学验证 3.3.1 假阳性率假阳性率是数据分析软件经设定的参数处理后所报告的分析结果,但经人为判断是错误的或验证实验无法证实的结果。通常采用空白样品(n=5)验证方法的假阳性率,一般要求假阳性率≤10%或者≤5%,且假阳性率越低越好。
取中药材样品1 g,5种中药材各5份,按样品前处理方法制备。计算假阳性结果的数量和比率。假阳性率=假阳性结果的数量/农药总数(71),结果见表 2。
|
|
表 2 假阳性率实验结果 Table 2 The results of the false positive test |
假阴性率是针对单个目标分析物在给定浓度下检出的概率,如在95%的样品中可测得目标物(即5%的假阴性率是可以接受的)。一般采用空白样品加标试验(3个水平,n=5)验证方法的假阴性率,要求假阴性率≤5%。
取中药材样品1 g,分3个水平,5种中药材各5份,分别加入1 μg·mL-1混合对照品溶液1 mL、0.1 mL和0.1 μg·mL混合对照品溶液0.1 mL,作为高、中、低浓度的加标样品,按“2.1.3”项下方法制备,计算检出的农药数。结果假阴性率均 < 5%。三水平添加试验-检出的农药数量见表 3。
|
|
表 3 三水平添加试验-检出的农药数量(n=5) Table 3 The false negative results-the amount of pesticides detected |
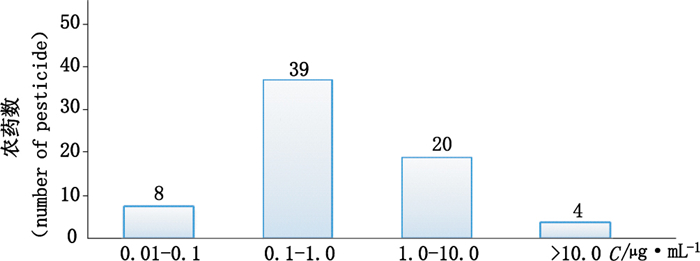
以低浓度加标样品(枸杞)计算信噪比和方法检测下限。加入量=0.1 μg·mL-1的混合标准品溶液×0.1 mL;检测下限=加入量(μg)×3/[信噪比×样品称样量(g)]测定71种农药在枸杞子基质中的检测下限结果见图 2。
|
图 2 71种农药在枸杞子基质中的检测下限结果 Figure 2 The LODs of the 71 pesticides in the fruit of Lycii Fructus |
根据以上方法,对5批实际样品进行测定,验证筛选的准确性。结果见表 4。
|
|
表 4 5批样品的农药残留筛查结果 Table 4 The screening results of pesticide align="right"esidues in the 5 batches of samples |
区别于LC-QTof开发的筛查方法,本平台着重研究LC-QTof方法中不易出峰或灵敏度低的易气化农药的筛查。另外,作为初步研究,参考国内禁限用农药、大量生产使用的农药以及中毒或高毒农药品种,针对所选择中药基质中常用农药类型,科学合理地确立了71种农药作为检测指标。
5.2 样品及前处理方法的选择中药基质比较复杂,QuEChERS仍是目前认可度较高的农药提取净化方法。本研究利用Waters样品前处理方法包,采用简化的QuEChERS法进行样品前处理,提取净化效率高,净化小管中加入适量甲苯,可以提高含平面苯环结构农药的回收率。另外,根据中药材基质性质进行合理分类,选择了西洋参,枸杞,金银花,大枣和白花蛇舌草等常用中药品种,也多为药食两用的品种,分别代表花、果实、种子、根、全草等不同药用部位和多糖、挥发油、黄酮、有机酸、色素等不同基质干扰情况,完成系统方法学研究。所建方法经验证,符合农药多残留筛查要求。
5.3 APCI电离源及数据采集模式的选择本研究通过APGC电离源,实现了气相色谱系统与Xevo G2-XS QTof高分辨质谱系统的联用。APGC电离源是1种软电离的方式,相比EI电离源,更易获得母离子的信息和专属性强的碎片信息,因而具有更高的灵敏度和选择性。相比CI电离源,APGC不需要真空条件,具有更好的重现性和稳定性。而且实验采用新型的MSE数据采集模式,可同时获得整个色谱分离阶段的每个可检测峰中的全部母离子和碎片离子的精确质量信息,简化了成分鉴定的过程,缩短了数据采集时间,也可用于后续数据溯源,扩大筛查范围或未知物鉴定。
5.4 数据库的建立本平台建立了包含71种农药的UNIFI数据库,基于高分辨质谱技术,通过保留时间、精确分子量及碎片信息的匹配,实现了不需标准品对照即可完成对不同中药基质中71种适合气相分析农药的筛查。避免了对照品溶液的重复配制,节省了对照品的处理和测定时间,达到了快速筛查的目的。待样品有阳性检出后,再做进一步的确证或含量测定。
5.5 方法学验证内容的选择相比于1个定量分析的方法学验证,筛查方法的验证要求更为严格。因为证实1个化合物存在与否,远比测定1个目标物的量更困难。本文方法学验证的内容主要参考欧盟和美国FDA的相关推荐原则。作为农药多残留定性筛查方法,采用检测灵敏度、假阳性和假阴性的方式来评价,更为科学、准确、可靠。
6 结语本研究应用APGC/Xevo G2-XS QTof提供的高灵敏度及高质量精度的分析技术,结合UNIFI农药筛查数据库,形成软硬件相结合,具有自动筛查识别功能的检测快速筛查系统,建立了中药材中71种适合气相分离农药的多残留筛查方法,此方法快速易操作,专属性好,灵敏度高。而且通过快速筛查得到农药指标后,也可通过更为准确的方式进行后续定量分析,使得检测更加有针对性,避免多种农药对照品的购买和测定,加快了检测速度,更加环保高效。但是本次初步探索,只针对中药材中常用风险较高的农药,作为完整全面的筛查方法,尚需继续增加农药检测指标,填充筛查数据库,并不断积累其他中药基质的研究数据,完善筛查方法。
| [1] |
邢振杰. 中药材种植业的演变与发展[J]. 中国现代中药, 2011, 13(5): 53. XING ZJ. The evolution and development of Chinese herbal medicines[J]. Mod Chin Med, 2011, 13(5): 53. DOI:10.3969/j.issn.1673-4890.2011.05.018 |
| [2] |
刘东静, 薛健, 吴晓波. 中药中农药多残留气质检测方法研究进展[J]. 中国中药杂志, 2011, 36(4): 396. LIU DJ, XUE J, WU XB. Research progress on the detection method of pesticide residues in traditional Chinese medicines[J]. China J Chin Mater Med, 2011, 36(4): 396. |
| [3] |
黄武, 章晶晶, 刘辉. QuEChERS结合在线凝胶渗透色谱-气相色谱-质谱联用法快速检测水产品中农药残留[J]. 食品安全质量检测学报, 2016, 7(2): 747. HUANG W, ZHANG JJ, LIU H, et al. Rapid determination of pesticide residues in aquatic products by QuEChERS and on-line gel permeation chromatography-gas chromatography-mass spectrometry[J]. J Food Safety Qual, 2016, 7(2): 747. |
| [4] |
王莹, 金红宇, 孙磊, 等. 中药材中198种农药残留测定样品前处理平台的建立[J]. 药物分析杂志, 2011, 31(12): 2199. WANG Y, JIN HY, SUN L, et al. Research of pretreatment platform for simultaneous determination of 198 pesticides in traditional Chinese medicine[J]. Chin J Pharm Anal, 2011, 31(12): 2199. |
| [5] |
李南, 石志红, 庞国芳, 等. 坚果中185种农药残留的气相色谱-串联质谱法测定[J]. 分析测试学报, 2011, 30(5): 513. LI N, SHI ZH, PANG GF, et al. Determination of 185 pesticide residues in nuts by gas chromatography tandem mass spectrometry[J]. J Instrum Anal, 2011, 30(5): 513. DOI:10.3969/j.issn.1004-4957.2011.05.008 |
| [6] |
庞国芳, 范春林, 李岩, 等. 茶叶中653种农药化学品残留GC-MS、GC-MS/MS与LC-MS/MS分析方法:国际AOAC方法评价预研究[J]. 分析测试学报, 2012, 31(9): 1017. PANG GF, FAN CL, LI Y, et al. Determination of 653 pesticides and chemical contaminants residues in tea by GC-MS, GC-MS/MS and LC-MS/MS:the pre-collaborative study of AOAC method efficiency evaluation[J]. J Instrum Anal, 2012, 31(9): 1017. DOI:10.3969/j.issn.1004-4957.2012.09.001 |
| [7] |
陈捷, 徐娟, 谢建军, 等. 气相色谱-串联质谱多反应监测及同步子离子全扫描定性定量分析蔬菜中287种农药残留[J]. 分析试验室, 2013, 32(6): 30. CHEN J, XU J, XIE JJ, et al. Determination of 287 pesticide residues in vegetables by gas chromatography-tandem mass sepctometry with multiple reaction monitoring and production scan[J]. Chin J Anal Lab, 2013, 32(6): 30. |
| [8] |
程志, 张蓉, 刘韦华, 等. 气相色谱-串联质谱法快速筛查测定中药材中144种农药残留[J]. 色谱, 2014, 32(4): 57. CHENG Z, ZHANG R, LIU WH, et al. Rapid screening and quantitive analysis of 144 pesticide residues in traditional Chinese medicinal herbs by gas chromatography-tandem mass spectrometry[J]. Chin J Chromatogr, 2014, 32(4): 57. |
| [9] |
曹静, 庞国芳, 王明林, 等. 液相色谱-电喷雾串联质谱法测定生姜中的215种农药残留[J]. 色谱, 2013, 28(6): 579. CAO J, PANG GF, WANG ML, et al. Determination of 215 pesticide residues in ginger using liquid chromatography coupled with electrospray ionizationtandem mass spectrometry[J]. Chin J Chromatogr, 2013, 28(6): 579. |
| [10] |
张爱芝, 王全林, 曹丽丽, 等. QuEChERS-超高效液相色谱-串联质谱法测定蔬菜中250种农药残留[J]. 色谱, 2016, 34(2): 158. ZHANG AZ, WANG QL, CAO LL, et al. Determination of 250 pesticide residues in vegetables using QuEChERS-ultra performance liquid chromatography-tandem mass spectrometry[J]. Chin J Chromatogr, 2016, 34(2): 158. |
| [11] |
中华人民共和国药典2015年版.四部[S].2015: 209 ChP 2015.Vol Ⅳ[S].2015: 209 |
| [12] |
赵志远, 石志红, 康健, 等. 液相色谱-四极杆/飞行时间质谱快速筛查与确证苹果、番茄和甘蓝中的281种农药残留量[J]. 色谱, 2013, 31(4): 373. ZHAO ZY, SHI ZH, KANG J, et al. Rapid screening and confirmation of 281 pesticide residues in apples tomatoes and cabbages by liquid chromatography/quadrupole time-of-flight mass spectrometry[J]. Chin J Chromatogr, 2013, 31(4): 373. |
| [13] |
余璐, 宋伟, 吕亚宁, 等. 超高效液相色谱-四极杆-飞行时间质谱法快速筛查茶叶中的204种农药残留[J]. 色谱, 2015, 33(6): 597. YU L, SONG W, LÜ YN, et al. Rapid determination of 204 pesticide residues in tea by ultra performance liquid chromatography coupled with quadrupole-time of flight mass spectrometry[J]. Chin J Chromatogr, 2015, 33(6): 597. |
| [14] |
曹新悦, 庞国芳, 金铃和, 等. 气相色谱-四极杆-飞行时间质谱和气相色谱-串联质谱对水果、蔬菜中208种农药残留筛查确证能力的对比[J]. 色谱, 2015, 33(4): 389. CAO XY, PANG GF, JIN LH, et al. Comparison of the performances of gas chromatography-quadrupole time of flight mass spectrometry and gas chromatography-tandem mass spectrometry in rapid screening and confirmation of 208 pesticide residues in fruit and vegetables[J]. Chin J Chromatogr, 2015, 33(4): 389. |
| [15] |
VALVERDE A, AGUILERA A, FERRER C, et al. Analysis of Forchlorfenuron in vegetables by LC/TOF-MS after extraction with the buffered QuEChERS method[J]. Agric Food Chem, 2010, 58(5): 2818. DOI:10.1021/jf904465s |
| [16] |
KAUFMANN A. Combining UHPLC and high-resolution MS:A viable approach for the analysis of complex samples[J]. Trend Anal Chem, 2014, 63: 115. |
| [17] |
SANCO/11945/2015, Guidance document on analytical quality control and method validation procedures for pesticide residues analysis in food and feed[S].2015: 12
|
| [18] |
FDA.Acceptance Criteria for Confirmation of Identity of Chemical Residues using Exact Mass Data for the FDA Foods and Veterinary Medicine Program[B/OL].US: U.S.Department of Health and Human Services, 2015[2017-09-22].https://www.fda.gov/scienceresearch/analyticallaboratorymethodsforfoodandfeedsafety/ucm520468.htm
|
 2018, Vol. 38
2018, Vol. 38 
