2. 江西省药品与医疗器械质量工程技术研究中心, 南昌 330029
2. Jiangxi Provincial Engineering Research Center for Drug and Medical Device Quality, Nanchang 330029, China
洛美沙星为第三代喹诺酮类抗菌药,1985年由日本北陆制药公司研制,国内从1989年开始研制。由于盐酸洛美沙星存在溶解度小和注射刺激性大的缺点,后又开始研发门冬氨酸洛美沙星。门冬氨酸氨基酸的亲水性基团--氨基和羧基,是一种亲水性的表面活性剂,具有增溶作用。根据洛美沙星结构特点,选用等电点最小的门冬氨酸与洛美沙星成盐,可大大增加溶解度,并明显降低注射刺激性。门冬氨酸洛美沙星葡萄糖注射液主要用于治疗敏感菌引起呼吸道、泌尿生殖道和胆道等组织感染,不良反应主要有中枢神经系统反应、光过敏和呼吸系统损害等。
拉曼光谱检测技术是利用拉曼光谱来研究分子振动、转动的一种光谱学方法,光子照射到分子上时,会与被检测物质分子发生相互作用,产生散射光,散射光谱可以表征分子振动或转动能级差的特征频移,从而反映物质中的分子结构和成分。多种拉曼光谱技术均具有无损、快速、灵敏度高的特点,引起了物质分析领域研究人员的极大关注。赵迎等[1]利用拉曼光谱技术可快速判断稻谷的新陈度,刘燕德等[2]基于共焦显微拉曼对柑橘的黄龙病进行了无损检测研究,卢明子等[3]对拉曼光谱检测技术在血红蛋白结构及功能的检测中的应用进行了综述,主要是关于病变血红蛋白的检测,为诊断提供依据,还有关于血红蛋白反应动力学的研究工作,以及定量评估血氧饱和度和高铁血红蛋白含量方面的拉曼光谱检测工作,为白血病的早期诊断奠定了基础。药物分析中常用的拉曼光谱技术包括傅立叶变换拉曼光谱技术[4]、表面增强拉曼光谱技术[5]、激光共振拉曼光谱技术[6]、共焦显微拉曼激光技术、拉曼光谱成像技术[7]、透射拉曼技术[8]、表面增强拉曼光谱技术及其联用技术[9-10]、小型拉曼光谱仪[11]、空间位移拉曼光谱技术[12]等。下面就小型拉曼光谱仪在门冬氨酸洛美沙星葡萄糖注射液的快速鉴别进行阐述。
1 仪器与试药 1.1 仪器Metage OPAL-3000型便携式拉曼光谱仪(Metage Scientific,Banbury),采用光纤测量方式,探头焦距5 mm,激发光源785 nm,分辨率4.5 cm-1,光谱范围2 000~400 cm-1,CCD检测器(工作温度-50℃)。特殊设计样品仓,可同时确保不同包装的液体注射剂测量时处于探头的焦点和完全避光环境。软件Essential FTIR(version3.00.047),用于光谱的采集和模型的建立。
1.2 试药7批样品均为本单位2017年国抽品种门冬氨酸洛美沙星葡萄糖注射液,来源于2家生产企业(武汉大安制药有限公司和湖北康沁药业股份有限公司);用于模型验证的3批乳酸环丙沙星氯化钠注射液、3批氧氟沙星氯化钠注射液,详细信息见表 1。洛美沙星对照品(批号130452-201603,含量90.4%,中国食品药品检定研究院),辅料5%葡萄糖溶液(江西科伦制药有限公司),辅料L-门冬氨酸对照品(批号140691-201602,中国食品药品检定研究院),辅料注射用水(江西润泽药业有限公司)。
|
|
表 1 样品信息表 Table 1 sample information |
把洛美沙星对照品、L-门冬氨酸对照品分别用注射用水配制成与样品浓度相同的溶液,采用上述条件分别对7批样品、洛美沙星对照品溶液、门冬氨酸溶液、5%葡萄糖溶液、注射用水、2家企业的输液瓶进行光谱采集,每份样品重复测量3次,光谱如图 1所示。

|
图 1 7批样品(A)、洛美沙星对照品(B)、L-门冬氨酸(C)、5%葡萄糖溶液(D)、注射用水(E)和2家企业的输液瓶(F)光谱图 Figure 1 Spectra of 7 batches of samples(A), lomefloxacin reference substances(B), L- aspartic acid(C), 5% glucose solution(D), injection water(E)and transfusion bottles from two enterprises(F) |
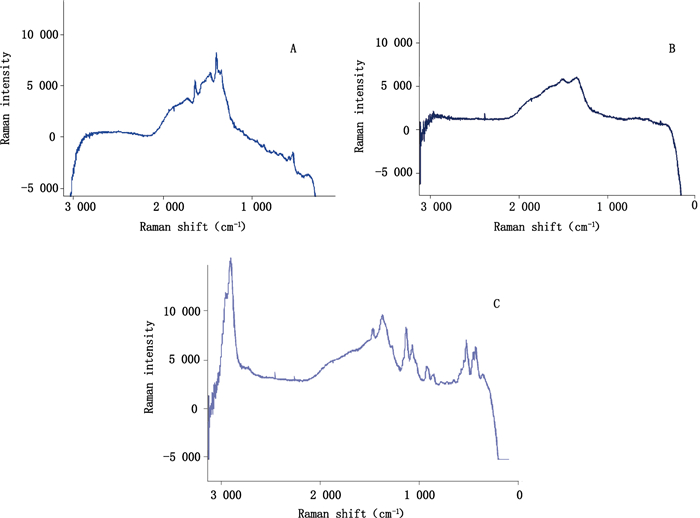
从图 1-E可看出,水在1 800~1 500 cm-1范围内也有拉曼信号,对各成分的自身信号产生了较大的干扰,因此用于建模的每种成分的光谱图须先扣减水的信号,通过EFTIR工作软件中比较不同计算谱区、自动差减和手动微调的方式,得到各成分自身光谱图,如图 2。
|
图 2 洛美沙星(A)、L-门冬氨酸(B)和5%葡萄糖(C)溶液光谱 Figure 2 Spectra of lomefloxacin(A), L- aspartic(B) acid and 5% glucose(C) solation |
从图中可以看出,在2 000~400 cm-1范围内,扣减水后的API洛美沙星、门冬氨酸、5%葡萄糖都具有一定程度的拉曼信号。
2.2.2 输液瓶从上述7批门冬氨酸洛美沙星葡萄糖注射液的样品光谱图(图 1-A)和输液瓶拉曼光谱(图 1-F)可以看出,大部分信号是输液瓶产生。而在以往差谱中,多使用主成分分析提取不同厂家或规格的液体包装拉曼信号,得到代表性光谱,用于差谱。但输液瓶比较厚,所以拉曼信号很强,一般光谱差减效果不好。本测试中将不同输液瓶的拉曼信号直接作为一个成分信号,加入辅料光谱中,使用经典最小二乘法计算差减,取得良好效果。
2.3 模型建立与验证 2.3.1 验证光谱7批门冬氨酸洛美沙星葡萄糖注射液(图 1-A),3批乳酸环丙沙星氯化钠注射液(图 3-A),3批氧氟沙星氯化钠注射液(图 3-B),39张13批样品(3-C)的原始光谱(图 3-C)。

|
图 3 3批乳酸环丙沙星氯化钠注射液(A)、3批氧氟沙星氯化钠注射液(B)和13批样品(C)原始光谱图 Figure 3 Original spectra of 3 batches of ciprofloxacin lactate and sodium chloride injection(A), 3 batches of ofloxacin and sodium chloride injection(B)and 13 batches of samples(C) |
通过EFTIR工作软件中选取比较不同的数据前处理方法所得的相关系数r,结果见表 2。
|
|
表 2 模型参数比较 Table 2 Comparison of model parameters |
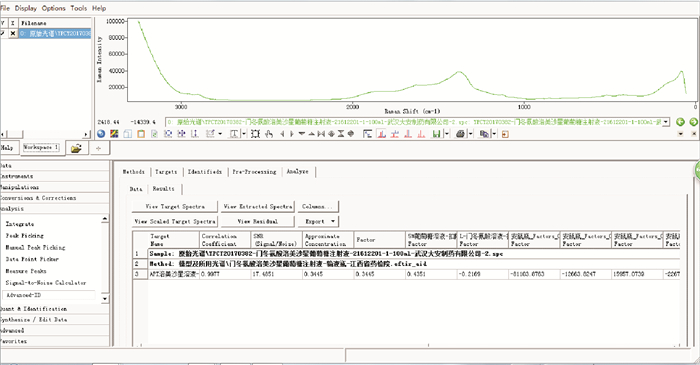
取所得r最大的预处理方法曲线校正作为门冬氨酸洛美沙星葡萄糖注射液的快速定性鉴别模型的光谱预处理方法(如图 4),最终的模型参数为:谱段范围2 000~400 cm-1,预处理方法为曲线校正,相关系数阈值98%。
|
图 4 建模结果 Figure 4 Modeling results |
7批门冬氨酸洛美沙星葡萄糖注射液与3批乳酸环丙沙星氯化钠注射液、3批氧氟沙星氯化钠注射液的共计39张原始光谱采用所建立的门冬氨酸洛美沙星葡萄糖注射液的快速定性模型进行鉴别,得到各光谱相关系数,如表 3所示。
|
|
表 3 验证结果 Table 3 Validation results |
39张原始光谱都能被正确检测,所有门冬氨酸洛美沙星葡萄糖注射液的光谱都显示√,且相关系数都在0.98以上,验证通过。乳酸环丙沙星氯化钠注射液与氧氟沙星氯化钠注射液的光谱都显示×,且相关系数都在0.98以下,未通过验证,也说明建立的该模型可以较好地区分门冬氨酸洛美沙星葡萄糖注射液与其他品种,可用于该品种的快速定性鉴别。
3 讨论对注射剂而言,各个厂家使用的安瓿瓶、西林瓶或大玻瓶都不同,同时玻璃表现出的光致发光效应也导致即使同一来源的2个玻璃瓶也不完全重合[13]。从门冬氨酸洛美沙星葡萄糖注射液的拉曼光谱图可以看出,主成分的拉曼信号被玻璃输液瓶的信号所掩盖,想要通过光谱的直接差减来得到主成分的拉曼信号几乎不可能。因此,分别采集了2家样品生产企业的多个玻璃输液瓶的拉曼光谱,并直接作为一个成分信号加入辅料光谱中,使用经典最小二乘法(CLS)计算差减,取得良好效果。
拉曼光谱是1种散射光谱,基于光与分子的非弹性碰撞,其定量分析原理不是基于朗伯-比尔定律,而是遵循拉曼效应原理。拉曼光谱和近红外光谱技术均具有高效、快速、无损伤检测的特点,可以同时检测样品的含量、水分、杂质、粒度、晶型、均匀性等信息,可对原料和制剂进行定性、定量分析。中国食品药品检定研究院自2002年来致力于假劣药品快速筛查技术的研究,进行了应用拉曼光谱快速分析化学药品、生物制品的相关研究[14-15]。
拉曼效应是一种由分子和晶格振动导致的非弹性散射。早在1923年,Smekal[16]就已经在理论上预言了这种效应,1928年印度科学家拉曼(Raman)[17]与Krishman首先在液体中观察到这种现象。在拉曼和Krishman的论文发表后不久,Landberg[18]就在俄国报道了他们在石英中观察到频率发生改变的光散射现象;并且Cabannes[19]和Rocard[20]在法国也证实了拉曼和Krishman的观察结果。
拉曼光谱分析技术由于具有丰富的物质特性信息,无损检验,无需样品制备等优点,作为一种行之有效的检测分析方法,目前已被广泛应用[21-26],是现代分析技术的重要组成部分。早期的拉曼光谱仪体积较大且安装不方便,主要应用于实验室中,随着光电、嵌入式软硬件、拉曼光谱分析技术的不断进步,体积小、重量轻、移动方便的手持便携式拉曼光谱仪具有检测快速准确等优点,迅速得到了发展,市场需求不断增加。
| [1] |
赵迎, 李明. 基于拉曼光谱快速鉴别新陈大米的方法研究[J]. 光谱学与光谱分析, 2016, 36(10): 303. ZHAO Y, LI M. Rapid identification of fresh rice based on Raman spectroscopy[J]. Spectrosc Spectral Anal, 2016, 36(10): 303. |
| [2] |
刘燕德, 肖怀春. 基于共焦显微拉曼的柑橘黄龙病无损检测研究[J]. 光谱学与光谱分析, 2018, 38(1): 111. LIU YD, XIAO HC. Nondestructive detection of Citrus Huanglong disease based on confocal Raman microscopy[J]. Spectrosc Spectral Anal, 2018, 38(1): 111. |
| [3] |
卢明子, 郭延军, 赵莲, 等. 拉曼光谱在血红蛋白结构及功能研究中的应用进展[J]. 光谱学与光谱分析, 2014, 34(2): 439. LU MZ, GUO YJ, ZHAO L, et al. Application of Raman spectroscopy in hemoglobin structure and function research[J]. Spectrosc Spectral Anal, 2014, 34(02): 439. DOI:10.3964/j.issn.1000-0593(2014)02-0439-06 |
| [4] |
FERRARO JR, NAKAMOTO K, BROWN CW. Introductory Raman Spectroscopy 2nd ed[M]. York: Elsevier/Academic Press, 2003: 83.
|
| [5] |
陈蓓蓓, 陆洋, 马宁, 等. 表面增强拉曼光谱技术在食品安全快递检测中的应用[J]. 贵州科学, 2012, 30(6): 24. CHEN BB, LU Y, MA N, et al. Application of surface enhanced Raman spectroscopy in food safety express detection[J]. Guizhou Science, 2012, 30(6): 24. DOI:10.3969/j.issn.1003-6563.2012.06.006 |
| [6] |
黄蓉, 杨永健. 拉曼光谱在药物分析中的研究进展[J]. 医药导报, 2018, 37(1): 81. HUANG R, YANG YJ. Research progress of Raman spectroscopy in pharmaceutical analysis[J]. Med Guide, 2018, 37(1): 81. |
| [7] |
ZHANG R, ZHANG Y, DONG ZC, et al. Chemical mapping of a single molecule by plasmon-enhanced Raman scattering[J]. Nature, 2013(498): 82. |
| [8] |
AINA A, HARGREAVES MD, MATOUSEK P, et al. Transmission Raman spectroscopy as a tool for quantifying polymorphic content of pharmaceutical formulations[J]. Analyst, 2010, 135(9): 2328. DOI:10.1039/c0an00352b |
| [9] |
ZHANG ZM, LIU JF, LIU R, et al. Thin layer chromatography coupled with surface-enhanced Raman scattering as a facile method for on-site quantitative monitoring of chemical reactions[J]. Anal Chem, 2014, 86(15): 7286. DOI:10.1021/ac5017387 |
| [10] |
WANG W, XU MM, GUO QH, et al. Rapid separation and on-line detection by coupling high performance liquid chromatography with surface-enhanced Raman spectroscopy[J]. RSC Adv, 2015, 5(59): 47640. DOI:10.1039/C5RA05562H |
| [11] |
孙振华, 余镇岗, 黄梅珍, 等. 小型化拉曼光谱仪的优化设计及应用[J]. 光电子·激光, 2015, 26(6): 1132. SUN ZH, YU ZG, HUANG MZ, et al. Optimization design and application of miniaturized Raman spectrometer[J]. Optoelect Laser, 2015, 26(6): 1132. |
| [12] |
黄蓉, 杨永健. 拉曼光谱在药物分析中的研究进展[J]. 医药导报, 2018, 37(1): 81. HUANG R, YANG YJ. Research progress of Raman spectroscopy in pharmaceutical analysis[J]. Med Guide, 2018, 37(1): 81. |
| [13] |
赵瑜, 纪南, 尹利辉, 等. 液体注射剂拉曼无损筛查数据库的建立[J]. 药物分析杂志, 2015, 35(7): 1263. ZHAO Y, JI N, YIN LH, et al. Establishment of a database for Raman nondestructive screening of liquid injections[J]. Chin J Pharm Anal, 2015, 35(7): 1263. |
| [14] |
赵瑜, 马讯, 沈雨婷, 等. 拉曼光谱法快速筛查盐酸哌替啶注射液[J]. 中国药学杂志, 2016, 51(11): 925. ZHAO Y, MA X, SHEN YT, et al. Rapid screening of pethidine hydrochloride injection by Raman spectroscopy[J]. Chin J Pharm, 2016, 51(11): 925. |
| [15] |
柳艳, 尹利辉, 陆峰. 拉曼光谱法在假药快检中的研究进展[J]. 药学实践杂志, 2012, 30(6): 401. LIU Y, YIN LH, LU F. Research progress of Raman spectroscopy in rapid detection of counterfeit drugs[J]. J Pharm Pract, 2012, 30(6): 401. DOI:10.3969/j.issn.1006-0111.2012.06.001 |
| [16] |
SMEKAL A.The quantum theory of dispersion[Z].Naturwiss, 1923, 11: 873
|
| [17] |
RAMAN CV, KRISHMAN KS. A new type of secondary radiation[J]. Nature, 1928, 121: 501. |
| [18] |
LANDSBERG G, MANDELSTAM L. A novel effect of light scattering in crystals[J]. Naturwiss, 1928, 16: 557. DOI:10.1007/BF01506807 |
| [19] |
CABANNES J. New optical phenomenon; pulsations produced when anisotropic molecules in rotation and vibration diffuse visible and ultra-violet light[J]. Conrend, 1928, 186: 1201. |
| [20] |
ROCARD Y. New diffused radiations[J]. Compt Rend, 1928, 186: 1109. |
| [21] |
李淑玲. 拉曼光谱仪及其应用进展[J]. 盐矿测试, 1998, 17(4): 312. LI SL. Raman spectrometer and its application progress[J]. Salt Mine Test, 1998, 17(4): 312. |
| [22] |
白利涛, 张丽萍, 赵国文. 拉曼光谱的应用及进展[J]. 福建分析测试, 2011, 20(2): 27. BAI LT, ZHANG LP, ZHAO GW. Application and progress of Raman spectroscopy[J]. Fujian Anal Test, 2011, 20(2): 27. DOI:10.3969/j.issn.1009-8143.2011.02.006 |
| [23] |
刘宸, 黄文倩. 拉曼光谱在食品无损检测中的应用[J]. 食品安全质量检测学, 2015, 6(8): 2981. LIU C, HUANG WQ. Application of Raman spectroscopy in food nondestructive testing[J]. Food Safety Quality Testing, 2015, 6(8): 2981. |
| [24] |
乐健, 李珺婵, 陈桂良, 等. 拉曼光谱法快速测定氨茶碱注射液中无水茶碱和乙二胺的含量[J]. 中国临床药学杂志, 2014, 23(3): 141. LE J, LI JC, CHEN GL, et al. Rapid determination of anhydrous theophylline and ethylenediamine in aminophyiline injection by Raman spectroscopy[J]. Chin J Clin Pharm, 2014, 23(3): 141. |
| [25] |
陈莉, 钱啸, 朱乃军. 拉曼光谱法快速测定注射用头孢他定溶液的含量[J]. 中国药事, 2015, 25(8): 874. CHEN L, QIAN X, ZHU NJ. Rapid determination of ceftazidime solution for injection by Raman spectroscopy[J]. Chin Pharm Aff, 2015, 25(8): 874. |
| [26] |
曹玲, 石蓓佳, 吴莉, 等. 常用羧酸类及其衍生物药用辅料的拉曼光谱鉴别[J]. 药物分析杂志, 2010, 30(3): 484. CAO L, SHI BJ, WU L, et al. Raman spectrum identification of commonly used carboxylic acids and their derivatives as pharmaceutical excipients[J]. Chin J Pharm Anal, 2010, 30(3): 484. |
 2018, Vol. 38
2018, Vol. 38 
