2. 中国食品药品检定研究院, 北京 100050;
3. 吉林省药品检验所, 长春 130033
2. National Institutes for Food and Drug Control, Beijing 100050, China;
3. Jilin Institute for Drug Control, Changchun 130033, China
目前用于检测药品中铅、镉、砷、汞、铜残留的标准物质,均为购买其他行业检测用的单元素标准物质,检测时需要有一系列复杂的稀释过程,进而引入了更多不确定因素,增加了检测结果的误差。根据《中华人民共和国药典》(简称《中国药典》)2015年版中重金属及有害元素分析项下规定[1],为了使实际检验工作标准物质溶液配制过程更加方便快捷,也为了更好地保证药品中重金属及有害元素残留检测结果的有效性、可靠性,研制了专业用于药品检验使用的铅(Pb)、镉(Cd)、砷(As)、汞(Hg)、铜(Cu)对照品溶液,本系列标准物质采用5%硝酸作为基质,安瓿瓶封装。为实现对照品溶液的准确定值,本研究参考了JJF 1343-2012《标准物质定值的通用原则及统计学原理》[2]、国际标准化组织(ISO)导则35[3]、JJF 1006-1994《一级标准物质技术规范》[4],采用多家实验室联合定值的方式对对照品溶液进行赋值,并进行了不确定度评定。本研究对金属离子混合标准物质的研制及相关研究具有极大的参考意义。
1 仪器与试药仪器:本实验室采用安捷伦7700电感耦合等离子体质谱仪,其他协作定值实验室使用的仪器分别为PE Nexion 300x电感耦合等离子体质谱仪、安捷伦8800电感耦合等离子体质谱仪、赛默飞世尔ICAP QC电感耦合等离子体质谱仪;Milli-Q超纯水处理系统。
试药:色谱级硝酸(Fisher Scientific公司),去离子水;Pb、Cd、As、Hg、Cu单元素标准溶液购于中国计量科学研究院,质量浓度均为1 000 μg·mL-1;调谐溶液为锂(Li)、镁(Mg)、钇(Y)、铈(Ce)、铊(Tl)、钴(Co)的混合标准溶液(Agilent公司,质量浓度为1 μg·L-1,);内标溶液为100 μg·mL-1的锂(Li)、钪(Sc)、锗(Ge)、铑(Rh)、铟(In)、铽(Tb)、镥(Lu)、铋(Bi)的混合内标溶液(Agilent公司,批号5188-6 525),稀释100倍使用。高纯氩气(北京诚维信科技发展公司)。
原料购买北京有色金属研究总院生产的Pb、Cd、As、Hg、Cu标准物质溶液,质量浓度分别为Pb 2 000 μg·mL-1、Cd 100 μg·mL-1、As 1 000 μg·mL-1、Hg 100 μg·mL-1、Cu 10 000 μg·mL-1,介质为5%硝酸。
2 方法与结果 2.1 Pb、Cd、As、Hg、Cu混合对照品溶液的制备由于药品中Pb、Cd、As、Hg、Cu残留量检测均为痕量分析检测,而研制的标准物质溶液相对于其他行业使用的单元素标准物质溶液来说浓度相对较低,因此,如在包装过程中引入其他污染会对标准物质溶液元素含量产生影响,最终导致产生不准确的分析结果。由于塑料容器对汞离子具有强烈的吸附,而国产GG-17玻璃是较为理想的容器材料,因此采用GG-17玻璃安瓿作为标准物质溶液的容器。随后采用容量法,精密吸取适量,稀释,充分混匀,用人工分装、流水线封装的方式,完成包装规格为每支2 mL的混合标准物质溶液的分装。
2.2 协作定值 2.2.1 质谱条件反馈功率为5 W,射频功率为1 550 W,载气(高纯氩气)流速为1.05 L·min-1,等离子气体流速为15.0 L·min-1,蠕动泵转速0.3 r·s-1,采样深度8 mm,检测质量数m/z 75(As),采样周期为0.1 s。
2.2.2 标准溶液的制备内标溶液:(0~5 ℃密封贮存)精密量取含72Ge、115In、209Bi的混合内标液适量,置量瓶中,用5%硝酸溶液(取70%硝酸溶液50 mL,用水稀释至1 000 mL)稀释至刻度(含72Ge、115In、209Bi各1 μg·mL-1)。
混合标准溶液:精密量取As标准溶液1 mL及Pb标准溶液2 mL,置10 mL量瓶中,以5%硝酸溶液定容至刻度,配成As、Pb混合标准储备溶液;另精密量取Cd标准溶液、Hg标准溶液各1 mL,置100 mL量瓶中,以5%硝酸溶液定容至刻度,配成Cd、Hg混合标准储备溶液。分别取Cd、Hg混合标准储备溶液、As、Pb混合标准储备溶液、Cu标准溶液各1 mL,置100 mL量瓶中,用5%硝酸溶液定容至刻度,摇匀,制成每1 mL含Cu 10 μg,Pb 2 μg,As 1 μg,Cd 0.1 μg,Hg 0.1 μg的混合标准溶液(临用现配)。精密量取混合标准溶液5.0 mL,置100 mL量瓶中,加5%硝酸溶液稀释至刻度,即得。
2.2.3 供试品溶液的制备取待标定溶液5支,混合均匀,精密量取1 mL,置20 mL量瓶中,加5%硝酸溶液稀释至刻度,摇匀,精密量取上述溶液1 mL置100 mL量瓶中,加5%硝酸溶液稀释至刻度,摇匀,即得。以5%硝酸溶液作为试剂空白溶液。
2.2.4 测定方法与结果测定方法:测定时选取的同位素为63Cu、75As、114Cd、202Hg和208Pb,其中63Cu、75As以72Ge作为内标,114Cd以115In作为内标,202Hg、208Pb以209Bi作为内标,并根据仪器的要求选用适宜校正方程对测定的元素进行校正。依次将样品管插入混合标准溶液和供试品溶液中进行测定,以外标法计算得相应的浓度。样品平行测定6份,计算测定结果平均值和RSD。
本次协作定值有中国食品药品检定研究院及其他6家省级食品药品检验所参加。测定结果见表 1。
|
|
表 1 协作定值测定结果 Table 1 Results of the collaborative calibration |
在各个实验室测定结果中,每个元素平行6组数据,7家实验室共42组数据,首先采用偏态系数和峰态系数法进行正态分布检验,5种元素的测定结果均呈正态分布。其次采用Grubbs法和Dixon法[5-7]对每个实验室数据进行异常值检验,为使分析结果更符合客观实际,可疑值的取舍结合了具体实验操作过程,分析原因后进行评估,随后剔除,C和D实验室铜元素数据中995.716 μg·mL-1和977.854 μg·mL-1为可疑值,舍去;B实验室砷元素数据中112.525 μg·mL-1为可疑值,舍去。随后按照科克伦准则[8-10]判断每个元素组间数据是否等精度,其中由科克伦法计算出的铜元素统计量C=0.572 1,汞元素统计量C=0.596 9,均大于统计量C临界值(0.01、7、6)0.465 9,表明被检验的最大方差为离群值,离群方差说明该组数据的精度比其他组差,计算定值结果可按不等精度情况处理;而铅、镉、砷元素统计量C均小于0.465 9,测定数据均为等精度。再对各实验室数据同样采用Grubbs法和Dixon法检验平均值有无显著性差异,其中B实验室汞元素平均值为可疑数据,故舍去。最后计算出总平均值:Pb 198.7 μg·mL-1,Cd 10.0 μg·mL-1,As 103.2 μg·mL-1,Hg 10.0 μg·mL-1,Cu 1 007.5 μg·mL-1。
2.3 定值的不确定度评定 2.3.1 不确定度评定数学模型Pb、Cd、As、Hg、Cu 5种元素含量的数学模型为
| $ {C_{\rm{s}}} = \frac{{{C_{{\rm{ref}}}} \times {T_{{\rm{ref}}}} \times {V_{\rm{s}}}}}{{{T_{\rm{s}}} \times {V_{{\rm{ref}}}}}} $ |
其中:Cs代表供试品浓度(μg·mL-1),Cref代表对照品浓度(μg·mL-1),Tref代表对照品溶液CPS计数,Ts代表供试品溶液CPS计数,Vs代表样品稀释倍数,Vref代表对照品稀释倍数。
2.3.2 不确定度来源分析根据检测方法和数学模型,本标准物质引入的不确定度分量主要来源为均匀性引入的不确定度、稳定性引入的不确定度定值过程引入的不确定度、样品溶液制备引入的不确定度、对照品溶液引入的不确定度和样品测定重复性引入的不确定度。
2.3.2.1 均匀性均匀性试验由本实验室完成,根据ISO导则35,均匀性引入的不确定度
| $ {u_{{\rm{bb}}}} = \sqrt {\frac{{M{{\rm{s}}_{{\rm{among}}}}^2 - M{{\rm{s}}_{{\rm{within}}}}^2}}{n}} $ |
由此公式计算得5种元素均匀性引入的不确定度分别为:Cu 3.820 9,Cd 0.042 0,As 0.391 4,Hg 0.096 2,铅0.893 7。
2.3.2.2 稳定性由于暂缺乏长期稳定性监测数据,无法将标准物质的不稳定性引入的不确定度合成到总不确定度中,此项需日后补充长期稳定性数据后再行完善。
2.3.2.3 定值过程Pb、Cd、As、Hg、Cu混合对照品的定值过程中,由于铜和汞数据为不等精度,检查测量方法、测量条件及操作过程,经确认测量方法、测量条件及操作过程均无误后,在对方法进行技术上的认真审定的基础上,采用不等精度加权方式处理,加权总平均值即为标准值,其定值过程引入的不确定度u。
| $ {U_{{\rm{char}}}} = U\left( {\bar X} \right) = \sqrt {\frac{{\sum\limits_{i = 1}^m {W_i^2u_i^2} }}{{{{\left( {\sum\limits_{i = 1}^m {{W_i}} } \right)}^2}}}} $ |
式中,Wi为实验室第i组测量的权,其为
| $ {S^{\rm{2}}} = \frac{1}{{p - 1}}\sum\limits_{i = 1}^p {{{\left( {{Y_i} - \bar Y} \right)}^2}\;\;\;\;{U_{{\rm{char}}}} = \frac{S}{{\sqrt p }}} $ |
式中,Y为总平均值;Yi为各组数据的平均值;p为实验室数目,由此计算得5种元素的不确定度分别为Cu 0.580 6,Cd 0.072 6,As 1.291 3,Hg 0.000 3,Pb 0.751 3。
2.3.2.4 供试品溶液制备供试品溶液制备引入的不确定度主要是由量瓶和移液管引入的不确定度,包括校准引入的不确定度和温度效应引入的不确定度。本实验对照品溶液配制过程中使用到100和20 mL A级量瓶,1 mL A级单标线移液管。不考虑重复性误差时,其不确定度评定如下:根据GB/T 12806-2011《实验室玻璃仪器单标线容量瓶》,100、20 mL A级量瓶的容量允差分别为±0.10mL和±0.020mL;根据GB/T 12808-91《实验室玻璃仪器单标线吸量管》,1 mL A级单标线吸量管的容量允差为±0.007 mL。温度效应引入的不确定度为溶液的温度与校正时温度不同引入的不确定度,结合实验室在定值时实际检测温度,选取最大的差值进行评估,此差值为4 ℃,水体积膨胀系数为2.1×10-4·℃-1,按均匀分布,k=1.732,则单标线量瓶和单标线吸量管的相对不确定度见表 2,由此计算出5种元素的相对不确定度
| $ {u_{{\rm{sam, rel}}}} = \sqrt {2{u_{1{\rm{ml}}}}^2 + {u_{{\rm{20ml}}}}^2 + {u_{100{\rm{ml}}}}^2} = 0.0058。$ |
|
|
表 2 5种元素的相对不确定度 Table 2 Relative uncertainty of five elements |
对照品溶液自身:中国计量科学研究院标准物质证书给出的Cu元素浓度(1 000±1)μg·mL-1,Cd元素浓度(1 000±2)μg·mL-1,As元素浓度(1 000±1)μg·mL-1,Hg元素浓度(1 000±1)μg·mL-1,Pb元素浓度(1 000±2)μg·mL-1,包含因子k=2。相对不确定度为ustd1,
对照品溶液配制:配制对照品溶液引入的不确定度主要是由量瓶和移液管引入的不确定度,包括校准引入的不确定度和温度效应引入的不确定度。本实验对照品溶液配制过程中使用到100和10 mL A级量瓶,1、2、5 mL A级单标线移液管。不考虑重复性误差时,其不确定度评定如下:根据GB/T 12 806-2011《实验室玻璃仪器单标线容量瓶》,100和10 mL A级量瓶的容量允差分别为±0.10 mL和±0.020 mL;根据GB/T 12808-91《实验室玻璃仪器单标线吸量管》,1、2、5 mL A级单标线吸量管的容量允差分别为±0.007、±0.010、±0.015 mL。温度效应引入的不确定度为溶液的温度与校正时温度不同引入的不确定度[11-12],假设二者相差4 ℃,水体积膨胀系数为2.1×10-4·℃-1,按均匀分布,k= 1.732,则单标线量瓶和单标线吸量管的相对不确定度见表 3,由此计算出5种元素的相对不确定度
| $ {u_{{\rm{std2, rel}}}} = \sqrt {2{u_{1{\rm{ml}}}}^2 + {u_{{\rm{2ml}}}}^2 + {u_{{\rm{5ml}}}}^2 + {u_{{\rm{10ml}}}}^2 + {u_{100{\rm{ml}}}}^2} = 0.0068。$ |
|
|
表 3 5种元素的相对不确定度 Table 3 Relative uncertainty of five elements |
合成对照品溶液引入的相对不确定度:
从7家协作标定单位中选择重复性数据标准差最大的数据计算由重复性引入的不确定度。
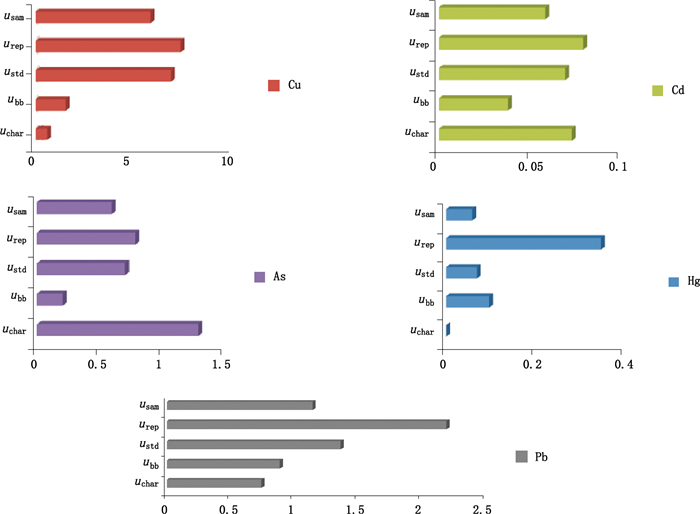
化学分析测量的不确定度来源多种多样,结合本研究,通过对比不同来源的各元素不确定度分量(图 1),由综合计算结果可以看出,不同元素的不确定度分量贡献不尽相同,其中Cu、Cd、Hg、Pb元素测定的不确定度来源主要是样品重复测定引入的不确定度,而砷元素测定的不确定度来源主要是定值过程引入的不确定度。综合来看,采用ICP-MS法时实验结果误差主要是由对样品的重复测量产生的;同时也说明测量过程的每一步都能够产生误差,这些误差随着测量过程逐渐累积,最后形成整个结果的不确定性。
|
图 1 不确定度分量条形图 Figure 1 The bar graph of uncertainty component |
最终的定值结果分别为Pb(198.7±6.1)μg·mL-1、Cd(10.0±0.3)μg·mL-1、As(103.2±3.6)μg·mL-1、Hg(10.0±0.7)μg·mL-1、Cu(1 007.5±24.6)μg·mL-1。
3 讨论本研究在研制出供药品检验用Pb、Cd、As、Hg、Cu混合对照品溶液之后,采用7家单位协作定值,涉及不同品牌的电感耦合等离子体质谱仪,并且包含了多个实验操作步骤,得出混合对照品溶液的标准值后,有必要对标准值不确定度进行详细评定。结合不确定度分量来源与评定结果,在实际工作中,应该注意以下几点:1)尽量合理减少稀释步骤;2)测定样品时,应严格控制空白溶液污染,确保仪器管路冲洗干净,避免系统残留元素影响试验结果;3)采用ICP-MS法时,应注意供试品溶液中的各元素(尤其是金属型阳离子,如汞等)浓度应在仪器允许的范围内,以免污染系统;4)整个实验过程应严格按照作业指导书规程操作。
《中国药典》2015年版四部通则2321法中硝酸介质选用10%(v/v)硝酸,在此次标定的方法中,选用5%(v/v)硝酸溶液作为稀释液,因为在具体实验时发现,10%(v/v)硝酸空白溶液部分元素响应值较大,影响了低点浓度的测定。针对混合对照溶液,此次标定并没有采用标准曲线法测定5种元素,而是采用ICP-MS外标法测定,这样很大程度上简化了操作,减少了在配制系列标准曲线溶液浓度时引入的操作误差,避免标准曲线带来的定值不确定度,对其他金属离子标准物质标定具有一定的参考意义。
在日常检验中,采用的对照物质品种数量多,且来源较为复杂,单体对照品在使用时,应该知道纯度,并且要符合分析要求。在对照品配制的过程中,一般先配成1~200 μg·mL-1的浓溶液,作为储备液使用。本次制备的Pb、Cd、As、Hg、Cu混合对照品溶液的浓度适合作为储备液直接使用,且各元素含量与《中国药典》2015年版5种重金属及有害元素限量基本保持一致,适于用ICP-MS法同时测定5种元素残留量时使用,节省时间成本,简化了实验操作。在对照品溶液使用时,配制的储备液应保存在合适的条件下,如密封、避光、低温等,针对浓度较低的对照品溶液使用时应该临用现配。本次制备的混合对照品溶液采用GG-17玻璃安瓿封装,包装规格为每支2 mL,这种小剂量包装可一次性使用,方便用户的同时避免资源浪费。
本研究制备的Pb、Cd、As、Hg、Cu混合对照品溶液,解决了单元素标液稀释步骤复杂的问题,满足了日常检验技术的需求,为相关药品重金属及有害元素残留检验结果的准确性和一致性提供了保障。
| [1] |
中华人民共和国药典2015年版.四部[S].2015: 6 ChP 2015.Vol Ⅳ[S].2015: 6 |
| [2] |
JJF 1343-2012标准物质定值的通用原则及统计学原理[S].2012 JJF 1343-2012 General and Statistical Principles for Characterization of Reference Materials[S].2012 |
| [3] |
ISO Guide 35: 2006 Reference Materials-General and Statistical Principles for Certification.The Third Edition[S].2006
|
| [4] |
JJG 1006-1994一级标准物质规范[S].1994 JJG 1006-1994 Technical Norm of Primary Reference Materials[S].1994 |
| [5] |
徐维盛, 杨德智, 张丽, 等. 丹皮酚化学纯度标准物质研制与定值分析方法研究[J]. 医药导报, 2011, 30(2): 143. XU WS, YANG DZ, ZHANG L, et al. Development of paeonol purity reference material and method of valuation[J]. Her Med, 2011, 30(2): 143. DOI:10.3870/yydb.2011.02.003 |
| [6] |
姚尚辰, 常艳, 胡昌勤. HPLC用β-内酰胺类抗生素化学对照品的不确定度分析[J]. 药物分析杂志, 2010, 30(11): 2104. YAO SC, CHANG Y, HU CQ. Study of uncertainty of β-lactam antibiotics chemical reference substance being used in HPLC[J]. Chin J Pharm Anal, 2010, 30(11): 2104. |
| [7] |
杨德智, 胡堃, 杨雪薇, 等. 国家一级标准物质氢溴酸加兰他敏的定值研究与不确定度评定[J]. 中国医药工业杂志, 2016, 47(6): 761. YANG DZ, HU K, YANG XW, et al. Characterization and uncertainty evaluation of national primary certified reference material of galanthamine hydrobromide[J]. Chin J Pharm, 2016, 47(6): 761. |
| [8] |
何风艳, 戴忠, 何轶, 等. 西红花苷对照提取物的定值及不确定度评估研究[J]. 药物分析杂志, 2016, 36(6): 1113. HE FY, DAI Z, HE Y, et al. Certification and uncertainty evaluation of crocin reference extract[J]. Chin J Pharm Anal, 2016, 36(6): 1113. |
| [9] |
吴坚, 宋海燕, 陈扉然, 等. 电感耦合等离子体质谱法测定糕点中铝含量的不确定度评定[J]. 质谱学报, 2013, 34(6): 368. WU J, SONG HY, CHEN FR, et al. Uncertainty evaluation of determination of aluminum in pastry by ICP-MS[J]. J Chin Mass Spectrum Soc, 2013, 34(6): 368. |
| [10] |
胡坪, 罗国安, 赵中振, 等. 中药材定量分析中测量不确定度的评定方法及其影响因素的研究[J]. 药物分析杂志, 2005, 25(4): 455. HU P, LUO GA, ZHAO ZZ, et al. Study on the evaluation method and the affecting factor of measurement uncertainty for the determination of marker compounds in Chinese materia medica[J]. Chin J Pharm Anal, 2005, 25(4): 455. |
| [11] |
王志龙. 铅、镉、铬、钴、镍混合标准溶液的不确定度评定[J]. 广东化工, 2016, 43(14): 216. WANG ZL. The uncertainty evaluation of Pb, Cd, Cr, Co and Ni mixed solution[J]. Guangdong Chem Ind, 2016, 43(14): 216. DOI:10.3969/j.issn.1007-1865.2016.14.102 |
| [12] |
张静, 张彦波. 用ICP-MS测定食品用复合塑料薄膜中的铅、铬及其不确定度评定[J]. 塑料科技, 2013, 41(5): 100. ZHANG J, ZHANG YB. Determination of lead and chromium in laminated film used for wrapping food by ICP-MS and evaluation of uncertainty[J]. Plast Sci Technol, 2013, 41(5): 100. |
 2018, Vol. 38
2018, Vol. 38 
