2. 天士力控股集团有限公司研究院现代中药开发中心, 天津 300410;
3. 天士力医药集团股份有限公司创新中药关键技术国家重点实验室, 天津 300410
2. Modern TCM Research Center, Tasly Academy in Tasly Holding Group Co., Ltd., Tianjin 300410, China;
3. State Key Laboratory of Core Technology in Innovative Chinese Medicine, Tasly Pharmaceutical Group Co., Ltd., Tianjin 300410, China
三黄睛视明丸由生蒲黄、炙黄芪、三七等8味药材采用现代制药技术制备而成,具有凉血散结和益气化瘀的功效。生蒲黄可止血、化瘀、利尿、通淋[1-2],其有效成分如香蒲新苷、异鼠李素-3-O-新橙皮苷可抑制血小板聚集[3];黄芪具有益气补中、升阳的功效[4],其中毛蕊异黄酮苷作为含量最高的活性成分,能够抗氧化和抗炎[5],而芒柄花苷具有提高免疫功能、抗氧化、清除自由基和抗心肌缺血等药理作用[6-7];三七生用可消肿止痛、止血化瘀,其主要有效成分皂苷类具有活血补血、镇痛镇静、抗炎、降血压等生理活性[8-9]。中药复方成分复杂,具有多组分多靶点协同作用的特点[10],使得传统的单一成分质量控制模式,已无法全面、准确地对中药复方进行质量评价。以多味药材中含有的多种成分作为质控指标,是目前对复方实现全面质控的发展方向[11]。本实验建立高效、快速的三黄睛视明丸中香蒲新苷、毛蕊异黄酮苷、异鼠李素-3-O-新橙皮苷、芒柄花苷、三七皂苷R1及人参皂苷多成分含量测定方法,为更准确有效地控制和评价三黄睛视明丸的质量提供科学的参考依据。
1 仪器与试药 1.1 仪器Waters公司超高效液相色谱(ACQUITY UPLC)仪(包括QSM二元溶剂管理器、二极管阵列检测器(PDA)、SM-FTN样品管理器、CH-A型柱温箱、Empower 3色谱工作站);昆山市超声仪器公司KQ-500DB型数控超声波清洗器(功率200 W,频率40 kHz);Mettler Toledo公司Xs205DU型十万分之一分析天平;密理博公司Milli Q超纯水系统;Thermo公司ST 16R离心机。
1.2 试药对照品:香蒲新苷(批号111573-201405,含量以97.0%计)、毛蕊异黄酮苷(批号111920-201505,含量以97.1%计)、异鼠李素-3-O-新橙皮苷(批号111571-201205,含量以93.2%计)、三七皂苷R1(批号110745-201318,含量以94.0%计)、人参皂苷Rg1(批号110703-201731,含量以93.6%计)、人参皂苷Re(批号110754-201324,含量以92.7%计)、人参皂苷Rb1(批号110704-201625,含量以95%计)、人参皂苷Rd(批号111818-201302,含量以94.2%计)均购自中国食品药品检定研究院;芒柄花苷(批号SD1510,含量以98%计)购自天津一方科技有限公司。3批三黄睛视明丸(批号分别为20160901、20160902、20160903)均由天士力控股集团有限公司生产。色谱级乙腈、甲醇(默克公司);水为纯化水。
2 方法与结果 2.1 色谱条件与系统适用性Waters Acquity UPLC® BEH C18色谱柱(2.1 mm×100 mm,1.7 μm);流动相水(A)-乙腈(B),梯度洗脱(0~2 min,5%B→10%B;2~4 min,10%B→15%B;4~7 min,15%B→19%B;7~12 min,19%B;12~19 min,19%B→28%B;19~25 min,28%B→40%B;25~28 min,40%B→50%B;28~31 min,50%B→53%B;31~38 min,53%B→90%B;38~39 min,90%B→99%B;39~40 min,99%B),流速0.3 mL·min-1,柱温30 ℃,检测波长203 nm,进样体积2 μL。40 min内所有组分可全部洗脱,理论塔板数以三七皂苷R1计不低于4 000。
2.2 溶液的制备 2.2.1 混合对照品储备液取香蒲新苷、毛蕊异黄酮苷、异鼠李素-3-O-新橙皮苷、芒柄花苷、三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、人参皂苷Rd的对照品适量,精密称定,甲醇超声溶解,并制成每1 mL含香蒲新苷18.469 μg,毛蕊异黄酮苷18.313 μg,异鼠李素-3-O-新橙皮苷18.099 μg,芒柄花苷9.545 2 μg,三七皂苷R1 385.02 μg,人参皂苷Rg1 1 036.3 μg,人参皂苷Re 305.17 μg,人参皂苷Rb1 782.04 μg和人参皂苷Rd 189.53 μg的混合溶液(各对照品浓度值为根据对照品实际含量折算后的浓度),即得。
2.2.2 供试品溶液将本品研细,取1 g,精密称定,于锥形瓶中,加甲醇20 mL,密塞,称量,超声(功率200 W,频率40 kHz)处理20 min,取出并冷却至室温,再次称量,用甲醇补足减失的量并摇匀,12 000 r·min-1离心10 min,取上清液,用0.22 μm微孔滤膜滤过,取续滤液,即得。
2.2.3 阴性样品溶液按处方比例和制备工艺,分别制备不含生蒲黄、炙黄芪、三七的阴性样品,按“2.2.2”项下方法制得各阴性样品溶液。
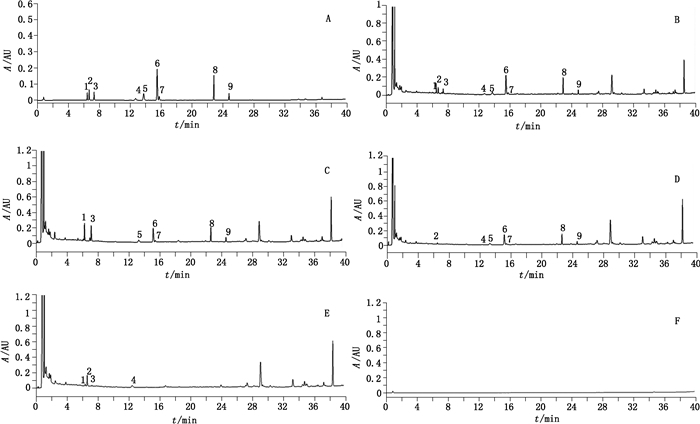
2.3 方法学考察 2.3.1 专属性试验分别精密吸取上述混合对照品溶液、供试品溶液、各阴性样品溶液、空白溶剂各2 μL,在“2.1”项条件下进行测定。结果9个成分与相邻峰分离度均大于1.5,空白溶剂和其他物质对9个成分的测定无干扰,表明该方法专属性强,见图 1。
|
1.香蒲新苷(typhaneoside)2.毛蕊异黄酮苷(calycosin-7-O-β-D-glucopyranoside)3.异鼠李素-3-O-新橙皮苷(isorhamnetin-3-O-neohesperidoside)4.芒柄花苷(ononin)5.三七皂苷R1(notoginsenoside R1)6.人参皂苷Rg1(ginsenoside Rg1)7.人参皂苷Re(ginsenoside Re)8.人参皂苷Rb1(ginsenoside Rb1)9.人参皂苷Rd(ginsenoside Rd) A.混合对照品(mixed reference substances)B.样品(sample)C.缺炙黄芪阴性样品(negative sample without Astragali Radix Praeparata Cum Melle)D.缺生蒲黄阴性样品(negative sample without Typhae Pollen)E.缺三七阴性样品(negative sample without Notoginseng Radix et Rhizoma)F.空白溶剂(blank solvent) 图 1 UPLC色谱图 Figure 1 UPLC chromatograms |
精密吸取“2.2.1”项下配制的混合对照品储备液8、6、5.2、4.6、2.5、0.5 mL,加甲醇分别定容至10 mL量瓶中,即得系列混合对照品溶液。精密吸取包括混合对照品储备液在内的7份不同浓度的混合对照品溶液各2 μL,注入液相色谱仪,记录色谱图。以进样量(ng)为横坐标,以峰面积积分值为纵坐标,绘制标准曲线,计算线性回归方程,见表 1。结果表明在一定进样量范围内,9个成分均有较好的线性关系。
|
|
表 1 9个成分的回归方程及线性范围 Table 1 Regression equations and linear ranges of nine components |
精密吸取混合对照品溶液2 μL,在“2.1”项色谱条件下,连续进样6次,记录色谱图,计算峰面积的RSD,结果香蒲新苷、毛蕊异黄酮苷、异鼠李素-3-O-新橙皮苷、芒柄花苷、三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、人参皂苷Rd峰面积的RSD分别为0.55%、1.4%、0.25%、1.2%、1.0%、1.2%、0.44%、1.2%、0.65%,均符合要求,表明仪器精密度良好。
2.3.4 稳定性试验精密吸取供试品溶液(样品批号20160901),分别于0、2、4、6、12、16、18、24 h按“2.1”项色谱条件进样2 μL,记录峰面积,结果香蒲新苷、毛蕊异黄酮苷、异鼠李素-3-O-新橙皮苷、芒柄花苷、三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、人参皂苷Rd峰面积的RSD分别为2.1%、2.1%、2.2%、1.8%、0.94%、1.7%、0.58%、1.8%、0.77%,表明在24 h内供试品溶液稳定性较好。
2.3.5 重复性试验取批号20160901的样品按“2.2.2”项下方法平行制备6份供试品溶液,精密吸取2 μL进样测定,记录色谱图。按外标法计算香蒲新苷、毛蕊异黄酮苷、异鼠李素-3-O-新橙皮苷、芒柄花苷、三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、人参皂苷Rd的平均含量分别为0.261、0.196、0.193、0.111、2.728、12.196、3.235、8.464、2.229 mg·g-1,RSD分别为0.60%、0.98%、1.8%、0.90%、1.2%、0.59%、1.9%、0.99%、0.68%,表明该方法重复性良好。
2.3.6 加样回收率试验精密称取“2.3.5”项下已测知含量的样品(批号20160901)0.5 g,共6份,分别精密加入“2.2.1”项下制备的混合对照品储备液5 mL,再精密加入甲醇15 mL,按“2.2.2”项下方法制备加样供试溶液,精密吸取2 μL进样测定,记录色谱图,计算回收率。结果表明该方法准确度良好,见表 2。
|
|
表 2 9个成分的加样回收率试验结果(n=6) Table 2 Results of recovery tests of nine components |
精密吸取3批三黄睛视明丸制得的供试品溶液各2 μL,在“2.1”项色谱条件下进样测定,记录峰面积,按外标法计算样品中9个成分的含量,结果见表 3。
|
|
表 3 3批样品中9个成分的含量(n=2) Table 3 Contents of nine components of three samples |
随着社会经济的发展和国际交流的增加,如何建立一个现代化、国际化的现代中药质量控制体系是中药研究的重中之重。目前,由于中药对照品缺乏等一些客观因素的存在,大多对代表性成分进行定量分析,一定程度上能够有效保证中药质量,但无法从整体上对其进行控制[12]。因此,本课题前期建立了三黄睛视明丸指纹图谱质量控制方法,并对共有峰进行了指认[13]。由于指纹图谱的模糊性,很难精确比较制剂批次间质量[14],故本研究在结合指纹图谱质控方法的基础上,建立了三黄睛视明丸中9个共有峰同时定量测定的方法,尽可能全面地表现出该复方的内在质量[15],所建立的方法快速准确,简便高效,重复性好,可作为三黄睛视明丸质量控制和评价的方法。
| [1] |
王潇毅, 田晓轩, 张砚, 等. 基于活性筛选和靶标网络预测的蒲黄和赤芍选择性抑制血小板聚集作用[J]. 中国实验方剂学杂志, 2017, 23(1): 120. WANG XY, TIAN XX, ZHANG Y, et al. Selective inhibitory effect of Typhae Pollen and Paeoniae Radix Rubra on platelet aggregation based on activity screening and target network prediction[J]. Chin J Exp Tradit Med Form, 2017, 23(1): 120. |
| [2] |
焦增华, 杨亚军, 刘希望, 等. 蒲黄药理作用研究进展[J]. 中兽医医药杂志, 2017, 36(3): 85. JIAO ZH, YANG YJ, LIU XW, et al. Research advances in extraction and detection of ursolic acid and oleanolic acid[J]. J Tradit Chin Vet Med, 2017, 36(3): 85. |
| [3] |
胡立宏, 房士明, 刘虹, 等. 蒲黄的化学成分和药理活性研究进展[J]. 天津中医药大学学报, 2016, 35(2): 136. HU LH, FANG SM, LIU H, et al. Research progress in chemical ingredients and pharmacoactive of Puhuang[J]. J Tianjin Univ TCM, 2016, 35(2): 136. |
| [4] |
祁晓霞, 董宇, 单晨啸, 等. 基于UFLC-Q-TOF/MS分析黄芪-丹参药对化学成分研究[J]. 南京中医药大学学报, 2017, 33(1): 93. QI XX, DONG Y, SHAN CX, et al. Analysis of the main components in herbal pair:Astragali Radix and Salviae Miltiorrhizae by UFLC-Q-TOF/MS[J]. J Nanjing Univ Tradit Chin Med, 2017, 33(1): 93. |
| [5] |
石剑.黄芪中异黄酮成分的药代动力学特征及肝肠处置机制研究[D].广州: 南方医科大学, 2016 SHI J.Pharmacokinetics and Enterohepatic Disposition of Isoflavonoids of Astragali Radix[D].Guangzhou: Southern Medical University, 2016 http://cdmd.cnki.com.cn/Article/CDMD-12121-1016266549.htm |
| [6] |
屠万倩, 张留记, 徐贞贞. HPLC法同时测定益心血脂康胶囊中3种成分[J]. 中成药, 2017, 39(2): 316. TU WQ, ZHANG LJ, XU ZZ. Simultaneous determination of three constituents in Yixin Xuezhikang capsules by HPLC[J]. Chin Tradit Pat Med, 2017, 39(2): 316. |
| [7] |
张蔚, 江曙, 钱大玮, 等. 芒柄花苷与人体肠道细菌的相互作用研究[J]. 药学学报, 2014, 49(8): 1162. ZHANG W, JIANG S, QIAN DW, et al. The interaction between ononin and human intestinal bacteria[J]. Acta Pharm Sin, 2014, 49(8): 1162. |
| [8] |
宋侠. 三七皂苷药理作用研究进展[J]. 中国现代药物应用, 2017, 11(14): 174. SONG X. Recent advances in the research of pharmacological activities of Panax notoginseng saponins[J]. Chin J Mod Drug Appl, 2017, 11(14): 174. |
| [9] |
泰瑞清, 谈文状, 杨恩, 等. LC-MS分析三七根腐病的皂苷类成分变化[J]. 昆明理工大学学报(自然科学版), 2015, 40(6): 85. TAI RQ, TAN WZ, YANG E, et al. Variation of saponins in Panax notoginseng root rot diseases by LC-MS[J]. J Kunming Univ Sci Technol (Nat Sci Ed), 2015, 40(6): 85. |
| [10] |
张华, 刘俊萍, 王菲菲, 等. 五味沙棘颗粒特征图谱及含量测定方法研究[J]. 药物分析杂志, 2017, 37(9): 1627. ZHANG H, LIU JP, WANG FF, et al. Study on characteristic fingerprint and quantitative analysis of Wuwei Shaji granules[J]. Chin J Pharm Anal, 2017, 37(9): 1627. |
| [11] |
王艳伟, 王青晓, 王晓伟, 等. HPLC波长切换法测定麦味地黄胶囊中5种有效成分的含量[J]. 药物分析杂志, 2017, 37(9): 1601. WANG YW, WANG QX, WANG XW, et al. Simultaneous determination of five constituents in Maiwei Dihuang capsules by HPLC with wavelength switching[J]. Chin J Pharm Anal, 2017, 37(9): 1601. |
| [12] |
徐容. 妇科千金片HPLC特征指纹图谱及多成分含量测定[J]. 中国实验方剂学杂志, 2017, 23(11): 84. XU R. Fingerprint and multi-component quantitative determination of Fuke Qianjin tablets by HPLC[J]. Chin J ExpTradit Med Form, 2017, 23(11): 84. |
| [13] |
吕燕男, 夏忠庭, 李响, 等. 三黄睛视明丸UPLC指纹图谱[J]. 中成药, 2018, 40(4): 880. LÜ YN, XIA ZT, LI X, et al. UPLC fingerprints of Sanhuang Jingshiming pills[J]. Chin Tradit Pat Med, 2018, 40(4): 880. DOI:10.3969/j.issn.1001-1528.2018.04.023 |
| [14] |
杨秀青, 石征蓉, 谷江华, 等. 银菊解毒口服液指纹图谱结合多指标成分定量测定的质量控制方法研究[J]. 中草药, 2017, 48(13): 2645. YANG XQ, SHI ZR, GU JH, et al. Quality assessment of Yinju Jiedu oral liquid based on HPLC fingerprint and multi-components simultaneous determination[J]. Chin Tradit Herb Drugs, 2017, 48(13): 2645. |
| [15] |
翟宏宇, 王海洋, 杨献玲, 等. 保心宁片HPLC特征图谱研究及8个指标性成分的含量测定[J]. 药物分析杂志, 2017, 37(9): 1633. ZHAI HY, WANG HY, YANG XL, et al. Study on HPLC specific chromatogram of Baoxinning tablets and simultaneous determination of its eight index components[J]. Chin J Pharm Anal, 2017, 37(9): 1633. |
 2018, Vol. 38
2018, Vol. 38 
