2. 吉化集团公司总医院, 吉林 132021
2. The General Hospital of CNPC in Jilin, Jilin 132021, China
栀芩清热合剂由栀子、黄芩、甘草、淡竹叶、连翘、薄荷油共6味药材组成,主要用于治疗三焦热毒产生的发热,口渴,尿赤[1],其中栀子有泻火除烦、凉血解毒、清利湿热的功效。栀子中主要活性成分有京尼平苷酸、京尼平龙胆双糖苷、京尼平苷、绿原酸;黄芩中的活性成分有黄芩苷、汉黄芩苷、黄芩素等,具有凉血解毒、清热燥湿的效果,主要治疗上呼吸道感染引起的肺炎、疮疥等病症;甘草中含有甘草酸,甘草性温,可以清热解毒、祛痰止咳,且可以调和各味中药[2]。栀芩清热合剂为《中华人民共和国药典》(简称《中国药典》)2015年版新收录的中药制剂,但只测定其中京尼平苷的含量,对其他成分未有规定,不利于整体控制药品质量,而有关栀芩清热合剂的含量测定和质量控制文献较少,都是单独测定其中黄芩苷的含量[3-5],目前未见同时测定此药多种组分含量的报道。本文建立了高效液相色谱法同时测定京尼平苷酸、京尼平龙胆双糖苷、京尼平苷、黄芩苷、汉黄芩苷、甘草酸、黄芩素、绿原酸8个成分的含量,对于栀芩清热合剂的质量控制具有重要意义。
1 仪器与试剂 1.1 仪器岛津公司LC-20AT高效液相色谱仪,包括SPD-M20A二极管阵列检测器、SIL-20A自动进样器、岛津LC-solution工作站;迪马科技有限公司DIKMA Platisil ODS色谱柱(250 mm×4.6 mm,5 μm;填料:十八烷基硅烷键合硅胶);Millipore公司Synergy 185超纯水仪,昆山市超声仪器有限公司KQ-250DE型数控超声波清洗器。
1.2 试剂对照品京尼平苷酸(批号111828-201403,纯度≥97.4%)、京尼平苷(批号110749-201316,纯度≥97.6%)、黄芩苷(批号110715-200514,纯度≥93.5%)、汉黄芩苷(批号112002-201501,纯度≥98.5%)、甘草酸(批号110731-201418,纯度≥93.0%)、黄芩素(批号111595-201306,纯度≥98.5%)、绿原酸(批号110753-201415,纯度≥99.3%)均购自中国食品药品检定研究院,京尼平龙胆双糖苷(批号141120,纯度≥98%)购自成都普菲德生物技术有限公司;栀芩清热合剂(批号150901,160702,170301,广东万年青制药有限公司)。乙腈为色谱纯,水为超纯化水,其他试剂均为分析纯。
2 方法与结果 2.1 溶液的制备 2.1.1 对照品溶液取0.117 mg·mL-1的京尼平苷酸的对照品溶液0.7 mL,0.100 mg·mL-1的京尼平龙胆双糖苷对照品溶液0.5 mL,0.108 mg·mL-1的京尼平苷的对照品溶液1.5 mL,0.57 mg黄芩苷对照品,0.105 mg·mL-1的汉黄芩苷的对照品溶液0.2 mL,0.109 mg·mL-1的甘草酸的对照品溶液0.5 mL,0.119 mg·mL-1的黄芩素的对照品溶液0.5 mL以及0.5 mL的0.082 mg·mL-1的绿原酸对照品溶液,将其置于同一10 mL量瓶中,用甲醇定容,制成含京尼平苷酸0.081 9 mg·mL-1、京尼平龙胆双糖苷0.005 mg·mL-1、京尼平苷0.016 2 mg·mL-1、黄芩苷0.057 mg·mL-1、汉黄芩苷0.002 1 mg·mL-1、甘草酸0.005 45 mg·mL-1、黄芩素0.005 95 mg·mL-1、绿原酸0.004 1 mg·mL-1的混合对照品溶液。
2.1.2 供试品溶液精密量取栀芩清热合剂1.25 mL,置25 mL量瓶中,加70%甲醇水至刻度,摇匀,滤过,称量,精密量取续滤液1.0 mL,置10 mL量瓶中,加70%甲醇水至刻度,摇匀,即得供试品溶液[1]。
2.1.3 阴性样品溶液按处方分别制备缺少栀子、黄芩、甘草的阴性样品,按“2.2”项方法操作,即得阴性样品溶液。
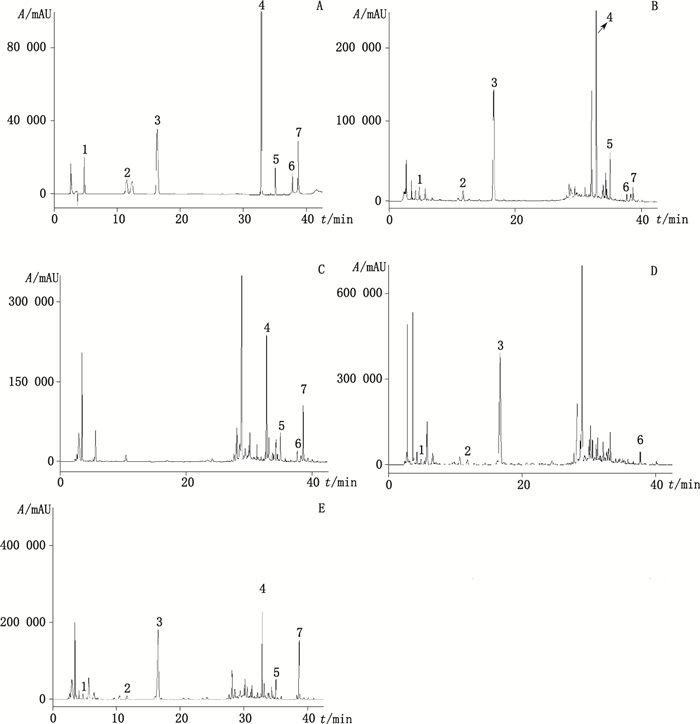
2.2 色谱条件色谱柱:DIKMA Platisil ODS(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱(0~20 min,10%A→16%A;20~30 min,16%A→40%A;30~50 min,40%A→80%A);流速:1 mL·min-1;柱温:30 ℃;检测波长:240 nm(京尼平苷酸、京尼平龙胆双糖苷、京尼平苷、黄芩苷、汉黄芩苷、甘草酸、黄芩素)、327 nm(绿原酸);进样量:20 μL。在上述色谱条件下,各待测组分分离度均大于1.5,理论塔板数均大于5 000。混合对照品溶液、样品溶液及各阴性样品溶液色谱图见图 1、图 2。
|
1.京尼平苷酸(geniposidic acid)2.京尼平龙胆双糖苷(genipin 1-gentiobioside)3.京尼平苷(geniposide)4.黄芩苷(baicalein)5.汉黄芩苷(wogonoside)6.甘草酸(glycyrrhizic acid)7.黄芩素(baicalein) 图 1 混合对照品(A)、样品(B)、不含栀子的阴性样品(C)、不含黄芩的阴性样品(D)和不含甘草的阴性样品(E)在240 nm处色谱图 Figure 1 HPLC chromatograms of mixed reference substances(A), sample(B), negative sample without Common Gardenia Fruit(C), negative sample without Baikal Skullcap Root(D), and negative sample without Liquorice Root(E)at 240 nm |
|
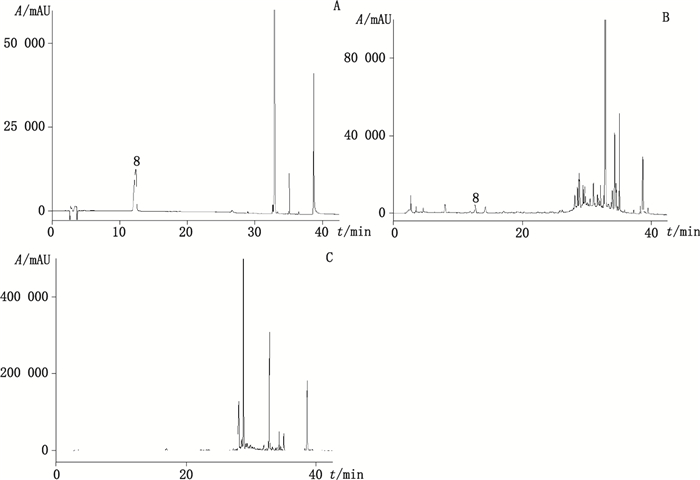
8.绿原酸(chlorogenic acid) 图 2 混合对照品(A)、样品(B)和不含栀子的阴性样品(C)在327 nm处色谱图 Figure 2 HPLC chromatograms of mixed reference substances(A), sample(B), and negative sample without Common Gardenia Fruit(C)at 327 nm |
精密吸取混合对照品溶液1、10、15、20、40、60 μL进样测定;以峰面积(Y)为纵坐标,进样量(X)为横坐标进行线性回归,得京尼平苷酸、京尼平龙胆双糖苷、京尼平苷、黄芩苷、汉黄芩苷、甘草酸、黄芩素、绿原酸的线性回归方程,见表 1。
|
|
表 1 8个成分的线性回归方程 Table 1 Linear regression equations of eight components |
取混合对照品溶液,按“2.2”项下色谱条件连续进样6次,测得混合对照品中京尼平苷酸、京尼平龙胆双糖苷、京尼平苷、黄芩苷、汉黄芩苷、甘草酸、黄芩素、绿原酸峰面积的RSD(n=6)分别为1.1%、0.95%、0.47%、0.28%、1.4%、0.44%、1.2%、1.3%。
2.5 稳定性试验取同一供试品溶液,室温放置,分别于0、2、4、6、12、24 h进行测定,测得京尼平苷酸、京尼平龙胆双糖苷、京尼平苷、黄芩苷、汉黄芩苷、甘草酸、黄芩素、绿原酸峰面积的RSD(n=6)分别为1.4%、1.6%、0.85%、0.48%、1.5%、1.7%、0.76%、1.2%,表明供试品溶液在常温下24 h内稳定。
2.6 重复性试验取栀芩清热合剂样品,按“2.1.2”项下方法平行制备6份供试品溶液,以“2.2”项下色谱条件进行测定,得京尼平苷酸、京尼平龙胆双糖苷、京尼平苷、黄芩苷、汉黄芩苷、甘草酸、黄芩素、绿原酸的平均含量(n=6)分别为1.768 7、1.147 9、10.188 5、11.261 5、2.777 5、1.031、0.973 1、0.178 8 mg·mL-1,RSD分别为1.5%、0.96%、1.3%、0.4%、1.5%、1.2%、1.0%、1.6%。
2.7 加样回收率试验精密称取“2.6”项已测知含量的样品0.6 mL,共9份,平均分为3组,按低、中、高浓度(80%、100%、120%)分别加入一定量的京尼平苷酸、京尼平龙胆双糖苷、京尼平苷、黄芩苷、汉黄芩苷、甘草酸、黄芩素、绿原酸对照品,按照“2.1.2”项下方法制备供试溶液,进样20 μL进行测定,结果见表 2。
|
|
表 2 回收率试验结果(n=9) Table 2 Results of recovery test |
取3批样品,按“2.1.2”项下方法制备供试品溶液,按“2.2”项下色谱条件进样测定,外标法计算待测成分含量,结果见表 3。
|
|
表 3 栀芩清热合剂中8个成分的测定(mg·mL-1,n=3) Table 3 Determination of eight components in Zhiqin Qingre mixture |
由于栀芩清热合剂是《中国药典》2015年版中新收录的中成药,测定其成分含量相关资料很少,在流动相的选择上,首先考察了药典中收录的方法[1],乙腈-水(15: 85)等度洗脱,待测组分不能全部出峰,由于测定的组分较多,等度洗脱较难实现分离,所以笔者接着测试了乙腈-磷酸水、甲醇-磷酸水2个溶剂系统梯度洗脱[6-15],结果发现甲醇-磷酸水为流动相时,栀子中的几个待测组分京尼平苷酸、京尼平龙胆双糖苷、京尼平苷、绿原酸分离不好,与杂质峰重合。而采用乙腈-磷酸水梯度洗脱时,可以达到分离要求。
3.2 波长的选择波长扫描得到绿原酸最大吸收波长为327 nm,黄芩苷、汉黄芩苷、黄芩素为278 nm,甘草酸为250 nm。本实验中,除绿原酸外,其余成分作者选取了240 nm,能兼顾各个组分,色谱图特征性强,各组分的响应值较为均匀,具有良好的代表性。
| [1] |
中华人民共和国药典2015年版.一部[S].2015: 659 Chp 2015.VolⅠ[S].2015: 659 |
| [2] |
陈峻, 徐华, 陈小轩. HPLC同时测定清肺抑火丸中3个苷类成分[J]. 中国实验方剂学杂志, 2013, 19(13): 134. CHEN J, XU H, CHEN XX. Simultaneous determination of three chemical constitutes in Qingfei Yihuo pills by HPLC[J]. Chin J Exp Tradit Med Form, 2013, 19(13): 134. |
| [3] |
赵阿华, 高兴武. HPLC法测定栀芩清热液中黄芩苷的含量[J]. 黑龙江医药, 2008, 21(4): 20. ZHAO AH, GAO XW. Determination of baicalin content in Zhiqin Qingre liquid by HPLC[J]. Heilongjiang Med J, 2008, 21(4): 20. DOI:10.3969/j.issn.1006-2882.2008.04.015 |
| [4] |
任剑雄, 潘梅英, 肖慧, 等. HPLC法测定栀芩清热合剂中黄芩苷的含量[J]. 今日药学, 2011, 21(7): 426. REN JY, PAN MY, XIAO H, et al. Content determination of baicalin in Zhiqin Qingre mixture by HPLC[J]. Pharm Today, 2011, 21(7): 426. |
| [5] |
陶君, 黄怀鹏. 栀芩清热软胶囊质量标准的研究[J]. 天津中医药, 2005, 22(4): 334. TAO J, HUANG HP. Qualitative criteria of Zhiqin Qingre malacotic capsules[J]. Tianjin J Tradit Chin Med, 2005, 22(4): 334. DOI:10.3969/j.issn.1672-1519.2005.04.029 |
| [6] |
杨世艳, 何兵, 张燕. HPLC同时测定银黄颗粒中7种有机酸及4种黄酮类成分[J]. 中草药, 2013, 44(3): 301. YANG SY, HE B, ZHANG Y. Simultaneous determination of seven organic acids and four flavonoids in Yinhuang granules by HPLC[J]. Chin Tradit Herb Drugs, 2013, 44(3): 301. |
| [7] |
郝乘仪, 张慧锋, 杨明慧. RP-HPLC法同时测定小儿肺热咳喘颗粒中两种主要活性成分的含量[J]. 吉林医药学院学报, 2017, 38(1): 18. HAO CY, ZHANG HF, YANG MH. Simultaneuos determination of two main components of Xiao'er Feire Kechuan granules by RP-HPLC[J]. J Jilin Med Coll, 2017, 38(1): 18. |
| [8] |
荆玉玲. 高效液相色谱法测定利咽口服液中绿原酸的含量[J]. 中国医院用药评价与分析, 2016, 16(12): 175. JING YL. Content determination of chlorogenic acid in Liyan oral liquid by HPLC[J]. Evaluat Anal Drug-Use Hosp China, 2016, 16(12): 175. |
| [9] |
郝乘仪, 冯波, 郭淑英, 等. 黄连上清片中9种成分的HPLC波长切换法测定[J]. 中国医药工业杂志, 2015, 46(9): 995. HAO CY, FENG B, GUO SY, et al. Determination of nine compounds in Huanglian Shangqing tablets by HPLC combined with wavelength switching method[J]. Chin J Pharm, 2015, 46(9): 995. |
| [10] |
郭东晓, 林林, 汪冰, 等. HPLC波长切换法同时测定抗感颗粒中7个成分的含量[J]. 药物分析杂志, 2015, 35(10): 1796. GUO DX, LIN L, WANG B, et al. Simultaneous determination of the content of seven components in Kanggan granules by HPLC wavelength switching technology[J]. Chin J Pharm Anal, 2015, 35(10): 1796. |
| [11] |
龙厚宁, 印酬, 孟小夏, 等. HPLC同时测定炎热清软胶囊中栀子苷黄芩苷和汉黄芩苷的含量[J]. 中国实验方剂学杂志, 2016, 22(6): 34. LONG HN, YIN C, MENG XX, et al. Simultaneous detemination of geniposide, baicalin and wogonoside inYanreqing soft capsules by HPLC[J]. Chin J Exp Tradit Med Form, 2016, 22(6): 34. |
| [12] |
陈帅, 王磊, 高双, 等. HPLC-DAD法同时测定加味逍遥丸中8种成分[J]. 中草药, 2016, 47(21): 3829. CHEN S, WANG L, GAO S, et al. Simultaneous determination of eight components in Jiawei Xiaoyao pills by HPLC-DAD[J]. Chin Tradit Herb Drugs, 2016, 47(21): 3829. |
| [13] |
蔡建明, 欧阳臻, 赵明, 等. HPLC法同时测定参梅养胃颗粒中4种成分[J]. 中成药, 2016, 38(11): 2391. CAI JM, OU YANG Z, ZHAO M, et al. Simultaneous determination of four constituents in Shenmei Yangwei granules by HPLC[J]. Chin Tradit Pat Med, 2016, 38(11): 2391. |
| [14] |
郭丽, 贾金艳, 李霞, 等. RP-HPLC法同时测定强力天麻杜仲胶囊中6种成分[J]. 中成药, 2016, 38(8): 1744. GUO L, JIA JY, LI X, et al. Simultaneous determination of six constituents in Qiangli Tianma Duzhong capsules by RP-HPLC[J]. Chin Tradit Pat Med, 2016, 38(8): 1744. |
| [15] |
张琳, 汪轩, 邢婧, 等. HPLC-DAD同时测定左归丸药液中没食子酸、原儿茶酸、绿原酸、马钱苷、阿魏酸含量[J]. 药物分析杂志, 2016, 36(8): 1364. ZHANG L, WANG X, XING J, et al. Simultaneous determination of gallic acid, protocatechuic acid, chlorogenic acid, loganin and ferulic acid of herb liquor of Zuogui pills by HPLC[J]. Chin J Pharm Anal, 2016, 36(8): 1364. |
 2018, Vol. 38
2018, Vol. 38 
