2. 广西壮族自治区食品药品检验所, 南宁 530021
2. Guangxi Institute for Food and Drug Control, Nanning 530021, China
核磁共振定量(qNMR)技术已经被包括《中华人民共和国药典》、美国药典与欧洲药典在内的各药典收载[1-4],qNMR法是一种绝对定量法,可以直接计算得到待测样品的含量,不受样品中含有的水分、灰分或无机盐等的干扰。qNMR方法包括内标加入法以及外标曲线法,由于外标法对仪器以及实验环境要求更为严苛,内标加入法更为常用。理论上每种有核磁共振响应的核素都可以作为被检测核进行定量测定,但是由于13C及15N等元素的自然丰度较低,结构中不同化学环境核的弛豫时间差异大,为了满足定量的要求,需要采用特殊的门控技术,检测时间过长,实际工作中较少使用对此类元素作为观测核进行定量测定。
1H由于广泛存在于有机药物分子中,且响应较高,弛豫时间短定量准确性好,一直是qNMR试验中应用最多的检测元素[5-7],但是1H试验中响应信号容易重叠以及易受杂质干扰,使这种方法的应用受到一定的限制。19F qNMR试验虽然仅适用于含氟的药物,但是其检测灵敏度高,时间短且很少发生响应信号重叠,是除了1H之外1种很适用于qNMR的磁性核。之前系统研究了利用19F qNMR技术测定含氟原料药中的药物含量[8-10],证明了19F qNMR方法的可行性。这种方法是否能不受辅料等的干扰,直接应用于含氟药物制剂含量研究还未见报道。本文中使用19F qNMR技术测定了卡格列净片剂中卡格列净含量,对可能的影响因素进行了系统的研究,并与传统的高效液相法结果进行了对比。
卡格列净片,商品名Invokana,原研厂家为美国强生制药公司,于2013年获FDA批准在美国上市,是第1个被批准用于糖尿病治疗的钠-葡萄糖协同转运蛋白2(SGLT2)药物,片剂规格为100 mg及300 mg,其中含有乳糖、微晶纤维素、羟丙基纤维素、交联羧甲基纤维素钠、硬脂酸镁、聚乙烯醇、聚乙二醇及二氧化钛等辅料。卡格列净分子结构见图 1,其中含有1个分子氟,虽然辅料较多,但均不含有氟,不干扰19F测定。

|
图 1 卡格列净分子结构 Figure 1 Chemical structure of canagliflozin |
Bruker Ascend 500型核磁共振仪(布鲁克公司),5 mm PABBO探头及Topspin3.2试验控制及数据处理软件;Waters高效液相色谱仪(Waters公司),Agilent Zorbax C18(150 mm×4.6 mm,3 μm)色谱柱;Mettler Toledo XP205电子天平(0.01 mg,梅特勒公司)。
1.2 样品及试剂卡格列净片(300 mg·片-1,公司A),卡格列净工作对照品(99.8%,公司A),氘代DMSO(> 99.9%,Sigma),4,4′-二氟二苯甲酮(含量99.0%,TCI Chemicals),乙腈(色谱纯,Fisher),三氟乙酸(色谱纯,Fisher),水(18.2 MΩ,实验室自制)。
2 方法与结果 2.1 核磁共振样品溶液制备取本品1片,精密称定后研细,精密称取细粉约20 mg(含卡格列净约10 mg),同时精密称取4,4′-二氟二苯甲酮约10 mg,置同一容器中,加DMSO-d6 2 mL后漩涡震荡1 min,使用0.45 μm尼龙膜滤过或在3 000 g离心5 min,取澄清溶液0.7 mL置5 mm核磁管中进行19F核磁共振定量测定
2.2 核磁共振实验条件采用zgfhigqn.2脉冲序列在恒温(25 ℃)下获取19F NMR谱。具体试验参数设置如下:谱宽SW=40×10-6,射频中心频率O1P为-110×10-6,采样点数TD为128 k,采样时间AQ为3.5 s,弛豫延迟时间D1为20 s,扫描次数为32次,增益(RG)为280。
2.3 HPLC试验样品制备及测定精密称取“2.1”项下细粉约100 mg,置500 mL量瓶中,加乙腈-水400 mL,机械振摇45 min,加乙腈-水(50:50)稀释至刻度,摇匀,静置20 min。精密量取8 mL,置100 mL量瓶中,加乙腈-水(50:50)稀释至刻度,混匀,用0.45 μm PTFE滤膜滤过,弃去初滤液2 mL,取续滤液作为供试品溶液。
按此药品标准中HPLC测定方法:使用Agilent Zorbax C18(150 mm ×4.6 mm,3 μm)色谱柱;流动相A为乙腈-水(5:95)(含0.02%三氟乙酸),流动相B为乙腈-水(95:5)(含0.02%三氟乙酸),梯度计洗脱,按外标法以峰面积计算含量。
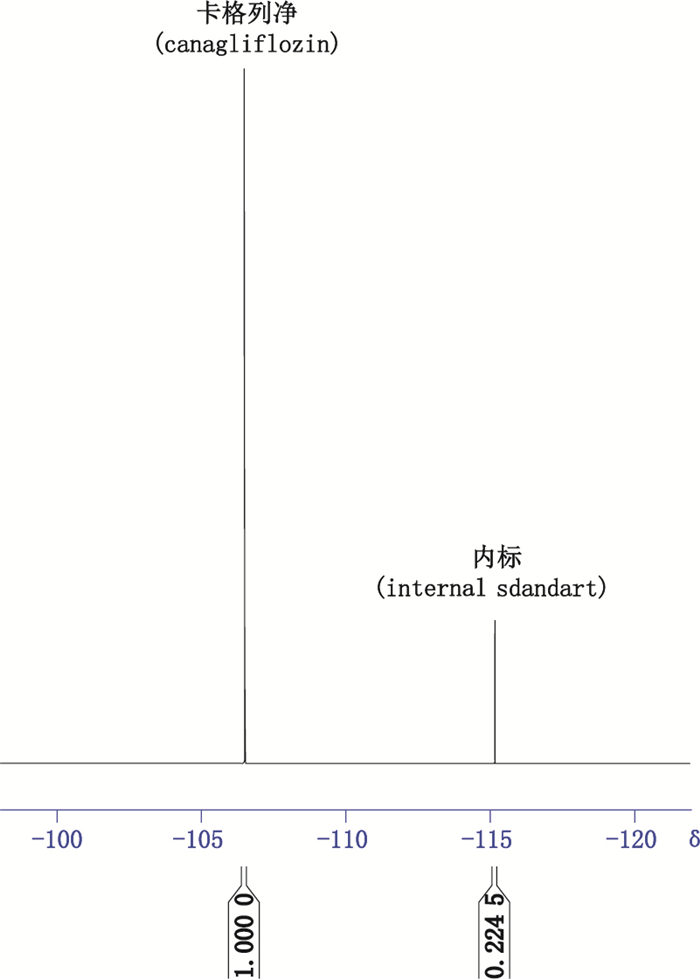
2.4 图谱测定按“2.1”项下方法配制供试品溶液,在“2.2”项下试验条件下测定卡格列净和内标混合溶液的19F qNMR谱,所得氟响应信号峰如图 2所示。卡格列净的单一响应信号出现在δ-106,内标的响应信号为δ-115,样品与内标的响应信号分离较好,相互不产生重叠干扰,也未有任何辅料产生干扰信号。
|
图 2 19F NMR响应信号及归属 Figure 2 19F NMR spectrum and assignments |
分别精密称取卡格列净片剂粉末20~60 mg,和4,4′-二氟二苯甲酮约10 mg混合,加氘代DMSO使待测样品浓度为5~15 mg·mL-1,在3 000 g下离心5 min后取上清液,按“2.2”项下试验条件测定19F qNMR谱,记录响应信号面积,以δ-106处样品响应信号和δ-115处内标响应信号比值为横坐标,样品和4,4′-二氟二苯甲酮质量比为纵坐标做线性回归,计算得回归方程为:
| $ Y=4.169X+0.0148\ \ \ \ \ \ {{r}^{2}}=0.9998 $ |
表明卡格列净质量浓度在5~15 mg·mL-1线性关系良好。
2.5.2 精密度及稳定性按“2.1”项下方法制备供试品溶液,在“2.2”项下试验条件下连续测定6次,记录响应信号面积,其样品与内标响应信号面积比的RSD为0.26%(n=6)。取同一供试品溶液在12 h后再次测定,2次测定样品响应信号面积比未发生明显变化,从试验结果可以看出该方法的精密度较高且样品在室温下放置12 h稳定。
2.5.3 含量测定按“2.1”项下方法平行制备6份样品,采用δ -106处样品定量信号与δ -115处内标定量信号,按下式计算片剂中卡格列净含量。
| $ 含量=\frac{\frac{{{A}_{\rm{S}}}}{{{A}_{\rm{r}}}}\times \frac{{{n}_{\rm{r}}}}{{{n}_{\rm{S}}}}\times \frac{{{M}_{\rm{S}}}}{{{M}_{\rm{r}}}}\times {{W}_{\rm{r}}}\times {{m}_{\rm{r}}}}{{{W}_{\rm{S}}}}\times 100% $ |
其中,As为卡格列净响应信号的面积,Ar为内标的响应信号面积,ns为卡格列净响应信号包含的氟原子数(ns=1),nr为内标响应信号包含的氟原子数(nr=1),Ms为卡格列净的相对分子质量(444.5),Mr为内标的相对分子质量(218.2),WS为卡格列净的称样量,Wr为内标的称样量,mr为内标纯度(99.0%)。经计算,5片样品中卡格列净含量分别为标示量的98.2%、98.9%、101.0%、99.7%、99.2%。
为了验证19F qNMR测定含量结果的准确性,同时利用HPLC外标法测定了相同6片中卡格列净的含量。5片中卡格列净含量分别为标示量的99.6%、99.4%、100.1%、100.0%、100.1%。2种分析方法测定含量结果接近,证明19F qNMR技术可以作为制剂中含氟药物含量测定的快速分析方法。
3 讨论 3.1 内标及仪器参数选择氟与氢qNMR对于内标的选择要求是相同的,包括性质稳定,不易引湿,不与待测样品及所用溶剂反应;响应信号较简单且不与待测样品信号产生重叠等[11-13]。氟核磁共振试验中由于辅料等均无响应且氟谱范围比较宽,内标选择比氢谱试验容易。4,4′-二氟二苯甲酮容易获得,纯度较高,因此选为内标。
氟的核磁共振响应较高,与氢响应接近,一般扫描16或者32次即可满足信噪比S/N大于600的要求[14]。本次试验中选择扫描32次。
3.2 弛豫时间的设定在所有的qNMR试验中,弛豫延迟时间都是一项非常重要的参数设定,设定时间过短会直接影响定量测定结果,设定时间较长会降低工作效率。一般弛豫延迟时间的长度应不短于纵向弛豫时间(T1)的5倍[15]。使用反转恢复法测定了样品及内标中氟原子的纵向弛豫时间分别为1.79 s和1.41 s,所以最终弛豫延迟时间设定为20 s。
3.3 样品前处理19F qNMR试验中,由于辅料中不含有氟原子,因此不会产生任何响应信号,不干扰样品及内标的测定。但是由于有些辅料不溶于核磁试验中常用的溶剂,有必要通过物理手段在实验前去除。在充分漩涡振荡溶解后,试验了使用0.45 μm滤膜或3 000 g离心5 min的前处理方法,处理后取澄清液置入核磁管中测定。最后结果表明2种方法对最后定量结果影响没有差异,均可以作为样品前处理手段。
4 结论19F qNMR技术检测灵敏度高,内标物质选择容易。由于常用药品辅料中不含有氟,十分适合复杂基质中以及含氟药物制剂中药物含量的测定。整个测定前处理简单,耗时短,抗干扰能力强,使用溶剂量少,适合大批量含氟药物制剂的高通量测定。
| [1] |
中华人民共和国药典2015年版. 四部[S]. 2015: 441 ChP 2015. Vol Ⅳ[S]. 2015: 441 |
| [2] |
USP 40-NF 35[S]. 2017: 761
|
| [3] |
BP 2017[S]. 2017: Appendix Ⅱ C
|
| [4] |
EP 9. 0[S]. 2017: 2. 2. 33
|
| [5] |
HOLZGRABE U. Quantitative NMR spectroscopy in pharmaceutical applications[J]. Prog Nucl Magn Reson Spectrosc, 2010, 57(2): 229. DOI:10.1016/j.pnmrs.2010.05.001 |
| [6] |
张芬芬, 蒋孟虹, 沈文斌, 等. 定量核磁共振(QNMR)技术及其在药学领域的应用进展[J]. 南京师范大学学报, 2014, 14(2): 8. ZHANG FF, JIANG MH, SHEN WB, et al. Progress in quantitative nuclear magnetic resonance technology in pharmaceutical applications[J]. J Nanjing Norm Univ, 2014, 14(2): 8. DOI:10.3969/j.issn.1672-1292.2014.02.002 |
| [7] |
张才煜, 吴建敏, 李憬, 等. 核磁共振法定量测定氢溴酸东莨菪碱的绝对含量[J]. 药物分析杂志, 2012, 32(2): 327. ZHANG CY, WU JM, LI J, et al. , Quantitative nuclear magnetic resonance determination of the absolute content of scopolamine hydrobromide[J]. Chin J Pharm Anal, 2012, 32(2): 327. |
| [8] |
LIU Y, LIU ZX, LIN L, et al. Direct comparison of 19F qNMR and 1H qNMR by characterizing atorvastatin calcium content[J/OL]. J Anal Methods Chem, 2016, 7627823/1-5[2016-08-09]. https://www.hindawi.com/journals/jamc/2016/7627823/
|
| [9] |
刘阳, 魏宁漪, 岳瑞齐, 等. 新型19F核磁共振定量技术测定氟哌利多含量[J]. 中国新药杂志, 2014, 23(16): 1960. LIU Y, WEI NY, YUE RQ, et al. Application of novel 19F quantitative NMR(19F-qNMR)in assay of droperidol[J]. Chin J New Drugs, 2014, 23(16): 1960. |
| [10] |
刘阳, 魏宁漪, 张琪, 等. 19F核磁共振定量技术测定酒石酸吉米格列汀倍半水合物含量[J]. 药物分析杂志, 2014, 34(7): 1197. LIU Y, WEI NY, ZHANG Q, et al. Quantitative analysis of gemigliptin tartrate sesquihydrate by 19F quantitative NMR(19F-qNMR)[J]. Chin J Pharm Anal, 2014, 34(7): 1197. |
| [11] |
PAULI GF, GODECKE T, dc JAKI BU, et al. , Quantitative 1H-NMR development and potential of an analytical method:an update[J]. J Nat Prod, 2012, 75(4): 834. DOI:10.1021/np200993k |
| [12] |
于小波, 沈文斌, 相秉仁. 定量核磁共振技术及其在药学领域中的应用进展[J]. 药学进展, 2010, 34(1): 17. YU XB, SHEN WB, XIANG BR. Advances in application of quantitative nuclear magnetic resonance technique in pharmaceutical field[J]. Prog Pharma Sci, 2010, 34(1): 17. DOI:10.3969/j.issn.1001-5094.2010.01.003 |
| [13] |
刘英, 胡昌勤. 核磁共振在抗生素药物定量分析中的应用[J]. 药物分析杂志, 2001, 21(6): 447. LIU Y, HU CQ. Application of NMR in quantitative analysis of antibiotics[J]. Chin J Pharm Anal, 2001, 21(6): 447. |
| [14] |
DIXON AM, LARIVE CK. Modified pulsed-field gradient NMR experiments for improved selectivity in the measurement of diffusion coefficients in complex mixtures:application to the analysis of the Suwannee River fulvic acid[J]. Anal Chem, 1997, 69(11): 2122. DOI:10.1021/ac961300v |
| [15] |
PAULI GF, JAKI BU, LANKIN DC. Quantitative 1H NMR:development and potential of a method for natural products analysis[J]. J Nat Prod, 2005, 68(1): 133. DOI:10.1021/np0497301 |
 2018, Vol. 38
2018, Vol. 38 
