2. 河北医科大学, 石家庄 050017
2. Fourth Hospital of Hebei; Medical University, Shijiazhuang 050017, China
风湿性疾病是一类临床常见病[1],发病机制不明,化学治疗一般副作用较大,因而临床多采用中成药来治疗[2]。中成药大多显效慢,疗程长,不法商家为谋求暴利,尝试在其中非法添加某些化学药,以达到明显疗效,常见的主要是非甾体抗炎药(NSAIDs)。NSAIDs具有解热、镇痛、抗炎作用,抗风湿效果显著,但长期大剂量给药可导致一系列严重的不良反应,若在不知情的情况下长期服用含有NSAIDs的药物,会给病人身体健康带来潜在危害[3-4]。近年来,抗风湿类中成药中非法添加化学药物的现象引起了广泛关注,国家食品药品监督管理局于2009年颁布了抗风湿类中成药中非法添加化学药品补充检验办法[5]。
抗风湿类中成药中通常含有多种成分,基质极其复杂,常用的分析方法如薄层色谱鉴别、化学鉴别法选择性较差[6-9];采用色谱法分析时,易出现假阳性结果,其中灵敏度较高的检测手段,对仪器设备的要求较高,且一般需要烦琐的样品前处理步骤[10-18],因此不适于现场快速筛查。
离子迁移谱(IMS)是基于大气压下在电场中进行气相离子分析的一种检测技术[19],灵敏度高,分析速度快,且体积小,便携,因而已广泛应用于毒品、爆炸物的快速检测中,目前在药品安全检测方面也有一定应用,但抗风湿类中成药中非法添加化学药物的IMS法检测尚未见报道[20-23]。
本文利用电喷雾-高效离子迁移谱法(ESI-HPIMS法),对抗风湿类中成药中常见的非法添加药物布洛芬、对乙酰氨基酚、萘普生、吲哚美辛、双氯芬酸钠进行分析,建立了抗风湿类中成药中非法添加NSAIDs类药物的现场快速筛查方法,并对收集到的抗风湿类中成药样品进行了鉴定。
1 仪器与试药Excellims GA2100高效离子迁移谱仪,电喷雾离子源,进样方式为直接进样。VisIon Analysis分析软件(Analysis_2_3_1_23),BP 211D(Sartorius)电子天平,Milli-Q50超纯水系统。
对照品布洛芬(北京莱耀生物科技有限公司,产品批号100179-201406)、对乙酰氨基酚(北京普天同创生物科技有限公司,产品批号100018-200408)、萘普生(北京莱耀生物科技有限公司,产品批号100198-201205)、吲哚美辛(北京莱耀生物科技有限公司,产品批号100258-200904)、双氯芬酸钠(北京中科质检生物技术有限公司,产品批号100334-200302),纯度均≥99.8%。甲醇:色谱纯(用于配制对照品溶液),Fisher公司;分析纯(用于5抗风湿中成药样品成分提取),天津市永大化学试剂有限公司。
抗风湿类中成药样品:样品1(抗风湿中药偏方),粉末,处方未知;样品2(曹清华薏辛除湿止痛胶囊),处方为当归、白芍、白术、薏苡仁、附子、桂枝、乌梢蛇、地龙、牛膝、细辛、甘草;样品3(风湿安泰片),处方为生川乌、生草乌、马钱子(制)、羌活、乌梢蛇、红花、骨碎补(制)、乌梅、金银花、细辛、红参、鹿茸、黄柏、没药、广地龙、地枫皮、老鹳草、五加皮、续断、麻黄、甘草、槲寄生、淫羊藿、牛膝、桂枝;样品4(腰膝痛胶囊),处方为白芷、草乌(制)、独活、续断、牛膝、三七、防风、威灵仙、秦艽、川加皮、防己、海风藤、杜仲、土草藓、何首乌、桑寄生、骨碎补、红花、千年健、赤芍、桂枝、扑热息痛;样品5(夏天无胶囊),处方为夏天无。
2 实验部分 2.1 溶液的配制 2.1.1 对照品溶液称取布洛芬、对乙酰氨基酚、萘普生、吲哚美辛、双氯芬酸钠的对照品各约10 mg,精密称定,分别置10 mL量瓶中,加甲醇溶解,定容至刻度,摇匀,即得1mg·mL-1的单一对照品溶液,加甲醇依次稀释得到系列浓度的单一对照品溶液,备用。
2.1.2 供试品溶液称取抗风湿类中成药样品1 g(若为胶囊剂则取内容物),充分研细,精密称定,加入甲醇10 mL,溶解,0.45 μm微孔滤膜过滤,作为供试品储备液。用甲醇将供试品储备液分别稀释10、25、50倍,作为系列供试品溶液,备用。
2.1.3 阴性样品溶液分别称取经LC-MS检测,不含NSAIDs类非法添加抗风湿类中成药的阴性样品(即样品2、样品3、样品4、样品5)各1 g,混匀,充分研细,分别精密称量,加入甲醇10 mL溶解,0.45 μm微孔滤膜过滤,依次得到阴性样品溶液A、B、C、D。
2.1.4 模拟阳性样品溶液称取4种抗风湿类中成药阴性样品(样品2、样品3、样品4、样品5)各1 g,混匀,充分研细,精密称定,分别精确加入对乙酰氨基酚、布洛芬、萘普生、双氯芬酸钠、吲哚美辛5种单一对照品适量,制备非法添加质量分数为1%的模拟阳性样品,按照“2.1.2”项下方法制备模拟阳性样品溶液A、B、C、D。
2.2 IMS分析进样前,取校正溶液(100 μg·mL-1柠檬酸)对仪器进行校正,校正完成后,取待测溶液30~40 μL,进行IMS分析。离子迁移谱工作参数如表 1所示。
|
|
表 1 IMS正离子模式检测参数 Table 1 IMS operating conditions in positive mode |
为比较NSAIDs在正负2种离子模式下的响应值,取系列对照品溶液在不同模式下分别进样分析,结果仅在正离子模式下发现NSAIDs的目标峰。在优化的实验条件下,对5个NSAIDs进行分析,NSAIDs单一对照及混合对照的离子迁移谱图分别见图 1、2。由图可见,分析不同组分时,t=5.60 ms处均出现1个强度相对较高的峰,根据ESI-IMS中的离子形成机制[19]可知,t=5.60 ms处的离子为反应物离子,即H+(H2O)x+2。
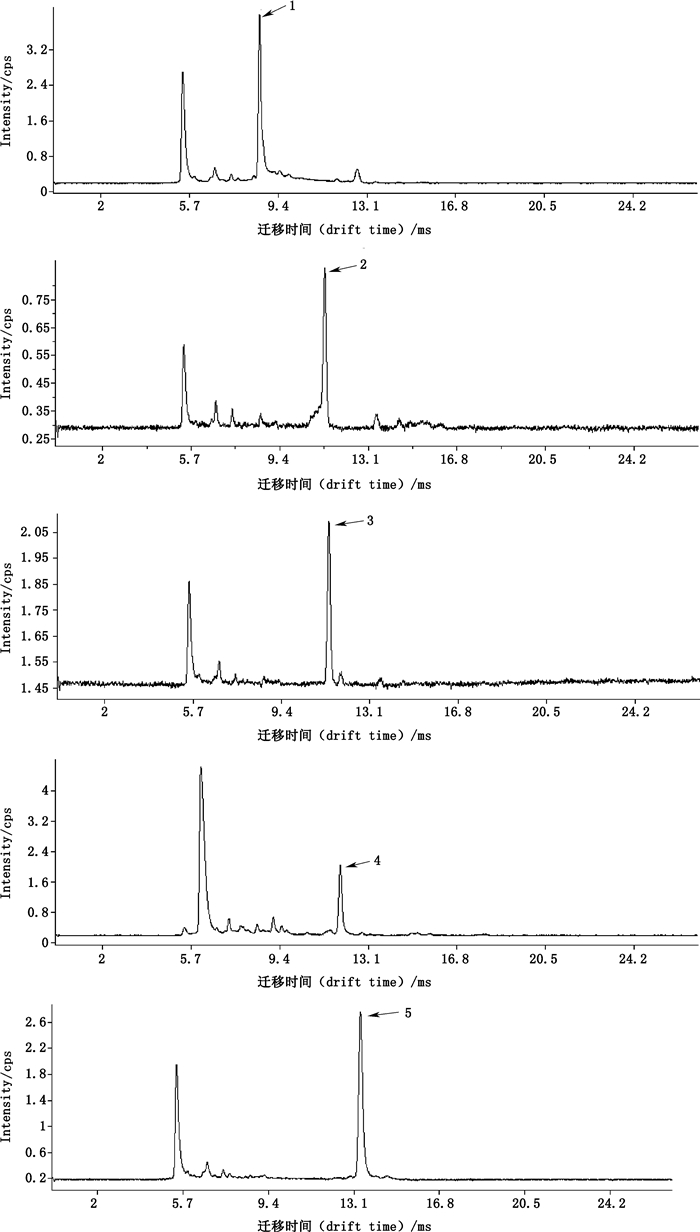
|
1.对乙酰氨基酚(acetaminophen) 2.萘普生(naproxen) 3.布洛芬(ibuprofen) 4.双氯芬酸钠(diclofenac sodium) 5.吲哚美辛(indomethacin) 图 1 5种NSAIDs单一对照(200 μg·mL-1)的IMS图谱 Figure 1 IMS spectrograms of 5 non-steroidal anti-inflammatory drugs |
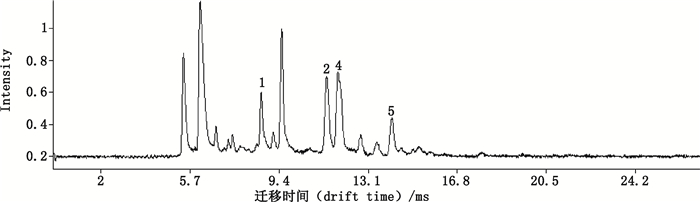
|
1.对乙酰氨基酚(acetaminophen) 2.萘普生或布洛芬(naproxen or ibuprofen) 4.双氯芬酸钠(diclofenac sodium) 5.吲哚美辛(indomethacin) 图 2 NSAIDs混合对照(50 μg·mL-1)的IMS图 Figure 2 IMS spectrogram of mixed standard of 5 non-steroidal anti-inflammatory drugs |
此外,由图 2可见,除布洛芬与萘普生迁移时间接近难以分离外,其余3个化合物彼此分离良好;为消除环境温度、气压等对各组分迁移时间的干扰,常按公式计算约化迁移率如下[24]:
| $ {K_0} = \left( {\frac{{273K}}{T}} \right)\left( {\frac{P}{{760T{\rm{oor}}}}} \right)\frac{{{L^2}}}{{Vt}} $ |
其中,V是迁移管电压,L是迁移管长度,t代表组分迁移时间,P是气压,T代表开尔文温度(单位:K)。由公式可见,当仪器工作条件确定时,约化迁移率K0只与迁移时间t相关。
3.2 真实样品测定取“2.1.2”项下制备得到的供试品溶液,进行IMS分析,除样品1抗风湿中药偏方检出吲哚美辛外(如图 3),其余样品均未检出5个NSAIDs,结果见表 2。
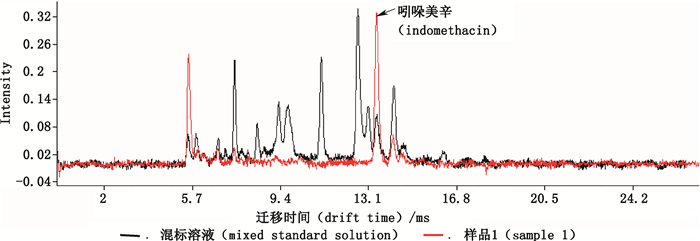
|
图 3 样品1(稀释25倍)的IMS图 Figure 3 IMS spectrogram of sample 1(diluted 25 times) |
|
|
表 2 真实样品测定 Table 2 Analysis of real samples |
取“2.1.3”和“2.1.4”项下阴性样品溶液和模拟阳性样品溶液,进行IMS分析,结果见图 4。同时,本文对5种抗风湿中成药的处方组成进行了梳理,由结果可见,48种常见抗风湿中药材的存在均不会干扰5个NSAIDs的检测,方法专属性良好。
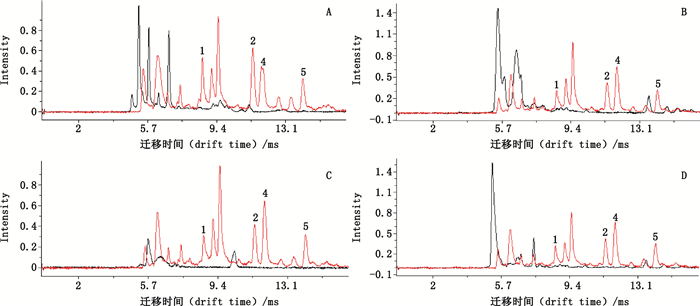
|
1.对乙酰氨基酚(acetaminophen) 2.萘普生或布洛芬(naproxen or ibuprofen) 4.双氯芬酸钠(diclofenac sodium) 5.吲哚美辛(indomethacin) A.样品2(sample 2) B.样品3(sample 3) C.样品4(sample 4) D.样品5(sample 5)
图 4 4种阴性样品(    |
取“2.1”项下系列对照品溶液进样分析,S/N=10和S/N=3时分别测得定量下限和检测下限,结果见表 3。
|
|
表 3 NSAIDs稳定性、耐用性考察 Table 3 Investigation of method reproducibility and robustness of NSAIDs |
取5个NSAIDs的对照品溶液进样分析,以峰强度为指标,考察日内和日间精密度,计算RSD,结果见表 3。
3.6 耐用性考察取5个NSAIDs的对照品溶液进样分析,连续6 d进样,分别以峰强度、迁移时间为指标,考察方法耐用性,计算RSD,结果见表 3。
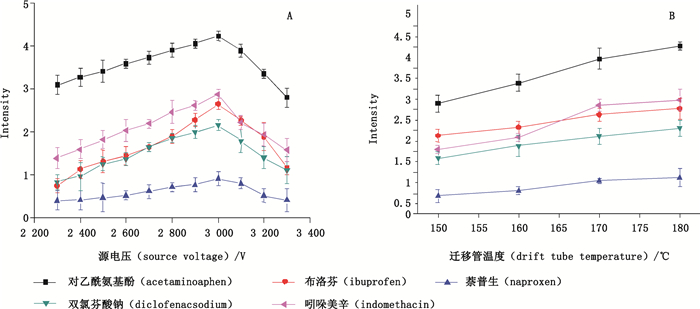
3.7 IMS条件的优化为达到最优的离子化效率,本文对IMS的工作参数进行了考察和优化,所有实验均重复3份。如图 5-A,随着离子源压力和迁移管温度的升高,响应信号增强,在3 kV时离子强度达到最高;但随着源电压继续升高,溶剂分子与待测物竞争增加,响应信号反而变弱。此外,门电压越低,门宽度越大,峰强度越高,但峰同时变宽,灵敏度降低,通过试验确定离子迁移谱的优化条件见表 1。
|
A.源电压(source voltage) B.迁移管温度(drift tube temperature) 图 5 IMS参数优化 Figure 5 Optimization of experimental parameters of IMS |
将已有文献发表的不同基质中NSAIDs的测定方法[25-30]与本文所建立的方法进行了比较,见表 4。
|
|
表 4 NSAIDs分析方法比较 Table 4 Comparision of the NSAIDs detection methods |
目前,关于色谱法、质谱或串联质谱法等方法在测定不同复杂基质中NSAIDs的应用已有诸多报道,这些方法定量准确,可靠性高,质谱或串联质谱更是能达到很高的灵敏度。然而,这些检测方法一般都需要冗杂的前处理,分析时间相对较长;此外,某些方法如质谱法常需要精密的仪器设备和专业操作人员,因此不适于现场快速筛查。与这些方法相比,ESI-HPIMS法具有几点优点:①方法简便快速,不需要任何前处理步骤;②方法专属性良好;③仪器体积小,便携,因此适合用于现场筛查。
同时,本文还对比了所建立方法与已有方法的灵敏度,由结果可见,本文所建立的方法检测下限在0.06~0.33 μg·mL-1之间,相比于MS(MS/MS)方法,灵敏度稍差。但实际上,为达到显著的治疗效果,非法添加的量一般较大,有的甚至可以达到mg级别;同时,只有当非法添加量达到一定的量,才会给消费者带来健康危害。在对这些非法添加药品进行检测时,有的方法如MS(MS/MS)甚至需要对样品进行多倍稀释,以防止检测系统过载。通过对真实样品、模拟阳性样品分析可知,本方法的灵敏度足以达到检测需求,不需要采用复杂的前处理步骤来提高方法灵敏度。
然而,IMS主要依靠迁移时间来对化合物进行定性,虽然各样品分子可以根据碰撞面积、核电荷数、分子折合质量不同而实现分离,但本文仅对5个NSAIDs进行了研究,当有多种未知干扰组分存在时,待测组分的迁移时间可能会受到干扰,若需进一步定性,常需要采用LC-MS等专属性更强的方法。
此外,本文还对5个NSAIDs进行了定量研究,结果可见,虽然检出峰的峰面积随待测物浓度增加而增大,但在大多数情况下,两者的线性关系不明显,因此尚不能实现准确定量。与LC/MS法受限于实验室操作相比,本文所建立的筛查方法虽然不能完成精确定量,但不需要前处理即可完成初步定性检测,方法简便快速,且专属性好,因此有望作为监管部门的现场初步筛查手段。
4 结论本文利用ESI-HPIMS,建立了抗风湿类中成药中非法添加5个NSAIDs(布洛芬、对乙酰氨基酚、萘普生、双氯芬酸钠、吲哚美辛)的快速筛查方法,方法简便快速(仅需2~3 min即可完成对样品的测定);对真实中成药样品、阴性样品、模拟阳性样品分析可见;方法专属性强,不受中成药中复杂基质的干扰。本文所建立的方法简便、快速、灵敏,特异性强,为抗风湿类中成药非法添加的现场筛查提供了一种简便易行的手段。
| [1] |
孔宁, 吕玲, 万伟国. 传统慢作用抗风湿药[J]. 上海医药, 2012, 33(13): 11. KONG N, L L, WAN WG. The traditional slow-acting anti-rheumatic drugs[J]. Shanghai Med Pharm J, 2012, 33(13): 11. DOI:10.3969/j.issn.1006-1533.2012.13.003 |
| [2] |
黄卫平, 李琴, 唐靓, 等. 超高效液相色谱-四极杆飞行时间质谱测定抗风湿类中药非法添加的化学药物成分[J]. 中华中医药学刊, 2014, 32(14): 2707. HUANG WP, LI Q, TANG L, et al. Determination of chemical components illegally mixed in antirheumatic traditional Chinese medicine by ultra-performance liquid chromatography-quadrupole-time-of-flight mass spectrometry[J]. Chin Arch Tradit Chin Med, 2014, 32(14): 2707. |
| [3] |
张念森. 非甾体抗炎药的临床应用及不良反应[J]. 中国药物评价, 2013, 30(1): 37. ZHANG NS. Clinical application and adverse reaction of non-steroidal anti-inflammatory drug[J]. Chin J Drug Eval, 2013, 30(1): 37. |
| [4] |
谢建翔, 牛丹. 非甾体抗炎药不良反应报告分析[J]. 中国药业, 2013, 22(23): 47. XIE JX, NIU D. Adverse drug reactions report of non-steroidal anti- inflammatory drugs[J]. China Pharm, 2013, 22(23): 47. |
| [5] |
中国食品药品监督管理局. 抗风湿类中成药中非法添加化学药品补充检验办法[S]. 2009 CFDA. The Approval Letter of Supplementary Detection of Drugs, 2009025[S]. 2009 |
| [6] |
王仕平, 黄炳泉, 刘卿, 等. 抗风湿类中成药及保健品中非法添加双氯芬酸钠与尼美舒利的快速筛查[J]. 中国药事, 2010, 24(12): 1207. WANG SP, HUANG BQ, LIU Q, et al. Rapid screening of diclofenac sodium and nimesulide illegally mixed into anti-rheumatic traditional Chinese medicine and health products[J]. Chin Pharm Aff, 2010, 24(12): 1207. |
| [7] |
池浩波, 张梦虹, 李国毅, 等. 抗风湿类中成药和保健食品中非法添加双氯芬酸钠快速筛查方法研究[J]. 中成药, 2011, 33(6): 1084. CHI HB, ZHANG MH, LI GY, et al. Research of rapid screening method of diclofenac sodium illegally added in anti rheumatoid proprietary Chinese medicine and health foods[J]. Chin Tradit Pat Med, 2011, 33(6): 1084. |
| [8] |
蓝献泉, 黄义纯, 黄红雯, 等. 抗风湿类中成药及保健品中非法添加双氯芬酸钠的快速筛查方法研究[J]. 中南药学, 2014, 12(9): 902. LAN XQ, HUANG YC, HUANG HW, et al. Rapid screening for illegal adding of diclofenac sodium in antirheumatic traditional Chinese medicine and health products[J]. Cent South Pharm, 2014, 12(9): 902. DOI:10.7539/j.issn.1672-2981.2014.09.020 |
| [9] |
宋辉, 陈为飞. 冯了性风湿跌打药酒假药中双氯芬酸钠定性、定量分析[J]. 中国现代应用药学, 2002, 19(5): 405. SONG H, CHEN WF. Qualitative and quantitative analysis of diclofenac sodium in the dummy Fenliaoxing Fengshi Dieda Yaojiu[J]. Chin J Mod Appl Pharm, 2002, 19(5): 405. |
| [10] |
来国防, 程宾, 鲁静. 液相色谱-质谱联用测定抗风湿类中药中非法添加化学药物成分[J]. 中国药师, 2010, 21(4): 847. LAI GF, CHENG B, LU J. Measurement of illegally added chemicals in anti rheumatoid medicine by LC-MS[J]. China Pharm, 2010, 21(4): 847. |
| [11] |
黎雪清, 谭渺, 蒋创杰, 等. HPLC法快速筛查抗风湿类中成药和保健食品中24种非法添加化学成分[J]. 中成药, 2014, 36(9): 1891. LI XQ, TAN M, JIANG CJ, et al. Rapid screening of 24 chemicals added illegally in anti-rheumatic herb preparations and health foods by HPLC[J]. Chin Tradit Pat Med, 2014, 36(9): 1891. |
| [12] |
励炯, 沈国芳, 朱建, 等. UPLC-MS/MS法测定抗风湿中成药中非法添加8种抗风湿性化学成分[J]. 中草药, 2014, 45(18): 2647. LI J, SHEN GF, ZHU J, et al. Detection of eight antirheumatic constituents illegally added in Chinese patent medicine by UPLC-MS/MS[J]. Chin Tradit Herb Drugs, 2014, 45(18): 2647. DOI:10.7501/j.issn.0253-2670.2014.18.014 |
| [13] |
李存金, 郭飞宇. HPLC检测抗风湿类中成药中非法添加非甾体类化学物质[J]. 中成药, 2010, 32(12): 2191. LI CJ, GUO FY. Detection of non-steroidal anti-inflammatory drugs illegally added in antirheumatoid Chinese traditional patent medicine by HPLC[J]. Chin Tradit Pat Med, 2010, 32(12): 2191. DOI:10.3969/j.issn.1001-1528.2010.12.051 |
| [14] |
刘志辉. HPLC法同时测定抗风湿类中成药及保健品中非法添加9种解热镇痛类化学药物[J]. 中国药师, 2015, 18(7): 1116. LIU ZH. Simultaneous determination of nine antipyretic analgesic drugs illegally added into antirheumatic traditional Chinese medicines and health products by HPLC[J]. China Pharm, 2015, 18(7): 1116. |
| [15] |
赵凤菊, 来国防, 孙刚, 等. UPLC/MS/MS法检测抗风湿类制剂中添加醋酸泼尼松、醋酸地塞米松、双氯芬酸钠和布洛芬[J]. 药物分析杂志, 2010, 30(6): 1035. ZHAO FJ, LAI GF, SUN G, et al. UPLC/MS/MS determination of prednisone acetate, dexamethasone acetate, diclofenac sodium and ibuprofen mixed in antirheumatic traditional Chinese medicine[J]. Chin J Pharm Anal, 2010, 30(6): 1035. |
| [16] |
廖瑜. HPLC快速筛查抗风湿类中成药及保健品中非法添加的10种化学药[J]. 中国现代应用药学, 2014, 31(7): 868. LIAO Y. Screening for 10 antirheumatism chemical components in health food and Chinese traditional medicine by HPLC[J]. Chin J Mod Appl Pharm, 2014, 31(7): 868. |
| [17] |
汪元符. 抗炎抗风湿功效中成药中非法添加非甾体抗炎药及激素类成分的检测[J]. 中国执业药师, 2015, 12(11): 19. WANG YF. Detection of non-steroidal anti-inflammatory drug and glucocorticoid added illegally in anti-inflammatory and antirheumatic traditional Chinese medicine[J]. China Lic Pharm, 2015, 12(11): 19. DOI:10.3969/j.issn.1672-5433.2015.11.005 |
| [18] |
朱小红, 李涛, 马鹏飞, 等. 气相色谱-质谱检测方法快速筛查保健食品及中成药中8种非甾体抗炎药[J]. 药物分析杂志, 2012, 32(10): 1847. ZHU XH, LI T, MA PF, et al. GC-MS rapid screening of eight non-steroidal anti-inflammatory drugs in health foods and traditional Chinese medicines[J]. Chin J Pharm Anal, 2012, 32(10): 1847. |
| [19] |
刘宪云, 孔祥和, 季仁东, 等. 离子迁移谱在环境污染物检测中的应用[J]. 原子与分子物理学报, 2007, 24(1): 163. LIU XY, KONG XH, JI RD, et al. Applications of ion mobility spectrometry in environmental monitoring[J]. J Atom Mol Phys, 2007, 24(1): 163. |
| [20] |
冯雪, 尹利辉, 金少鸿, 等. 离子迁移谱及其在药学领域的应用[J]. 药物分析杂志, 2013, 33(7): 1109. FENG X, YIN LH, JIN SH, et al. Ion mobility spectrometry and its applications in pharmaceutical research and development[J]. Chin J Pharm Anal, 2013, 33(7): 1109. |
| [21] |
焦建东, 李俊卿, 王金凤, 等. 离子迁移谱快速检测改善睡眠类保健品中非法添加的巴比妥类药物[J]. 药物分析杂志, 2016, 36(2): 321. JIAO JD, LI JQ, WANG JF, et al. Rapid detection of illegally added barbiturates in sleep-improving healthy foods by ion mobility spectrometry[J]. Chin J Pharm Anal, 2016, 36(2): 321. |
| [22] |
李灵锋, 王铁松, 韩可, 等. 利用高场非对称波形离子迁移谱技术快速鉴别降糖中药中的西药成分[J]. 分析化学研究报告, 2014, 42(4): 519. LI LF, WANG TS, HAN K, et al. Rapid identification of illegally addition in traditional Chinese antidiabetic medicine by field asymmetric ion mobility spectrometric technique[J]. Chin J Anal Chem, 2014, 42(4): 519. |
| [23] |
冯雪, 尹利辉, 金少鸿, 等. 离子迁移谱法快速检测保健食品中添加的5型磷酸二酯酶抑制剂[J]. 药物分析杂志, 2016, 36(2): 313. FENG X, YIN LH, JIN SH, et al. Rapid detection of undeclared phosphodiesterase type 5 inhibitors in dietary supplements by ion mobility spectrometry[J]. Chin J Pharm Anal, 2016, 36(2): 313. |
| [24] |
KIM HI, JOHNSON PV, BEEGLE LW, et al. Electrospray ionization ion mobility spectrometry of carboxylate anions:ion mobility and a mass-mobility correlation[J]. J Phys Chem A, 2005, 109(35): 7888. DOI:10.1021/jp051274h |
| [25] |
SARAFRAZ A, AMIRI A, ROUNAGHI G, et al. Determination of non-steroidal anti-inflammatory drugs in urine by hollow-fiber liquid membrane-protected solid-phase microextraction based on sol-gel fiber coating[J]. J Chromatogr B, 2012, 908(1): 67. |
| [26] |
ZHANG HJ, DU ZX, JI Y, et al. Simultaneous trace determination of acidic non-steroidal anti-inflammatory drugs in purified water, tap water, juice, soda and energy drink by hollow fiber-based liquid-phase microextraction and ultra-high pressure liquid chromatography coupled to tandem mass spectrometry[J]. Talanta, 2013, 109(5): 177. |
| [27] |
MANZO V, MIRO M, RICHTER P. Programmable flow-based dynamic sorptive microextraction exploiting an octadecyl chemically modified rotating disk extraction system for the determination of acidic drugs in urine[J]. J Chromatogr A, 2014, 1368(14): 64. |
| [28] |
PAYAN MR, LOPEZ MÁ, FERNANDEZ-TORRES R, et al. HPLC determination of ibuprofen, diclofenac and salicylic acid using hollow fiber-based liquid phase microextraction (HF-LPME)[J]. Anal Chim Acta, 2009, 653(2): 184. DOI:10.1016/j.aca.2009.09.018 |
| [29] |
MAGIERA S, GULMEZ S, MICHALIK A, et al. Application of statistical experimental design to the optimisation of microextraction by packed sorbent for the analysis of nonsteroidal anti-inflammatory drugs in human urine by ultra-high pressure liquid chromatography[J]. J Chromatogr A, 2013, 1304: 1. DOI:10.1016/j.chroma.2013.06.047 |
| [30] |
SUN Y, TAKABA K, KIDO H, et al. Simultaneous determination of arylpropionic acidic nonsteroidal anti-inflammatory drugs in pharmaceutical formulations and human plasma by HPLC with UV detection[J]. J Pharm Biomed, 2003, 30(5): 1611. DOI:10.1016/S0731-7085(02)00549-6 |
 2018, Vol. 38
2018, Vol. 38 
