2. 广州中医药大学第二附属医院, 广州 510006
2. The Second Affiliated Hospital, Guangzhou University of Chinese Medicine, Guangzhou 510006, China
马钱子始载于《本草纲目》,为马钱科植物马钱Strychnos nux-vomica L.的干燥成熟种子,收录于《中华人民共和国药典》(简称《中国药典》)2015年版一部,具有通经止痛、散结消肿的功效,用于跌打损伤、骨折肿痛、风湿顽痹、麻木瘫痪、痈疮疮毒、喉咙肿痛的治疗[1-2]。
马钱子为剧毒中药,有效剂量和中毒剂量比较接近,其有效成分为生物碱类,其中士的宁及其氮氧化物和马钱子碱及其氮氧化物含量占总生物碱的82%以上,这类成分毒性极大,临床多以炮制品入药[3]。《中国药典》中共收录了19种含有马钱子的中药复方制剂,16种成药要求检查士的宁含量(其中3种要求同时检查士的宁和马钱子碱含量)。为了解决中药化学对照品对纯度要求高,制备难度大,检测成本高,以及士的宁和马钱子碱对照品为剧毒化学品,其发放和运输均受到严格管控的问题,本文研制马钱子碱对照提取物,既可有效降低单体对照品的剧毒危害,又可满足药品检验检测的要求,确保临床用药安全;同时,本文还对对照提取物的色谱行为、均匀性、稳定性和赋值准确性进行了研究。
本研究对5批不同来源的马钱子药材和3批骨刺片样品(含马钱子饮片)进行了测定,结果初步验证了马钱子对照提取物替代士的宁和马钱子碱对照品对马钱子药材、饮片及其复方制剂进行质量控制的可行性。
1 仪器与试药Waters e2695-2998 PAD液相色谱仪(Waters公司),梅特勒AE240型电子天平(十万分之一,梅特勒公司),Millipore超纯水仪(Millipore公司)。
马钱子药材3批由中国食品药品检定研究院标本馆提供(编号为1~3),士的宁(批号110705-201307)、马钱子碱(批号110706-201306)和马钱子对照药材(批号121164-200302、121164-200603,编号为4、5)来源于中国食品药品检定研究院;骨刺片3批次,均为市售(编号为6~8)。色谱纯甲醇购自Theremo Fisher试剂有限公司;其他试剂为分析纯,均购自国药集团化学试剂有限公司。
2 方法和结果 2.1 对照提取物的研究 2.1.1 制备参考药典方法进行优化[2],确定对照提取物制备方法:取马钱子药材粉末100 g,加三氯甲烷-乙醇(10:1)1 000 mL与浓氨试液100 mL,浸泡过夜,滤过,减压回收三氯甲烷和乙醇,冷冻干燥,即得。
2.1.2 标定以士的宁和马钱子碱对照品为对照,测定对照提取物中2个成分的含量。
2.1.2.1 色谱条件采用Waters Symmetry ShieldTM RP C18色谱柱(4.6 mm×250 mm,5 μm),以乙腈-0.01 mol·L-1庚烷磺酸钠与0.02 mol·L-1磷酸二氢钾等量混合溶液(21:79)为流动相,流速1 mL·min-1,检测波长260 nm。
2.1.2.2 混合对照品溶液制备分别精密称取士的宁和马钱子碱的对照品适量(约10 mg),置于100 mL量瓶中,加甲醇溶解并稀释至刻度,制成混合对照品溶液,即得。
2.1.2.3 供试品溶液制备精密称取对照提取物(约20 mg)于100 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得对照提取物溶液。
2.1.2.4 线性关系考察精密吸取“2.1.2.2”项下混合对照品溶液1、2、5、10、15 μL,分别注入液相色谱仪,测定峰面积。以峰面积Y为纵坐标,进样量X(μg)为横坐标,绘制标准曲线。士的宁和马钱子碱的回归方程分别为:
| $ \begin{array}{l} Y = 1 \times {10^7}X - 2 \times {10^6}\;\;r = 1.000\\ Y = 2 \times {10^7}X - 3 \times {10^6}\;\;r = 1.000 \end{array} $ |
结果表明,士的宁进样量在0.14~2.10 μg范围内,马钱子碱进样量在0.11~1.65 μg范围内与峰面积呈良好线性关系。
2.1.2.5 精密度试验取同一混合对照品溶液,按“2.1.2.1”项下色谱条件连续进样6次,士的宁和马钱子碱峰面积的RSD(n=6)分别为0.86%和0.92%,表明仪器精密度良好。
2.1.2.6 稳定性试验取同一供试品溶液,分别于0、2、4、8、12、24 h按“2.1.2.1”项下色谱条件测定,结果士的宁和马钱子碱峰面积的RSD(n=6)分别为0.41%和0.62%,表明供试品溶液在24 h内稳定性良好。
2.1.2.7 均匀性试验在对照提取物分装的初始、中间和终结阶段均随机抽取15支对照提取物,分别测定峰面积,采用单因素方差分析法,对样品均匀性进行考察[5]。
设从对照提取物总体单元中抽取m个单元,计算方法如下,
| $ \begin{array}{l} {x_{11}}, {x_{12}}, \cdots , {x_{1{n_1}}}, \;\;平均值{{\bar x}_1};\\ {x_{21}}, {x_{22}}, \cdots , {x_{2{n_1}}}, \;\;平均值{{\bar x}_2};\\ \ldots \\ {x_{m1}}, {x_{m2}}, \cdots , {x_{m{n_m}}}, \;\;平均值{{\bar x}_m}; \end{array} $ |
设
| $ \begin{array}{*{20}{c}} {\overline{\overline x} = \frac{1}{N}\sum\nolimits_{i = 1}^m {\sum\nolimits_{j = 1}^n {{x_{ij}}} } }\\ {N = \sum\nolimits_{i = 1}^m {{n_i}} } \end{array} $ |
组间方差和
| $ {Q_1} = {\sum\nolimits_{i = 1}^m {{n_i}\left( {{x_i} - \overline{\overline x} } \right)} ^2} $ |
组内方差和
| $ {Q_2} = \sum\nolimits_{i = 1}^m {\sum\nolimits_{j = 1}^{{n_i}} {{{\left( {{x_{ij}} - {{\bar x}_i}} \right)}^2}} } $ |
| $ {v_1} = m - 1;\;\;{v_2} = N - m $ |
组间方差
| $ s_1^2 = {Q_1}/{v_1} $ |
组内方差
| $ s_1^2 = {Q_2}/{v_2} $ |
该方法也可用来判断数据组间是否等精度(F-test):
作统计量F:
| $ F = \frac{{s_1^2}}{{s_2^2}} $ | (1) |
根据自由度(v1,v2)及给定的显著性水平α,可由F分布临界值表查得临界的Fα值。按公式(1)算得的F值满足F < Fα,则认为数据组间无明显差异。计算结果为士的宁F(=0.62) < F(14,15),马钱子碱F(=0.62) < F(14,15),其中F(14,15)为2.42,表明对照提取物样品均匀。
2.1.3 对照提取物的定值取分装后的对照提取物,3人分别使用不同色谱柱[Waters Symmetry ShieldTM RP C18(4.6 mm×250 mm,5 μm),Aglient SB C18(4.6 mm×250 mm,5 μm),Phemomenex Luna C18(4.6 mm×250 mm,5 μm)]和液相色谱仪(高效液相色谱仪Waters 2695-2996 DAD,Waters e2695-2998 PAD液相色谱仪,Shimadzu LC-2010A HT液相色谱仪)进行定值,每人取样3支。按“2.1.2.3”项下方法制备供试品溶液,按“2.1.2.1”项下色谱条件测定,采用外标法计算含量,结果士的宁和马钱子碱的平均含量(n=9)分别为49.9%和45.4%,RSD分别为1.0%和0.59%。
2.1.4 加样回收率试验称取已知含量的马钱子对照提取物约10 mg,精密称定6份,再分别精密加入士的宁和马钱子碱质量浓度分别为0.5426、1.0852 mg·mL-1的混合对照品溶液5 mL,按“2.1.2.3”项下方法制备供试溶液,按“2.1.2.1”项下色谱条件测定。计算士的宁的平均回收率(n=6)为98.6%,RSD为1.2%;马钱子碱的平均回收率(n=6)为99.2%,RSD为1.5%。
2.2 对照提取物在马钱子药材及骨刺片(含马钱子饮片)质量控制中的应用 2.2.1 色谱条件同“2.1.2.1”项下条件。
2.2.2 对照提取物溶液的制备精密称取已标定的马钱子对照提取物22.12 mg于100 mL量瓶中,加甲醇溶解并稀释至刻度,充分溶解。精密吸取1 mL于10 mL量瓶中,加甲醇至刻度,摇匀,即得22.12 mg ·L-1对照提取物溶液(其中士的宁的质量浓度为11.04 mg ·L-1,马钱子碱的质量浓度为10.01 mg ·L-1)。
2.2.3 供试品溶液取药材粉末(过3号筛)约0.6 g,精密称定,置具塞锥形瓶中,加氢氧化钠试液3 mL,混匀,放置30 min,精密加入三氯甲烷20 mL,密塞,称量,置水浴中回流提取2 h,放冷,再称量,用三氯甲烷补足减失的量,摇匀,分取三氯甲烷液,用铺有少量无水硫酸钠的滤纸过滤,弃去初滤液,精密量取续滤液3 mL,置10 mL量瓶中,加甲醇至刻度,摇匀,即得马钱子药材供试品溶液;取骨刺片50片,去包衣,精密称定,研细,精密称取6 g,置圆底烧瓶中,加三氯甲烷20 mL,氨水1 mL,水浴加热回流1 h,放冷滤过,滤渣用三氯甲烷洗涤,合并,洗液置水浴蒸干,残渣加三氯甲烷溶解并定量转移至5 mL量瓶中,以三氯甲烷稀释至刻度,摇匀,即得骨刺片供试品溶液[4]。
2.2.4 方法学考察 2.2.4.1 线性关系考察精密吸取“2.2.2”项下对照提取物溶液1、2、5、10、15、20 μL,分别注入液相色谱仪,测定峰面积。以峰面积Y为纵坐标,进样量X(μg)为横坐标,绘制标准曲线。士的宁、马钱子碱的回归方程:
| $ \begin{array}{l} Y = 1 \times {10^7}X - 2 \times {10^6}\;\;r = 1.000\\ Y = 2 \times {10^7}X - 3 \times {10^6}\;\;r = 1.000 \end{array} $ |
结果表明,士的宁进样量在0.11~2.21 μg范围内,马钱子碱进样量在0.10~2.00 μg范围内与峰面积呈良好线性关系。
2.2.4.2 精密度试验取同一对照提取物溶液,按上述色谱条件连续进样6次,士的宁和马钱子碱峰面积的RSD(n=6)分别为0.15%和0.21%,表明仪器精密度良好。
2.2.4.3 稳定性试验取“2.2.3”项下马钱子药材供试品溶液,分别于0、2、4、8、12、24 h按“2.1.2.1”项下色谱条件测定,结果士的宁和马钱子碱峰面积的RSD(n=6)分别为0.75%和0.55%,表明供试品溶液在24 h内稳定性良好。骨刺片:取“2.2.3”项下骨刺片供试品溶液,分别在0、2、4、8、12、24 h按“2.1.2.1”项下色谱条件测定,结果士的宁和马钱子碱峰面积的RSD(n=6)分别为0.98%和1.4%。表明供试品溶液在24 h内稳定。
2.2.4.4 重复性试验马钱子药材:分别精密称取同一批次马钱子药材6份,按“2.2.3”项下方法制备供试品溶液,按“2.1.2.1”项下色谱条件进样测定,计算士的宁和马钱子碱的平均含量(n=6)分别为1.34%和1.11%,RSD分别为0.98%和0.86%,表明方法重复性良好。骨刺片:分别精密称取同一批次骨刺片6份,按“2.2.3”项下方法制备供试品溶液,按“2.1.2.1”项下色谱条件进样测定,计算士的宁和马钱子碱的平均含量(n=6)分别为0.53%和0.15%,RSD分别为1.2%和1.0%,表明方法重复性良好。
2.2.4.5 回收率试验马钱子药材:称取已知含量的马钱子药材粉末0.3 g共6份,精密称定,再精密加入2.2 mg·mL-1的对照提取物溶液2 mL,按“2.2.3”项下方法制备供试溶液,按上述条件测定,计算士的宁和马钱子碱的平均回收率(n=6)分别为99.0%和99.1%,RSD均为1.1%。骨刺片:称取已知含量的骨刺片粉末3 g共6份,精密称定,再精密加入2.2 mg·mL-1的对照提取物溶液5 mL,按“2.2.3”项下方法制备供试溶液,按上述条件测定,计算士的宁和马钱子碱的平均回收率(n=6)分别为98.8%和99.5%,RSD分别为1.2%和0.92%。
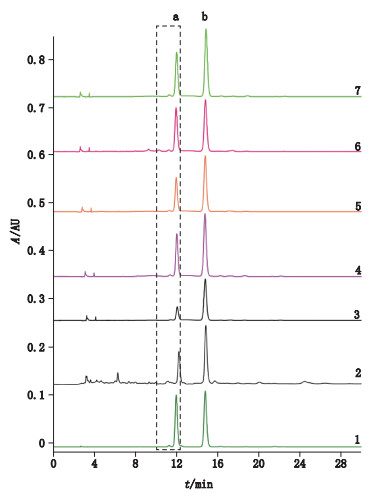
2.2.5 样品测定取5份马钱子药材样品和3批次骨刺片样品,分别按“2.2.3”项下方法制备供试品溶液,分别以本研究制备的对照提取物和士的宁、马钱子碱单体对照品为对照,按“2.1.2.1”项下色谱条件测定,色谱图见图 1,测定结果见表 1。
|
a.马钱子碱(brucine)b.士的宁(strychnine) 1.对照提取物(reference extract)2.骨刺片(Guci tablet)3~4.马钱子药材(crude drugs of Strychni Semen)5~6.马钱子对照药材(reference crude drug of Strychni Semen)7.士的宁、马钱子混合对照品溶液(mixed chemical reference substances of strychnine and brucine) 图 1 样品中的士的宁和马钱子碱的HPLC图 Figure 1 HPLC chromatograms of strychnine and brucine in samples |
|
|
表 1 马钱子药材及复方制剂中士的宁和马钱子碱的测定结果(n=3) Table 1 Content of strychnine and brucine in crude drugs and compound preparations |
根据《中国药典》2015年版一部对马钱子药材含量测定要求为本品按干燥品计算,含士的宁应为1.20%~2.20%,马钱子碱不得少于0.80%[2]。根据《卫生部药品标准》中药成方制剂第十七册,原标准项下马钱子粉的含量测定采用薄层扫描法(TLCS)测定士的宁的含量为每1 g含士的宁应为0.15~1.20 mg[4-5]。表 1均按百分比含量进行计算,结果表明采用对照提取物和对照品进行测定,结果之间没有显著性差异。其中1号药材中士的宁和马钱子碱含量均低于标准要求,认定为不合格样品。
3 讨论对照提取物易制备,价格低,稳定性好,配制操作简单,作为标准物质可以大大减少单体对照品的使用,从而节约中药稀有资源,降低检验成本[6]。本文研究士的宁和马钱子碱对照提取物,既可以达到降低对照品成本的目的,还可以减少单体对照品毒性剧烈所带来的风险[7]。
本提取物为定量对照提取物,标示了士的宁和马钱子碱2个指标成分含量,可用于定量分析中的量值传递。本文进行了均匀性、稳定性考察以及定值,为马钱子药材及含马钱子成分的中药制剂质量控制提供了另一个可选方案,既是一项探索性研究,又符合实际需要[8-10]。
| [1] |
王伟. 马钱子的炮制质量研究[J]. 内蒙古中医药, 2017, 36(3): 98. WANG W. Preparation research of Strychnos nux-vomica L.[J]. Nei Mongol J Tradit Chin Med, 2017, 36(3): 98. |
| [2] |
中华人民共和国药典2015年版. 一部[S]. 2015: 50 ChP 2015. Vol Ⅰ[S]. 2015: 50 |
| [3] |
徐晓月, 蔡宝昌, 潘扬, 等. 马钱子生物碱在大鼠体内的药代动力学研究[J]. 药学学报, 2003, 38(6): 458. XU XY, CAI BC, FAN Y, et al. Pharmacokinetics of the alkaloids from the processed seeds of Strychnos nux-vomica in rats[J]. Acta Pharm Sin, 2003, 38(6): 458. |
| [4] |
卫生部药品标准. 中药成方制剂. 第十七册[S]. 1998: 56, 202 Drug Standard of Ministry of Public Health of the People's Republic of China. Chinese Medicine Prescription Preparation. Volume 17[S]. 1998: 56, 202 |
| [5] |
曹玲, 冯有龙, 王亚超, 等. 骨刺片的质量标准研究[J]. 中国药品标准, 2011, 12(3): 191. CAO L, FENG YL, WANG YC, et al. Study on quality control of Guci tablets[J]. Drug Stand China, 2011, 12(3): 191. |
| [6] |
陈沛, 金红宇, 孙磊, 等. 对照提取物在中药整体质量控制中的应用[J]. 药物分析杂志, 2016, 36(2): 185. CHEN P, JIN HY, SUN L, et al. Application of extractive reference substance in holistic quality control of traditional Chinese medicine[J]. Chin J Pharm Anal, 2016, 36(2): 185. |
| [7] |
邢跃文. 马钱子炮制与毒性关系的研究[J]. 中国民间疗法, 2005, 13(2): 57. XING YW. Relationship of crude drug preparation of Strychnos nux-vomica seed and its toxicity[J]. China Naturopathy, 2005, 13(2): 57. |
| [8] |
何风艳, 戴忠, 何轶, 等. 西红花苷对照提取物的研究及其在西红花饮片质量控制中的应用[J]. 中国中药杂志, 2015, 40(12): 2378. HE FY, DAI Z, HE Y, et al. Study on crocins regerence extract and application to assay of Croci Stigma[J]. China J Chin Mater Med, 2015, 40(12): 2378. |
| [9] |
王菲菲, 吴寿海, 王明娟, 等. 马钱子生物碱混合对照溶液稳定性研究[J]. 广州中医药大学学报, 2018, 35(2): 335. WANG FF, WU SH, WANG MJ, et al. Study on stability of mixture reference solution of Strychni alkaloids[J]. J Guangzhou Univ Tradit Chin Med, 2018, 35(2): 335. |
| [10] |
陆兔林, 翟为民, 蔡宝昌, 等. 对照提取物在中药质量控制中的应用[J]. 中国中药杂志, 2013, 38(3): 462. LU TL, ZHAI WM, CAI BC, et al. Application of reference extracts in quality control of traditional Chinese medicines[J]. China J Chin Mater Med, 2013, 38(3): 462. |
 2018, Vol. 38
2018, Vol. 38 
