B族维生素是维持人体正常机能与代谢活动重要的水溶性维生素,其中多是酶的辅基和酶的组成部分,缺乏时能导致代谢障碍,从而引发多种疾病。而人体自身又无法合成这些化合物,须通过食物或服用复合维生素制剂予以补充。复合维生素B片是由多种维生素、重酒石酸胆碱和肌醇组成的复方制剂,可用于预防和治疗B族维生素缺乏所致的营养不良、厌食、脚气病、糙皮病等。复合维生素B片中含有8种维生素,其中维生素B1、维生素B2、维生素B3、维生素B5和维生素B6的含量较高,标示量均为50 mg·片-1,而叶酸的标示量为400 μg·片-1,维生素B12与生物素为50 μg·片-1,最高相差1 000倍。虽然同属水溶性维生素,但化学结构并不相关,理化性质和色谱行为差异大,再加上药品中的含量相差十分悬殊,因此实现同时分析测定的难度较大。
本实验室前期已建立了以高效液相色谱-二极管阵列检测(HPLC-DAD)技术,同时测定复合维生素B片中维生素B1、维生素B2、维生素B3、维生素B5和维生素B6 5个含量较高的活性成分的方法。由于叶酸、维生素B12以及生物素在药品中的含量很低,并且与5个含量较高成分的溶解性差异大,维生素B2与维生素B6在碱液中不稳定,而叶酸和生物素在水中溶解性较差,易溶于稀碱溶液,故采用同一种提取方法无法同时对上述8个维生素进行定量。因此,需要建立一个可以同时测定这3个微量成分含量的方法。
文献报道关于药品或食品中叶酸、维生素B12和生物素的含量测定方法包括紫外分光光度法(UV法)[1-2]、HPLC法[3-16]、液相色谱-质谱联用法(LC-MS法)[17-18]、毛细管电泳法[19]以及微生物法[20-21]等。《中华人民共和国药典》(2015年版)[22]中采用HPLC法对叶酸进行含量测定,以加入0.5 mol·L-1四丁基氢氧化铵甲醇溶液的磷酸盐缓冲液作为流动相,溶液配制方法较为复杂;利用紫外-可见分光光度法对维生素B12进行含量测定。虽然已有关于叶酸、维生素B12和生物素含量测定方面的报道,但均为单独测定这3种成分中的1个或2个,目前同时对复合维生素B片这种复杂基质中的微量叶酸、维生素B12和生物素进行含量测定的方法尚未见报道。
本研究通过优化提取方法和色谱条件,建立了同时测定复合维生素片中3个微量成分叶酸、维生素B12和生物素的方法,该方法准确、快速,专属性强,可以为该药品的质量控制提供科学依据。
1 仪器与试药 1.1 仪器Agilent 1260液相系统:配有G1311C四元梯度泵、G1329B自动进样器、Alltima C18色谱柱(250 mm × 4.6 mm,5 μm;填料:十八烷基硅烷键合硅胶)、G1316A柱温箱、G4212B DAD检测器(Agilent Technologies);Mettler XP-205电子天平(梅特勒公司);KQ-800KDE型超声仪(昆山市超声仪器有限公司);Millipore超纯水处理系统。
1.2 试药乙腈(色谱纯,Fisher公司,批号158031);磷酸(色谱纯,Fluka公司,批号BCBB0522);磷酸二氢铵(分析纯,国药集团化学试剂有限公司,批号20130121);氢氧化钠(分析纯,北京化学试剂公司);实验用水为超纯水。叶酸对照品(批号15H0968)购自Sigma公司;维生素B12对照品(批号100248-200802)购自中国食品药品检定研究院;生物素对照品(批号20160919)购自国药集团化学试剂有限公司。复合维生素B片(规格:含叶酸400 μg·片-1,维生素B12和生物素均为50 μg·片-1,批号3973052、3989178和3972021,Jamieson公司)。
2 方法与结果 2.1 色谱条件色谱柱:Alltima C18(250 mm ×4.6 mm,5 μm);流动相:乙腈(A)-50 mmol·L-1磷酸二氢铵溶液(磷酸调至pH 3.0)(B),梯度洗脱(0~7 min,13%A;7~15 min,13%A~40%A;15~19 min,40%A);流速:1.0 mL·min-1;检测波长:200 nm;柱温:30 ℃;进样体积:50 μL。
2.2 混合对照品溶液的制备分别精密称取叶酸、维生素B12、生物素的对照品适量,叶酸和生物素用0.1%氢氧化钠溶液溶解,分别配制成质量浓度约480 μg·mL-1和60 μg·mL-1的储备液,维生素B12用水溶解,配制成质量浓度约60 μg·mL-1的储备液。分别精密量取各储备液10 mL于100 mL量瓶中,加水稀释至刻度,配制成叶酸质量浓度约48 μg·mL-1以及维生素B12和生物素浓度均约6 μg·mL-1的混合对照品储备液。精密量取混合对照品储备液2.5、4、5、6、7.5 mL,分别置于10 mL量瓶中,加水稀释至刻度,摇匀,获得叶酸质量浓度约为12、19.2、24、28.8、36 μg·mL-1,维生素B12和生物素浓度均约为1.5、2.4、3、3.6、4.5 μg·mL-1的混合对照品溶液。中间浓度的混合对照品溶液(浓度和供试品溶液的相当)作为标准工作液,应用于方法的系统适用性研究。以上所有溶液均在棕色量瓶中配制,避光操作。混合对照品溶液进样前,经0.22 μm微孔滤膜滤过。
2.3 供试品溶液的制备取复合维生素B片20片,精密称定,研细,精密称取粉末适量(约相当于叶酸1.2 mg,维生素B12 0.15 mg,生物素0.15 mg),置于50 mL量瓶中,加入0.1%氢氧化钠溶液30 mL,振荡2 min,超声(800 W,40 kHz)60 min,加0.1%氢氧化钠溶液稀释至刻度,摇匀,经0.22 μm微孔滤膜滤过,取续滤液作为供试品溶液。以上过程应避光操作。
2.4 阴性溶液的制备依据复合维生素B片说明书提供的辅料配方,按“2.3”项下方法操作,制备阴性溶液。
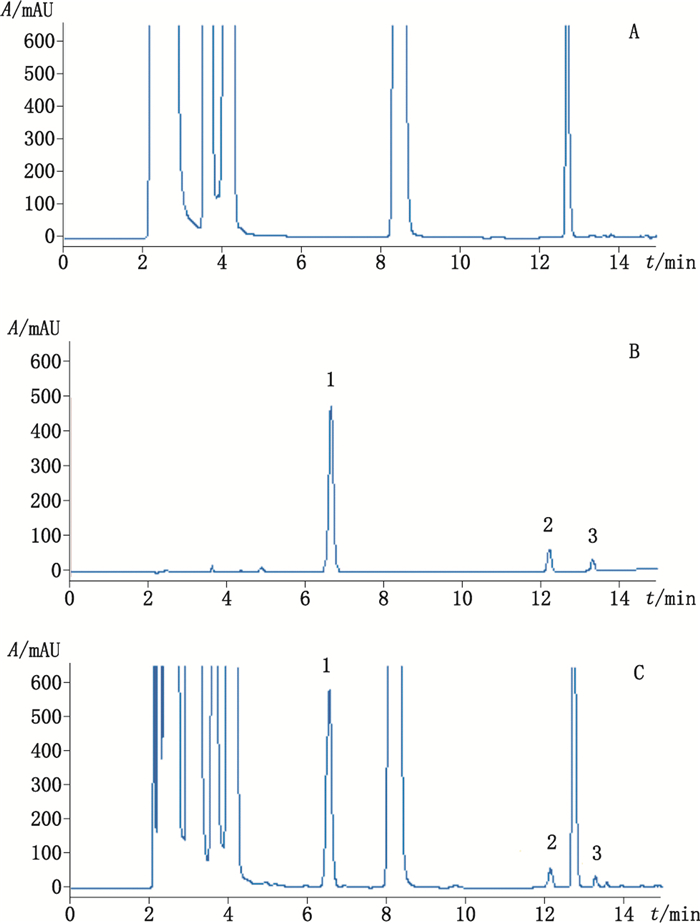
2.5 专属性试验分别对阴性溶液、混合对照品溶液和供试品溶液进样分析,考察样品中辅料对待测成分色谱峰的干扰。阴性溶液、混合对照品溶液和供试品溶液的色谱图(图 1)显示:样品中辅料和其他成分不干扰叶酸、维生素B12和生物素的测定。
|
1.叶酸(folic acid) 2.维生素B12(vitamin B12) 3.生物素(biotin) 图 1 阴性溶液(A)、混合对照品溶液(B)和供试品溶液(C)的HPLC色谱图 Figure 1 HPLC chromatograms of placebo solution(A), mixed reference solution(B), and analytical sample solution(C) |
取标准工作液连续进样6次,考察叶酸、维生素B12和生物素色谱峰的平均理论塔板数、对称因子和分离度,结果见表 1。分别精密吸取“2.2”项下各浓度混合对照品溶液50 μL注入液相色谱仪,按上述色谱条件测定,以峰面积Y为纵坐标,质量浓度X(μg·mL-1)为横坐标作标准曲线,得到回归方程和线性相关系数(r)。将混合对照品溶液逐级稀释后,以信噪比(S/N)约为3.0时的质量浓度为各成分的检测下限(LOD),S/N约为10.0时的质量浓度为各成分的定量下限(LOQ)。结果见表 2。
|
|
表 1 系统适应性考察结果(均值±SD,n=6) Table 1 Results of system suitability(mean±SD, n=6) |
|
|
表 2 标准曲线、线性范围、检测下限及定量下限 Table 2 The regression equations, linear ranges, LODs and LOQs |
对批号为3973052的1份供试品溶液连续进样6次,计算得到叶酸、维生素B12和生物素色谱峰峰面积的RSD(n=6)分别为0.063%、0.10%和0.31%,表明仪器的精密度良好。取低、中、高浓度的3份混合对照品溶液,每隔4 h进样1次,做日内精密度试验;每隔12 h进样1次,做日间精密度试验,连续做3 d。根据峰面积积分值计算分析日内及日间精密度,结果见表 3。
|
|
表 3 日内及日间精密度考察结果 Table 3 Results of intra-day and inter-day precision |
对批号3973052的样品独立制备供试品溶液6份,分别进样分析,计算得到叶酸、维生素B12和生物素的含量测定结果分别为484.1、48.31和51.89 μg·片-1,RSD(n=6)分别为1.8%、0.51%和0.41%,说明方法的重复性良好。
2.9 回收率试验取空白基质约2.0 g,精密称定,再分别精密加入混合对照品储备液适量,按照“2.3”项下方法操作,制备各回收率溶液,在相当于供试品溶液80%、100%、120%的浓度水平下,分别考察回收率。每个浓度制备3份,共9份供试溶液。以实际测得量和理论加入量的比值作为回收率,计算回收率的RSD,结果见表 4,表明方法回收率良好。
|
|
表 4 回收率试验结果 Table 4 Results of recovery test |
对批号为3973052的供试品溶液分别于配制后的0、2、4、8、12、24 h进样分析,计算得到24 h内叶酸、维生素B12和生物素色谱峰峰面积的RSD(n=6)分别为0.12%、0.11%和0.98%,表明供试品溶液在24 h内稳定性良好。
2.11 样品测定应用建立的方法对批号为3973052、3989178和3972021的复方维生素B片进行含量测定,每个样品测定2份,取平均值。测定结果见表 5。
|
|
表 5 样品中3个维生素成分的含量 Table 5 Contents of three vitamins in samples |
根据各成分在流动相中的紫外吸收谱图来确定检测波长。叶酸、维生素B12和生物素的紫外谱图分别在196、206、195 nm处有最大吸收,兼顾3个成分综合考虑,在200 nm处均有较强吸收,并且3个成分的含量低,在200 nm处色谱峰的响应值适合定量,故选择200 nm作为检测波长。
3.2 色谱条件的优化本研究采用乙腈-50 mmol·L-1磷酸二氢铵溶液(磷酸调至pH 3.0)为流动相,叶酸、维生素B12和生物素色谱峰的对称性及理论塔板数均良好,并且可以保证样品中的其他活性成分和辅料不干扰3个待测成分的测定。考察了不同梯度洗脱程序,并比较了不同流速(0.5、0.8、1.0 mL·min-1)、不同进样体积(5、10、20、50 µL)的影响,在最终确定的色谱条件下,3个待测成分间以及与样品中含量高的活性成分、辅料中的其他成分之间分离度良好,保留时间适宜,在15 min内即可实现对3个成分的含量测定。
3.3 提取方法的选择叶酸和生物素易溶于稀碱溶液,而在水中的溶解性较差。本研究比较了用不同浓度的氢氧化钠溶液(0.01%、0.05%、0.1%)作为提取溶剂对3个成分的影响,结果显示用0.1%氢氧化钠提取时可以将3个待测成分提取完全,故选为最终的提取溶剂。比较了不同超声提取时间(15、30、60 min),结果显示超声时间为60 min时对各成分的提取率最高,因3个待测成分的含量低,采用短时间超声难以将其提取完全。比较了不同取样量(0.2、0.5、0.8、3片)的影响,结果显示当取样量为0.2片、0.5片和0.8片时叶酸、维生素B12和生物素的峰高较低,不适合定量分析,当取样量为3片量(约相当于叶酸1.2 mg,维生素B12 0.15 mg,生物素0.15 mg),加提取溶剂定咅至50 mL时各成分的响应值合适。叶酸和维生素B12对光较敏感,本研究采取避光操作,并且采用棕色量瓶和液相进样小瓶,结果显示对照品及样品的溶液在避光条件下稳定性良好。
3.4 方法学验证本研究的方法学验证参照国际通行的ICH方法学验证原则[23-24]进行,内容包括系统适用性(理论塔板数、对称因子、分离度)、线性、检测限、定量下限、专属性、精密度、重复性、稳定性、准确度(回收率),结果表明建立的分析方法准确、可靠,适合于复合维生素B片中微量叶酸、维生素B12和生物素的准确测定,可为复合维生素B片的质量控制提供参考。
| [1] |
叶立, 田义梅. 紫外分光光度法测定叶酸片的含量[J]. 天津药学, 2000, 12(3): 63. YE L, TIAN YM. Determination of folic acid tablets by UV spectrophotometry[J]. Tianjin Pharm, 2000, 12(3): 63. |
| [2] |
靳月琴, 郭丽敏, 宋建荣, 等. 紫外可见分光光度法测定维生素B12含量[J]. 长治医学院学报, 2007, 21(4): 251. JIN YQ, GUO LM, SONG JR, et al. The content measurement of VB12 by UV-Vis[J]. J Changzhi Med Coll, 2007, 21(4): 251. |
| [3] |
夏瑞, 车宝泉, 张喆, 等. RP-HPLC测定复方硫酸亚铁叶酸片中叶酸的含量[J]. 中国药学杂志, 2006, 41(23): 1835. XIA R, CHE BQ, ZHANG Z, et al. Determination of folic acid in compound ferrous sulfate and folic acid tablets by RP-HPLC[J]. Chin Pharm J, 2006, 41(23): 1835. DOI:10.3321/j.issn:1001-2494.2006.23.022 |
| [4] |
孙䶮. 多元维生素片中叶酸含量的HPLC测定方法验证[J]. 海峡药学, 2012, 24(4): 46. SUN Y. Determination of folic acid in centrum tablets by HPLC[J]. Strait Pharm J, 2012, 24(4): 46. |
| [5] |
陈航, 邓丽明. 高效液相法测定叶酸片中叶酸的含量[J]. 分析科学学报, 2012, 28(4): 587. CHEN H, DENG LM. Determination of folic acid in folic acid tablets by HPLC[J]. J Anal Sci, 2012, 28(4): 587. |
| [6] |
刘淑华, 郑琰, 孙素杰. RP-HPLC法测定维生素B12片的含量[J]. 中国药事, 2007, 21(10): 825. LIU SH, ZHENG Y, SUN SJ. Determination of vitamin B12 tablets by RP-HPLC[J]. Chin Pharm Aff, 2007, 21(10): 825. DOI:10.3969/j.issn.1002-7777.2007.10.019 |
| [7] |
曹玮, 刘梅妍, 冉俐. HPLC法测定注射用水溶性维生素中维生素B12和生物素的含量[J]. 中国药房, 2007, 18(8): 543. CAO W, LIU MY, RAN L. Determination of vitamin B12 and biotin in water-soluble vitamin for injection by HPLC[J]. J China Pharm, 2007, 18(7): 543. |
| [8] |
宋新康, 姚海燕, 陈彬. HPLC法测定维生素B12片含量及含量均匀度[J]. 中国药师, 2014, 17(9): 1598. SONG XK, YAO HY, CHEN B. Determination of content and content uniformity of vitamin B12 tablets by HPLC[J]. China Pharm, 2014, 17(9): 1598. |
| [9] |
蔡美香, 华永有, 黄宏南, 等. HPLC法测定保健食品中生物素的含量[J]. 海峡预防医学杂志, 2009, 15(5): 45. CAI MX, HUA YY, HUANG HN, et al. Determination of biotin in health foods by HPLC[J]. Strait J Prev Med, 2009, 15(5): 45. |
| [10] |
杜碧莹, 刘丽芳. 注射用水溶性维生素中生物素含量测定方法改进[J]. 临床合理用药, 2010, 3(2): 11. DU BY, LIU LF. Improvement on the determination of biotin in water-soluble vitamin for injection[J]. Chin J Clin Ration Drug Use, 2010, 3(2): 11. |
| [11] |
HAYAKAWA K, KATSUMATA N, HIRANO M. Determination of biotin(vitamin H)by the high-performance affinity chromatography with a trypsin-treated avidin-bound column[J]. J Chromatogr B, 2008, 869(1-2): 93. DOI:10.1016/j.jchromb.2008.05.016 |
| [12] |
吴宏富, 黄卫平, 刘放. 高效液相色谱法测定叶酸片的含量与有关物质[J]. 医药导报, 2014, 33(3): 389. WU HF, HUANG WP, LIU F. Determination of folic acid tablets and its related substances by HPLC[J]. Her Med, 2014, 33(3): 389. |
| [13] |
刘毅, 岳志华. HPLC测定维生素B12注射液的含量和有关物质[J]. 中国药学杂志, 2010, 45(4): 304. LIU Y, YUE ZH. Determination of content and related substances in vitamin B12 injection by HPLC method[J]. Chin Pharm J, 2010, 45(4): 304. |
| [14] |
黄东萍, 张国柱, 周永丽, 等. 反相高效液相色谱法测定维生素B12片的含量[J]. 中国药业, 2010, 19(23): 30. HUANG DP, ZHANG GZ, ZHOU YL, et al. Content determination of vitamin B12 tablets by RP-HPLC[J]. China Pharm, 2010, 19(23): 30. DOI:10.3969/j.issn.1006-4931.2010.23.019 |
| [15] |
OHNISHI Y, YOMOTA C. Determination of biotin following derivatization with 2-nitrophenylhydrazine by high-performance liquid chromatography with on-line UV detection and electrospray-ionization mass spectrometry[J]. J Chromatogr A, 2007, 1142(2): 231. DOI:10.1016/j.chroma.2006.12.058 |
| [16] |
MARKOPOULOU CK, KAGKADIS KA, KOUNDOURELLIS JE. An optimized method for the simultaneous determination of vitamins B1, B6, B12 in multivitamin tablets by high performance liquid chromatography[J]. J Pharm Biomed Anal, 2002, 30(4): 1403. DOI:10.1016/S0731-7085(02)00456-9 |
| [17] |
RYCHLIK M. Simultaneous analysis of folic acid and pantothenic acid in foods enriched with vitamins by stable isotope dilution assays[J]. Anal Chim Acta, 2003, 495(1-2): 133. DOI:10.1016/j.aca.2003.08.020 |
| [18] |
NELSON BC, SHARPLESS KE, SANDER LC. Quantitative determination of folic acid in multivitamin/multielement tablets using liquid chromatography/tandem mass spectrometry[J]. J Chromatogr A, 2006(1135): 203. |
| [19] |
ZHAO SL, YUAN HY, XIE C, et al. Determination of folic acid by capillary electrophoresis with chemiluminescence detection[J]. J Chromatogr A, 2006(1107): 290. |
| [20] |
李跃中, 王晗, 唐靓, 等. 微生物法测定食品中生物素含量的研究[J]. 中国卫生检验杂志, 2010, 20(6): 1406. LI YZ, WANG H, TANG L, et al. Study on microbiological method of biotin determination in food[J]. Chin J Health Lab Technol, 2010, 20(6): 1406. |
| [21] |
郑巍振, 裘娟萍, 赵春田, 等. 一种简捷的生物素含量测定方法[J]. 食品与发酵工业, 2009, 35(10): 135. ZHENG WZ, QIU JP, ZHAO CT, et al. A simple method for detecting content of biotin[J]. Food Ferment Ind, 2009, 35(10): 135. |
| [22] |
中华人民共和国药典2015年版. 二部[S]. 2015: 194, 1235 ChP 2015. Vol Ⅱ[S]. 2015: 194, 1235 |
| [23] |
ICH-Q2A. Text on Validation of Analytical Procedures[S]. 1995
|
| [24] |
ICH-Q2B. Validation of Analytical Procedures: Methodology[S]. 1996
|
 2018, Vol. 38
2018, Vol. 38 
