田七痛经胶囊由三七、五灵脂、蒲黄等8味中药组成,具通调气血、止痛调经之功效,用于经期腹痛及因寒所致的月经失调。方中,三七为君药,蒲黄与五灵脂配伍使用,是本方起活血化瘀、散结止痛作用的基础药对,为臣药[1-4]。蒲黄主含黄酮类、甾醇类、多糖类、氨基酸类、挥发油等化学成分[5-6]。现阶段药理研究表明,黄酮糖苷类化合物,尤其是香蒲新苷和异鼠李素-3-O-新橙皮苷是蒲黄起活血镇痛作用的主要有效成分[7-10]。现有的蒲黄含量测定的主要方法是高效液相色谱法[11-13],但是由于本方成分较多,相互干扰,高效液相色谱法不适合测定田七痛经胶囊中的蒲黄含量。
目前,现行的田七痛经胶囊的质量标准共3种,均未对蒲黄的含量加以控制,存在标准过低,无法全面控制药品质量的问题[14-16]。为了更全面地评价田七痛经胶囊的质量,本实验采用UPLC-MS/MS技术建立了田七痛经胶囊中蒲黄的主要有效成分香蒲新苷和异鼠李素-3-O-新橙皮苷的含量测定方法,为进一步完善田七痛经胶囊的质量标准提供实验依据。
1 仪器与试药Agilent 1290/Agilent 6460超高效液相色谱-质谱联用系统,配有QQQ Quantitative Analysis工作站和Quantitative Analysis B.05.00工作站(Agilent公司);BP211D型(0.01 mg)和LE244S型电子天平(0.000 1 g)(Satorius公司)。
香蒲新苷对照品(批号111573-201405,含量97.0%)异鼠李素-3-O-新橙皮苷对照品(批号111571-201205,含量93.2%)均购自中国食品药品检定研究院。田七痛经胶囊由云南白药集团股份有限公司生产(批号ZBA1602、ZBA1606、ZBA1607)。水为超纯水,其他试剂均为色谱纯。
2 方法与结果 2.1 色谱及质谱条件色谱柱:Agilent公司Infiniti Lab Poroshell 120 SB-C18色谱柱(2.7 μm,4.6 mm×100 mm;填料:十八烷基硅烷键合硅胶);流动相:以乙腈为流动相A,含0.02 mol·L-1乙酸铵的0.2%乙酸为流动相B,梯度洗脱(0~8 min,20% A→40% A;8~10 min,40% A→90% A);流速:0.3 mL·min-1;柱温:35 ℃;进样量:5 μL;采用电喷雾离子源(ESI),多反应监测模式(MRM),正离子监测,雾化气压力0.28 MPa;毛细管电压3.5 kV;干燥气温度300 ℃;干燥气流量6 L·min-1。香蒲新苷和异鼠李素-3-O-新橙皮苷的MS参数见表 1。
|
|
表 1 田七痛经胶囊中2个成分的保留时间和主要质谱参数 Table 1 Retention time(tR)and main mass parameters of two constituents in Tianqi Tongjing capsules |
取对照品香蒲新苷10.16 mg、异鼠李素-3-O-新橙皮苷10.90 mg,置同一100 mL量瓶中,加80%甲醇水溶解并稀释至刻度,摇匀,作为储备液;精密量取上述储备液3 mL,置10 mL量瓶中,加80%甲醇水稀释至刻度,摇匀,作为混合对照品储备液(香蒲新苷和异鼠李素-3-O-新橙皮苷的质量浓度分别为0.029 57 mg·mL-1和0.030 48 mg·mL-1)。
2.2.2 供试品溶液取本品内容物1 g,精密称定,精密加入80%甲醇水50 mL,称量,浸泡过夜,加热回流1 h,用80%甲醇水补足减失的量,摇匀,滤过;精密量取续滤液1 mL置10 mL量瓶中,加80%甲醇水定容至刻度,摇匀,用微孔滤膜(0.22 μm)滤过,取续滤液作为供试品溶液。
2.2.3 阴性样品溶液按本品处方制备缺少蒲黄的阴性样品,照“2.2.2”项下方法制备阴性样品溶液。
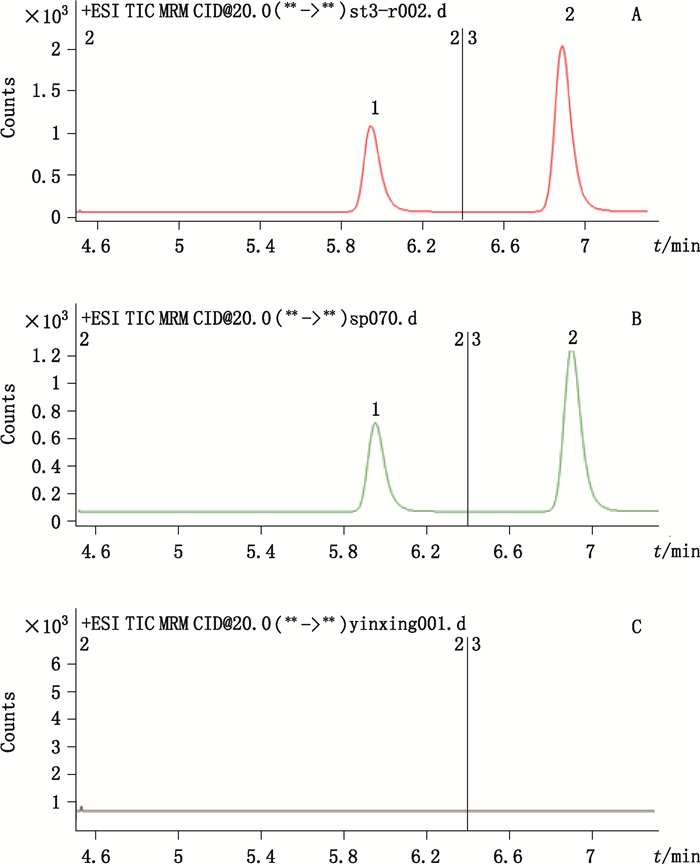
2.3 方法学考察 2.3.1 专属性考察分别精密吸取混合对照品溶液、供试品溶液和阴性样品溶液,按“2.1”项下色谱及质谱条件进行测定,结果见图 1。
|
图 1 混合对照品(A)、样品(B)和阴性样品(C)中香蒲新苷(峰1)和异鼠李素-3-O-新橙皮苷(峰2)的LC-MS/MS图 Figure 1 LC-MS/MS chromatograms of typhaneoside(peak 1)and isorhamnetin-3-O-neohesperidoside(peak 2)in reference substance(A), sample(B)and negative sample(C) |
精密吸取上述混合对照品储备液,分别稀释成约0.3、0.6、1.2、1.5、3.6、6.0 μg·mL-1的系列混合对照品溶液,按照“2.1”项下的条件进行测定。以对照品进样质量浓度X(ng·mL-1)为横坐标,各成分的峰面积Y为纵坐标,绘制标准曲线。结果表明各成分在相应的线性范围内线性关系良好。结果见表 2。
|
|
表 2 田七痛经胶囊中2个成分的线性关系、检测下限和定量下限 Table 2 Linear relations, LODs and LOQs of the 2 constituents in Tianqi Tongjing capsules |
取批号为ZBA1602的样品,按照“2.2.2”项下方法制备供试品溶液,按“2.1”项下条件连续进样6次,记录峰面积,计算香蒲新苷和异鼠李素-3-O-新橙皮苷峰面积的RSD(n=6)分别为0.9%和0.3%。结果表明,仪器精密度良好。
2.3.4 稳定性试验取批号为ZBA1602的样品,按照“2.2.2”项下方法制备供试品溶液,分别于0、1、2、5、8、10、12 h按“2.1”项下条件进样,记录峰面积,计算香蒲新苷和异鼠李素-3-O-新橙皮苷峰面积的RSD(n=6)分别为2.7%和2.3%。结果表明供试品溶液中香蒲新苷和异鼠李素-3-O-新橙皮苷在12 h内稳定性良好。
2.3.5 重复性试验取批号为ZBA1602的样品,按照“2.2.2”项下方法平行制备6份供试品溶液,按“2.1”项下条件分别进样,记录峰面积并计算含量。计算香蒲新苷和异鼠李素-3-O-新橙皮苷的平均含量(n=6)分别为0.305 6 mg·g-1和0.289 9 mg·g-1,RSD分别为1.7%和2.0%。结果表明方法的重复性良好。
2.3.6 检测下限和定量下限将混合对照品溶液逐步稀释,分别以信噪比S/N=3和S/N=10时各对照品溶液的质量浓度作为检测下限和定量下限。结果见表 2。
2.3.7 回收率试验精密称定已知含量的同一批样品(批号ZBA1602含香蒲新苷0.305 6 mg·g-1异鼠李素-3-O-新橙皮苷0.289 9 mg·g-1)0.5 g,共6份,分别精密加入混合对照品溶液5 mL,80%甲醇水45 mL, 称定重量,浸泡过夜,加热回流1 h,用80%甲醇水补足减失重量,摇匀,滤过。精密量取续滤液1 mL置10 mL量瓶中,加80%甲醇水定容至刻度,摇匀,用微孔滤膜(0.22 μm)滤过,取续滤液,按“2.1”项下条件进样,记录峰面积并计算含量。计算香蒲新苷和异鼠李素-3-O-新橙皮苷的平均回收率(n=6)分别为94.5%和103.5%,RSD分别为2.9%和2.7%。回收率良好。
2.3.8 含量测定取3批田七痛经胶囊样品各2份,按照“2.2.2”项下方法制备供试品溶液,按“2.1”项下条件进样,记录峰面积并计算含量。结果见表 3。
|
|
表 3 样品含量测定结果(mg·g-1) Table 3 Content determination of samples |
作为本方的臣药,蒲黄具有止血、化瘀、通淋的作用[17],尤其是与五灵脂配伍使用后,是田七痛经胶囊活血化瘀、散结止痛作用的基础,因此,对蒲黄加以质量控制是十分必要的。田七痛经胶囊的组方中,其他药材的含量测定方法均已有相关的文献报道[18-24],而蒲黄的含量测定虽有文献报道,但针对的是其中总黄酮的水解产物槲皮素、山柰素和异鼠李素[25]。这3种成分来源较为广泛,不属于蒲黄的特征性成分,专属性不强;且研究表明,香蒲新苷和异鼠李素-3-O-新橙皮苷等黄酮苷类成分有抑制凝血、活血化瘀的功效,而其主要苷元异鼠李素等则无明显影响[26]。香蒲新苷和异鼠李素-3-O-新橙皮苷既是有效成分,又是特征性成分,且在蒲黄的黄酮中含量最多[27]。因此,选择蒲黄作为研究对象,并以香蒲新苷和异鼠李素-3-O-新橙皮苷为质量控制指标,对田七痛经胶囊的质量控制而言,是较为合理的补充。
3.2 检测方法的选择曾尝试用HPLC-UV法测定本品中香蒲新苷和异鼠李素-3-O-新橙皮苷的含量,但实验发现存在严重的阴性干扰,经过多次调整洗脱梯度及更换色谱柱,均未能将这2个成分与干扰成分完全分离。因此,必须采用专属性强的检测手段建立上述2种成分的含量测定方法。而质谱法具有高选择性及高灵敏度等特点,可避开其他成分的干扰,有效地提高本品的质量控制水平,故选择液质联用方法作为检测方法[28]。
3.3 样品处理方法的选择本实验条件对样品的处理方法进行了优化筛选:分别以甲醇、80%甲醇水和40%乙醇水为溶剂,溶剂体积分别为25、50和100 mL,使用冷浸过夜后加热回流1 h,冷浸过夜超声1 h和直接加热回流2 h共3种提取方式,以检测的2种成分总量计,结果显示80%甲醇水50 mL,浸泡过夜,加热回流1 h提取较为完全,且方法经济,简便易行。
3.4 小结田七痛经胶囊作为市场主流产品,其现行质量标准较低,对产品质量的控制起不到较好的约束作用,应对其建立全面统一的质量规范,以保证药品的疗效。本文采用UPLC-MS/MS技术,针对田七痛经胶囊质量控制的研究空白,建立有效成分的定量测定方法,方法简单、灵敏度高,可准确快速的分析测定蒲黄中的2个有效成分,为田七痛经胶囊的质量控制提供有效的补充。
| [1] |
肖培根. 新编中药志.第二卷[M]. 北京: 化学工业出版社, 2002, 812. XIAO PG. Modern Chinese Materia Medica.Volumn two[M]. Beijing: Chemical Industry Press, 2002, 812. |
| [2] |
宿树兰, 华永庆, 段金廒, 等. 少腹逐瘀汤对小鼠离体子宫收缩模型的生物效应及物质基础评价[J]. 中国药科大学学报, 2007, 38(6): 544. SU SL, HUA YQ, DUAN JA, et al. In vitro inhibition on the contraction of isolated mouse uterine and chemical components of Shaofu Zhuyu decoction[J]. J China Pharm Univ, 2007, 38(6): 544. DOI:10.11665/j.issn.1000-5048.20070615 |
| [3] |
王丽君, 廖矛川, 肖培根. 中药蒲黄的化学与药理活性[J]. 时珍国药研究, 1998, 9(1): 49. WANG LJ, LIAO MC, XIAO PG. Chemistry and pharmacological activity of a traditional Chinese drug Pollen Typhae[J]. Shizhen J Tradit Chin Med Res, 1998, 9(1): 49. |
| [4] |
王潇毅, 田晓轩, 张砚, 等. 基于活性筛选和靶标网络预测的蒲黄和赤芍选择性抑制血小板聚集作用[J]. 中国实验方剂学杂志, 2017, 23(1): 120. WANG XY, TIAN XX, ZHANG Y, et al. Selective inhibitory effect of Typhae Pollen and Paeoniae Radix Rubra on platelet aggregation based on activity screening and target network prediction[J]. Chin J Exp Tradit Med Form, 2017, 23(1): 120. |
| [5] |
张淑敏, 曲桂武, 解飞霞, 等. 蒲黄化学成分研究[J]. 中草药, 2008, 39(3): 350. ZHANG SM, QU GW, XIE FX, et al. Study on chemical constituents in pollen of Typha angustifolia[J]. Chin Tradit Herb Drugs, 2008, 39(3): 350. |
| [6] |
李芳, 陈佩东, 丁安伟. 蒲黄化学成分研究[J]. 中草药, 2012, 43(4): 667. LI F, CHEN PD, DING AW. Study on chemical constituents in pollen of Typha angustifolia[J]. Chin Tradit Herb Drugs, 2012, 43(4): 667. |
| [7] |
宿树兰, 薛萍, 欧阳臻, 等. 蒲黄-五灵脂配伍前后效应成分变化及其抗血小板聚集和抗凝血酶活性评价[J]. 中国中药杂志, 2015, 40(16): 3187. SU SL, XUE P, OUYANG , et al. Study on antiplatelet and antithrombin activities and effective components variation of Puhuang-Wulingzhi before and after compatibility[J]. China J Chin Mater Med, 2015, 40(16): 3187. |
| [8] |
薛萍, 欧阳臻, 宿树兰, 等. 蒲黄-五灵脂配伍前后化学成分溶出变化的定量分析[J]. 中成药, 2013, 35(12): 2689. XUE P, OUYANG , SU SL, et al. Analysis of the changes of chemical components dissolution of Puhuang-Wuling-zhi before and after compatibility[J]. Chin Tradit Pat Med, 2013, 35(12): 2689. DOI:10.3969/j.issn.1001-1528.2013.12.029 |
| [9] |
冯绪强, 曾光尧, 谭健兵, 等. 水烛香蒲花粉镇痛活性部位化学成分研究[J]. 中南药学, 2012, 10(3): 202. FENG XQ, ZENG GY, TAN JB, et al. Chemical constituents of active analgesic parts in the pollen of Typha angustifolia L[J]. Central South Pharm, 2012, 10(3): 202. |
| [10] |
胡立宏, 房士明, 刘虹, 等. 蒲黄的化学成分和药理活性研究进展[J]. 天津中医药大学学报, 2016, 35(2): 136. HU LH, FANG SM, LIU H, et al. Research progress on chemical constituents and pharmacological activities of Pollen Typhae[J]. J Tianjin Univ Tradit Chin Med, 2016, 35(2): 136. DOI:10.11656/j.issn.1673-9043.2016.02.17 |
| [11] |
陈路晓, 刘斌, 郭凤霞, 等. 蒲黄药材中香蒲新苷和异鼠李素-3-O-新橙皮苷含量测定方法优化研究[J]. 北京中医药大学学报, 2016, 39(4): 304. CHEN LX, LIU B, GUO FX, et al. Optimization of determination method of typhaneoside and isorhamnetin-3-O-neohesperidoside in Pollen Typhae[J]. J Beijing Univ Tradit Chin Med, 2016, 39(4): 304. |
| [12] |
高珊, 张婷婷, 崔邵婧, 等. 市售蒲黄饮片的品质考察[J]. 中国药事, 2014, 28(3): 292. GAO S, ZHANG TT, CUI SJ, et al. Quality investigation on commercial Pollen Typhae decoction pieces[J]. Chin Pharm Aff, 2014, 28(3): 292. |
| [13] |
王俐萱, 牛立营, 潘英妮, 等. UPLC法测定蒲黄提取物中总黄酮醇苷的含量[J]. 中国现代中药, 2014, 16(9): 755. WANG LX, NIU LY, PAN YN, et al. Content determination of total favonol glycosideds of Typhae Pollen extract by UPLC[J]. Mod Chin Med, 2014, 16(9): 755. |
| [14] |
卫生部药品标准. 中药成方制剂. 第10册[S]. 1995: 38 Drug Specifications Promulgated by the Ministry of Public Health, PR China. Vol 10[S]. 1995: 38 |
| [15] |
YBZ01402005国家食品药品监督管理局标准(试行)[S]. 2005 YBZ01402005 The State Food and Drug Adminstration Issued a Drug Standard(Trail)[S]. 2005 |
| [16] |
YBZ13502009国家食品药品监督管理局标准[S]. 2009 YBZ13502009 The State Food and Drug Adminstration Issued a Drug Standard[S]. 2009 |
| [17] |
中华人民共和国药典2015年版. 一部[S]. 2015: 353 ChP 2015. VolⅠ[S]. 2015: 353 |
| [18] |
来国防, 杨东, 杜江, 等. HPLC法测定田七痛经散中三七皂苷R1、人参皂苷Rg1、Rb1的含量[J]. 中国药师, 2010, 13(1): 28. LAI GF, YANG D, DU J, et al. Determination the contents of notoginsenoside R1, ginsenoside Rg1 and ginsenoside Rb1 in Tianqi Tongjing powder by HPLC[J]. China Pharm, 2010, 13(1): 28. |
| [19] |
梁秀清, 廖卫国, 刘强, 等. HPLC法测定新田七痛经胶囊中藁本内酯和欧当归内酯A的含量[J]. 中国医药指南, 2015, 13(18): 3. LIANG XQ, LIAO WG, LIU Q, et al. HPLC determination of the liguistilide and levistolide A in New Tianqi Tongjing capsules[J]. Guide China Med, 2015, 13(18): 3. |
| [20] |
辛丹敏, 周光明, 黄成, 等. 反相高效液相色谱法同时测定田七痛经胶囊中延胡索乙素和阿魏酸[J]. 西南大学学报(自然科学版), 2009, 31(1): 41. XIN DM, ZHOU GM, HUANG C, et al. Determination of the contents of tetrahydropalmatine and ferulic acid in Tianqi Tongjing powder by HPLC[J]. J Southwest Univ(Nat Sci Ed), 2009, 31(1): 41. |
| [21] |
赵严丽, 曾奇风. 高效液相色谱法测定田七痛经胶囊中原儿茶酸含量[J]. 中国药业, 2013, 22(3): 11. ZHAO YL, ZENG QF. Content determination of protocatechuic acid in Tianqi Tongjing capsules by HPLC[J]. China Pharm, 2013, 22(3): 11. |
| [22] |
廖卫国, 朱红霞, 刘强, 等. 超微田七痛经胶囊的质量标准研究[J]. 今日药学, 2015, 25(7): 482. LIAO WG, ZHU HX, LIU Q, et al. Study on quality standard of ultramicro powder of Tianqi Tongjing capsules[J]. Phram Today, 2015, 25(7): 482. |
| [23] |
梁懿, 孟连琼. 田七痛经胶囊检测方法的研究[J]. 药物分析杂志, 2008, 28(2): 278. LIANG Y, MENG LQ. Study on the quality control standard of Tianqi Tongjing capsules[J]. Chin J Pham Anal, 2008, 28(2): 278. |
| [24] |
杨燕飞, 陈晓风. 气相色谱法测定田七痛经胶囊中冰片和茴香醚含量[J]. 中国药业, 2009, 18(24): 42. YANG YF, CHEN XF. GC-FID quantitative determination of synthetic borneol and anisole in Tianqi Tongjing capsules[J]. China Pharm, 2009, 18(24): 42. DOI:10.3969/j.issn.1006-4931.2009.24.029 |
| [25] |
黄俊忠, 曾小平. HPLC法同时测定田七痛经胶囊中异鼠李素、槲皮素、山柰素[J]. 中成药, 2012, 34(10): 1912. HAUNG JZ, ZENG XP. Assay of quercetin, kaempferol, isorhamnetin in Tianqi Tongjing capsules by HPLC[J]. Chin Tradit Pat Med, 2012, 34(10): 1912. DOI:10.3969/j.issn.1001-1528.2012.10.017 |
| [26] |
胡立宏, 房士明, 刘虹, 等. 蒲黄的化学成分和药理活性研究进展[J]. 天津中医药大学学报, 2016, 35(2): 136. HU LH, PANG SM, LIU H, et al. Research progress on chemical constituents and pharmacological activities of pollen Typhae[J]. J Tianjin Univ Tradit Chin Med, 2016, 35(2): 136. DOI:10.11656/j.issn.1673-9043.2016.02.17 |
| [27] |
TAO WW, YANG NY, DUAN JA. Simultaneous determination of eleven major flavonoids in the pollen of Typha angustifolia by HPLC-PDA-MS[J]. Phytochem Anal, 2011, 22(5): 455. DOI:10.1002/pca.v22.5 |
| [28] |
赵振霞, 王敏, 王钰宁, 等. UPLC-MS/MS法测定心可舒胶囊中5种皂苷类成分的含量[J]. 药物分析杂志, 2016, 36(3): 494. ZHAO ZX, WANG M, WANG YN, et al. Simultaneous determination of five saponins in Xinkeshu capsules by UPLC-MS/MS[J]. Chin J Pharm Anal, 2016, 36(3): 494. |
 2018, Vol. 38
2018, Vol. 38 
