2. 秦皇岛市第一医院药学部, 秦皇岛 066000;
3. 白求恩国际和平医院药剂科, 石家庄 050082
2. Department of Pharmacy, The First Hospital of Qinhuangdao, Qinhuangdao 066000, China;
3. Department of Pharmacy, Bethune International Peace Hospital, Shijiazhuang 050082, China
曲匹地尔(trapidil),化学名称为5甲基-7-二乙胺基-1,2,4-三唑并[1,5-α]嘧啶,具有对血小板衍生生长因子(PDFG)高度选择性的抑制作用,阻抑血栓素2(TXA2)的合成和活性,促进前列环素2(PGI2)的生成,预防SMC的增殖,保护血管内皮细胞,发挥血小板生长因子拮抗剂作用[1-2],临床上主要用于预防和治疗心绞痛、心肌梗塞、合并高血压症、高血脂症和脑血管疾病。近期的研究结果表明,曲匹地尔对肾脏、睾丸和心脏缺血再灌注损伤具有保护作用[3-6],能够用于预防和治疗烧伤引起多器官损伤和骨骼破坏性疾病[7-8]。
目前,曲匹地尔的检测方法有HPLC[9-10]、UV[11]和UPLC-MS[12],本文首次建立了液相色谱串联质谱(LC-MS/MS)法测定人血浆中曲匹地尔浓度的方法,该方法简便快速,专属性强,可用于测定人血浆中曲匹地尔的药物浓度,并将该方法应用于检测20名健康受试者口服曲匹地尔胶囊和曲匹地尔片后血浆样本中曲匹地尔药物浓度。依据药动学结果,对受试制剂的生物等效性进行评价,为曲匹地尔胶囊注册提供依据。
1 仪器与试药 1.1 仪器TSQ Quantum三级四极杆质谱仪(Thermo Fisher公司),包括Surveyor MS Pump Plus,Surveyor AS Plus,大气压化学离子化源(APCI),LCquan数据系统。BP211D型十万分之一天平(Sartorius公司);XW-80A旋涡混合器(上海精科实业有限公司);lDZ5-2型离心机(北京医用离心机厂)。
1.2 药品与试剂受试制剂:曲匹地尔胶囊(河北长天药业有限公司,规格为每粒50 mg,批号090609);参比制剂:曲匹地尔片(武汉迪奥药业有限公司,规格为每片50 mg,批号20090302);曲匹地尔对照品(中国食品药品检定研究院,批号100440-200301,含量99.7%);盐酸苯海拉明对照品(中国食品药品检定研究院,批号100066-199705,含量99.9%);甲醇(天津市康科德科技有限公司,批号090902),甲酸(天津市光复精细化工研究所,批号20040610)为色谱纯;甲酸铵(中国医药上海化学试剂公司,批号F20011023)为分析纯;实验用水为市售乐百氏纯净水;健康人空白血浆购自于白求恩国际和平医院血液中心。
2 试验方法 2.1 色谱条件保护柱:Phenomenex C18(4 mm×2.0 mm);色谱柱:MG S-5 C18分析柱(50 mm×4.6 mm,5 μm,十八烷基硅烷键合硅胶);流动相:甲醇-10 mol·L-1甲酸铵溶液(80:20);流速:0.4 mL·min-1;柱温:30 ℃。进样量:10 μL。
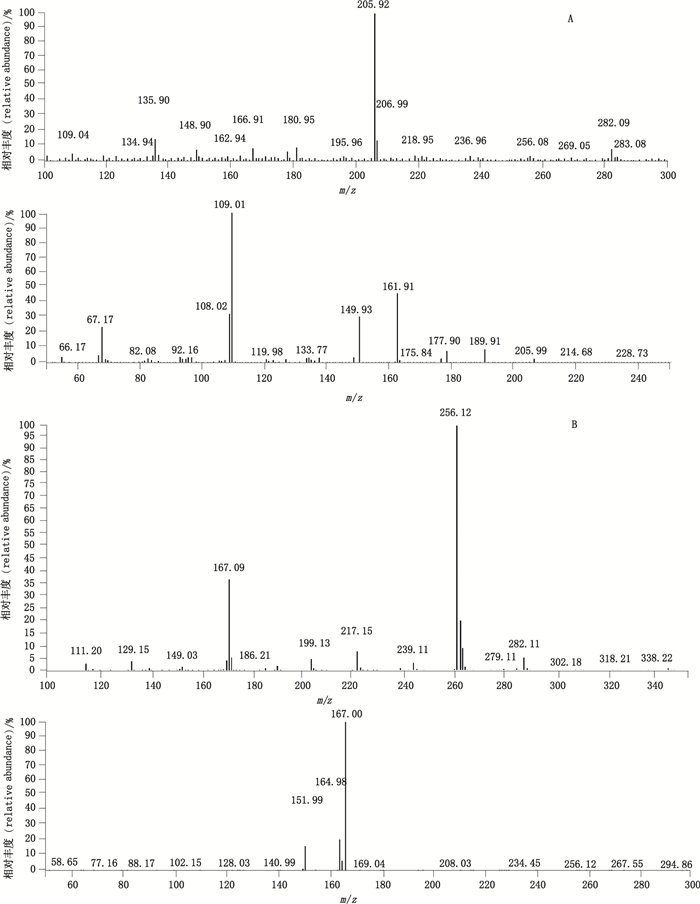
2.2 质谱条件大气压化学离子化源,离子检测方式:选择离子反应监测,离子极性:正离子;鞘气为241.3 kPa;辅助气为34.5 kPa;碰撞气为1.5 mTorr;雾化气温度为400 ℃;离子传输管温度为250 ℃;用于定量的离子分别为曲匹地尔m/z 206.0→109.0,碰撞诱导解离电压为23 V;内标苯海拉明m/z 256.1→167.1,碰撞诱导解离(CID)电压13 V;扫描时间均为200 ms。曲匹地尔和苯海拉明的质谱扫描图见图 1。
|
图 1 曲匹地尔(A)和苯海拉明(B)全扫描质谱图 Figure 1 Full scan product ion spectra of trapidil(A) and diphenhydramine(B) |
精密称取盐酸苯海拉明10.06 mg,置于10 mL瓶量中,用甲醇溶解并定容至刻度,配制成质量浓度为1.0 mg·mL-1的储备液。用甲醇将1.0 mg·mL-1苯海拉明储备液分别稀释成400 ng·mL-1和200 ng·mL-1的内标工作液,置于4 ℃冰箱中保存,备用。
2.3.2 曲匹地尔对照品溶液精密称取曲匹地尔对照品16.4 mg,置于10 mL量瓶中,用甲醇溶解并定容至刻度,配制成曲匹地尔质量浓度为1.64 mg·mL-1的储备液。取曲匹地尔储备液适量,用甲醇稀释后与400 ng·mL-1内标工作液等比混匀成质量浓度为6 400 ng·mL-1的对照品溶液,然后用200 ng·mL-1的内标工作液稀释成质量浓度为8、20、40、100、200、400、800、1 600、3 200、5 120 ng·mL-1的曲匹地尔系列对照品溶液,置于4 ℃冰箱中保存,备用。
2.3.3 质控样品分别取不同浓度的曲匹地尔系列对照品溶液适量,用空白血浆稀释,配制成曲匹地尔质量浓度为10、200、2 560 ng·mL-1的质控样品,备用。
2.4 血浆样品处理固相萃取小柱加甲酸3 mL和水3 mL活化后备用。取血浆100 mL,加入内标工作液(200.0 ng·mL-1苯海拉明)50 mL,涡旋混匀20 s,加水1 mL,涡旋混合20 s,4 000 r·min-1离心10 min,取上清液1 mL上样。先后用2 mL水和0.4 mL洗脱溶剂[甲醇-10 mol·L-1甲酸铵(80:20),含甲酸0.2%]洗去杂质,再用1 mL洗脱溶剂洗脱样品,洗脱溶液涡旋混合20 s,取上清液200 mL置于进样器瓶中,进样量为10 μL,进行LC-MS/MS分析。
2.5 试验方案设计受试者选择:20名健康男性受试者,平均年龄(23±1)岁,体质量(64±6)kg,身高(1.72±0.06)m,体重指数在19~24范围。试验前进行病史询问和体格检查,血常规、尿常规、肝肾功能及心电图检查均正常。无体位低血压史,心率55~100次·min-1;无烟、酒嗜好;为避免其他药物干扰,试验前2周内及试验期间禁服任何其他药物;试验期间禁烟、酒及含咖啡因的饮料,或某些可能影响代谢的果汁等,以免干扰药物体内代谢;无滥用药物史;无晕针、晕血史。受试者了解试验目的、方法、意义以及可能发生的不良反应后签署知情同意书。试验方案经白求恩国际和平医院伦理委员会审查批准。
给药方案与样本采集:采用单剂量口服、随机、开放、两制剂、双周期、交叉设计方法进行曲匹地尔胶囊与曲匹地尔片的生物等效性试验。在试验周期,20名受试者于试验前一天进食清淡晚餐后禁食10 h以上,试验当日早晨空腹口服受试制剂或参比制剂,剂量均为50 mg。2个周期间清洗周期为1周。分别于服药前(0 h)及服药后0.17、0.33、0.5、0.75、1、1.5、2、3、4、6、8、10、12 h肘静脉采血3 mL,置肝素抗凝试管中,摇匀,3 000 r·min-1离心10 min,分离血浆,置-20 ℃下冻存,待测。
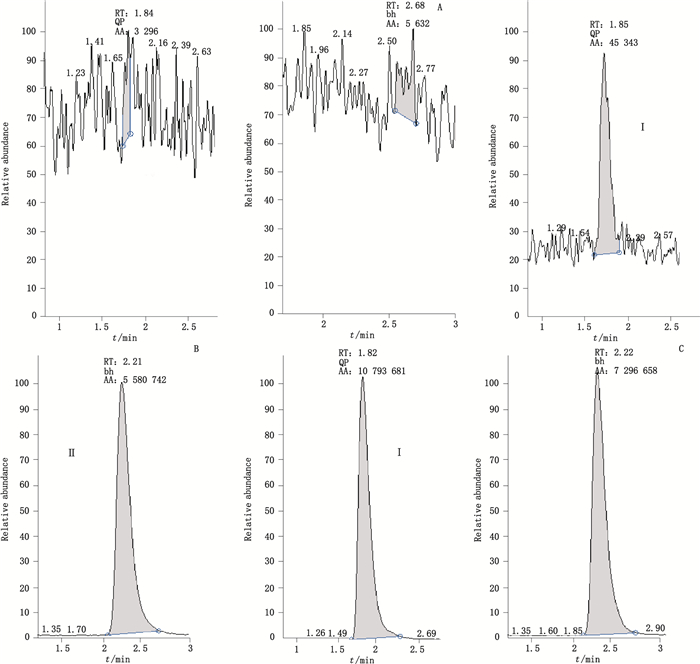
3 结果 3.1 专属性取空白血浆,除不加内标工作液外(以甲醇代替),按“2.4”项方法操作,获得空白样品的色谱图;空白血浆样品中加入待测物对照品溶液和内标工作液,按“2.4”项方法操作,获得加标血浆样品色谱图,考察方法专属性。结果见图 2,由图可知,曲匹地尔和内标物峰形良好,分离效果佳,曲匹地尔和内标的保留时间分别为1.9 min和2.2 min,血浆中的内源性物质不干扰曲匹地尔和内标的测定。本方法具有高度的专属性。
|
1.曲匹地尔(trapidil) 2.苯海拉明(diphenhydramine) A.空白血浆(blank plasma)B.曲匹地尔对照品血浆(plasma of trapidil control,4.0 ng·mL-1)+内标溶液(internal standard solution,10.0 ng·mL-1)C.健康志愿者口服曲匹地尔胶囊(50 mg)后1 h的血浆样本+内标溶液(10.0 ng·mL-1)[plasma sample from a healthy volunteer 1 h after oral administration of trapidil capsule 50 mg + internal standard solution(10.0 ng·mL-1)] 图 2 典型色谱图 Figure 2 Typical chromatograms |
分别取不同浓度的曲匹地尔对照品溶液适量,加入0.1 mL空白血浆中,配成曲匹地尔质量浓度为4.0、10.0、20.0、50.0、100、200、400、800、1 600、3 200 ng·mL-1的血浆样品,除不加内标外,其余按“2.4”项下方法处理后,以曲匹地尔质量浓度(X)为横坐标,曲匹地尔与内标的峰面积比(Y)为纵坐标,用加权最小二乘法进行线性回归,加权系数为1/X2,计算求得回归方程:
| $ Y = 1.562 \times {10^{ - 3}}X + 4.061 \times {10^{ - 4}}\;\;\;\;r = 0.999\;5 $ |
结果表明,血浆中曲匹地尔质量浓度在4.0~3 200 ng·mL-1范围内线性关系良好。
3.3 定量下限按“线性范围”项下方法,每天平行配制曲匹地尔质量浓度为4.0 ng·mL-1的加标血浆样品6份,连续配制3 d,除不加内标外,其余按“2.4”项下方法处理后进样分析,由随行标准曲线计算质量浓度。测得曲匹地尔的定量下限(LLOQ)为4.0 ng·mL-1,RSD为10.3%(n=18)。
3.4 精密度与准确度分别取曲匹地尔低、中、高质量浓度质控样品各6份,除不加内标外,其余按“2.4”项下方法处理后进样分析,由随行标准曲线计算各样品质量浓度,并计算方法的精密度与准确度(n=6);连续测定4批,计算批间精密度与准确度,结果见表 1。
|
|
表 1 血浆中曲匹地尔的日内和日间精密度与准确度试验结果 Table 1 Results of intra-day, inter-day precision and accurcy of trapidil in plasma |
分别取曲匹地尔低、中、高质量浓度质控样品各6份,除不加内标外,其余按“2.4”项下方法处理后进样分析,得到峰面积,以待测物的峰面积与相应浓度的对照品溶液经固相萃取后直接进样的峰面积比计算回收率。结果见表 2。
|
|
表 2 血浆中曲匹地尔和内标的提取回收率和基质效应 Table 2 Extraction recoveries, matrix effects of trapidil and I S(n=6) |
分别取低、中、高3个(10、200、2 560 ng·mL-1)浓度的曲匹地尔系列对照品溶液,45 ℃水浴氮气吹干后,流动相取6个志愿者1 mL空白血浆分别用1 mL洗脱液按“2.4”项下方法处理后进样分析,得到峰面积。以两者峰面积比值计算基质效应。结果表明本方法曲匹地尔和内标的测定均不受基质效应干扰。结果见表 2。
3.7 稳定性试验对曲匹地尔室温4 h、室温8 h和样品处理后室温放置24 h、-20 ℃冰箱中循环冻融3次及-20 ℃长期冷冻保存22 d稳定性进行考察。结果显示,中、高浓度样品的RSD均 < 15%,偏差系数 < ±15%,稳定性均在85%~115%之间;低浓度样品的RSD均 < 15%,偏差系数 < ±20%,稳定性均在80%~120%之间。结果表明,曲匹地尔血浆样品在室温放置8 h,样品处理后室温放置24 h、-20 ℃循环冻融2次及-20 ℃长期冷冻保存22 d稳定较好。
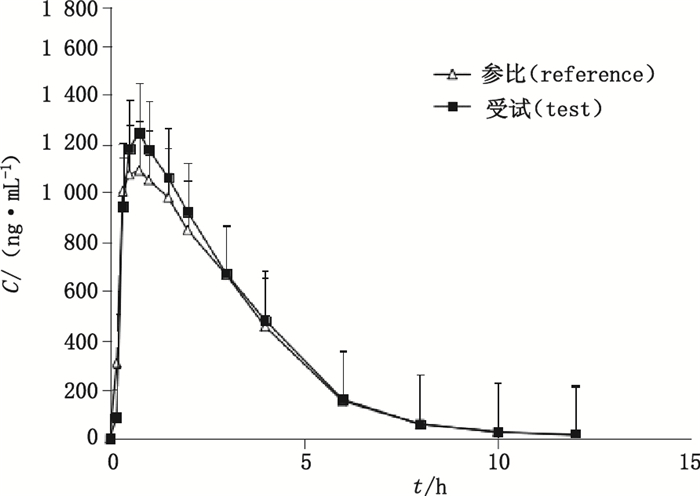
3.8 生物等效性研究按“2.4”项下进行操作,测定受试者口服受试制剂和参比制剂后不同时间曲匹地尔血药浓度,采用DAS 2.1.1统计软件计算各药动学参数,结果见表 3。20名健康受试者口服受试制剂和参比制剂后平均药-时曲线见图 3。Tmax经非参数秩和检验,受试制剂与参比制剂无统计学显著差异(P > 0.05);主要药动学参数Cmax、AUC0-t、AUC0-∞经对数转换后进行方差分析,受试制剂与参比制剂均无统计学显著差异(P > 0.05)。双向单侧t检验结果表明,受试制剂Cmax的90%可信限为95.9%~115.7%,落在参比制剂的80%~125%范围,AUC0~12 h的90%可信限为97.6%~111.6%,落在参比制剂的80%~125%范围。结果表明,2种制剂具有生物等效性。
|
|
表 3 20名受试者口服单剂量曲匹地尔(50 mg)后的药代动力学参数 Table 3 Main pharmacokinetic parameters in 20 healthy volunteer after oral administration of test preparation and reference preparation |
|
图 3 20名受试者口服单剂量受试和参比制剂后曲匹地尔的平均血药浓度-时间曲线 Figure 3 Mean plasma concentration-time profile of trapidil in 20 volunteer after oral administration of test preparation and reference preparation |
本试验首次采用了LC-MS/MS法测定人血浆中曲匹地尔浓度,该方法灵敏度高、特异性强、重复性好,且检测速度快(检测时间3 min),适用于大批量样品检测。与文献报道的HPLC[9-10]相比,血浆样品用量减少,检测时间缩短。首先,本试验所建立的LC-MS/MS法旨在测定人血浆中的曲匹地尔浓度,而文献报道的UPLC-MS/MS法[10]旨在测定猪肉中210种药物残留,曲匹地尔只是210种残留药物的1种,而不是作为唯一目标物;其次,样品基质不同,样品处理方法不同,采用固相萃取法处理人血浆样品,将基质效应降到最低,样品中的内源性物质不干扰曲匹地尔及内标的测定,方法专属性强,适用于人血浆中曲匹地尔药物浓度检测。苯海拉明与曲匹地尔理化性质相似,且在本试验条件下,响应值良好, 能够与曲匹地尔完全分离,因此选取苯海拉明作为内标。
本试验中,20名健康受试者单次口服50 mg曲匹地尔后,均未出现不良反应。统计结果显示曲匹地尔胶囊剂与片剂生物等效。本研究首次给出曲匹地尔在中国健康受试者中的药代动力学参数,与已有国外文献报道[13]相比:德国健康男性受试者在单次口服200 mg曲匹地尔后t1/2为(1.13±0.28)h,Tmax为1.0(0.5~2.0)h,与本研究基本结果一致; 而Cmax为(5.14±1.01)μg·mL-1,AUC0~∞为(20.5±7.0)μg·mL-1·h, 与本研究结果相比,Cmax和AUC0~∞呈明显的剂量相关性,因此可知曲匹地尔在我国健康男性体内经时过程与德国健康男性基本一致,说明曲匹地尔在不同人种中的药动学行为不存在差异,其药动学参数具有可比性。
参比制剂说明书中药代动力学结果显示:成人口服后,血中浓度迅速上升,达峰时间(Tmax)为2 h,半衰期(t1/2)为6 h,与本试验达峰时间和半衰期结果差异较大,可能与受试者的健康情况、饮食习惯和服药依从性有关。因此,曲匹地尔相关剂型在不同群体的药代动力学有待进一步研究。
5 结论本文建立了固相萃取LC-MS/MS法测定人血浆中曲匹地尔浓度,方法准确、简便快捷,固相萃取确保基质中杂质不干扰测定,方法学指标均达标,适用于曲匹地尔血浆浓度测定。药动学结果显示曲匹地尔胶囊与曲匹地尔片具有生物等效性,为曲匹地尔胶囊注册提供依据。
| [1] |
李虔桢, 陈良万. 曲匹地尔的药理作用及机制[J]. 中国实用医药, 2007, 2(3): 111. LI QZ, CHEN LW. Pharmacological action and mechanism of trapidil[J]. China Pract Med, 2007, 2(3): 111. |
| [2] |
伍前发, 张宜青, 林青. 冠状动脉介入治疗后血管再狭窄的药物防治进展[J]. 武警医学院学报, 2010, 19(9): 753. WU QF, ZHANG YQ, LIN Q. Advances on prevention and treatment of restenosis after coronary artery intervention with drugs[J]. Acta Acad Med CPAF, 2010, 19(9): 753. |
| [3] |
DINCER A, LILUFER T, LOKMAN A, et al. Effects of trapidil on renal ischemia-reperfusion injury[J]. J Pediatr Surg, 2006, 41(10): 1686. DOI:10.1016/j.jpedsurg.2006.05.064 |
| [4] |
MURAT B, DENIZ A, SELAHITTIN C, et al. Protective effect of trapidil on long-term histologic damage in a rat model of testicular ischemia-reperfusion injury[J]. World J Urol, 2009, 27(1): 117. DOI:10.1007/s00345-008-0323-7 |
| [5] |
ERTAN E, GOCER P, NAYCI A, et al. The effect of trapidil and bevacizumab on tracheal anastomotic wound healing[J]. Curr Ther Res Clin Exp, 2013, 75: 5. DOI:10.1016/j.curtheres.2013.04.002 |
| [6] |
LIU MJ, SUN Q, WANG Q, et al. Effect of trapidil in myocardial ischemia-reperfusion injury in rabbit[J]. Indian J Pharmacol, 2014, 46(2): 207. DOI:10.4103/0253-7613.129320 |
| [7] |
DINCER A, HAKAN T, LILUFER T, et al. Protective effect of trapidil against oxidative organ damage in burn injury[J]. Burns, 2005, 31(7): 859. DOI:10.1016/j.burns.2005.04.013 |
| [8] |
SUN DK, HA NK, JONG HL, et al. Trapidil, a platelet-derived growth factor antagonist, inhibits osteoclastogenesis by down-regulating NFATc1 and suppress bone loss in mice[J]. Biochem Pharmacol, 2013, 86(6): 782. DOI:10.1016/j.bcp.2013.07.015 |
| [9] |
闫辉, 闫凯, 李金凤. HPLC法测定曲匹地尔胶囊及片剂中有关物质的含量[J]. 中国药房, 2011, 22(21): 1990. YAN H, YAN K, LI JF. Content determination of related substances in trapidil capsules and trapidil tablets by HPLC[J]. China Pharm, 2011, 22(21): 1990. |
| [10] |
HERRMANN R. Automated high-performance liquid chromatographic assay for trapidil in human plasma[J]. J Pharm Biomed Anal, 1990, 8(8): 1045. |
| [11] |
RAGNO G, RISOLI A, LUCA MD, et al. Determination of trapidil in human serum and urine by derivative UV spectrophotometry after selective solid-phase extraction[J]. Anal Bioanal Chem, 2007, 389(7): 923. |
| [12] |
YIN ZQ, CHAI TT, MU PQ, et al. Multi-residue determination of 210 drugs in pork by ultra-high-performance liquid chromatography-tandem mass spectrometry[J]. J Chromatogr A, 2016, 1463(1): 49. |
| [13] |
HARDER S, THURMANN PA, HELLSTERN A, et al. Pharmacokinetics of trapidil, an antagonist of platelet derived growth factor, in healthy subjects and in patients with liver cirrhosis[J]. Br J Clin Pharmacol, 1996, 42(3): 443. |
 2018, Vol. 38
2018, Vol. 38 
