2. 中国药科大学, 南京 210024;
3. 光瞻智能科技(上海)有限公司, 上海 201405
2. China Pharmaceutical University, Nanjing 210024, China;
3. Quantspec Technology(Shanghai) Co., Ltd., Shanghai 2014005, China
目前, 制药行业主要通过对原材料、中间产物及最终产品进行人工抽样检测以控制药品质量, 抽样检测结果不能完全反映药品整体质量, 且抽样检测是离散型的, 不利于理解生产过程变化, 此外, 抽样检测滞后于生产过程, 不利于及时发现问题。为了进一步提高药品质量及加深对生产过程的理解, 美国FDA于2002年推出过程分析技术(PAT)规划, 并于2004年提出相应的工业指南。随后, PAT成为制药工业质量控制领域改革方向及研究热点。在PAT发展过程中, 出现实时放行(RTR)、质量源于设计(QbD)、设计空间(DS)、质量风险管理(QRM)等一系列相关概念, 同时, PAT研究中涉及多种技术的开发应用。根据近几年的文献报道, 文中探讨了PAT与RTR、QbD、DS、QRM的关系, 综述了PAT研究及应用现状以期对我国制药行业质量控制发展有所启示。
1 PAT及相关概念 1.1 PAT概念PAT是通过对原材料和处于加工中材料的关键质量品质和性能特征进行及时测量, 来设计、分析和控制生产加工的过程[1]。PAT中的分析是涉及多学科的综合分析, PAT中的过程是贯穿于整个药品生产的过程。FDA提出的PAT测量包括3种类型, 即:近线检测(at-line)、在线检测(on-line)、线内检测(in-line); PAT包括4种工具:设计、数据采集及分析的多变量工具, 过程分析工具, 过程控制工具, 持续改进和知识管理工具。相比传统的分析技术, PAT具有以下优势:减少生产周期时间; 防止废品、废料再加工; 实时放行; 提高自动化程度, 提高操作人员的安全性; 减少人为错误; 提高能源和材料的利用率; 能够确定和解释所有的变异的关键来源; 过程可变性是可以控制的; 使用的材料所建立的设计空间、工艺参数、制造、环境和其他条件可以准确可靠地预测产品质量属性[2]。
1.2 PAT与RTRFDA在PAT指南文件中提出了RTR概念, 即:根据工艺数据, 评估和保证中间品和/或成品达到可接受质量的能力[2]。2009年, ICH Q8(R2)将RTR修改为实时放行检测(RTRT), "检测"二字将关注点转移到测量方法上。相比成品检测, RTRT在生产过程中进行质量监测将质量控制向上游转移, 从而实现对每个单元操作关键质量属性进行监控。RTR优势如下:1)在生产过程中产生更多数据来改善工艺; 2)在生产过程中加强监测, 提高对产品和工艺的理解; 3)实现了非破坏性检测, 从而提高了生产和库存效率[2]。RTR是PAT优势也是其目的之一。PAT实时记录生产工艺过程数据为判定产品达标提供可靠的数据支持, 从而实现RTR。
1.3 PAT与QbDQbD通过合理的实验设计(DOE), 研究产品质量属性与原料质量属性和过程参数之间的关系, 目的是加强对产品和过程的理解以及过程控制[4]。在药品质量控制中, PAT可视为执行QbD的控制策略, 两者相辅相成[5]。QbD在前期规划中, 研究确定哪些参数是关键物料属性, 关键质量属性和关键工艺参数, PAT在生产过程中实时监控经QbD确定的关键因素。两者联合控制生产过程质量参数, 可以更好地保证产品质量, 降低对终点产品检测的依赖[6]。
1.4 PAT与DSDS是已被证明有质量保障作用的物料变量和工艺参数的多维组合和交互作用, 简单讲就是各种影响质量的关键因素和参数范围的组合[7]。DS的建立依靠先验知识, 风险评估与实验设计的计算, 目的决定了DS与控制空间的相对大小和范围。在定义下的DS内运行通常不被认为是变更, 进而增加了工艺运行的灵活性, 一旦操作超出了DS就会被看作是变更, 但DS建立在有限的信息之上, 需要根据PAT获得的信息不断完善。完善的DS使得工艺操作的限度更加合理并具弹性, 从而建立健全完善的药品质量标准。在申报药物审核时, DS或实时放行测验并非QbD的必选项目, 但必须依赖PAT的早期研究与执行。
1.5 PAT与QRMQRM属于质量管理体系的一部分, 是一种更高级的管理。风险管理概念的形成主要源自保险领域[8]。2005年, ICH Q9中提出QRM, 在制药行业正式引入QRM概念[9]。QRM是指在产品生命周期内, 对药品的质量风险进行评估、控制、交流和评审的系统程序[10]。QRM目的是药品生产中可能发生的质量风险控制在可接受范围内, 保障药品的安全、有效、可控[11]。实现QRM目标, 首先应该建立和完善药品生产过程质量风险管理体系, 其次要加强PAT的应用[12]。QRM和PAT理念一致, QRM是在生产过程中控制质量风险, PAT是实时分析控制生产过程。通过PAT及QRM理念, 能够在生产过程中发现并及时控制质量风险, 最终保证药品质量。
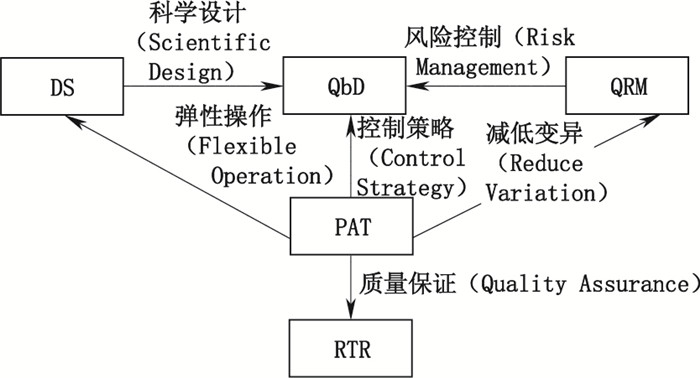
1.6 小结PAT、RTR、QbD、DS、QRM是现在质量管理理念的组成部分, RTR、QbD、DS、QRM促进对PAT概念的理解与实施, PAT是实现RTR、QbD、DS、QRM重要工具。其中DS是实现QbD的科学设计, QRM是实现QbD风险控制的策略, PAT是实现QbD的控制策略, 是降低QRM评估的工艺变异风险, 是采取DS的弹性操作, 也是施行RTR全方位质量保证的工具。具体关系如图 1所示。
|
图 1 PAT、QBD、QRM、DS、RTR关系图 Figure 1 Diagram of PAT, QBD, QRM, DS and RTR |
方法验证是一个阐述方法适用于其使用目的的过程[2], 它能够证明分析方法是否稳定、可靠。PAT方法验证有3种方式, 传统的方法验证是根据各国药典及ICH等指南文件要求进行, 此外还有AP(accuracy profile)法及方法验证源于设计(method validation by design, MVbD)理念。AP法由Feinberg提出, 是一种验证分析方法是否有效的图形化决策工具。通过合理实验设计及结果统计分析, 计算得到不同条件下验证内容的期望容许区间, 从而给出分析方法的准确性轮廓[13]; MVbD利用实验设计(DoE)和QbD原则, 定义无需再验证的设计空间。MVbD不仅包含ICHQ2(R1)验证项目, 还延伸考虑到相互作用、测量不确定度、控制策略及持续改进[14]。MVbD验证理念更适合用于PAT方法验证。3种验证方式都包含准确度、精密度、专属性、线性范围、检测下限、定量下限、耐用性等常用验证指标, 不同的分析项目侧重点不同, 因而采用的验证理念及验证项目不同。
Schaefer等[15]以NIR技术作为PAT工具, 监测一个新API生产过程并进行了全面的方法验证。方法验证中综合了上述3种验证方式。Schaefer等首先根据ICH Q2 (R1)的验证标准验证了NIR技术的精确度、精密度、准确度、剂量范围、线性、特异性、耐用性。此外利用AP法估算甲醇定量下限的范围, 并根据MVbD理念评价NIR技术的不确定度。实际研究中可根据相关要求及研究的具体内容进行分析方法验证。仪器是获得准确可靠的质量数据的基础。分析方法验证之前需要进行仪器确认, 只有保证仪器确认正确进行, 才能实现可靠的过程分析技术[16]。
3 PAT中的多变量数据分析药品生产过程中会产生实时监控参数、生产操作参数等大量数据。利用PAT及QbD理念, 建立科学的生产过程质量控制方法, 离不开上述数据的支撑。生产过程中多变量数据获取及分析也是PAT关键组成部分, 多元统计过程控制(MSPC)是PAT中应用较多的多变量分析方法, 其主要思想是借助统计学方法, 对生产过程进行监控[10]。MSPC主要内容是收集生产过程产生的数据, 建立PCA或PLS模型, 计算各个时间点的得分、Hotelling T2统计量及预测残差平方和(SPE)统计量的控制限[17]。
MSPC能够从过程分析产生的复杂数据提取潜在的有用信息, 监测并诊断生产过程的性能, 进而预测下游的质量属性[18]。Silva等[19]采用基于PCA的MSPC策略, 监测连续双螺杆造粒及流化床干燥工艺, 采用Hotelling T2和Q残差统计控制图评价生产过程中施加干扰因数的影响。结果表明2种控制图均监测到干扰, 说明MSPC可以监测连续生产过程并监测到生产过程的异常情况。
4 PAT工具概要PAT在制药生产过程的现行法规中发挥着核心作用, 实际药品生产过程复杂, 涉及参数较多, 因此需要应用多种技术监控生产过程。目前, PAT研究的分析工具包括光谱技术、光学成像技术, 动态光散射、气相色谱(GC)、质谱(MS)、核磁共振(NMR)、红外光谱(IR)、紫外-可见(UV~Vis)光谱及X射线荧光(XRF)等[1]。其中制药行业研究最多的是光谱技术包括近红外光谱法(NIR)技术、拉曼(Raman)光谱技术、荧光光谱法(LIF), 其次是光学成像技术。
4.1 光谱技术光谱技术中, NIR技术研究广泛成为制药行业主流的PAT工具。20世纪70年代, NIR技术就已成为检测样品中水分的PAT工具。目前, NIR技术已经成功用于药品生产过程, NIR技术利用生产过程中实时采集的近红外光谱图, 建立定性及定量模型, 预测或实时监测药品生产过程关键质量属性的变化。NIR技术是二级分析方法需要选择合适的参比方法, 一同控制生产过程。Karande等[20]采用在线NIR技术, 对生产过程中主成分(API)及辅料的含量进行实时定量研究。研究者将光纤探头安装在金属压片设备片剂形成区域附近的支架上, 装置如图 2所示。在片剂生产过程中采集NIR, 利用采集的动态光谱制备校准模型。验证使用实验设计的方法, 参比方法是紫外光谱法。校准和验证统计所获得的结果证实了用模型预测片剂含量的准确性。

|
A.装置于旋转式压片机的近红外探头(rotary tablet press with NIR probe) B.料斗(hopper) 图 2 药物及辅料在线定量压片的实验装置[20] Figure 2 Experimental setup for the in-line quantification of drug and excipients during tableting[20] |
拉曼光谱具有指纹性, 主要用于药物分子结构分析及现场快检。目前, 拉曼光谱技术已发展成监测药品生产过程的PAT工具。与NIR技术应用相似, 拉曼光谱技术也是在生产过程中实时采集拉曼光谱, 进而建立定性或定量模型监测药品生产过程。Saerens等[21]使用拉曼光谱在线监测不同浓度下酒石酸美托洛尔(MPT)-丙烯酸树脂(RLPO)的混合物, 建立及验证了MPT浓度的PLS回归模型, 实时监控API的含量。预测的MPT浓度与实际浓度的相关性在可接受范围内(R2=0.997), 校准模型的预测性能由根均方误差评价(0.59%)。通过比较在线拉曼光谱图与离线的DSC热分析图可知, 拉曼光谱技术能够获得聚合物药物固体状态的信息。
NIR技术灵敏度较低, 因此仍需开发或提高在线技术, 解决对低浓度成分的敏感性。光致荧光(LIF)光谱技术可以达到一定的药物分子定量检测下限, 是一种潜在的互补技术, LIF光谱技术特别适合低浓度的成分。Guay等[22]采用一种能够进行多变量测量的较先进的荧光分析仪在线监测7个批次湿法造粒过程, 目的是评估粉末的关键参数, 在准确预测API浓度的同时, 评估在线监测混合操作的技术性能。研究发现, 水分含量和颗粒尺寸对荧光发射影响最显著, 通过控制或减轻这些因素, 可以得到可靠的定量模型, 装置如图 3所示。

|
图 3 安装在中试规模的V-混合器的ePAT801 LIF系统[22] Figure 3 ePAT801 LIF system mounted on a 1-cu. ft. pilot-scale V-blender[22] |
除光谱技术外, 光学成像技术也可作为PAT工具应用于药品的生产过程。Soppela等[23]利用光学成像技术在线监测流化床造粒过程, 研究者将三维表面成像装置的摄像头连接到自动采样造粒机的比色皿上, 利用该装置检测含有不同数量的乳糖及微晶纤维素的5批对乙酰氨基酚。图像提供了直接的实时信息, 包括每个批次生产、磨损和包装过程。此外, 干燥阶段的图像亮度降低表明颗粒干燥。结合互补的过程分析工具(NIR技术), 光学成像提供了实时评价流化床造粒的可能性。装置如图 4所示。Närvänen等[24]则利用数码相机(图 5)在线监测流化床造粒过程。此法使用3个颜色(红、绿、蓝), 从3个不同的方向照射颗粒床表面拍摄彩色图形, 然后构建颗粒床表面三维图形。从图像数据计算颗粒大小分布及颗粒尺寸趋势的中位数, 得到的实时平均趋势线直观反映了颗粒粒径的变化趋势。

|
图 4 连接在造粒机上的光学成像装置(1)和NIR光谱仪(2)[23] Figure 4 The photometric imaging device (1) and NIR spectrometer (2) connected to the granulator bowl[23] |
综上所述, 鉴于过程分析的要求及特点, 用于药物生产过程中的实时分析技术主要是以光谱技术为主。光学成像技术尚在开发中。
5 PAT工具在药品生产过程中的应用PAT工具研究的技术较多, 但在国内真正投入实际药品生产过程的较少。查阅国内外文献发现, NIR技术是制药行业用于实际过程分析的主要PAT工具。NIR技术具有分析速度快, 不破坏样品, 无污染成本低等优点。目前, NIR技术在化学药品及中药的生产过程中已有所应用, 为药品生产过程提供了更多有用信息。
5.1 NIR技术在化学药品生产过程中的应用化学药品智能化生产随着数据化管理逐渐进步, 而质量控制依赖人工手段滞后于生产过程。在美国FDA推动下, 国外部分大型制药企业研究的在线NIR技术在化学药品合成、混合、干燥、压片、结晶、包衣、包装等生产过程已发挥作用。
5.1.1 合成过程合成是药品生产的起始步骤, 也是决定药品安全有效的关键步骤。合成过程目前主要根据离线分析方法控制, 离线分析对反应过程认识不足; 而PAT工具可实时监测合成过程变化趋势, 判断合成终点, 实现智能化控制合成过程。Mitic等[25]在管层流反应器进行9-烯丙基-2-氯硫杂蒽-9-开环("N714乙烯基乙醇")脱水反应, 研究者设计在线FT-NIR装置实时监测该化合物反应过程并建立PLS模型, 在线分析结果通过了近线NIR结果及离线的HPLC结果验证并具有较高的预测准确率。此外, 利用在线分析所得数据建立反应的动力学模型反映生产过程更精确。Schaefer等[15]在一新API合成反应的蒸馏过程中, 利用在线NIR技术实时准确测量API及残留溶剂含量, 测定的数据用于判断反应是否到达结晶步骤。上述研究使得自动控制合成过程成为可能。
5.1.2 混合过程药品活性成分与辅料的混合是固体制剂生产中的关键环节。混合时间短则混合不均匀, 混合时间长则浪费资源或造成过混合结块现象, 实时NIR技术的应用解决了混合问题的难点。混合过程中在线采集NIR, 利用近红外分析软件进行趋势分析, 通过混合过程中API含量变化确定最佳混合时间及混合终点。J?rvinen等[26]利用2台德国生产的NIR仪器(如图 6), 分别在线检测混合及压片2个连续生成过程并采集光谱, 并对采集的光谱建立PLS模型, 计算药粉及药片中对乙酰氨基酚的含量。试验结果表明, 近红外预测结果很可靠, 混合及压片建立的模型的预测均方根误差(RMSEP)分别为0.96%及1.37%。美国辉瑞全球研究及发展部的Sasic等[27]也深入研究了NIR技术在药物混合过程中的应用及其应用的复杂程度, 研究者在旋转式压片机进料口安装在线NIR光谱仪获得光谱, 分析光谱证明, NIR技术监测药物生产过程具有可行性。Scheibelhofer等[28]采用多个NIR探头监测药粉连续混合过程, 不同的空间位置"趋近同时"监测混合过程, 可以对混合的差异进行鉴定。

|
A.由2个进料器、连续混合器、压片机及2个近红外仪器组成的连续压片系统(the continuous tableting line consisting of two feeders, the continuous mixer, the tablet press and two VisioNIR ls instruments) B.带有卸料斜槽的连续搅拌机, 装在卸料斜槽上在线近红外可以从蓝宝石窗口进行测量(the continuous mixer with the discharge chute. The in-line NIR measurements were performed from underneath through a sapphire window present in the discharge chute) C.压片机上的NIR传感器探头(Visio NIR ls sensor head in the tablet press) 图 6 NIR仪器[26] Figure 6 NIR instrument[26] |
干燥过程一般包含在制粒或冷冻干燥等过程中, 常规的放行方法为卡尔费休式(KF)法。其局限在于代表性不强, 不能够保证同批次其他产品是否合格[29]。近红外区水分子有很强的特征吸收峰, 干燥过程中通过光纤探头实时采集NIR, 建立判别模型便可判断干燥程度。Chablani等[26]采用NIR技术, 在线实时测量流化床造粒过程中颗粒的水分含量。该生产过程使用大生产规模连续双螺杆造粒流化床干燥机, 与KF、干燥失重(LOD)测定的水分进行比较。NIR技术相对于KF水分含量预测的R2值及NIR技术相对于检测下限的R2值分别为0.94和0.85。冷冻干燥在制药行业应用广泛, 但过程复杂、耗时, 处理不好会导致产品多孔, 因此需要开发过程分析技术以提高对该过程的理解, 从而更好地优化过程。Rosas等[30]利用NIR技术在线监测的多组分药物制剂整个冻干过程; 结果表明在冰冷的环境下, 使用NIR技术在线测量是可行的。Kauppinen等[31]也利用多点NIR技术分析方法在线冷冻干燥过程水分含量。最终确定了NIR技术在冻干过程分析中的有效性。
5.1.4 压片过程压片是片剂生产过程必不可少的步骤。含量均一, 硬度适当, 崩解时间合理等是生产片剂的要求, 目前企业主要根据生产经验控制压片过程。压片过程可监测参数多, NIR技术可量化压片过程, 为其提供智能化监测手段。Wahl等[32]在压片机的料架上安装近红外探头, 实时测量压片过程中粉末的NIR反射光谱。建立PLS模型及PCA分析压片过程中API及2个辅料的含量, 确定片剂的含量均匀度。分析发现压片终点时, API含量有一个显著的峰值并得到可见-紫外光谱的分析证实。在Pestieau等[33]的研究中, 选取了压片过程中含量均匀度、片剂硬度和崩解时间3个参数, 对采集的NIR透射光谱建立PLS模型, 预测含量均匀度及片剂硬度, 基于K-近邻法测试片剂脆碎度。
5.1.5 结晶过程结晶是制药工艺中常用的纯化方法。结晶过程的工艺参数多导致批间差异大, 产品质量不稳定, NIR技术可测定结晶过程组分的浓度变化, 为控制结晶过程提供实时信息。Schaefer等[34-35]使用NIR技术研究了实验室及工业生产规模的结晶过程, 并建立了API及残留甲醇的定量模型。与参比方法相比, API及残留甲醇的最大相对偏差分别为2.88%及0.02%。Mafalda等[36]使用在线NIR技术监控呋塞米和腺嘌呤共结晶过程, 通过装有反射光纤探头的FT-NIR光谱仪进行在线监测。测得的结果与离线NIR技术、中红外、DSC和XRPD方法进行比较, 在线测得结果与参比方法差异不大, 表明在线NIR技术可用于检测共结晶过程。
5.1.6 包衣过程均匀完整的包衣是保证片剂外观品质的关键。包衣的厚度影响片剂的释放度, 严格控制包衣过程工艺参数, 才能保证包衣效果, 包衣厚度与NIR变化相关。Avalle等[37]在中试规模, 用近红外快速分析仪采集包衣过程的NIR。以自动显微镜作为参考方法, 利用化学计量学考察NIR和涂层质量、涂层厚度和溶解性能之间的关系。此研究策略找出了包衣过程中相关参数的变化, NIR和产品性能之间的相关性应仅取决于产品的特性。如果成功地放大这些关系, 能将在中试规模得到的结论应用于大规模生产过程。
5.2 NIR技术在中药生产过程中的应用中药是中国的特色药, 中国是中药生产大国, 但中药成分复杂, 处理工艺烦琐, 药品质量不易控制, 精确控制中药生产过程才能实现中药工业化生产。国内医药企业及院校研究了在线NIR技术, 并在中药提取、纯化、干燥、含量测定、混合、浓缩等过程获得的成功应用。
5.2.1 提取过程提取工艺是大多数中药生产过程的起点, 也是中药生产的关键环节, 直接关系到药材的利用率。整个中药生产过程中, 提取过程使用在线NIR技术最多。2005年, 罗国安团队[38]成功构建中药注射剂NIR在线监控系统, 并将该技术应用于清开灵注射液水提过程及参麦注射液的醇提过程, 提高了中药生产过程质量控制水平。2006年, 罗国安等[39]以在线近红外光谱仪为核心设备, 设计了一整套中药提取过程基于质量参数的智能化控制系统。基于在线NIR技术, 实现了对安神补脑液、血府逐淤口服液提取过程中药液有效成分或指标成分含量的实时监测, 对提取充分程度的趋势分析, 对提取工艺是否正常做出快速诊断, 为生产过程提供了实时质量反馈信息。
瞿海斌教授团队自2001年起, 也一直从事NIR技术在中药质量控制及中药制药过程分析方面的研究。2008年, 瞿海斌团队[38]以NIR技术为主要技术工具, 以丹参注射液、痰热清注射液、复方苦参注射液为载体, 深入研究了提取工艺。2012年, 陈晨等[40]究复方苦参注射液渗漉过程的NIR技术在线检测方法。在复方苦参注射液的工业化生产中引入NIR技术, 设计了在线光谱采集装置, 建立了复方苦参注射液渗漉过程生物碱和固体总量的快速测定方法, 并应用于实际生产的在线分析。
周正[41]、李洋[42]等在中试规模的条件下研究了黄柏及黄芩配方颗粒提取工艺的在线近红外质量监测研究, 为中药提取过程质量控制提供了可靠的方法。
5.2.2 纯化过程2002年, 国内开始利用NIR技术研究纯化工艺, 蒲登鑫等[43]将在线NIR技术监控用于葛根素生产过程。监测大孔树脂吸附、解吸及聚酰胺树脂层析分离纯化过程。2010年, 刘雪松等[44]发明了一种大孔树脂在线NIR技术监测系统, 该系统可用于判别中药分离纯化过程的关键点。除了树脂吸附, 醇沉及水沉也是中药生产过程常用的纯化手段。基于PAT和DS方法, 徐冰等[45]收集多批醇沉NIR光谱, 采用主成分分析及移动块相对标准偏差法确定各个批次生产过程的理想终点样本, 建立多变量统计过程控制模型对终点进行判断。刘雪松等[46]还研制一种中药水沉过程的在线监测装置, 该装置能够真实有效地采集NIR, 且可以滤除水沉过程中产生的杂质, 进而防止杂质对采集的近红外光谱产生影响, 实现了对水沉过程中有效成分含量的在线实时检测。
5.2.3 混合过程中药成分多, 将各组分混合均匀更加困难。传统的混合均匀性试验耗时长且难以确保混合程度最佳。实时采集混合过程中混合料液或药物粉末的NIR, 分析NIR的变化, 能够对混合过程进行合理的判断。龚益飞等[47]用透反射光纤探头在线采集混合过程中料液的近红外光谱, 以光谱偏差作为混合均匀度指标, 判断混合终点。结果表明, 经本法终点判断后制备的滴丸重均匀, 有效成分含量稳定, 能有效保证产品质量。针对中药药粉混合过程, 李云霞等[48]发明了一种在线近红外光谱仪, 控制中药药粉二维混合过程的均匀度。该仪器根据混合过程中预定的时间长度内不同时间点的近红外光谱差异, 判断是否混合均匀, 并以腰痛宁胶囊混合为例进行验证。
5.2.4 含量测定生产过程中药物含量是关键参数, 可用于均匀度的判定及混合终点的控制。章顺楠等[49]用近红外透反射光谱仪采集料液NIR, 研究复方丹参滴丸滴料液中丹参素、原儿茶醛含量的快速分析方法。NIR可实时反映料液中采集点位置的成分含量变化及生产过程中料液的均一性, 该研究在中试规模进行了验证。李文龙等[50]通过FT-NIR在线分析仪器, 对黄芪提取过程进行监测; 他们利用远程光纤流通池在线采集黄芪提取过程中提取液的近红外光谱, 并建立定量模型分析黄芪中总皂苷的含量; 以黄芪总皂苷为检测指标, 对黄芪提取过程的在线监测, 为黄芪提取过程的终点判断和工艺优化提供参考。此外, 张金巍[51]等发明了一种NIR分析方法在线检测白芍提取液中药物苷的含量。
6 问题与展望虽然医药工业发展规划指南(2016)、智能制造工程实施指南(2016-2020)和ICH Q8、Q9、Q10质量文件中提倡过程分析技术的运用。PAT在国内药品生产领域的研究仍处于起始阶段, 一些问题成为制药企业实行PAT的潜在障碍。例如:1)PAT前期研究需技术了解及大量资金支持, 能否给制药企业带来经济效益也不明确, 目前只有少部分企业在做PAT研究, 而真正进入常规大生产更少; 2)PAT监管要求不确定, 缺乏国家标准或指导文件, 因此在新药申报或变更审批上存在挑战; 3)PAT应用范围烦琐, 在缺乏经验条件下, 如何选择及落实适合某一生产工艺的PAT技术需要进一步研究。4)PAT转化与创新尚不够成熟, 应考虑如何深化并确保高等学校与制药企业研究PAT项目的实用性与稳健性。此外, PAT自身和实际应用上也存在很多必须克服的问题, 包括:(1)在危险的生产环境中如何配置仪器; (2)如何在生产系统中安装监测探头, 安装位置如何确定, 如何确认设备合规性; (3)数据如何处理, 数据安全性及模型传递问题[52]; (4)PAT硬件与软件的稳定性与操作灵活性是否足够; (5)如何确保PAT工具与模型在药品生命周期中应用的性能一致性。
随着科学技术的不断发展, 基于科学与风险管理的PAT应用项目, 存在的问题与挑战将会迎刃而解。所幸国外部分企业已将PAT成功应用于化学药与制剂生产过程, 国内在药物生产过程研究的PAT也逐渐取得很大观念突破, 明白生产质量一致性与高效率的重要性。PAT加深了企业对生产过程的理解, 提高了药品生产效率, 加强质量均质性, 给企业带来了巨大的经济效益。未来配合药品监管系统与法规对QbD/PAT的逐渐认可, PAT将会成为药品生产过程智能化监测的必然方法。
| [1] |
陆婉珍, 褚小立. 近红外光谱(NIR)和过程分析技术(PAT)[J]. 现代科学仪器, 2007(4): 13. LU WZ, CHU XL. Near infrared spectroscopy(NIR) and process analysis technology (PAT)[J]. Mod Sci Instrum, 2007(4): 13. |
| [2] |
Department of Health and Human Services Food and Drug Administration. Guidance for industry: PAT-A framework for innovative pharmaceutical development, manufacturing, and quality assurance[EB/OL]. (2004-12)[2018-01-02].https://www.fda.gov/downloads/drugs/guidancecomplianceregulatoryinformation/guidances/ucm070305.pdf
|
| [3] |
杜雯君, 梁毅. 药品实时放行检测简介[J]. 机电信息, 2012(8): 23. DU WJ, LIANG Y. A brief introduction to the real time release of drugs[J]. Electromechan Inf, 2012(8): 23. |
| [4] |
戴胜云, 徐冰, 张毅, 等. 质量源于设计(QbD)在药物分析方法开发中的应用研究进展[J]. 药物分析杂志, 2016, 36(6): 950. DAI SY, XU B, ZHANG Y, et al. Application progress of quality by design based pharmaceutical analysis method[J]. Chin J Pharm Anal, 2016, 36(6): 950. |
| [5] |
YU L X, AMIDON G, KHAN MA, et al. Understanding pharmaceutical quality by design[J]. AAPS J, 2014, 16(4): 771. DOI:10.1208/s12248-014-9598-3 |
| [6] |
严斌俊. 数据驱动的中药制药过程质量控制方法及应用研究[D]. 杭州: 浙江大学, 2015: 129 YAN BJ. Data Driven Quality Control Method and Its Application in Traditional Chinese Medicine Manufacturing Process[D]. Hangzhou: Zhejiang University, 2015: 129 |
| [7] |
吕东, 黄文龙. FDA有关"质量源于设计"的初步实施情况介绍[J]. 中国药事, 2008, 22(12): 1131. LÜ D, HUANG WL. Introduction of FDA implementation of quality by design[J]. Chin Pharm Aff, 2008, 22(12): 1131. |
| [8] |
林琳. 药品质量风险规制研究[D]. 沈阳: 沈阳药科大学, 2011 LIN L. Study on Drug Quality Risk Regulation[D]. Shenyang: Shenyang Pharmaceutical University, 2011 |
| [9] |
吕锐. 在药品GMP实施中运用质量风险管理的探讨[J]. 中国药事, 2013, 27(10): 1097. LÜ R. Investigation on application of QRM in GMP implementation[J]. Chin Pharm Aff, 2013, 27(10): 1097. DOI:10.3969/j.issn.1002-7777.2013.10.024 |
| [10] |
Draft Consensus Guideline Q9 Quality Risk Management[EB/OL]. (2005-3-22)[2018-01-02]. https://wenku.baidu.com/view/eaa53bd6de80d4d8d05a4fcc.html
|
| [11] |
李付惠. 药品生产质量的风险管理[J]. 中医药管理杂志, 2017, 25(13): 78. LI FH. Risk management of the quality of drug production[J]. J Adm Tradit Chin Med, 2017, 25(13): 78. |
| [12] |
王培, 曾英姿, 臧恒昌. 药品生产过程质量风险产生的原因及控制[J]. 中国药学杂志, 2011, 46(13): 969. WANG P, CENG YZ, ZANG HC. The cause and control of the quality risk in the process of drug production[J]. Chin Pharm J, 2011, 46(13): 969. |
| [13] |
戴胜云. 中药HPLC分析设计空间的建立与可靠性研究[D]. 北京: 北京中医药大学, 2016 DAI SY. Establishment and Reliability Study of HPLC Analysis Design Space of Traditional Chinese Medicine[D]. Beijing: Beijing University of Chinese Medicine, 2016 |
| [14] |
MARK ALASANDRO TL, FLEITMAN J. Method validation by design to support formulation development[J]. Pharm Technol, 2013, 37(4): 84. |
| [15] |
SCHAEFER C, CLICQ D, LECOMTE C, et al. A process analytical technology(PAT) approach to control a new API manufacturing process:development, validation and implementation[J]. Talanta, 2014, 120: 114. DOI:10.1016/j.talanta.2013.11.072 |
| [16] |
赵俭, 刘树林, 郑树朝, 等. 制药企业分析仪器确认研究[C]//2008年中国药学会学术年会暨第八届中国药师周论文集. 2008: 1210 ZHAO J, LIU SL, ZHENG SC, et al. Discussion of the Analytical Instrument Qualification in Pharmaceutical Manufacture[C]//Proceedings of 2008 Annual Meeting of Chinese Pharmaceutical Association and the Eighth Chinese Pharmacists Week. 2008: 1210 http://cpfd.cnki.com.cn/Article/CPFDTOTAL-YYWS200810002194.htm |
| [17] |
KOURTI T. Multivariate dynamic data modeling for analysis and statistical process control of batch processes, start-ups and grade transitions[J]. J Chemometr, 2003, 17(1): 93. DOI:10.1002/(ISSN)1099-128X |
| [18] |
HUANG J, GOOLCHARRAN C, UTZ J, et al. A PAT approach to enhance process understanding of fluid bed granulation using in-line particle size characterization and multivariate analysis[J]. J Pharm Innovation, 2010, 5(1-2): 58. DOI:10.1007/s12247-010-9079-x |
| [19] |
SILVA A F, A M S, FONTEYNE M, et al. Multivariate statistical process control of a continuous pharmaceutical twin-screw granulation and fluid bed drying process[J]. Int J Pharm, 2017, 528: 242. DOI:10.1016/j.ijpharm.2017.05.075 |
| [20] |
KARANDE AD, HENG PWS, LIEW CV. In-line quantification of micronized drug and excipients in tablets by near infrared (NIR) spectroscopy:real time monitoring of tabletting process[J]. Int J Pharm, 2010, 396(1-2): 63. DOI:10.1016/j.ijpharm.2010.06.011 |
| [21] |
LIN ZH, LIU LL, MAHAJAN A, et al. Real-time endpoint monitoring and determination for a pharmaceutical salt formation process with in-line FT-IR spectroscopy[J]. J Pharm Biomed Anal, 2006, 41(1): 99. DOI:10.1016/j.jpba.2005.10.028 |
| [22] |
Guay JM, Lapointe-Garant PP, Gosselina R, et al. Development of a multivariate light-induced fluorescence (LIF) PAT tool for in-line quantitative analysis of pharmaceutical granules in a V-blender[J]. Eur J Pharm Biopharm, 2014, 86(3): 524. DOI:10.1016/j.ejpb.2013.12.013 |
| [23] |
Soppela I, Antikainen O, Sandler N, et al. On-line monitoring of fluid bed granulation by photometric imaging[J]. Eur J Pharm Biopharm, 2014, 88(3): 879. DOI:10.1016/j.ejpb.2014.08.009 |
| [24] |
NÄRVÄNEN T, SEPPÄLÄ K, ANTIKAINEN O, et al. A new rapid on-line imaging method to determine particle size distribution of granules[J]. AAPS PharmSciTech, 2008, 9(1): 282. DOI:10.1208/s12249-008-9043-y |
| [25] |
MITIC A, CERVERAPADRELL AE, MORTENSEN AR, et al. Implementation of near-infrared spectroscopy for in-line monitoring of a dehydration reaction in a tubular laminar reactor[J]. Org Proc Res Dev, 2016, 20(2): 395. DOI:10.1021/op5004055 |
| [26] |
JÄRVINEN K, HOEHE W, JÄRVINEN M, et al. In-line monitoring of the drug content of powder mixtures and tablets by near-infrared spectroscopy during the continuous direct compression tableting process[J]. Eur J Pharm Sci, 2013, 48(4-5): 680. DOI:10.1016/j.ejps.2012.12.032 |
| [27] |
ŠAŠIĆS, BLACKWOODD, LIUA, 等. Detailed analysis of the online near-infrared spectra of pharmaceutical blend in a rotary tablet press feed frame[J]. J Pharm Biomed Anal, 2015, 103: 73. |
| [28] |
SCHEIBELHOFER O, BALAK N, KOLLER DM, et al. Spatially resolved monitoring of powder mixing processes via multiple NIR-probes[J]. Powder Technol, 2013, 243: 161. DOI:10.1016/j.powtec.2013.03.035 |
| [29] |
臧恒昌, 臧立轩, 张惠, 等. 近红外光谱分析技术在制药领域中的应用研究进展[J]. 药学研究, 2013, 33(3): 125. ZANG HC, ZANG LX, ZHANG H, et al. Research progress in application of near- infrared spectroscopy in pharmaceuticals[J]. J Pharm Res, 2013, 33(3): 125. |
| [30] |
ROSAS JG, de WAARD H, de BEER T, et al. NIR spectroscopy for the in-line monitoring of a multicomponent formulation during the entire freeze-drying process[J]. J Pharm Biomed Anal, 2014, 97: 39. DOI:10.1016/j.jpba.2014.04.010 |
| [31] |
KAUPPINEN A, TOIVIAINEN M, LEHTONEN M, et al. Validation of a multipoint near-infrared spectroscopy method for in-line moisture content analysis during freeze-drying[J]. J Pharm Biomed Anal, 2014, 95: 229. DOI:10.1016/j.jpba.2014.03.008 |
| [32] |
WAHL PR, FRUHMANN G, SACHER S, et al. PAT for tableting:in-line monitoring of API and excipients via NIR spectroscopy[J]. Eur J Pharm Biopharm, 2014, 87(2): 271. DOI:10.1016/j.ejpb.2014.03.021 |
| [33] |
PESTIEAU A, KRIER F, THOORENS G, et al. Towards a real time release approach for manufacturing tablets using NIR spectroscopy[J]. J Pharm Biomed Anal, 2014, 98: 60. DOI:10.1016/j.jpba.2014.05.002 |
| [34] |
SARRAGUÇA MC, PAISANA M, PINTO J, et al. Real-time monitoring of cocrystallization processes by solvent evaporation:a near infrared study[J]. Eur J Pharm Sci, 2016, 90: 76. DOI:10.1016/j.ejps.2015.12.025 |
| [35] |
SCHAEFER C, LECOMTE C, CLICQ D, et al. On-line near infrared spectroscopy as a process analytical technology (PAT) tool to control an industrial seeded API crystallization[J]. J Pharm Biomed Anal, 2013, 83: 194. DOI:10.1016/j.jpba.2013.05.015 |
| [36] |
SARRAGUÇA MC, RIBEIRO PRS, SANTOS AO, et al. A PAT approach for the on-line monitoring of pharmaceutical co-crystals formation with near infrared spectroscopy[J]. Int J Pharm, 2014, 471(1-2): 478. DOI:10.1016/j.ijpharm.2014.06.003 |
| [37] |
AVALLE P, POLLITT MJ, BRADLEY K, et al. Development of process analytical technology (PAT) methods for controlled release pellet coating[J]. Eur J Pharm Biopharm, 2014, 87(2): 244. DOI:10.1016/j.ejpb.2014.01.008 |
| [38] |
褚小立, 张莉, 燕泽程. 现代过程分析技术交叉学科: 发展前沿与展望[M]. 北京: 机械工业出版社, 2016, 76. CHU XL, ZHANG L, YAN ZC. Modern Process Analysis Technology:Current Status And Future Prospests[M]. Beijing: Machinery Industry Press, 2016, 76. |
| [39] |
罗国安, 梁琼麟, 杨辉华, 等. 近红外在线分析与中药智能化控制体系研究[C]//BCEIA 2009分析仪器应用技术报告会议论文集. 2009: 5 LUO GA, LIANG QL, YANG HH, et al. Research on Near Infrared On-line Analysis and Intelligent Control System of Chinese Medicine[C]//Proceedings of Technical report of BCEIA2009 analytical instruments application. 2009: 5 http://cpfd.cnki.com.cn/Article/CPFDTOTAL-ZFCX200911002011.htm |
| [40] |
陈晨, 李文龙, 瞿海斌, 等. 复方苦参注射液渗漉过程的近红外光谱在线检测方法[J]. 中国药学杂志, 2012, 47(21): 1698. CHEN C, LI WL, QU HB, et al. An on-line near-infrared spectroscopy approach for content determination in the percolation process of compound Kushen injection[J]. Chin Pharm J, 2012, 47(21): 1698. |
| [41] |
周正, 吴志生, 史新元, 等. Bagging-PLS的黄柏中试提取过程在线近红外质量监测研究[J]. 世界中医药, 2015, 10(12): 1939. ZHOU Z, WU ZS, SHI XY, et al. Study on online NIR for monitoring the extraction process of Cortex Phellodendri in pilot scale base[J]. World Chin Med, 2015, 10(12): 1939. DOI:10.3969/j.issn.1673-7202.2015.12.030 |
| [42] |
李洋, 吴志生, 史新元, 等. 中试规模和不同提取时段的黄芩配方颗粒质量参数在线NIR监测研究[J]. 中国中药杂志, 2014, 39(19): 3753. LI Y, WU ZS, SHI XY, et al. Research on quality parameters of Scutellariae Radix(formula particles)using on-line NIR in pilot with different extraction processes[J]. China J Chin Mater Med, 2014, 39(19): 3753. |
| [43] |
蒲登鑫, 王文茂, 李军会, 等. 近红外在线质量监控技术在中药葛根素生产中的应用[J]. 现代仪器, 2003(5): 27. PU DX, WANG WM, LI JH, et al. The application of near infrared analytical technique in the puerarin production for the on-line quality inspection and control[J]. Mod Instrum, 2003(5): 27. |
| [44] |
刘雪松, 陈勇, 李页瑞, 等. 一种中药大孔树脂分离纯化过程关键点的判别方法: 中国, 201010515830. X[P]. 2011-03-09 LIU XS, CHEN Y, LI YR, et al. A Discriminant Method for Key Points of Separation and Purification Process of Macroporous Resin for Traditional Chinese Medicine: China, 201010515830. X[P]. 2011-03-09 |
| [45] |
徐冰, 罗赣, 林兆洲, 等. 基于过程分析技术和设计空间的金银花醇沉加醇过程终点检测[J]. 高等学校化学学报, 2013, 34(10): 2284. XU B, LUO G, LIN ZZ, et al. End-point detection of the alcohol adding process in alcohol precipitation of Lonicerae Japonicae Flos based on design space and process analytical technology[J]. Chem J Chin Univ, 2013, 34(10): 2284. DOI:10.7503/cjcu20130523 |
| [46] |
刘雪松, 王龙虎, 陈勇, 等. 一种中药水沉过程的在线检测装置: 中国, 201320000687. X[P]. 2013-09-18 LIU XS, WANG LH, CHEN Y, et al. An on-line Detection Device for the Process of Water Precipitation in Chinese Medicine: China, 201320000687. X[P]. 2013-09-18 |
| [47] |
龚益飞, 刘雪松, 章顺楠, 等. 近红外光谱法在线判断滴丸料液混合终点[J]. 中国药学杂志, 2007, 42(7): 509. GONG YF, LIU XS, ZHANG SN, et al. On-line endpoint determination in blending process of dripping solution by near infrared spectroscopy[J]. Chin Pharm J, 2007, 42(7): 509. |
| [48] |
李云霞, 鲍建才, 李沈明, 等. 近红外在线检测控制中药药粉二维混合的均匀度的方法: 中国, 200910119221. X[P]. 2010-09-15 LI YX, BAO JC, LI SM, et al. Near Infrared On-line Detection Method for Controlling the Uniformity of Two Dimensional Mixture of Traditional Chinese Medicine Powder: China, 200910119221. X[P]. 2010-09-15 |
| [49] |
章顺楠, 杨海雷, 刘占强, 等. 近红外光谱法在线监测复方丹参滴丸料液中有效成分含量[J]. 药物分析杂志, 2009, 29(2): 192. ZHANG SN, YANG HL, LIU ZQ, et al. On-line monitoring of the content of active components in the solution for Fufang Danshen dripping pills by near-infrared spectroscopy[J]. Chin J Pharm Anal, 2009, 29(2): 192. |
| [50] |
李文龙, 瞿海斌. 黄芪提取过程总皂苷质量浓度的在线监测[J]. 中草药, 2012, 43(8): 1531. LI WL, QU HB. On-line monitoring of total saponins in extracting process of Astragali Radix[J]. Chin Tradit Herb Drugs, 2012, 43(8): 1531. |
| [51] |
张金巍, 张廷莹, 刘岩, 等. 一种白芍提取液中的芍药苷含量的NIR在线检测方法: 中国, 200910228468. X[P]. 2009-11-17 ZHANG JW, ZHANG TY, LIU Y, et al. An On-line NIR Method for the Determination of Paeoniflorin in Radix Paeoniae Alba Extract: China, 200910228468. X[P]. 2009-11-17 |
| [52] |
SIMON LL, PATAKI H, MAROSI G, et al. Assessment of recent process analytical technology (PAT) trends:a multiauthor review[J]. Org Proc Res Dev, 2015, 19(1): 3. DOI:10.1021/op500261y |
 2018, Vol. 38
2018, Vol. 38 

