2. 中国食品药品检定研究院, 北京 100050;
3. 北京师范大学中药资源保护与利用北京市重点实验室, 北京 100875
2. National Institutes for Food and Drug Control, Beijing 100050, China;
3. Beijing Key Laboratory of Traditional Chinese Medicine Protection and Utilization, Beijing Normal University, Beijing 100875, China
锥叶柴胡是伞形科柴胡属锥叶柴胡 Bupleurum bicaule Helm的干燥根,是收载于内蒙古中药材标准的地方习用药材,主产于内蒙古、东北地区。柴胡在《中华人民共和国药典》[1]中收载2个种,即柴胡 B. chinense DC.(又称北柴胡)和狭叶柴胡 B. scorzonerifolium Willd.(又称南柴胡),锥叶柴胡在原植物特征及药材外观性状上与《中华人民共和国药典》南柴胡的特征相近,极易混淆。由于近年来柴胡需求量大,资源紧缺,锥叶柴胡常混充南柴胡在全国多个药材市场流通,亳州药市、安国祁州药市以及哈尔滨三棵树药材市场均见到锥叶柴胡冒充南柴胡大量出售。皂苷类成分为柴胡属药用植物的主要活性成分,现代药理学研究表明柴胡皂苷具有抗炎[2]、镇痛镇静[3]、保肝[4]、抗抑郁[5]、抗菌[6]、抗癌[7-9]等作用,《中华人民共和国药典》通过考察柴胡皂苷A和D的含量评价其质量。锥叶柴胡具有较悠久的使用历史,市场流通量较大,开展其化学成分及质量控制方法等方面的研究对扩充柴胡资源,提高质量控制水平均具有重要的意义。锥叶柴胡主要化学成分为皂苷类,已发现其含有柴胡皂苷元D、E、F、G,柴胡次皂苷A、D、F、G,柴胡皂苷A、C、D、b2、b4等皂苷类成分,此外有少量甾醇类、酚酸类、醌类、黄酮类化合物被分离鉴定[10-13]。但关于其质量控制方法鲜有报道,少数学者仅对锥叶柴胡中柴胡皂苷A、C、D的含量进行了测定[13-14],但对其他皂苷类成分未作研究,另外前处理较为烦琐,易导致操作误差。
本文在前期化学成分提取、分离、鉴定的研究基础上,对锥叶柴胡中含量较高的柴胡皂苷A、C、D,柴胡次皂苷F、G以及首次从柴胡属植物中分离得到的3-[(6-去氧-β-D-吡喃葡萄糖)氧基]-13,28-环氧-23-羟基-11-齐墩果烯-16-酮(本文中将其命名为柴胡次皂苷I)进行了含量测定研究,建立了6个成分的测定方法,方法经验证简便可行,为锥叶柴胡的质量控制及推广应用提供了科学依据。
1 仪器与试药 1.1 仪器沃特世公司Waters 2695-2998高效液相色谱仪;梅特勒托利多公司METTLER XS105Du型十万分之一电子天平,METTLER AE240型万分之一电子天平;岛津技迩(上海)商贸有限公司InertSustain AQ-C18色谱柱(4.6 mm×250 mm,5 μm;填料:十八烷基硅烷键合硅胶);密理博中国有限公司Millipore Milli-Q Academic超纯水机;昆山市超声仪器有限公司KQ-300DA型数控超声波清洗器。
1.2 试药对照品柴胡皂苷A(批号110777-201510,纯度93.20%)、柴胡皂苷D(批号110778-201510,纯度97.30%)来自中国食品药品检定研究院;柴胡皂苷C(批号MUST-17031402,纯度98.47%)购自成都曼思特生物科技有限公司;柴胡次皂苷F、柴胡次皂苷G、3-[(6-去氧-β-D-吡喃葡萄糖)氧基]-13,28-环氧-23-羟基-11-齐墩果烯-16-酮(柴胡次皂苷I)为从锥叶柴胡根中分离所得,纯度分别91.10%、95.20%、89.22%,结构式见图 1。
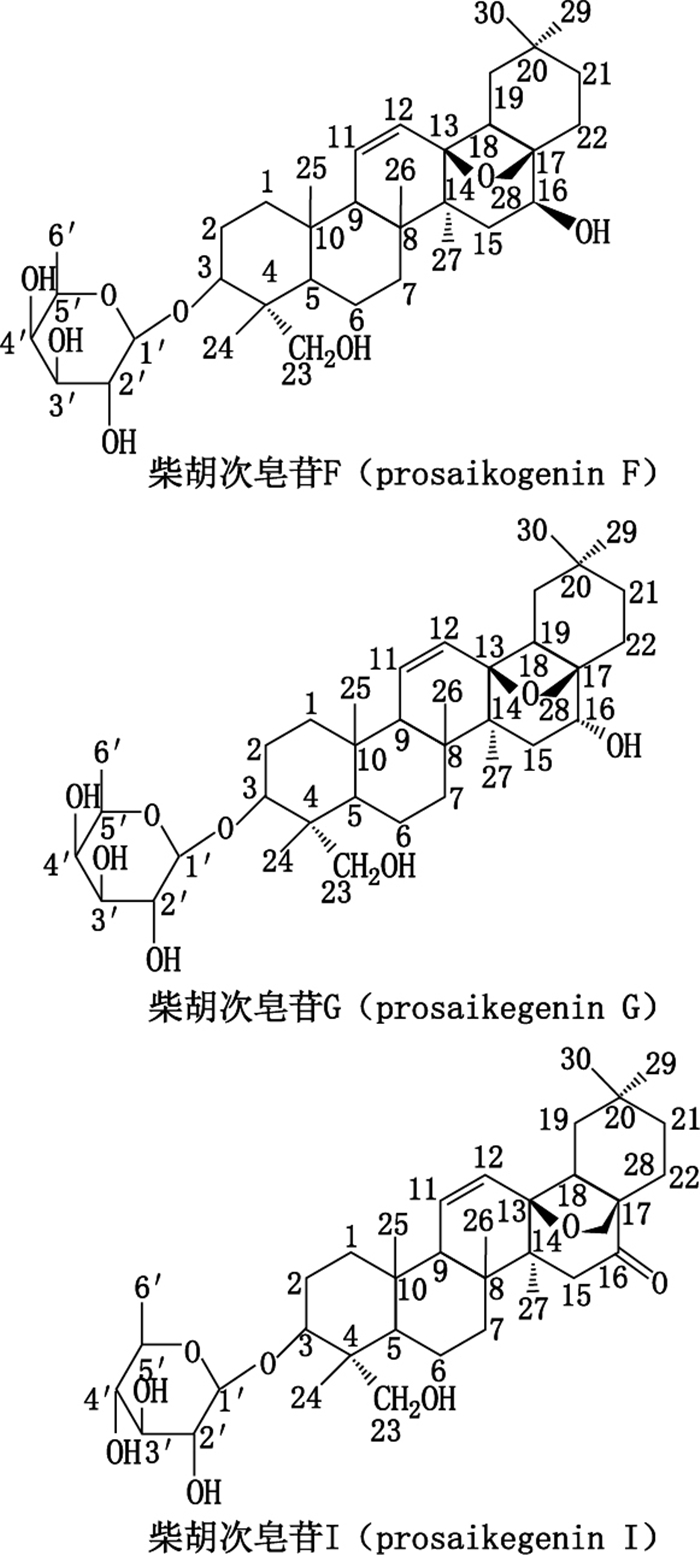
|
图 1 分离的化合物结构 Figure 1 The structures of isolated compounds |
乙腈为色谱纯(Fisher公司),水为超纯水,甲醇为分析纯(国药集团化学试剂有限公司)。
锥叶柴胡样品由产地采集及药材市场或饮片加工厂收集,其中1~6号样品采集自内蒙古海拉尔,7~10号样品收集自亳州药材市场,11号样品收集自哈尔滨市盛泰中药饮片加工厂,12号样品来自杭州桐君堂医药药材有限公司中药饮片厂,所有样品由中国食品药品检定研究院严华副主任药师鉴定为伞形科柴胡属植物锥叶柴胡(Bupleurum bicaule Helm)的干燥根。
2 方法与结果 2.1 溶液配制 2.1.1 混合对照品溶液分别取柴胡皂苷A、C、D和柴胡次皂苷F、G、I的对照品适量,精密称定,用80%甲醇水溶液配制得质量浓度(经对照品纯度折算)为每1 mL含柴胡皂苷A 0.208 0 mg,柴胡皂苷C 0.088 2 mg,柴胡皂苷D 0.600 0 mg,柴胡次皂苷F 0.331 0 mg,柴胡次皂苷G 0.783 0 mg,柴胡次皂苷I 0.166 3 mg的混合溶液,即得。
2.1.2 供试品溶液取锥叶柴胡样品粉末(过4号筛)约0.5 g,精密称定,置于具塞锥形瓶中,精密加入80%甲醇水溶液15 mL,密塞,称量,超声(功率200 W,频率40 kHz)提取45 min,放冷至室温,称量后用80%甲醇水溶液补足减失的量,摇匀,用微孔滤膜过滤,取续滤液,即得。
2.2 色谱条件采用InertSustain AQ-C18色谱柱(4.6 mm×250 mm,5 μm),以乙腈-水作为流动相进行梯度洗脱,梯度程序见表 1,流速1.0 mL·min-1,柱温25 ℃,检测波长210 nm。色谱图见图 2。
|
|
表 1 梯度洗脱时间表 Table 1 Gradient elution |
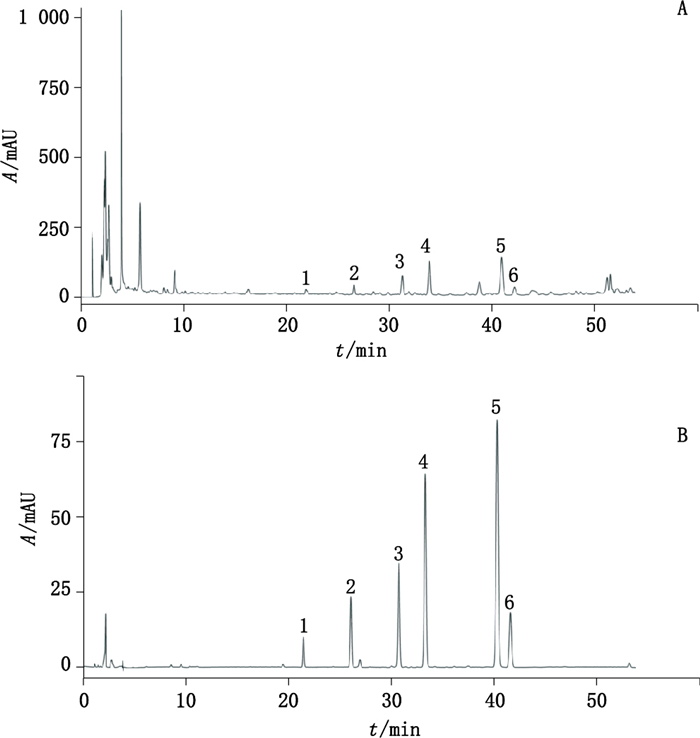
|
1.柴胡皂苷C(saikosaponin C)2.柴胡皂苷A(saikosaponin A)3.柴胡次皂苷F(prosaikogenin F)4.柴胡皂苷D(saikosaponin D)5.柴胡次皂苷G(prosaikegenin G)6.柴胡次皂苷I(prosaikegenin I) 图 2 1号样品(A)及混合对照品(B)色谱图 Figure 2 HPLC chromatograms of sample No. 1(A) and mixed reference substances(B) |
分别精密吸取“2.1.1”项下混合对照品溶液0.2、0.5、1.0、2.0、3.0、5.0 mL至5 mL量瓶中,加80%甲醇水溶液定容至刻度;分别精密吸取10 μL注入HPLC仪进行分析,以峰面积Y对进样浓度X进行回归方程计算。另取“2.1.1”项下混合对照品溶液逐级稀释,进样测定,当信噪比10:1时测得定量下限(LOQ),信噪比3:1时测得检测下限(LOD)。结果见表 2。
|
|
表 2 6个成分的回归方程、线性范围、相关系数和检出下限、定量下限 Table 2 Linear regression data, LODs and LOQs of six compounds |
精密吸取“2.1.1”项下混合对照品溶液,按“2.2”项下色谱条件连续进样6次,记录峰面积,柴胡皂苷A、C、D及柴胡次皂苷F、G、I峰面积的RSD分别为0.98%、2.0%、0.70%、0.67%、0.40%、0.59%,表明仪器精密度良好。
2.3.3 稳定性试验取锥叶柴胡(1号样品)粉末,按“2.1.2”项下方法制备供试品溶液,按“2.2”项下色谱条件分别于0、2、4、8、12、24 h进样分析,柴胡皂苷A、C、D及柴胡次皂苷F、G、I峰面积的RSD分别为1.2%、1.5%、2.7%、1.8%、0.71%、2.3%,表明供试品溶液在24 h内稳定性良好。
2.3.4 重复性试验取同一批次的锥叶柴胡(1号样品)粉末,按“2.1.2”项下方法平行制备6份供试品溶液,按“2.2”项下色谱条件进样分析,记录峰面积,计算平均含量及RSD。结果显示柴胡皂苷A、C、D及柴胡次皂苷F、G、I的平均含量分别为1.122、0.546、3.953、2.046、4.676、0.947 mg·g-1,RSD分别为2.6%、2.7%、1.6%、2.2%、1.7%、1.1%,表明该方法重复性良好。
2.3.5 加样回收试验精密称取已知含量的同一批次锥叶柴胡(1号样品)粉末6份,每份0.25 g,加入约与样品中待测成分含量等量的对照品,按“2.1.2”项下方法制备供试溶液,按“2.2”项下色谱条件进样分析,计算回收率。结果显示柴胡皂苷A、C、D及柴胡次皂苷F、G、I的平均回收率分别96.8%、107.7%、107.6%、93.4%、98.0%、91.1%,RSD分别为2.7%、0.73%、1.2%、2.8%、0.78%、1.7%。
2.4 样品含量测定按“2.1.2”项下方法制备12批样品的供试品溶液,按“2.2”项下色谱条件进行测定,外标法计算6个成分的含量,结果见表 3。
|
|
表 3 12批锥叶柴胡中6个成分含量测定结果 Table 3 Contents of six components from 12 batches of B. bicaule |
结合《中华人民共和国药典》和文献方法,在提取柴胡皂苷时常加入一定量的碱性试剂以防止原生皂苷次生化,本实验中考察了5%氨水-甲醇,100%甲醇和80%甲醇水溶液对6个成分的提取效果,结果表明,加入氨水与否6个成分的含量无明显差别,而以80%甲醇水溶液提取效果最好。在提取时间上,考察了30、45、60 min的提取效果,结果表明,提取45和60 min含量相近,因此选择45 min作为提取时间。回收率考察结果证明成分提取完全。
3.2 检测波长及流动相的选择根据柴胡皂苷类化合物的结构特点,最大吸收波长通常在210 nm左右,因此选择210 nm为检测波长。甲醇的最大吸收波长与检测波长相近,易造成对测定的干扰,故本实验选择乙腈和水作为流动相。
3.3 含量测定含量测定结果显示,不同批次的锥叶柴胡均含有上述6个成分,且大部分成分含量较为稳定。由表 3可以看出,12批锥叶柴胡中柴胡皂苷D含量(0.35%~1.92%)明显高于柴胡皂苷A(0.11%~0.34%),与文献结果[14-15]一致;总体来看柴胡次皂苷G的含量(0.18%~1.49%)与柴胡皂苷D相当,柴胡次皂苷F含量(0.13%~0.87%)略高于柴胡皂苷A,柴胡皂苷C含量较低(0.05%~0.20%),而柴胡次皂苷I为首次从柴胡属植物中分离得到,其含量虽然也相对较低(0.04%~0.37%),但对于锥叶柴胡的鉴别和质量控制仍具有一定的指导意义。产地采集和市场收集样品各成分含量差异明显,同产地不同批次相同成分含量也存在一定差异,因此对锥叶柴胡的质量控制进行深入研究,建立合理的含量测定限度尤为重要。此外,为扩大锥叶柴胡应用,仍需收集更多产地和批次的样品,对其化学成分和药理作用等多方面进行分析。
3.4 小结本文建立了同时测定锥叶柴胡中柴胡皂苷A、C、D及柴胡次皂苷F、G、I 6个皂苷类成分含量的分析方法,操作简便准确,重复性好,所考察的6个成分可作为锥叶柴胡的特征性成分用于其质量控制与评价,为其进一步开发利用提供理论基础。
| [1] |
中华人民共和国药典2015年版. 一部[ S]. 2015: 280 ChP 2015. Vol Ⅰ[S]. 2015: 280 |
| [2] |
ZHAO H, LI S, ZHANG H, et al. Saikosaponin A protects against experimental sepsis via inhibition of NOD2-mediated NF-κB activation[J]. Exp Ther Med, 2015, 10(2): 823. DOI:10.3892/etm.2015.2558 |
| [3] |
陈伟军. 柴胡皂苷a的抗惊厥及镇静催眠作用的实验研究[D]. 广州: 南方医科大学, 2013 CHEN WJ. Experiment Studies on Anticonvulsant and Sedative-hypnotic Effect of Saikosaponin a[D]. Guangzhou: Southern Medical University, 2013 |
| [4] |
黄伟, 赵燕, 孙蓉. 基于柴胡皂苷类成分的保肝作用与肝毒性研究进展[J]. 中国药物警戒, 2011, 8(1): 38. HUANG W, ZHAO Y, SUN R. Research development on hepatoprotective effect and hepatotoxicity based on Bupleurum saikosaponin components[J]. Chin J Pharmacovigil, 2011, 8(1): 38. |
| [5] |
戈宏焱. 柴胡皂苷抗抑郁作用及其机制的研究[D]. 长春: 吉林大学, 2010 GE HY. Studies on the Antidepressant Effect and Mechanisms of Saikosaponin a[D]. Changchun: Jilin University, 2010 |
| [6] |
陈志宝, 欧阳红生, 邓旭明, 等. 柴胡皂苷a对金黄色葡萄球菌基因转录表达谱的影响[J]. 中国兽医学报, 2010, 30(7): 966. CHEN ZB, OUYANG HS, DENG XM, et al. Effects of saikosaponin a on gene transcriptional expression spectrum in Staphylococcus aureus[J]. Chin J Vet Sci, 2010, 30(7): 966. |
| [7] |
袁鹏. 柴胡皂甙D诱导HeLa细胞自噬及其机制初步研究[D]. 长春: 吉林大学, 2014 YUAN P. A Preliminary Study on the Saikosaponin D Induced Hela Cells Autophagy And Its Mechanisms[D]. Changchun: Jilin University, 2014 |
| [8] |
王艳丽, 宋涛, 胡雅楠, 等. 柴胡皂甙d对实验性大鼠肝癌Ang-2及VEGF表达的影响[J]. 西安交通大学学报(医学版), 2013, 34(5): 664. WANG YL, SONG T, HU YN, et al. Effects of saikosaponins d on Ang-2 and VEGF expressions in experimental hepatocarcinoma in rats[J]. J Xi'an Jiaotong Univ (Med Sci), 2013, 34(5): 664. |
| [9] |
YAO M, YANG J, CAO L, et al. Saikosaponin d inhibits proliferation of DU145 human prostate cancer cells by inducing apoptosis and arresting the cell cycle at G0/G1 phase[J]. Mol Med Rep, 2014, 10(1): 365. DOI:10.3892/mmr.2014.2153 |
| [10] |
许枬, 钟旭, 石亚囡, 等. 锥叶柴胡化学成分的分离与鉴定[J]. 沈阳药科大学学报, 2014, 31(4): 256. XU N, ZHONG X, SHI YN, et al. Isolation and identification of chemical constituents from Bupleurum bicaule Helm[J]. J Shenyang Pharm Univ, 2014, 31(4): 256. |
| [11] |
XU N, SHI YN, ZHONG X, et al. A new saikogenin from the roots of Bupleurum bicaule[J]. Chin J Nat Med, 2014, 12(4): 305. |
| [12] |
朱占军, 潘瑞乐, 斯建勇, 等. 锥叶柴胡化学成分研究[J]. 天然产物研究与开发, 2008, 20(5): 833. ZHU ZJ, PAN RL, SI JY, et al. Study on the chemical constituents of Bupleurum bicaule Helm[J]. Nat Prod Res Dev, 2008, 20(5): 833. |
| [13] |
唐智芳. 锥叶柴胡化学成分和质量研究[D]. 北京: 北京中医药大学, 2010 TANG ZF. Study on Chemical Composition and Quality of Bupleurum bicaule Helm[D]. Beijing: Beijing University of Chinese Medicine, 2010 |
| [14] |
林东昊, 茅仁刚, 王智华, 等. 23种国产柴胡属植物中柴胡皂苷a、c、d含量的RP-HPLC测定[J]. 药物分析杂志, 2004, 24(5): 479. LIN DH, MAO RG, WANG ZH, et al. Quantitative analysis of saikosaponin a, c, d from 23 species of Radix Bupleuri in China by RP-HPLC[J]. Chin J Pharm Anal, 2004, 24(5): 479. |
| [15] |
潘瑞乐, 陈迪华, 陈建民, 等. RP-HPLC法测定中柴1号及其他产地柴胡中柴胡皂苷a、d的含量[J]. 中南药学, 2004, 2(4): 198. PAN RL, CHEN DH, CHEN JM, et al. Determination of saikosaponin a and d in Radix Bupleuri by RP-HPLC[J]. Cent South Pharm, 2004, 2(4): 198. |
 2018, Vol. 38
2018, Vol. 38 
