右旋糖酐40系蔗糖经肠膜状明串珠菌L.M-1226号菌(leuconostoc mesenteroides)发酵后生成的高分子葡萄糖聚合物,经处理精制而得。主要有右旋糖酐40氯化钠注射液和右旋糖酐40葡萄糖注射液2种。其中,右旋糖酐40氯化钠注射液是常用的血容量扩充药,主要用于治疗各种休克、血栓性疾病、及体外循环时,代替部分血液等[1-3]。目前,其执行标准为中国药典2015年版二部,采用旋光度及沉淀滴定的方法测定含量[4],该方法对操作者技能、仪器及操作环境的要求较高。同时,国家大力发展现场快速检测事业,以解决现场及偏远地区药品检测问题,应对突发自然灾害。
近红外(near infrared,NIR)光谱分析技术具有操作简便、分析速度快、非破坏性、无污染、易于实现现场分析的特点,因此在药物的定性鉴别、定量分析、在线检测及质量控制等方面显示了巨大的优势[5]。本文采用近红外透反射光谱分析技术结合化学计量学方法,研究建立多厂家右旋糖酐40氯化钠注射液快速定量分析方法并进行验证。
1 仪器及试药 1.1 仪器Matrix-F近红外光谱仪(德国Bruker公司),配有1.5 m长固体光纤探头及1号液体测样附件,铟镓砷(InGaAs)检测器,OPUS5.5光谱分析软件(德国Bruker公司)附带Quant 2软件包。
P850全自动旋光仪(济南海能仪器有限公司),BP211D电子分析天平(德国赛多利斯公司)。
1.2 样品4个厂家30批右旋糖酐40氯化钠注射液,均为陕西省食品药品检验所抽验样品。同时,每个厂家分别选取1批样品,稀释制成12个不同浓度梯度样品。共42批样品。
2 试验方法 2.1 含量测定依据中国药典2015年版二部,采用旋光法测定右旋糖酐40的含量,沉淀滴定法测定氯化钠的含量。42批样品含量测定结果均以[%和(mg·mL-1)]表示。
2.2 NIR光谱测定以透反射方式采集样品的NIR光谱。采用光纤探头和液体采样附件,将样品滴加到1号采样附件(光程1 mm)上测定样品的光谱。光谱采集条件:扫描范围为12 000~4 000 cm-1,分辨率8 cm-1,室温,扫描次数64次,每批样品测定3瓶作为原始光谱,再求平均光谱作为建模光谱。
2.3 定量模型的建立采用OPUS5.5光谱分析软件附带的Quant 2软件包,运用偏最小二乘法(partial least square,PLS)建立初步的定量校正模型[6]。模型总的预测准确性用交叉验证均方根误差(root mean square errors of cross validation,RMSECV)(式1)
| ${\rm{RMSECV}} = \sqrt {\sum\limits_{{\rm{i}} = 1}^{{N_{\rm{C}}}} {\frac{{{{\left( {{{\mathord{\buildrel{\lower3pt\hbox{$\scriptscriptstyle\frown$}} \over Y} }_{{\rm{CVi}}}} - {Y_{\rm{i}}}} \right)}^2}}}{{{N_{\rm{C}}}}}} } $ | (1) |
式1中,
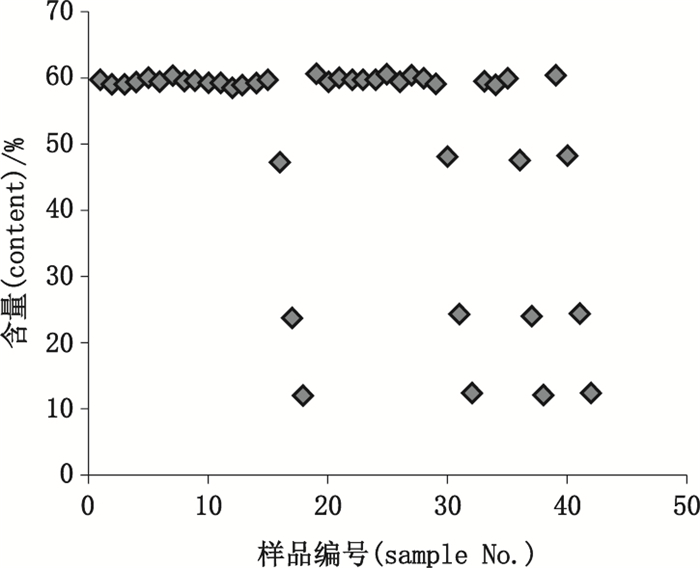
根据建模样品的数量,采用内部交叉验证法建模,42批样品全部作为校正集建立模型[7]。其含量分布如图 1~2所示。
|
图 1 右旋糖酐40含量分布图 Figure 1 Distribution of dextran 40 |
|
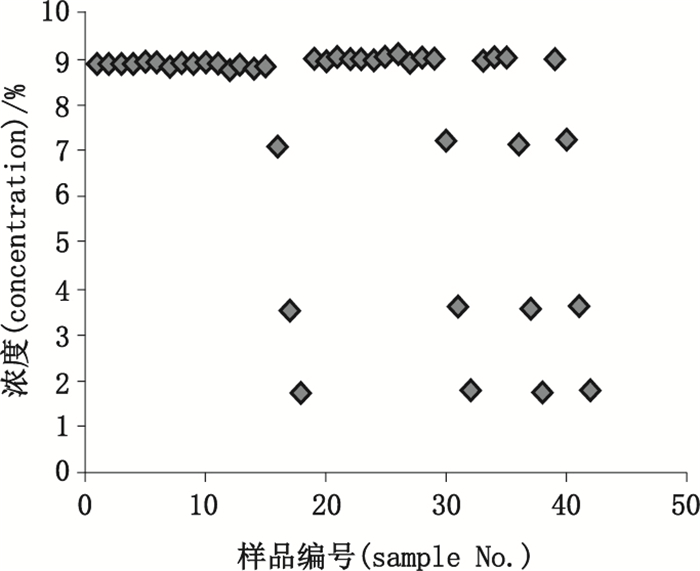
图 2 氯化钠含量分布图 Figure 2 Distribution of sodium chloride |
近红外建模有2种验证方式,一种是内部交叉验证,另一种是外部验证,2种验证方式的选择主要取决于建模样品量。通常,样本量充足(> 100)选用外部验证,样本量不足,选用内部交叉验证。本实验全国范围内共42批样品,我们选择内部交叉验证,即所有样本均作为校正集,该方法每个样本均参与建模,同时也均参与验证。无论选择哪种验证方式,只要模型参数不变,模型的预测结果便是同样的。
3.2 NIR校正模型选取特定建模谱段、适当的光谱预处理方法及合理的化学计量学方法以突出活性成分的信息,建立稳健的NIR校正模型。
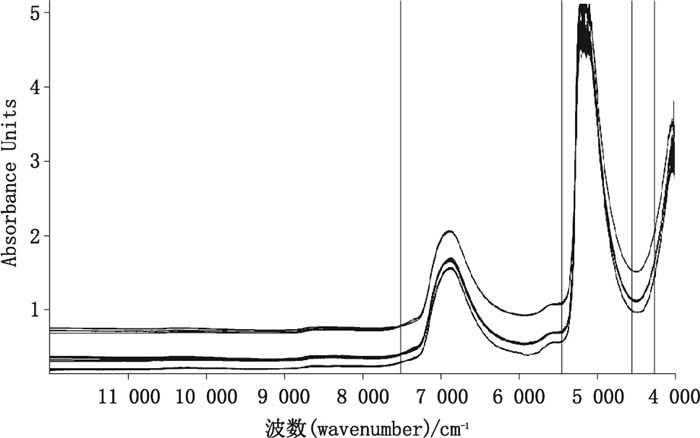
3.2.1 建模谱段的选择建立NIR校正模型时,大于10 000 cm-1的末端吸收较弱且容易形成噪音干扰,小于4 200 cm-1会因为边缘效应和和噪音形成干扰,故我们选择建模谱段时避开此区域[8-9]。波数5 155 cm-1左右处为水合频吸收,峰较强且谱带较宽,已溢出,故避开此区域[10-12]。实验中,选取的建模谱段为7 502~5 446 cm-1和4 602~4 247 cm-1,见图 3。
|
图 3 建模谱段选取图 Figure 3 The picture of different spectral range |
选取不同谱段建立NIR模型并根据RMSECV、R2及Rank值做一比较,结合OPUS软件优化的结果,最终选取7 502~5 446 cm-1和4 602~4 247 cm-1为建模谱段,其RMSECV最小,R2最大且Rank值在6~10之间,预测准确性及稳健性均良好。表 1为选取不同谱段的建模结果,表明模型1所选谱段最优。
|
|
表 1 选取不同谱段的建模结果 Table 1 The calibration models constructed using different spectral range |
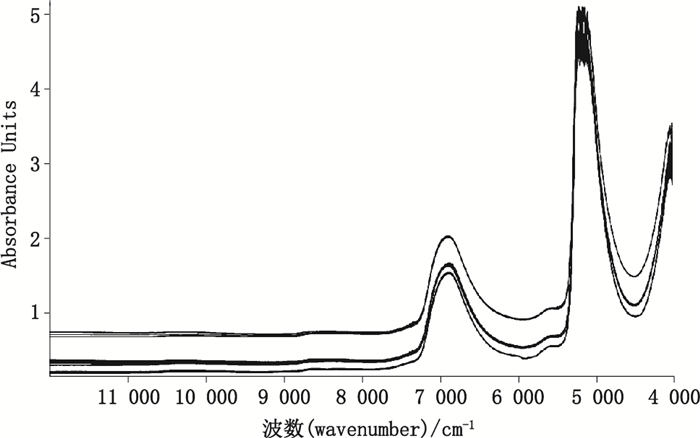
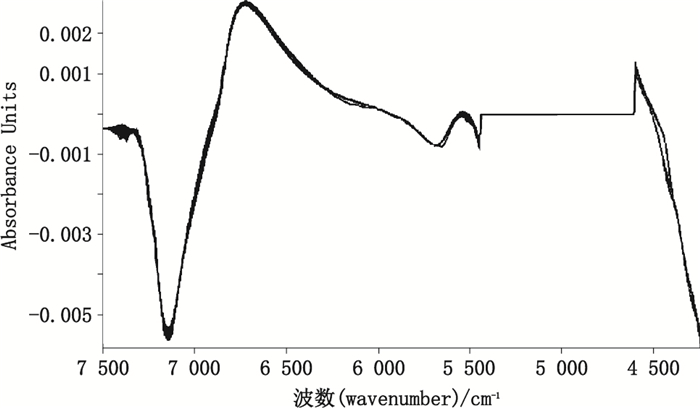
实验选取一阶导数(first derivative,FD)的预处理方法,17点平滑。FD预处理方法可以有效地消除基线的漂移,改善背景干扰,分辨重叠峰,提高分辨率和灵敏度;平滑处理是消除噪声常用的方法[13-14]。建模样品的原始NIR漫反射光谱如图 4所示,经FD、VD及平滑预处理后的光谱如图 5所示,可知光谱经过预处理之后,降低了背景及噪声干扰,提高了信噪比,增强了光谱特征。
|
图 4 建模样品原始NIR图谱 Figure 4 Original NIR spectra of dextran 40 sodium chloride injection |
|
图 5 建模样品经过FD和VD预处理后的NIR漫反射光谱 Figure 5 NIR spectra of dextran 40 sodium chloride injection pretreated by FD and VD |
结合OPUS软件自动优化结果、模型稳健性理论[15]及外部验证结果,在多次尝试之后,认为最有模型的参数如表 2所示。其内部交叉验证相关性结果如图 6~9所示。
|
|
表 2 最优模型的各项参数 Table 2 Characteristics of the final calibration model |
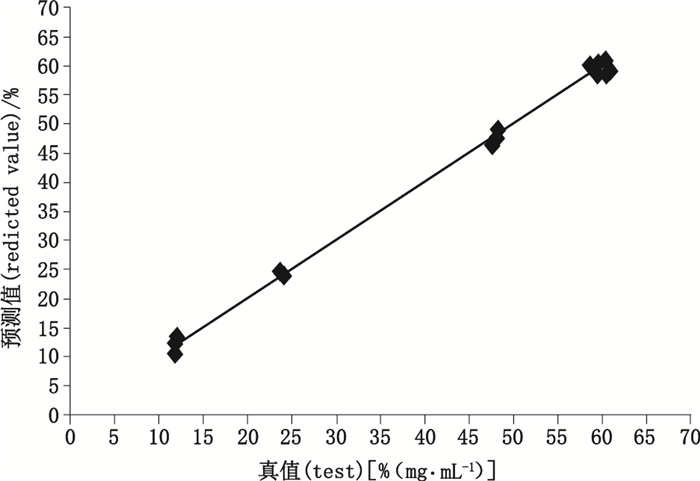
|
图 6 右旋糖酐40 NIR内部交叉验证结果相关性图 Figure 6 The cross validation results for dextran 40 |
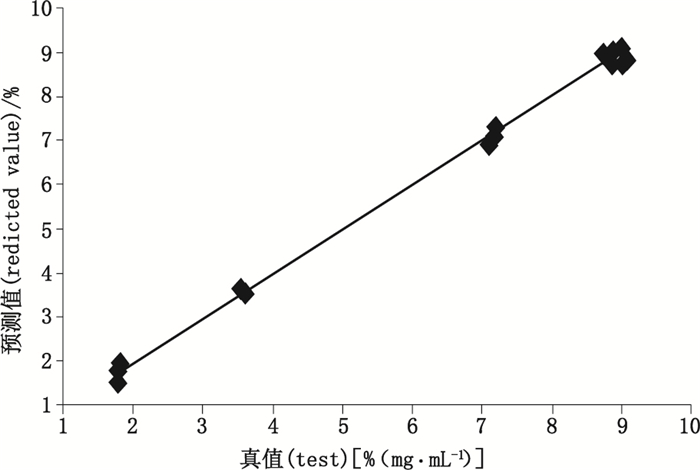
|
图 7 氯化钠NIR内部交叉验证结果相关性图 Figure 7 The cross validation results for sodium chloride |
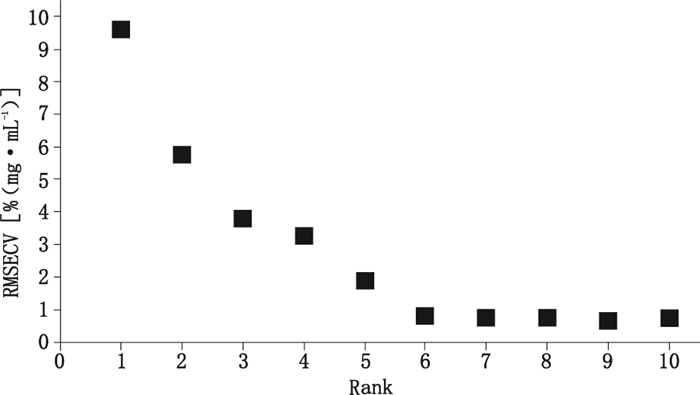
|
图 8 右旋糖酐40 NIR定量模型Rank & RMSECV图 Figure 8 RMSECV vs. Rank value of dextran 40 |
|
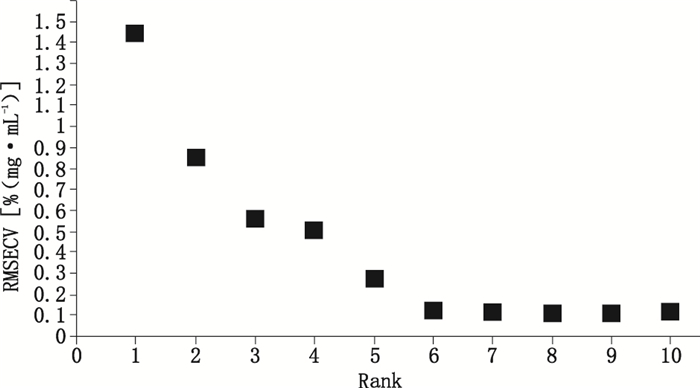
图 9 氯化钠NIR定量模型Rank & RMSECV图 Figure 9 RMSECV vs. Rank value of sodium chloride |
选取来自另4个不同厂家的15批右旋糖酐40氯化钠注射液及实验室自制的9批不同浓度梯度的样品,共21个样本来测试所建模型的准确性。NIR预测值与真值比较,右旋糖酐40平均偏差为0.43%,最大偏差为1.4%;平均相对偏差为1.1%,最大相对偏差为3.9%。氯化钠平均偏差为0.07%,最大偏差为0.15%;平均相对偏差为1.2%,最大相对偏差为3.7%,均小于近红外快速检测对于偏差的限度要求5%,见表 3。由表可知,即使在浓度范围低至2%左右时,所建模型的预测偏差亦小于5%,满足快检需求。同时,将验证集样品NIR预测结果与真值在95%可信区间内进行配对t-检验,右旋糖酐40的p为1.213,大于0.05;氯化钠的p为1.307,大于0.05。表明所建模型NIR预测结果与真值没有显著性差异。
|
|
表 3 模型准确性预测结果 Table 3 The predictive results of model accuracy |
马氏距离常用来测定PLS校正模型的溢出值,以评价其专属性。右旋糖酐40氯化钠注射液定量模型的马氏距离限定值(式2),在所选谱段范围内被设定为0.33,选取5批另年抽取的右旋糖酐40氯化钠注射液(T)测试模型的专属性。所有样品测试结果均为通过,其马氏距离均小于0.33。另选取5批同剂型相似品种右旋糖酐40葡萄糖注射液(S)测试,5批样品均未通过,其马氏距离均大于模型阈值。表明所建模型对右旋糖酐40氯化钠注射液具有专属性。
| ${\rm{Threshold = }}\frac{{{\rm{Factor}} \times {\rm{Rank}}}}{M} = 0.33$ | (2) |
式中:Rank为PLS矢量数;M为建模样本数;Factor为2。
3.3.3 线性近红外为二级方法,一般采用多元回归,通常用待分析物的NIR预测结果与参考值之间的关系来评价其线性。右旋糖酐40和氯化钠线性方程分别为:
| $Y{\rm{ = 0}}{\rm{.995}}X{\rm{ + 0}}{\rm{.252 }}\;r{\rm{ = 0}}{\rm{.999}}$ | (3) |
| $Y{\rm{ = 0}}{\rm{.995}}X{\rm{ + 0}}{\rm{.036}}\;r{\rm{ = 0}}{\rm{.998}}$ | (4) |
试验以重复性和中间精密度来考察该方法的精密度,方法及结果见表 4。
|
|
表 4 右旋糖酐40氯化钠注射液模型精密度结果 Table 4 Precision of the model for dextran 40 sodium chloride injection |
本文采用NIR透反射光谱分析技术建立了多厂家右旋糖酐40氯化钠注射液快速定量分析模型。和传统方法相比,所建立新方法简便,快速,节省人力、物力,适用于药品的快速检验及不具备试验条件的现场和基层检测,有广阔的应用前景。同时,也为实现在线监控药品质量提供了依据。
| [1] |
赵峰辉, 李新图, 陈建中, 等. HPLC法测定右旋糖酐20氯化钠注射液的含量[J]. 中国医药指南, 2013, 11(22): 402. ZHAO FH, LI XT, CHEN JZ, et al. HPLC determination of two components in dextran 20 sodium chloride injection[J]. Guide Chin Med, 2013, 11(22): 402. |
| [2] |
李娜. 右旋糖酐-40葡萄糖注射液中葡萄糖的含量测定[J]. 抗感染药学, 2017, 14(3): 491. LI N. Determination of glucose in dextran-40 glucose injection by HPLC[J]. Anti Infect Pharm, 2017, 14(3): 491. |
| [3] |
杨燕妮, 冯雪梅, 楚莉辉, 等. 85例右旋糖酐40注射液致严重不良反应报道分析[J]. 临床合理用药, 2016, 9(6C): 175. YANG YN, FENG XM, CHU LH, et al. Analysis of 85 cases of serious adverse reactions induced by dextran 40 injection[J]. Chin J Clin Ration Drug Use, 2016, 9(6 C): 175. |
| [4] |
中国药典2015年版. 一部[S]. 2015: 1583 ChP 2015. Vol Ⅰ[S]. 2015: 1583 |
| [5] |
王小亮, 傅强, 绳金房, 等. 近红外光谱分析技术在制药过程分析中的应用进展[J]. 西北药学杂志, 2009, 24(03): 228. WANG XL, FU Q, SHENG JF, et al. Advanced on process analytical technology in pharmaceutics using near infrared spectroscopy technology[J]. Pharm Northwest J, 2009, 24(3): 228. |
| [6] |
李朋成, 朱军桃, 马云栋, 等. 基于偏最小二乘法的近红外光谱分析应用[J]. 测绘地理信息, 2015, 40(2): 536. LI PC, ZHU JT, MA YD, et al. Near infrared spectral analysis based on partial least squares[J]. J Geomat, 2015, 40(2): 536. |
| [7] |
詹雪艳, 赵娜, 林兆洲, 等. 校正集选择方法对于积雪草总苷中积雪草苷NIR定量模型的影响[J]. 光谱学与光谱分析, 2014, 34(12): 3267. ZHAN XY, ZHAO N, LIN ZZ, et al. Effect of algorithms for calibration set selection on quantitantive determination of asiaticoside content in centella total glucosides by near infrared spectroscopy[J]. Spectrosc Spect Anal, 2014, 34(12): 3267. DOI:10.3964/j.issn.1000-0593(2014)12-3267-06 |
| [8] |
王小亮, 贾建忠, 杨欣, 等. 近红外透射光谱法快速测定布洛芬缓释胶囊释放度[J]. 药物分析杂志, 2012, 32(10): 1898. WANG XL, JIA JZ, YANG X, et al. Quick analysis of the releasing rate for ibuprofen sustained-release capsules using near infrared transmission spectroscopy technology[J]. Chin J Pharm Anal, 2012, 32(10): 1898. |
| [9] |
DENG RR, HE YQ, QIN Y, et al. Measuring pure water absorption coefficient in the near-infrared spectrum(900-2500)[J]. J Remote Sensing, 2012, 16(1): 192. |
| [10] |
柳艳云, 胡昌勤. 近红外分析中光谱波长选择方法进展与应用[J]. 药物分析杂志, 2010, 30(5): 968. LIU YY, HU CQ. Progress and application of spectral wavelength selection methods in NIR analytical technique[J]. Chin J Pharm Anal, 2010, 30(5): 968. |
| [11] |
洪明坚, 温泉, 温志渝. 一种基于蒙特卡罗方法的近红外波长选择算法[J]. 光学学报, 2010, 30(12): 3637. HONG MJ, WEN Q, WEN ZY. New near infrared wavelength selection algorithm based on monte-carlo method[J]. Acta Opt Sin, 2010, 30(12): 3637. |
| [12] |
WANG XL, FU Q, SHENG JF, et al. Construction of a universal quantitative model for ibuprofen sustained-release capsules from different manufacturers using near-infrared diffuse reflection[J]. Vib Spectrosc, 2010, 53: 214. DOI:10.1016/j.vibspec.2010.03.002 |
| [13] |
严衍禄. 近红外光谱分析基础与应用[M]. 北京: 中国轻工业出版社, 2005, 177. YAN YL. Basis and Application of Near Infrared Spectroscopy Analysis[M]. Beijing: China Light Industry Press, 2005, 177. |
| [14] |
FENG YC, YANG XL, YANG ZH, et al. Monitoring the quality of drugs in circulation using rapid NIR spectral comparison methods[J]. J Chin Pharm Sci, 2011, 20: 290. |
| [15] |
周熙艳, 岳勇, 王涛, 等. PLS因子数对定量模型性能稳定性的影响分析[J]. 计算机工程与设计, 2014, 35(5): 1788. ZHOU XY, YUE Y, WANG T, et al. Analysis of impact of PLS component number on stability of quantitative model[J]. Comp Eng Design, 2014, 35(5): 1788. |
 2018, Vol. 38
2018, Vol. 38 