2. 唐山市第二医院药剂科, 唐山 063000;
3. 解放军白求恩国际和平医院药剂科, 石家庄 050082;
4. 中国石油天然气集团公司中心医院药学部, 廊坊 065000
2. Pharmacy Department, the Second Hospital of Tangshan, Tangshan 063000, China;
3. Pharmacy Department, Bethune International Peace Hospital of PLA, Shijiazhuang 050082, China;
4. Pharmaceutical Department, China National Petroleum Corporation Center Hospital, Langfang 065000, China
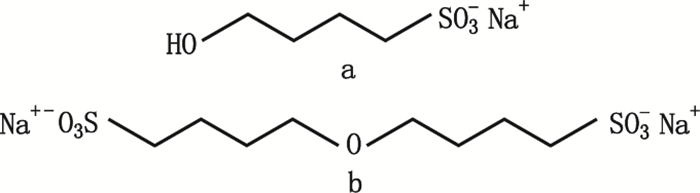
磺丁基醚-β-环糊精(betadex sulfobutyl ether sodium,SBE-β-CD)是一种肾毒性小、水溶性好、溶血作用小的优良药用辅料,由1,4-丁烷磺内酯(1,4-BS)在碱性条件下与β-CD的2,3,6位碳上的羟基发生取代反应而得[1-7]。4-羟基丁磺酸为原料1,4-BS和目标化合物SBE-β-CD的副产物,二磺烷基化醚为1,4-BS的合成原料,在合成SBE-β-CD时,两者极有可能以4-羟基丁磺酸钠(4-HSS)(结构见图 1-a)、二磺烷基化醚钠(BES)(结构见图 1-b)的形式存在于SBE-β-CD中,由于两者均有潜在的基因毒性风险,为保证产品质量,需要对其进行质量控制。这2种潜在杂质均为烷基磺酸钠盐,属于离子型化合物,且无紫外吸收,不能采用常规的HPLC-UV法进行测定。目前磺酸盐的含量测定方法有紫外分光光度法[8]、离子色谱法[9-12]、两相滴定法[13]、电喷雾质谱法[14-15]等,而对于4-HSS、BES的测定尚未见文献报道。本研究采用高效液相色谱-质谱联用技术,对4-HSS和BES同时进行定量分析,以期为SBE-β-CD的质量控制提供实用、便捷、灵敏的分析方法。
|
图 1 4-HSS(a)和BES(b)结构式 Figure 1 Structures of 4-HSS(a)and BES(b) |
Agilent 1260液相色谱仪(美国Agilent公司),配有四元泵、在线脱气机,示差折光检测器(1260 Infinity,美国Agilent公司);Waters alliance 2695液相色谱仪(美国Waters公司),配有四元泵、在线脱气机,Waters 2420蒸发光散射检测器(ELSD)(美国Waters公司);3200 QTRAP型串联四极杆线性离子阱质谱仪配有Analyst 1.5.2数据采集、分析软件(美国AB公司);Agilent 1200液相色谱仪,配有四元泵、在线脱气机、自动进样器(美国Agilent公司);Inertsil ODS-SP色谱柱(4.6 mm×250 mm,5 μm;填料:十八烷基硅烷键合硅胶;日本GL Sciences株式会社);TDL-5台式离心机(北京雷勃尔离心机有限公司);雷磁pH S-25型pH计(上海仪电科学仪器股份有限公司)。
1.2 试药正戊胺(纯度 > 99%,美国Sigma公司);四丁基氢氧化铵(分析纯,国药集团化学试剂北京有限公司);醋酸铵(色谱纯,美国Dikma公司);甲醇(色谱纯,J.T Baker);乙酸(色谱纯,美国Dikma公司);纯净水(杭州娃哈哈集团有限公司);对照品4-HSS、BES(河北医科大学药物化学实验室提供);SBE-β-CD(批号:20111201、20111202、20111203,由石药集团提供)。
2 方法与结果 2.1 检测条件 2.1.1 色谱条件色谱柱:Inertsil ODS-SP(4.6 mm×250 mm,5 μm),柱温为30 ℃;流动相:甲醇-10 mmol·L-1正戊胺溶液(用乙酸调节pH至5.5)(30:70);流速1.0 mL·min-1;进样量10 μL。
2.1.2 质谱条件离子源:电喷雾离子(ESI)源;检测方式:多反应监测(MRM)模式;负离子监测模式:源喷射电压:-4.5 kV;离子源温度:650 ℃;帘气:0.21 MPa;雾化气:0.42 MPa,加热气:0.45 MPa,均为氮气。4-HSS和BES的监测离子对分别为m/z 153.0/79.8和m/z 289.0/152.9;碎裂电压(DP)分别为-36、-50 V;碰撞能量(CE)分别为-34、-29 eV。
2.2 溶液的配制 2.2.1 对照品溶液取4-HSS对照品适量,精密称定,用流动相溶解并定量稀释制成每1 mL中约含50 ng的溶液,作为4-HSS对照品储备液。精密量取上述溶液1 mL,置10 mL量瓶中,用流动相稀释至刻度,摇匀,即得每1 mL中约含5 ng的4-HSS对照品溶液。
取BES对照品适量,精密称定,用流动相溶解并定量稀释制成每1 mL中约含200 ng的溶液,作为BES对照品储备液。精密量取上述溶液1 mL,置10 mL量瓶中,用流动相稀释至刻度,摇匀,即得每1 mL中约含20 ng的BES对照品溶液。
分别取4-HSS和BES对照品储备液各0.5 mL,置10 mL量瓶中,用流动相稀释至刻度,即得混合对照品溶液。
2.2.2 供试品溶液取SBE-β-CD供试品约20 mg,精密称定,置10 mL量瓶中,用流动相溶解并稀释至刻度,得2 mg·mL-1的供试品储备液;精密量取上述溶液1 mL,置10 mL量瓶中,用流动相稀释至刻度,即得每1 mL中约含0.2 mg的供试品溶液。
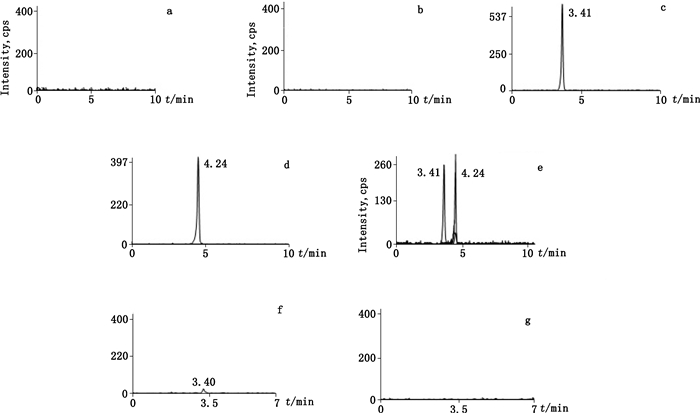
2.3 专属性分别取空白溶剂(流动相)、4-HSS对照品溶液、BES对照品溶液、混合对照品溶液、供试品溶液进行分析,见图 2。4-HSS与BES的保留时间分别为3.41、4.24 min,空白溶剂无干扰,表明该方法专属性良好。
|
a. 4-HSS的空白溶剂(blank solvent of 4-HSS)b. BES的空白溶剂(blank solvent of BES)c. 4-HSS对照品(4-HSS reference susstance)d. BES对照品溶液(BES reference susstance)e.混合对照品溶液(mixture of 4-HSS and BES)f.样品中的4-HSS(4-HSS sample)g.样品中的BES(BES in sample) 图 2 多重反应监测色谱图 Figure 2 Multiple-reaction monitoring chromatograms for specificity |
取4-HSS、BES对照品溶液逐级稀释,进行分析,分别以信噪比S/N=3时各对照品的浓度为检测下限,以S/N=10时各对照品的浓度为定量下限。4-HSS、BES的检测下限分别为0.005、0.02 ng·mL-1,定量下限分别为0.01、0.04 ng·mL-1。
2.5 线性关系考察分别取4-HSS、BES对照品储备液适量,制成系列浓度的混合对照品溶液,4-HSS的质量浓度依次为0.1、0.25、0.5、1.0、2.5、5.0 ng·mL-1;BES的质量浓度依次为0.4、1.0、2.0、4.0、10.0、20.0 ng·mL-1,分别进样。以对照品浓度(X,ng·mL-1)为横坐标,峰面积(Y)为纵坐标,进行线性回归。4-HSS和BES回归方程分别为:
Y=114.2X+29.60 r=0.999 7
Y=21.68X+18.69 r=0.999 6
表明4-HSS在0.1~5.0 ng·mL-1范围内和BES在0.4~20.0 ng·mL-1范围内线性关系良好。
2.6 精密度试验取混合对照品溶液连续进样6次,进行分析,4-HSS与BES峰面积的RSD分别为2.5%、3.5%,表明仪器精密度良好。
2.8 重复性与加样回收率试验平行配制6份供试品溶液(批号:20111203),进样分析,记录峰面积,以标准曲线法计算含量,即为原有量,6份供试品溶液中4-HSS的平均含量为0.000 57%,RSD为3.7%,表明4-HSS的方法重复性良好,由于未能检测到BES,故采用加样供试品测定,结果见加样回收率试验。
取供试品(批号:20111203)约20 mg,精密称定,置10 mL量瓶中,精密加入4-HSS和BES对照品储备液各2.5 mL,用流动相溶解并稀释至刻度,平行制备6份,分别精密量取上述溶液1 mL,置10 mL量瓶中,用流动相稀释至刻度,进行分析,记录峰面积,以标准曲线法计算,即为测得量,根据回收率=(测得量-原有量)/加入量×100%,计算回收率,结果见表 1,并计算BES 6次测定结果的RSD。6份添加对照品的供试品溶液中BES含量测定结果的RSD为4.1%,表明该方法的重复性良好。
|
|
表 1 加样回收率试验结果(n=6) Table 1 Results of recovery test |
精密量取供试品储备液1 mL,置10 mL量瓶中,再精密加入4-HSS和BES对照品储备液各0.25 mL,用流动相稀释至刻度,分别在室温下放置0、4、8和12 h时进样,记录峰面积。与0 h相比,供试品浓度的相对误差(RE)为-4.0%~4.4%,表明供试品溶液在室温下放置12 h基本稳定。
2.9 含量测定取各批供试品,制备供试品溶液,进行分析,记录峰面积,以标准曲线法计算4-HSS和BES的含量。3批供试品中4-HSS的含量依次为0.001 6%、0.001 3%、0.000 57%,BES均低于检测限,满足美国药典4-HSS不大于0.09%,BES不大于0.05%的规定[12]。
3 讨论 3.1 分析方法的选择4-HSS和BES均为烷基磺酸钠盐,无紫外吸收,且在普通反相C18柱上不保留,因此只能选择通用型检测器,如(示差折光检测器、蒸发光散射检测器)和离子色谱法。首先考察了C18柱、季铵盐类离子对试剂、示差折光检测器系统,结果出现消除不掉的倒峰;后又考察了C18柱、挥发性离子对试剂(三乙胺、正戊胺)、蒸发光散射检测器系统,结果出现未知峰,且经常产生基线漂移现象;还曾尝试过HILIC柱,虽与之前方法相比有一定改善,但仍达不到分析要求。最终使用C18柱、挥发性离子对试剂(正戊胺)、LC-MS系统,能够产生保留,且灵敏度较高,因此选择该方法,并做进一步优化。
3.2 质谱条件的选择为获得最佳的质谱条件,4-HSS和BES用流动相溶解后分别注入到质谱仪,在正、负离子模式下进行优化,结果表明2种杂质均在负离子模式下更稳定,响应值更高。然后在Q1模式下优化DP电压,选择响应值最高的峰作为待测物的母离子,在MS2模式下优化CE电压,根据离子的响应值和稳定性,获得最佳定量子离子。
3.3 液相条件的优化4-HSS和BES含有一个相同的离子对(153.0/79.8),同时这一离子对也是4-HSS唯一的定量离子对,因此,在优化色谱条件时需要使两者达到基线分离。在甲醇-水(pH 5.5)(30:70)条件下,考察了不同离子对试剂浓度(2、5、10 mmol·L-1)时2种杂质的分离度,结果显示正戊胺浓度为2 mmol·L-1时样品不保留,浓度为5 mmol·L-1时2种杂质未完全分离,浓度为10 mmol·L-1时2种杂质完全分离,且峰形较好,因此选择正戊胺的浓度为10 mmol·L-1。在甲醇-10 mmol·L-1正戊胺溶液(30:70)条件下,用乙酸调节pH,考察了不同pH(5.5、5.0、4.5、4.0)对响应值的影响,结果表明随着pH的降低,分析物的响应值降低,故选择pH 5.5。研究发现,pH在6.0~9.0范围内pH变化较快,溶液不容易配制,且平行性差,故仅考察到pH 5.5,在此条件下灵敏度和分离度均能满足测定要求。
| [1] |
谷福根, 高永良, 崔福德. 磺丁基醚-β-环糊精及其在药剂学中的应用[J]. 中国新药杂志, 2004, 13(1): 15. GU FG, GAO YL, CUI FD. Betadex sulfobutyl ether sodium-a new excipient and its applications in pharmaceutics[J]. Chin J New Drugs, 2004, 13(1): 15. |
| [2] |
姜锡娟, 李闻新, 杜玉民, 等. 磺丁基醚-β-环糊精的高效毛细管电泳-间接UV法分析[J]. 中国医药工业杂志, 2012, 43(3): 201. JIANG XJ, LI WX, DU YM, et al. Analysis of betadex sulfobutyl ether sodium by high performance capillary electrophoresis with indirect UV detection[J]. Chin J Pharm, 2012, 43(3): 201. |
| [3] |
王双, 周娜, 李闻新, 等. 分散液液微萃取-GC法测定磺丁基醚-β-环糊精中杂质1, 4-丁烷磺内酯[J]. 沈阳药科大学学报, 2016, 33(4): 298. WANG S, ZHOU N, LI WX, et al. Determination of 1, 4-butane sultone in betadex sulfobutyl ether sodium by dispersive liquid-liquid microextraction coupled with gas chromatography[J]. J Shenyang Pharm Univ, 2016, 33(4): 298. |
| [4] |
曹雅培, 王静, 曹德英. 药用辅料磺丁基醚-β-环糊精在不同制剂中的应用进展[J]. 中国药房, 2012, 23(1): 79. CAO YP, WANG J, CAO DY. Application of betadex sulfobutyl ether sodium in different preparations[J]. China Pharm, 2012, 23(1): 79. |
| [5] |
杨学敏, 杨波, 廖霞俐, 等. 不同取代度磺丁基醚-β-环糊精的合成工艺研究[J]. 化学世界, 2013, 54(2): 110. YANG XM, YANG B, LIAO XL, et al. Study on the synthesis technology of sulfobutyl ether β-cyclodextrins with different degrees of substitution[J]. Chem World, 2013, 54(2): 110. |
| [6] |
刘春冬, 王建华, 徐世荣. 磺丁基醚-β-环糊精对药物的增溶作用[J]. 中国现代应用药学杂志, 2006, 23(8): 742. LIU CD, WANG JH, XU SR. Pharmaceutical application of sulfobutyl ether β-cyclodextrin for solubilization[J]. Chin J Mod App Pharm, 2006, 23(8): 742. |
| [7] |
王建华, 宋爱晶. 一种新型辅料磺丁基醚-β-环糊精的药学应用进展[J]. 材料导报, 2007, 21(3): 40. WANG JH, SONG AJ. Progress in pharmaceutical applications of a new excipient sulfobutyl-β-cyclodextrins[J]. Mater Rev, 2007, 21(3): 40. |
| [8] |
徐广义, 李敏. 紫外分光光度法测定石油中的重烷基苯磺酸盐[J]. 广州化工, 2013, 41(10): 162. XU GY, LI M. Determination of heavy alkylbenzene sulfonate in oil by UV spectrophotometry[J]. Guangzhou Chem Ind, 2013, 41(10): 162. DOI:10.3969/j.issn.1001-9677.2013.10.062 |
| [9] |
刘家胜, 孙建合. 离子色谱法测定托吡酯中氨基磺酸盐和硫酸盐的含量[J]. 药学研究, 2015, 34(9): 519. LIU JS, SUN JH. Determination of sulfamate and sulfate in topiramate by ion chromatographic[J]. J Pharm Res, 2015, 34(9): 519. |
| [10] |
王伟, 项素云, 孙文芳, 等. 离子色谱法测定磺丁基醚-β-环糊精中4-羟基丁磺酸[J]. 药学进展, 2012, 36(3): 128. WANG W, XIANG SY, SUN WF, et al. Determination of 4-hydroxy-1-butanesulfonic acid in betadex sulfobutyl ether sodium by ion chromatography[J]. Prog Pharm Sci, 2012, 36(3): 128. |
| [11] |
宋阳, 于彬, 邹佳, 等. 反相离子对色谱法测定2, 5-二羟基苯磺酸盐及有关物质[J]. 药物分析杂志, 2010, 30(1): 130. SONG Y, YU B, ZOU J, et al. Ion-pair-RP-HPLC determination of dobesilates and their related substances[J]. Chin J Pharm Anal, 2010, 30(1): 130. |
| [12] |
USP39-NF34[S].2015:5425
|
| [13] |
陈东平, 盖轲. 以庆化裂解油为原料气相法制备石油磺酸盐[J]. 山东化工, 2015, 44(22): 19. CHEN DP, GAI K. Preparation of petroleum sulfonate by the cracking oil of Qingyang refineery as raw material[J]. Shandong Chem Ind, 2015, 44(22): 19. DOI:10.3969/j.issn.1008-021X.2015.22.006 |
| [14] |
黄晓兰, 吴惠勤, 黄芳, 等. 液相色谱-质谱法测定纺织品和皮革制品中痕量全氟辛烷磺酸盐[J]. 分析化学研究报告, 2007, 35(11): 1591. HUANG XL, WU HQ, HUANG F, et al. Determination of perfluorooctane sulphonate in fabric and leather by liquid chromatography-mass spectrometry[J]. Chin J Anal Chem, 2007, 35(11): 1591. |
| [15] |
王丽娟. 液质联用技术在石油磺酸盐质量控制中的应用[J]. 石油化工应用, 2014, 33(4): 88. WANG LJ. Application of LC-MS technology in quality control of petroleum sulfonate[J]. Petrochem Ind Appl, 2014, 33(4): 88. |
 2018, Vol. 38
2018, Vol. 38 
