维生素B6(C8H10NO5P,VB6)可用于预防和治疗由维生素B6缺乏而引起的疾病,在合成反应过程中会产生氢氰酸。2-噻吩乙酸为鳞片状结晶性粉末,是头孢噻定等药物中间体,在农药、染料等方面也有广泛的应用,但其反应原料中含有氰化物。
氰化物是合成树脂、医药、农药、杀虫剂和化肥等的重要原料,但游离的氰化物是剧毒物质,可通过呼吸道或消化道进入人体,与体内细胞色素氧化酶中的Fe3+结合,从而使细胞不能利用氧,失去传递氧的作用,使机体缺氧死亡[1]。氰化物杂质的含量影响合成药物的安全与质量,因此在制药工业中鉴别、定量控制氰化物的含量十分重要。
氰化物含量测定方法主要有异烟酸-巴比妥酸、异烟酸-吡唑啉酮等分光光度法[2-3]、流动注射分析法[4]、极谱法[5-6]、顶空气相色谱法[7]、荧光法[8-13]。中华人民共和国国家环境保护标准HJ 484-2009[14]和HJ 745-2015[15]国标中规定氰化物的测定方法,在样品的采集与制备过程中需要将氰化物转化为氰化氢,蒸馏出来用碱液吸收,但该过程操作复杂,且操作不当会导致氢氰酸泄露,对人体及环境存在严重的安全隐患;荧光光度法[8]虽然准确度、精密度比较高,操作快速,但是需要配制多种试剂,操作步骤多,系统误差大;近几年发展起来的荧光化学传感器方法[9-11],利用氰离子与荧光物质的特异性化学反应,通过测定荧光物质的荧光性质变化检测氰离子含量,但找到有效表达的荧光传感器分子有一定难度;气相色谱虽然灵敏度高,快速,但需要加入衍生化试剂,常采用的衍生化试剂有氯胺T和次氯酸钠,这2种试剂都容易失效不易保存,且衍生化试剂的使用量对结果也会产生一定的影响;中国药典中氰化物的检查采用普鲁士蓝法或紫外可见-分光光度法[16],前者只能定性,灵敏度欠佳,往往造成漏检,后者的定量需使用极易爆炸的三硝基苯酚或恶臭且致癌的吡啶,危害健康及环境,且操作烦琐费时;美国药典USP 36-NF 31[17]采用普鲁士蓝法来鉴定氰化物的存在,只可定性,不能定量。当氰化物含量极低时,以上几种方法无法准确测定。离子色谱法不仅操作简便快速、灵敏度高[18-19],而且样品前处理简单,可以满足药物中痕量氰化物的检测要求。
氰化物是弱酸根,会与H+结合形成弱电离物质HCN,电导值极低,不适合用电导检测,但利用氰化物有还原性的特点,可使用安培检测器检测。对于环境样品中氰化物的离子色谱检测有过文献报道[20-23],龙素群等[21]建立了安培检测-离子色谱法测定水中的氰化物,检出限为0.05 μg·L-1,但合成药物中痕量氰化物的检测鲜有报道。合成药物是有机物,在纯水中一般难溶,本工作借助甲醇将药物溶解,加入氢氧化钠溶液,通过超声将氰化物尽可能萃取出来,或者直接将合成药溶解在热的氢氧化钠中,然后用离子色谱安培法检测溶液中的氰化物。该方法分析速度快,灵敏度高,前处理简单,不需加入其他衍生化试剂,对操作人员和环境无危害,是一种符合绿色化学的分析手段,对VB6和2-噻吩乙酸(2-TPA)药物中的氰化物进行检测,取得了令人满意的结果。
1 试验部分 1.1 仪器与试剂Dionex 600离子色谱仪,配有安培检测器,Chromeleon 6.8色谱工作站(美国Thermo Fischer公司);50%氢氧化钠为优级纯(德国Merck公司);50 mg·L-1氰标准水溶液(上海市计量测试技术研究院);所有溶液均用电阻率为18.2 MΩ·CM的二次去离子水配制;OnGuard RP前处理柱(上海安谱),0.22 μm一次性过滤头(上海安谱)。
VB6-1、VB6-2、VB6-Y1、VB6-Y2、2-TPA-1、2-TPA-2样品均来自于生产企业。
1.2 色谱条件IonPac AG18阴离子保护柱(50 mm×4 mm,Dionex),IonPac AS18阴离子分析柱(250 mm×4 mm,Dionex);安培检测器;流动相为20 mmol·L-1氢氧化钠溶液,等度淋洗;流速1.0 mL·min-1;进样量为25 μL。
1.3 样品处理根据2种合成药物的不同性质,采用不同的前处理方法。准确称取一定质量的样品(约1 g)于10 mL量瓶中,VB6样品先用少量甲醇溶解,再加入氢氧化钠溶液超声(200 W,40 kHz)、溶解、定容。2-TPA样品直接用热氢氧化钠溶液溶解,超声20 min后,定容。溶液用0.22 μm的尼龙滤膜和OnGuard RP前处理柱处理后,进入离子色谱分析。
2 结果与讨论 2.1 色谱条件的选择 2.1.1 色谱分析柱的考察考察了IonPac AS18和IonPac AS11-HC阴离子分析柱(填料为乙基-乙烯基苯-二乙烯基苯多孔基球,表面覆有阴离子交换涂层)在流速为1.0 mL·min-1,进样量为25 μL的条件下对氰化物分析的影响。由图 1可以看出,在流动相氢氧化钠浓度一定,氰化物浓度一定,流速一定,波形相同的条件下,采用IonPac AS11-HC柱分析氰化物(图 1-A),峰形拖尾,半峰宽过大,峰形对称性差,不适于分析氰化物。而IonPac AS18柱(图 1-B),峰形尖锐且对称,最终选择IonPac AS18柱作为检测氰化物的分析柱。

|
A. IonPac AS11-HC分析柱(CN- with 1.0 mg·L-1 by using IonPac AS11-HC column)B. IonPac AS18分析柱(CN- with 1.0 mg·L-1 by using IonPac AS18 column) 图 1 不同色谱柱对1.0 mg·L-1 CN-的分析效果 Figure 1 Effect of different columns on the analysis of 1.0 mg·L-1 CN- |
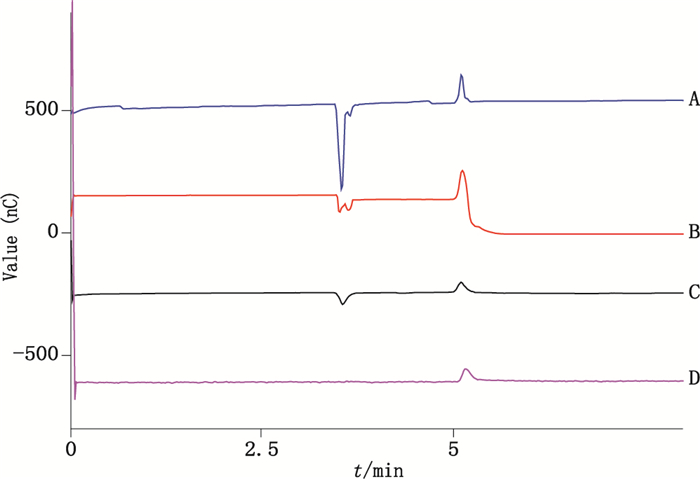
分别考察了a、b、c、d 4种波形电位下的CN-,得到图 2。由图 2可以看出,采用IonPac AS18色谱柱,色谱条件一定(1.0 mL·min-1流速,流动相为20 mmol·L-1氢氧化钠溶液,进样量为25 μL),在4种不同波形下,峰形发生改变。结果表明,采用d(图 2-D)检测波形电位下氰化物的峰面积和峰高都很好,响应值和灵敏度更高,更适合药物中痕量氰化物的检测。综合考虑最终选择d检测波形电位条件。
|
A. a波形(waveform)B. b波形(waveform)C. c波形(waveform)D. d波形(waveform) 图 2 IonPac AS18柱在不同检测波形电位下对1.0 mg·L-1 CN-的色谱图 Figure 2 Chromatograms of different waveforms for the column of IonPac AS18 on the analysis of 1.0 mg·L-1 CN- |
在色谱条件下,对质量浓度为0.20、0.50、1.0、2.0、4.0、8.0、10.0 mg·L-1的CN-标准溶液进行测定,以峰面积Y对离子质量浓度X(mg·L-1)作图,结果表明CN-在0.20~10.0 mg·L-1的浓度范围内呈良好的线性关系,其线性回归方程:
Y=17.92X+0.521 7 r2=0.999 9
根据3倍信噪比计算出CN-的检出下限为1.64 μg·L-1,实际合成药物中CN-的检出下限为0.016 4 μg·g-1。
2.3 精密度试验在优化的色谱条件下,将1.0 mg·L-1的CN-标准溶液连续7次检测,考察保留时间、峰面积的精密度。所得CN-的保留时间、峰面积的RSD分别为0.11%、1.7%、2.0%。结果表明该离子色谱分析方法精密度良好。
2.4 样品测定及加标回收率对合成药物分别按上述方法处理后,在优化的色谱条件下测定,多个VB6及2-TPA合成药物中氰化物的检测结果列于表 1,从结果中可以看出,合成原料和粗产品中都含有一定的氰化物,精制产品中的氰化物非常低,有的甚至因含量低于检出下限(0.016 4 μg·g-1)而未检出。
|
|
表 1 离子色谱法检测样品中的CN-结果 Table 1 The results of CN- in the samples by IC |
为了验证检测结果,采用药典中规定的普鲁士蓝方法进行比较。分别配制0.01、0.03、0.08、0.12、0.18、0.5、1.0、2.0、6.0、10.0 mg·L-1 CN-溶液,依次向溶液中加入新配制10% FeSO4 5滴,5% FeCl3 5滴,100 mmol·L-1 HCl 1 mL,静置30 min,观察现象。结果表明,只有10.0 mg·L-1 CN-溶液才观察到普鲁士蓝现象。将样品制备成溶液,CN-的含量见表 1中第三列,按照普鲁士蓝的方法进行试验,由于浓度太低,均没有观察到普鲁士蓝。这表明离子色谱安培法的检测灵敏度高,检测限低;而普鲁士蓝方法的检出限高,不适用于相关药物中痕量CN-的检测。
为验证方法的准确性,在稀释10倍的VB6-Y1和2-TPA-1样品中,分别加入一定量的标准溶液,在同样的色谱条件下测定加标后氰化物的含量,结果见表 2。CN-的回收率在92.4%~97.9%之间,根据2015年版中国药典的规定,回收率在合理范围内。结果表明离子色谱安培法检测CN-,前处理简单,环保,准确度高,灵敏度高,可以满足实际样品中氰化物的分析需求。
|
|
表 2 氰离子的加标回收率(n=3) Table 2 Recoveries of CN- spiked in the sample |
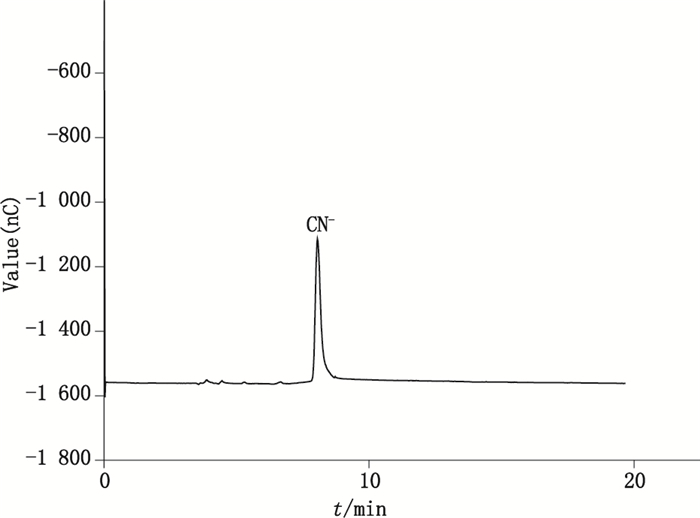
由于强酸无机离子在安培检测条件下不出峰,实际合成药物VB6粗品中氰化物的色谱图见图 3。从图 4中可以看出无杂质峰的干扰,氰化物的峰形合理,响应值高。
|
图 3 VB6-Y1中CN-的色谱图 Figure 3 The chromatogram of CN- inVB6-Y1 |
建立离子色谱积分安培检测法快速测定VB6与2-TPA-1药物中氰化物。药物样品用少量甲醇或氢氧化钠溶液溶解后,经过滤和RP前处理柱处理后,用电化学检测器进行检测,在0.20~10.0 mg·L-1浓度范围内,氰离子具有良好的线性关系。该方法前处理简单,环保,不受其他杂质离子的干扰,灵敏度高,准确度和重复性好,对实际VB6和2-TPA-1合成药物中氰化物的检测结果满意。该方法为基体复杂的合成药物中痕量氰化物的检测提供了一种新的检测思路和方法,对制药工业中残留氰化物含量的监测具有很大的实践意义。但该方法也有需要改进之处,比如,对于高盐,尤其是氯盐含量很高的药物中的氰根检测,需要考虑和研究氯离子对氰根的影响。
| [1] |
王磊, 尹宗杰. 氰化物测定方法的研究进展[J]. 广东化工, 2012, 39(6): 114. WANG L, YIN ZJ. Research advance of cyanide determination methods[J]. Guangdong Chem Ind, 2012, 39(6): 114. |
| [2] |
李悦, 李彦懿, 肖得力. 氰化物定量检测方法应用研究进展[J]. 药物分析杂志, 2016, 36(12): 2075. LI Y, LI YY, XIAO DL. Progress in the application of cyanide quantitative detection[J]. Chin J Pharm Anal, 2016, 36(12): 2075. |
| [3] |
杜传强, 聂磊. 异烟酸-吡唑啉酮比色法测定咖啡因中残留氰化物[J]. 药学研究, 2014, 33(8): 454. DU CQ, NIE L. Determination of cyanide in caffeine by isonicotinic acid-pyrazolone colorimetric method[J]. J Pharm Res, 2014, 33(8): 454. |
| [4] |
王艳春, 王宝旺, 魏玉霞. 白酒中氰化物的流动注射分光光度测定法[J]. 中国医学装备, 2014, 11: 146. WANG YC, WANG BW, WEI YX. Determinaton of cyanide in wine by continuous flow-injection-photometry[J]. China Med Equip, 2014, 11: 146. |
| [5] |
田亚赛, 李晓惠, 刘海军. 异烟酸-巴比妥酸极谱法测定水中痕量氰化物[J]. 分析试验室, 2016, 35(2): 201. TIAN YS, LI XH, LIU HJ. Determination of trace cyanide in water by isonicotinic acid-barbituric acid polarography[J]. Chin J Anal Lab, 2016, 35(2): 201. |
| [6] |
MAHERNIA S, AMANLOU A, KIAEE G, et al. Determination of hydrogen cyanide concentration in mainstream smoke of tobacco products by polarography[J]. J Env Health Sci Engin, 2015, 13(1): 1. DOI:10.1186/s40201-015-0157-3 |
| [7] |
聂融, 马文杰, 刘俊娓. 顶空-气相色谱法测定饮用水中微量氰化物[J]. 疾病预防控通报, 2015, 30(4): 64. NIE R, MA WJ, LIU JW. Determination of trace cyanide in drinking water by headspace gas chrematography[J]. Bull Disease Control Prev, 2015, 30(4): 64. |
| [8] |
李文奇, 白芸. 荧光光度法测定食用酒精中氰化物含量的研究)[J]. 理化检验-化学分册, 2000, 36(2): 49. LI WQ, BAI Y. Study on the fluorospectrophotometry determination of cyanide content in edible alcohol[J]. Phy Testing Chem Anal Part B(Chem Anal), 2000, 36(2): 49. |
| [9] |
BADUGU R, LAKOWICZ JR, GEDDES CD. Cyanide-sensitive fluorescent-probes[J]. Dyes Pigm, 2005, 64(1): 49. DOI:10.1016/j.dyepig.2004.04.002 |
| [10] |
LEE KS, KIM HJ, KIM GH, et al. Fluorescent chemodosimeter for selective detection of cyanide in water[J]. Org Lett, 2008, 10(1): 49. DOI:10.1021/ol7025763 |
| [11] |
CHO DG, KIM JH, SESSLER JL. The benzyl-cyanide reaction and its application to the development of a selective cyanide anion indicator[J]. J Am Chem Soc, 2008, 130(36): 12163. DOI:10.1021/ja8039025 |
| [12] |
CHENG C, CHEN HY, WU CS, et al. A highly sensitive and selective cyanide detection using a gold nanoparticle-based dual fluorescence-colorimetric sensor with a wide concentration range[J]. Sens Actuators B:Chem, 2016, 227: 283. DOI:10.1016/j.snb.2015.12.057 |
| [13] |
ZHOU C, SUN M, YAN C, et al. A new colorimetric and fluorescent chemodosimeter for fastdetection of cyanide[J]. Sens Actuators B:Chem, 2014, 203(1): 382. |
| [14] |
HJ 484-2009水质氰化物的测定: 容量法和分光光度法[S]. 2009: 2 HJ 484-2009 Water Quality-Determination of Cyanide Volumetric and Spectrophotometry Method[S].2009:2 |
| [15] |
HJ 745-2015, 土壤氰化物和总氰化物的测定: 分光光度法)[S]. 2015: 4 HJ 745-2015, Soil-Determination of Cyanide and Total Cyanide Spectrometric Method[S].2015:4 |
| [16] |
中国药典2015年版. 四部[S]. 2015: 附录100 ChP 2015.Vol Ⅳ[S].2015:Appendix 100 |
| [17] |
USP 36-NF 31.Vol Ⅱ[S].2013:1247
|
| [18] |
钱敏, 耿志旺, 彭茗, 等. 离子色谱法测定头孢曲松钠中的钠离子含量以及成盐率[J]. 药物分析杂志, 2015, 35(3): 435. QIAN M, GENG ZW, PENG M, et al. Determination of sodium ion and salt-forming rate in ceftriaxone sodium by ion chromatography[J]. Chin J Pharm Anal, 2015, 35(3): 435. |
| [19] |
刘英, 李茜. 离子色谱在抗生素药物分析中的应用[J]. 药物分析杂志, 2012, 32(1): 179. LIU Y, LI Q. Application of ion chromatography method in analysis of antibiotics[J]. Chin J Pharm Anal, 2012, 32(1): 179. |
| [20] |
CENGIZ MF, DURAK MZ, NILUFER S, et al. Ion chromatographic determination of free cyanide in different classes of bottled natural mineral water consumed in Turkey[J]. Intern J Food Prop, 2015, 18(4): 746. DOI:10.1080/10942912.2014.885044 |
| [21] |
王喜全, 杨蓓德. 离子色谱法测定工业废水中的微量氰化物[J]. 环境工程, 2003, 21(4): 58. WANG XQ, YANG BD. Determiantion of cyanide in waste water with ion chromatography[J]. Environ Eng, 2003, 21(4): 58. |
| [22] |
龙素群, 钟志京, 辉永庆, 等. 水中氰化物的安培检测-离子色谱测定法[J]. 环境与健康杂志, 2009, 26(8): 719. LONG SQ, ZHONG ZJ, HUI YQ, et al. Determination of cyanide in water by ion chromatography with direct amperometric detector[J]. J Environ Health, 2009, 26(8): 719. |
| [23] |
鲁蕴甜. 离子色谱-电化学检测器测定电镀废水中的氰化物[J]. 广州化工, 2014, 42(12): 156. LU YT. Determination of cyanide in plating waste water by ion chromatography with electrochemical detector[J]. Guangzhou Chem Ind, 2014, 42(12): 156. DOI:10.3969/j.issn.1001-9677.2014.12.057 |
 2018, Vol. 38
2018, Vol. 38 
