选择性IgA缺乏症(Selective Immunoglobulin A deficiency,SIgAD)是一种较为常见的原发性免疫缺陷病,占原发性免疫缺陷病的60%以上[1]。当SIgAD患者输入含有微量IgA的人免疫球蛋白类制品后可产生抗IgA的抗体,当再次输入该类制品时可产生严重的过敏反应,甚至危及患者生命,因此,严格控制人免疫球蛋白类生物制品药物中杂质IgA的含量具有积极的临床意义。目前,中国药典所收载的人免疫球蛋白类制品并没有检测IgA含量的要求,国外药典也只是提出采用合适的免疫化学方法,并没有介绍具体的检测方法。据文献报道,IgA含量测定方法有酶联免疫法[2-4]、免疫比浊法[5-7]、琼脂单向免疫扩散法[8]和火箭免疫电泳法等[9-13]多种方法。其中,酶联免疫法(enzyme-linked immunosorbent assay,ELISA)由于其简便、快速、灵敏、精确等优点而被广泛使用。我们以目前人免疫球蛋白类制品中生产量最大、风险性更高的静注人免疫球蛋白(pH 4)为研究对象,建立了可用于该类制品中IgA含量测定的ELISA方法,并应用此方法对来自全国不同企业的22批静注人免疫球蛋白(pH 4)样品中的IgA含量进行了检测。
1 仪器与试剂 1.1 仪器Versa max型酶标仪(美国Molecular Devices公司);隔水式恒温培养箱(上海一恒科学仪器有限公司);移液器(德国Eppendorf公司);Milli-Q超纯水仪(美国密理博公司)。
1.2 试剂IgA ELISA定量检测试剂盒(批号:314873、315630、316809,美国ZeptoMetrix Corporation(ZMC)生产);IgA国际标准品(来源:NIBSC,批号:67/086,规格:每支100 IU);静注人免疫球蛋白(pH 4)分别来自22家企业,每家企业各1批样品,包括山梨醇和麦芽糖2种辅料的处方;水为Milli-Q超纯水制备系统处理的去离子水。
2 方法与结果 2.1 方法建立与验证 2.1.1 标准曲线的建立取国际标准品1支,加水1 mL复溶,浓度为100 IU·mL-1。取复溶后标准品溶液,用试剂盒中稀释液定量稀释制成浓度为1.562 5×10-3、3.125×10-3、6.25×10-3、1.25×10-4、2.5×10-4 IU·mL-1的溶液,按照试剂盒说明书中步骤进行测定。以标准品溶液IgA浓度的对数对其相应的吸收度作直线回归,求得回归方程:
Y=1.668 6X-0.035 97 r=0.996 3
在1.562 5×10-3~2.5×10-4 IU·mL-1浓度范围内,标准品溶液吸收度与IgA浓度的对数呈良好线性。
2.1.2 专属性考察取主成分为IgG1的3种单抗(西妥昔:批号141308;托珠:批号B1017;阿达木:批号49058LX03)原液进行测定。结果3种单抗的吸光度分别为0.006、0.008和0.098,与试剂盒中稀释液吸光度(0.007)接近,说明交叉反应少,该方法的专属性好。
2.1.3 定量限考察取试剂盒中稀释液10份,按照试剂盒说明书中步骤进行测定,计算其吸光度值的均值(X)和标准差(σ)分别为0.050和0.002。以吸光度值均值X+10σ代入标准曲线计算对应的IgA含量作为定量限。计算获得定量限为2.167×10-4 IU。
2.1.4 回收率试验采用加标回收率法,取复溶后标准品溶液分别稀释至3.125×10-3、6.25×10-3和1.25×10-4 IU·mL-1,将供试品溶液也分别稀释至浓度约为3.125×10-3、6.25×10-3和1.25×10-4 IU·mL-1,再将标准品和供试品浓度相当的溶液按体积比1:1进行混合,分别制成3个浓度水平的样加标混合溶液,每个浓度制备3份,按照试剂盒说明书中步骤进行测定。按上述方法,对2种处方的供试品溶液(处方1:批号为20150503Z,辅料为麦芽糖;处方2:批号为201504G007,辅料为山梨醇)分别进行考察。按以下公式:回收率(%)=(加标样品测定浓度×2-供试品测定浓度)/加入的标准品浓度×100%计算回收率,结果见表 1。处方1和处方2样品不同浓度水平的平均加样回收率(n=9)分别为102.2%和98.5%。结果表明该方法受样品基质影响小,能够准确测定静注人免疫球蛋白(pH4)中IgA的含量。
|
|
表 1 回收率测定结果 Table 1 Determination results of recoveries |
取“2.1.4”项下加标混合溶液进行重复性考察,结果见表 2,不同处方样品低、中、高3个浓度水平测定值的RSD(n=3)均小于10%,表明该方法重复性好。
|
|
表 2 重复性测定结果 Table 2 Determination results of repeatability |
取供试品溶液(批号201504G007),由2名分析人员在不同日期分别进行测定,每人每次测定3份,结果详见表 3,RSD < 10%(n=18),表明该方法中间精密度好。
|
|
表 3 中间精密度测定结果 Table 3 Determination results of intermediate precision |
为了考察试剂盒的批间一致性,选取低、中、高浓度供试品各1批,分别采用2个批号的试剂盒进行测定,每批样品重复测定3份,结果详见表 4。结果显示低、中、高浓度的供试品采用不同批号试剂盒检测时测定值的RSD均小于10%(n=6),表明方法的耐用性良好。
|
|
表 4 不同浓度样品采用不同批号试剂盒检测的测定结果 Table 4 Determination results of samples at different concentration using ELISA kits with different batch numbers |
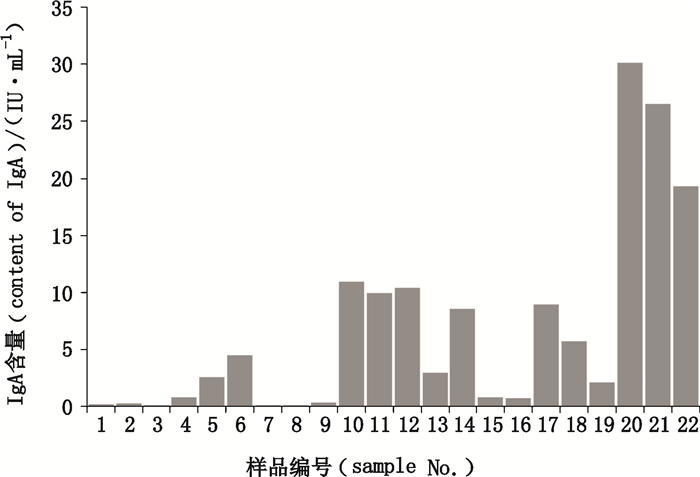
取来自不同企业的22批静注人免疫球蛋白(pH 4)样品,用试剂盒中稀释液定量稀释制成适当浓度,使IgA含量在标准曲线范围内,采用上述经验证的方法进行测定,结果见表 5和图 1。根据测定结果可以发现,大多数企业生产的静注人免疫球蛋白(pH 4)中IgA含量在10 IU·mL-1以下,但是也有个别企业达到甚至超过了14.1 IU·mL-1(目前国外产品中的最高限度),且具备纯化步骤的生产工艺所生产的样品IgA含量明显低于未经纯化的样品测定值(表 5中厂家1~9生产工艺具备纯化步骤,其他厂家生产工艺均无纯化步骤)。
|
图 1 22批样品中IgA含量 Figure 1 Content of IgA in 22 samples |
|
|
表 5 22批样品信息及测定结果 Table 5 The batch numbers and the determination results of 22 samples |
目前市场上有很多种人IgA含量检测试剂盒,根据其说明书主要适用于人血清、血浆、尿液和脑脊液等液体中IgA含量的测定,该类试剂盒是否适用于人免疫球蛋白类制品中IgA含量的测定尚未见相关报道。因此,要保证测定结果的准确性,首先必须选择合适的试剂盒。在建立本法的初期,我们对包括ZMC厂家在内的国内外3种试剂盒进行了比较和筛选,发现其中一个试剂盒线性较差,样品稀释液本底高,且复孔间的重复性差;另一个试剂盒受样品基质影响较严重;而ZMC厂家的试剂盒较适用于本法测定(本文未显示相关结果)。为降低检测成本和考虑试剂盒长期供应性的问题,建议其他实验室也可以考虑筛选出性能相当的试剂盒,考量指标主要从标准曲线的线性、空白背景值的大小、样品的基质效应、专属性、复孔间的精密度等方面来评价。同时鉴于ZMC厂家的试剂盒为研究用试剂盒,其中自带的标准品无明确的量值溯源,因此在建立本法时我们采用了NIBSC来源的国际标准品。国际标准品目前仅标示了效价单位,在使用中可按1 IU相当于14.2 μg将样品测定结果换算成质量单位[14]。本研究的方法学验证结果显示,本法灵敏度高,专属性好,不同处方样品不同浓度水平的平均加标回收率均在80%~120%范围内,重复性及中间精密度RSD均小于10%,试剂盒的批间一致性也较好,能满足ELISA分析方法的基本要求。
通过对全国22家企业的静注人免疫球蛋白(pH 4)样品的IgA含量进行检测发现,大部分企业生产的静注人免疫球蛋白(pH 4)的IgA含量较低(< 10 IU·mL-1),但是也有少数企业生产的产品中IgA含量超过了国外同类产品的最高限度。分析可能与各企业的生产工艺有关,具有纯化工艺(层析)的企业生产的产品IgA含量相对要低一些。因此,为了控制该类制品中IgA的含量,建议一些生产企业在生产工艺中增加纯化步骤。另外,本研究中系用静注人免疫球蛋白(pH 4)样品作为研究对象,若要将该法应用于其他人免疫球蛋白类制品的IgA含量测定,尚需进行相应的方法学验证。
本研究建立的人免疫球蛋白类制品中IgA含量ELISA检测方法灵敏度高,专属性强,线性范围宽,操作简单,适合大量样品的批量分析,不仅满足了对人免疫球蛋白类制品质量控制的需要,也为更好地区分不同工艺生产的产品差异,以便提高产品质量奠定了基础。
| [1] |
沈迪, 邹萍. 内科免疫学[M]. 武汉: 湖北科学技术出版社, 1998, 61. SHEN D, ZOU P. Immunology[M]. Wuhan: Hubei Publishers of Science and Technology, 1998, 61. |
| [2] |
PEEBLES R, STOKES J, LIU MC, et al. IgA, IgG and IgM quantification in bronchoalveolar lavage fluids from allergic rhinitics, allergicasthmatics, and normal subjects by monoclonal antibody-based immunoenzymetric assays[J]. J Immunol Methods, 1995, 179(1): 77. DOI:10.1016/0022-1759(94)00275-2 |
| [3] |
BIANCHI ATJ, MOONEN-LEUSEN HWM, VANDERHEIJDEN PJ, et al. The use of a double antibody sandwich ELISA and monoclonal antibodies for the assessment of porcine IgM, IgG and IgA concentrations[J]. Vet Immunol Immunopathol, 1995, 44(3-4): 309. DOI:10.1016/0165-2427(94)05307-E |
| [4] |
HIZURU N, MAIKO Y, YUKI K, et al. A flow-based enzyme-linked immunosorbent assay on a polydimethylsiloxane microchip for the rapid determination of immunoglobulin A[J]. Talanta, 2006, 70(1): 122. DOI:10.1016/j.talanta.2005.12.059 |
| [5] |
汪敬武, 王兆喜, 杨伟平. 流动注射免疫比浊法测定血清中免疫球蛋白A[J]. 分析化学, 2004, 32(6): 724. WANG JW, WANG ZX, YANG WP. Determination of immunoglobulin A in human serum by flow injection-turbidimetry[J]. Chin J Anal Chem, 2004, 32(6): 724. |
| [6] |
梁爱惠, 王娜, 侯明. IgA免疫复合物微粒的共振散射光谱研究及其分析应用[J]. 光谱学与光谱分析, 2007, 27(11): 2325. LIANG AH, WANG N, HOU M. Resonance scattering spectral study of IgA immune complex particlesand its analytical application[J]. Spectrosc Spect Anal, 2007, 27(11): 2325. |
| [7] |
王世平. 微量免疫比浊法测定血清免疫球蛋白、转铁蛋白和载脂蛋白含量[J]. 中国运动医学杂志, 2001, 20(4): 392. WANG SP. Determination of immunoglobulins, transferring and apolipoproteins by turbidimetric immunoassay[J]. Chin J Sports Med, 2001, 20(4): 392. |
| [8] |
常玉荣, 石俊, 殷华, 等. 透射比浊法与单向琼脂扩散法检测血清免疫球蛋白的比较和分析[J]. 中国煤炭工业医学杂志, 2004, 7(12): 1209. CHANG YR, SHI J, YIN H, et al. Comparison of methods between transmission turbidimetry and one-way agar diffusion for the detection of serum immunoglobulin[J]. Chin J Coal Industry Med, 2004, 7(12): 1209. DOI:10.3969/j.issn.1007-9564.2004.12.063 |
| [9] |
刘德生. 火箭免疫电泳测定免疫球蛋白及补体C3方法的改进[J]. 武汉医学院学报, 1985, 14(3): 206. LIU DS. Improvement of the method of RIE determination of immunoglobulin and complement C3[J]. J Wuhan Med, 1985, 14(3): 206. |
| [10] |
吴佩, 姚建, 王伟铭, 等. 血清IgA-纤连蛋白聚合物的测定及其对IgA肾病的临床意义[J]. 中国实验诊断学, 1997, 1(4): 16. WU P, YAO J, WANG WM, et al. Determination of serum fibronectin IgA-polymer and its clinical significance in patients with IgA nephropathy[J]. Chin J Lab Diagn, 1997, 1(4): 16. |
| [11] |
SWART RL, VOS HW, UYTDEHAAG FGCM, et al. Measles virus fusion protein and hemagglutinin-transfected cell lines are a sensitive tool for the detection of specific antibodies by an FACS-measured immunofluorescence assay[J]. J Virol Methods, 1998, 71(1): 35. DOI:10.1016/S0166-0934(97)00188-2 |
| [12] |
蒋治良, 王娜, 梁爱惠. 免疫纳米金共振散射光谱探针检测痕量免疫球蛋白A[J]. 化学学报, 2008, 66(9): 1047. JIANG ZL, WANG N, LIANG AH. Immunonanogold resonance scattering spectral probe for assay of trace IgA[J]. Acta Chim Sin, 2008, 66(9): 1047. |
| [13] |
向知峰, 楚霞. 基于纳米金标记的阳极溶出伏安免疫分析用于免疫球蛋白A的测定[J]. 化学传感器, 2005, 25(2): 57. XIANG ZF, CHU X. Anodic stripping immunoassay based on gold label for the determination of immunoglobulin A[J]. Chem Sensors, 2005, 25(2): 57. |
| [14] |
ROWE DS, GRAB B, ANDERSEN SG. An international reference preparation for human serum immunoglobulins G, A and M content of immunoglobulins by weight[J]. Bull World Health Organ, 1972, 46(1): 67. |
 2018, Vol. 38
2018, Vol. 38 
