2. 中国药科大学, 南京 211198
2. China Pharmaceutical University, Nanjing 21198, China
替格瑞洛一种新型具有选择性的治疗急性冠状动脉综合征(acute coronary syndrome,ACS)的小分子抗凝血药物[1],该药物属于新型环戊基三唑嘧啶类(cyclopentyl triazole,CPTP)可逆性[2]P2Y12受体拮抗剂[3],通过抑制新血凝块的形成[4],有效抑制动脉粥样化血栓的形成。美国心脏病学院基金会和美国心脏协会已经将替格瑞洛作为重要的抗血小板药物推荐应用[5]。
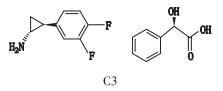
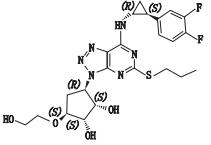
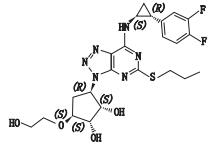
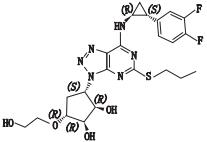
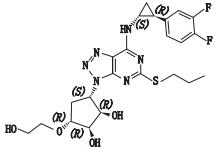
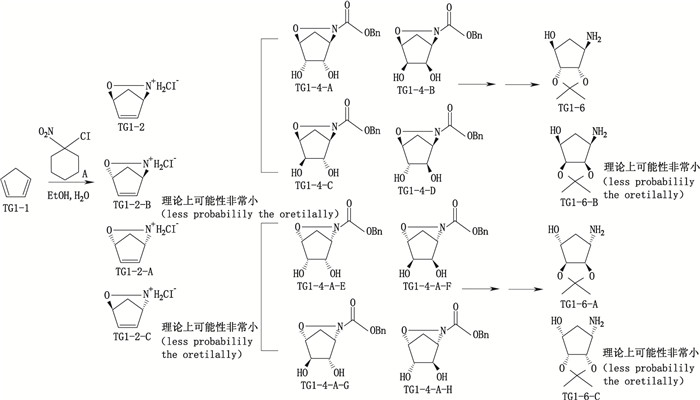
替格瑞洛的分子结构式见表 1,化学名为(1S,2S,3R,5S)-3-[7-{[(1R,2S)-2-(3,4-二氟苯基)环丙基]氨基}-5-(丙硫基)-3H-[1, 2, 3]三唑并[4,5-d]嘧啶-3-基]-5-(2-羟乙氧基)环戊烷-1,2-二醇,由C5部分(含4个手性中心)与C3(含2个手性中心)构成。C5中异构体产生的机理如图 1所示,从理论上分析,最后可能存在于C5成品中的异构体只有其对映异构体。
|
|
表 1 替格瑞洛及其相关异构体的化学结构式 Table 1 Chemical structural formula of the ticagrelor and related isomers |
|
图 1 C5的对映异构体产生机理 Figure 1 Mechanism of production of C5's enantiomers |
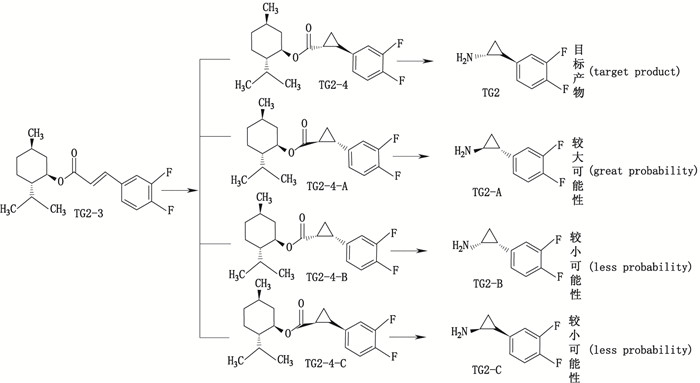
C3中异构体产生的机理如图 2所示,从理论上分析,最后可能存在于C3成品中的异构体只有其对映异构体。
|
图 2 C3的对映异构体产生机理 Figure 2 Mechanism of production of C3's enantiomers |
综上所述,虽然替格瑞洛从分子结构上分析含有6个手性中心,但其手性中心来自C5和C3,而C5和C3中只有可能存在其各自的对映异构体,纳入错误的C3对映异构体或C5对映异构体才可能会导致产生替格瑞洛异构体,即非对映异构体Ⅰ、非对映异构体Ⅱ、对映异构体,见表 1。药物对映体在体内多数情况下,会呈现出明显的差异,这种差异性主要表现在代谢途径、药理活性以及毒副作用等许多方面。主要包括以下4种情况:对映体之一具有活性,另外一种无显著的药理作用;对映体之一有活性,另外一种具有等同或者相近的药理活性;2个对映体具有完全不同的生理活性;对映体之一有活性,另外一个不但没有活性,反而有很强的毒副作用或者拮抗作用[6]。因此,建立灵敏度高、专属性好的手性分析方法对控制本品的质量具有重要意义[7]。替格瑞洛与异构体的分离属于手性拆分,手性拆分的方法包括直接结晶拆分法、化学拆分法、动力学拆分法(包括酶拆分法[8])、色谱拆分法以及手性膜拆分法[9]。近年来色谱拆分的方法应用越来越广泛,主要包括液相色谱法[10]、毛细管电泳色谱法[11]、超临界流体色谱法[12]、薄层色谱法[8, 13]等。应用于手性化合物分离的正相高效液相色谱已成为异构体拆分的重要手段之一[9]。因此,本文建立了用于手性拆分的正相高效液相色谱法对替格瑞洛中的异构体进行分离,并进行了详细的方法学验证。
1 仪器与试药仪器:岛津LC-20A高效液相色谱仪;试药及试剂:替格瑞洛(TG7-140401R,纯度99.9%;自制);非对映异构体Ⅰ(TG-Isomer1-20131125,纯度98.67%;自制);非对映异构体Ⅱ(TG-Isomer2-20140228S7D005,纯度99.8%;自制);对映异构体(TG-E-20131125,纯度98.68%;自制);正己烷(色谱级,美国TEDIA);批号13100080);无水乙醇(色谱级;美国ROE;批号2H1472);异丙醇(色谱级;阿拉丁);三氟乙酸(色谱级;阿拉丁)。
2 方法与结果 2.1 色谱条件色谱柱:硅胶表面涂布直链淀粉-三(3,5-二甲苯基氨基甲酸酯)为填充剂的手性色谱柱(250 mm×4.6 mm,5 μm,推荐使用Chiralpak AD-H色谱柱或同等效力色谱柱);流动相:正己烷-无水乙醇-异丙醇-三氟乙酸(90:5:5:0.1);流速:1.0 mL·min-1;柱温:40 ℃;检测波长:245 nm;进样体积:10 μL。
2.2 专属性与系统适用性试验取非对映异构体Ⅰ、非对映异构体Ⅱ、对映异构体、替格瑞洛各适量,分别用无水乙醇配制成各杂质的储备液,即得各杂质的定位溶液。称取替格瑞洛样品约25 mg,置25 mL量瓶中,分别加入适量非对映异构体Ⅰ、非对映异构体Ⅱ及对映异构体储备液,加无水乙醇稀释至刻度,摇匀,作为系统分离度考察溶液。
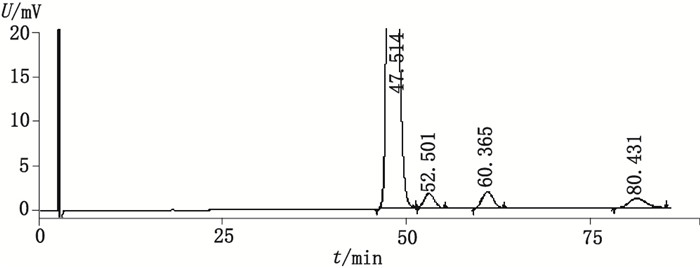
分别量取无水乙醇(空白溶剂)、各杂质储备液及系统分离度考察溶液各10μL,注入液相色谱仪,记录色谱图,见图 1。由色谱图可知,空白溶剂不干扰主峰和异构体的测定且各异构体峰和主峰均能有效分离。
|
图 1 替格瑞洛与异构体分离情况色谱图 Figure 1 Chromatogram of the ticagrelor and its isomers on the base of their separation |
取“2.2”项下的系统分离度考察溶液,连续进样6针,考察该条件下的进样精密度。结果替格瑞洛及各异构体的峰面积RSD符合要求,表明进样精密度良好。
2.4 耐用性试验取“2.2”项下的系统分离度考察溶液,在一定范围内改变乙醇的浓度、检测波长、流速及柱温,考察色谱条件的改变对系统适应性的影响。结果显示异构体检查色谱条件的细微变化,对系统分离度考察溶液的分离度、各峰的柱效、保留时间等无显著影响。
2.5 定量限与检测限分别取替格瑞洛及各异构体杂质适量,精密称定,加无水乙醇溶解并逐级稀释成合适浓度的溶液,精密量取10 μL,注入液相色谱仪,记录色谱图,按信噪比S/N=10确立为定量限,S/N=3确立为检测限。替格瑞洛、非对映异构体Ⅰ、非对映异构体Ⅱ及对映异构体的定量限分别为:0.21、0.49、0.26、0.38 μg·mL-1;检测限分别为:0.053、0.024、0.07、0.01 μg·mL-1;并将各定量限溶液连续进样6针,其各峰面积RSD为2.2%、3.3%、0.85%、1.5%,说明定量限溶液的进样精密度良好。
2.6 线性和范围分别量取替格瑞洛及各异构体杂质储备液系列体积,置相应体积的量瓶中,分别加无水乙醇稀释至刻度,摇匀,配制成6个浓度的线性溶液,分别量取各待测液10 μL注入液相色谱仪,记录色谱图,以浓度(X,μg·mL-1)为横坐标轴,峰面积Y为纵坐标轴,作线性回归,并计算校正因子,结果见表 2。由此说明,替格瑞洛、非对映异构体Ⅱ、非对映异构体Ⅰ及对映异构体在相应的线性范围内,线性关系均良好;以替格瑞洛为参照,各异构体的校正因子均在0.9~1.1之间,故采用不加校正因子的峰面积归一化法。
|
|
表 2 替格瑞洛及其异构体的线性结果 Table 2 Linear results of ticagrelor and its isomers |
称取替格瑞洛约10 mg,置10 mL量瓶中,加无水乙醇溶解并稀至刻度,摇匀,作为供试品溶液,平行配制6份。在替格瑞洛异构体检查的色谱条件下,精密量取供试品溶液10 μL,注入液相色谱仪,记录数据图谱。结果6份供试品中均未检出异构体。
2.8 加样回收率分别取替格瑞洛各异构体适量于同一量瓶中,定容,即得杂质混合储备液。取本品9份,各约10 mg,精密称定,置10 mL量瓶中,分成3组,分别加异构体混合储备液适量,用无水乙醇溶解并稀释至刻度,摇匀,配成含各异构体0.05%、0.1%、0.15%的加样回收率溶液,在替格瑞洛异构体检查的色谱条件下进样,采集数据图谱,按峰面积归一化法计算各异构体的测得量,根据测得量减去原有量与加入量的比值,计算回收率;结果表明在供试品中加入各杂质,非对映异构体Ⅰ、非对映异构体Ⅱ及对映异构体回收率分别为99.1%、100.5%、101.4%,RSD分别为1.5%、1.6%、1.3%,均符合标准,说明该方法准确度良好。
2.8 溶液稳定性取本品约10 mg,置10 mL量瓶中,加无水乙醇溶解并稀释至刻度,摇匀,于室温室内散光条件下放置,分别于0、2、4、6、8 h精密量取溶液10 μL,在异构体检查的色谱条件下,注入液相色谱仪,记录数据图谱,实验数据显示溶液在8 h内其主峰峰面积RSD为0.1%,且没有异构体峰出现,表明在8 h内供试品溶液稳定。
3 讨论 3.1 色谱柱的选择替格瑞洛与异构体的分离属于手性拆分,在HPLC中拆分对映体时通常有3种方法:①利用手性试剂与被拆分物进行衍生化反应生成非对映异构体,从而可被传统的非手性HPLC所拆分;②在流动相中加入手性添加剂,利用非手性固定相HPLC进行拆分;③利用手性固定相的HPLC进行拆分。其中最有效的方法是手性固定相法[9],于海云等[14]利用手性固定相对焦谷氨酸对映异构体实现分离;赵静等[15]利用手性固定相正相高效液相色谱法拆分了普萘洛尔对映体;韩小茜等[16]利用纤维素-三(3,5-二甲基苯基氨基甲酸酯)手性固定相高效液相色谱法使氟环唑外消旋体得到分离,因此在替格瑞洛异构体分离时采用硅胶表面涂布直链淀粉-三(3,5-二甲苯基氨基甲酸酯)为填充剂的Chiralpak AD-H色谱柱,在分离时,异构体与手性固定相会生成不稳定的复合物,使之在色谱柱的保留时间不同,从而实现分离。
3.2 流动相的选择由于采用正相色谱,流动相一般采用非极性的溶剂(如己烷、庚烷等烃类溶剂)加入少量极性调节剂溶剂(如乙腈、三乙胺、三氟乙酸等),以调节流动相的洗脱强度,同时由于这些调节剂极性较强,随流动相进入色谱柱后,可立即占据固定相表面的活性位点形成均匀吸附面,从而提高样品的保留重现性,进而使色谱峰形得到改善[17],所以在替格瑞洛异构体检测时,同时考虑替格瑞洛的分子结构,其结构中含有-OH,选择加入三氟乙酸作为调节剂,流动相采用正己烷-无水乙醇-异丙醇-三氟乙酸的混合溶剂系统。
3.3 三氟乙酸含量的优化在替格瑞洛异构体检测中,考察流动相中调节剂的含量对色谱峰的影响,调节三氟乙酸的含量分别为0.05%、0.1%、0.15%、0.2%、0.3%,结果表明在三氟乙酸含量为0.05%时,色谱峰拖尾严重,峰形扁塌,增加三氟乙酸至0.1%,色谱峰不再拖尾,峰形良好,继续增加三氟乙酸含量,色谱峰无明显变化,峰形依旧良好,所以在替格瑞洛异构体检查中将流动相中三氟乙酸的含量设置为0.1%。
3.4 检测波长通过对替格瑞洛、非对映异构体Ⅰ、非对映异构体Ⅱ、对映异构体进行紫外全波长扫描,结果显示在245 nm处,4种成分的吸收度及响应灵敏度均良好,因此将检测波长设定为245 nm。
3.5 柱温的优化以正己烷-无水乙醇-异丙醇-三氟乙酸(90:5:5:0.1)为流动相,在流速1.0 mL·min-1的条件下,测定在25、30、35、40、45下替格瑞洛与异构体的分离,结果表明在40 ℃条件下,色谱峰的分离度、灵敏度及峰形良好。因此将40 ℃设置为检测温度。
| [1] |
缪世峰, 蔺宇, 张海波, 等. 新型抗凝血药替格瑞洛的合成[J]. 海峡药学, 2015, 27(4): 249. MIAO SF, LIN Y, ZHANG HB, et al. Synthesis of novel anticoagulant ticagrelor[J]. Strait Pharm J, 2015, 27(4): 249. |
| [2] |
ZHANG H, LIU J, ZHANG LY, et al. Synthesis and biological evaluation of ticagrelor derivatives as novel antiplatelet agents[J]. Bioorg Med Chem Lett, 2012(22): 3598. |
| [3] |
李慕鹏, 熊艳, 陈小平. 抗血小板药物替格瑞洛药代药效动力学及遗传药理学研究进展[J]. 中国临床药理学与治疗学, 2014, 19(2): 214. LI MP, XIONG Y, CHEN XP. Research progress in pharmacodynamics and pharmacogenetics of antiplatelet Ticagrelor[J]. Chin J Clin Pharmacol Ther, 2014, 19(2): 214. |
| [4] |
王仙, 朱慧, 胡燕, 等. 抗血小板聚集新药-替格瑞洛[J]. 医院药学杂志, 2013, 33(11): 900. WANG X, ZHU H, HU Y, et al. The novel antiplatelet drug-Ticagrelor[J]. Chin Hosp Pharm J, 2013, 33(11): 900. |
| [5] |
马文涛, 颜红兵. 新型的口服抗血小板药物替格瑞洛[J]. 中华老年心脑血管病杂, 2012, 14(11): 1217. MA WT, TAN HB. Novel oral antiplatelet drug-Ticagrelor[J]. Chin J Geriatr Heart Brain Vessel Dis, 2012, 14(11): 1217. DOI:10.3969/j.issn.1009-0126.2012.11.029 |
| [6] |
张金彦, 吉绍长. 药物的手性拆分[J]. 化学通报, 2013, 76(8): 725. ZHANG JY, JI SC. Chiral separation of medicines[J]. Chem Bull, 2013, 76(8): 725. |
| [7] |
杨庆云, 王志鹏, 邓愉凤, 等. 正相高效液相色谱法拆分普拉克索对映异构[J]. 药物分析杂志, 2014, 34(11): 2005. YANG QY, WANG ZP, DENG YF, et al. Chiral separation of pramipexole enantiomers by normal phase high performance liquid chromatography[J]. Chin J Pharm Anal, 2014, 34(11): 2005. |
| [8] |
苏镜娱, 郑义森. 对映异构体光学拆分法的进展[J]. 药学学报, 1985, 20(9): 710. SU JY, ZHENG YS. Enantiomer progress of optical resolution method[J]. Acta Pharm Sin, 1985, 20(9): 710. |
| [9] |
黄蓓, 杨立荣, 吴坚平. 手性拆分技术的工业应用[J]. 化工进展, 2002, 21(6): 375. HUANG B, YANG LR, WU JP. Chiral resolution techniques in industrial practice[J]. Chem Ind Eng Prog, 2002, 21(6): 375. |
| [10] |
翁文, 姚碧霞, 陈秀琴, 等. 液相色谱手性拆分机理的热力学方法研究[J]. 化学进展, 2006, 18(7/8): 1056. WENG W, YAO BX, CHEN XQ, et al. Thermodynamic studies on mechanism of chiral resolution by liquid chromatography[J]. Prog Chem, 2006, 18(7/8): 1056. |
| [11] |
朱晓峰, 林炳承. 毛细管电泳的手性拆分[J]. 色谱, 1999, 17(2): 153. ZHU XF, LIN RC. Chiral resolution of capillary electrophoresis[J]. Chin J Chromgr, 1999, 17(2): 153. |
| [12] |
李根荣, 李志良. 手性药物拆分技术研究进展[J]. 中国新药杂志, 2005, 14(8): 969. LI GR, LI ZL. Advances in the chiral drug resolutions[J]. Chin J New Drugs, 2005, 14(8): 969. |
| [13] |
王林. 对映异构体的薄层色谱直接拆分法[J]. 国外医学药学分册, 1992, 19(4): 205. WANG L. Enantiomorphism isomers TLC separation method directly[J]. Foreign Med Sci Sec Pharm, 1992, 19(4): 205. |
| [14] |
于海云, 宋俊梅, 陈志从. 利用手性固定相高效液相色谱法对焦谷氨酸对映异构体的分离[J]. 中国现代药物应用, 2011, 5(21): 83. YU HY, SONG JM, CHEN ZC. The separation of glutamic acid enantiomorphism isomers by chiral stationary phase high performance liquid chromatography[J]. Chin J Mod Drug Appl, 2011, 5(21): 83. DOI:10.3969/j.issn.1673-9523.2011.21.075 |
| [15] |
赵静, 邹卫, 赵华, 等. 手性固定相正相高效液相色谱法拆分普萘洛尔对映体[J]. 光谱实验室, 2011, 28(1): 7. ZHAO J, ZOU W, ZHAO H, et al. The separation of propranolol enantiomers by Chiral stationary phase normal high performance liquid chromatography[J]. Chin J Spectr Lab, 2011, 28(1): 7. |
| [16] |
韩小茜, 魏燕, 刘艳华, 等. 氟环唑外消旋体在纤维素-三(3, 5-二甲基苯基氨基甲酸酯)手性固定相上的高效液相色谱法拆分[J]. 色谱, 2008, 9: 631. HAN XQ, WEI Y, LIU YH, et al. Chiral separation of racemic epoxiconazoleon cellulose tris (3, 5-dimethyl phenyl carbamate) chiral stationary phase using high performance liquid chromatography[J]. Chin J Chromgr, 2008, 9: 631. DOI:10.3321/j.issn:1000-8713.2008.05.021 |
| [17] |
丁黎. 药物色谱分析[M]. 北京: 人民卫生出版社, 2008, 162. DING L. Chromatographic Analysis of Drugs[M]. Beijing: People's Medical Publishing House, 2008, 162. |
 2017, Vol. 37
2017, Vol. 37