苯丙哌林(benproperine)为非成瘾性镇咳药。能抑制咳嗽中枢,也能抑制肺及胸膜牵张感受器引起的肺-迷走神经反射,且有平滑肌解痉作用,是中枢性和末梢性双重作用的强效镇咳药,其镇咳作用比可待因强[1-3]。该药目前在我国使用广泛,但至今尚无有关苯丙哌林杂质NMR谱的数据报道,现有文献[3-8]多是使用液相进行有关物质或含量测定的研究。本文首次通过HPLC-MS/MS及NMR对苯丙哌林原料药中的2个未知杂质进行了分析,确定杂质为杂质A:1-[2-(2-苯甲酰基苯氧基)-1-甲基乙基]哌啶;杂质B:1-[2-(2-苄基-6-氯苯氧基)-1-甲基乙基]哌啶,结构式见图 1。并对两杂质的1H-NMR和13C-NMR谱进行了全归属,确定其结构,为该药杂质的结构解析提供了NMR数据,对该药的质量研究和应用具有指导意义。
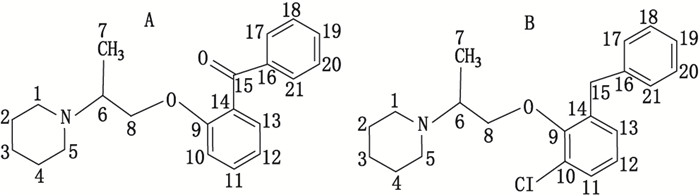
|
图 1 苯丙哌林中杂质A(A)和杂质B(B)结构式 Figure 1 Structure of impurity A(A) and B(B) in benproperine |
Bruker 400核磁共振仪;Thermofisher TSQ Quantum Discovery MAX质谱仪,配有ESI离子源;Thermofisher U3000型高效液相色谱仪。
甲醇、冰醋酸、乙酸铵均为色谱纯,购自默克公司;氘代甲醇购自CIL公司;水为实验室自制超纯水;磷酸苯丙哌林原料药由厂家提供;磷酸苯丙哌林对照品(批号100237-201303)购自中国食品药品检定研究院。
2 实验条件[3, 12-14]色谱柱:Inertsil ODS-3(十八烷基硅烷键合硅胶,4.6 μm,2.1 mm×150 mm,迪马公司);流动相:甲醇-0.01 mol·L-1醋酸铵缓冲液(取醋酸铵0.77 g,加水800 mL溶解,用冰醋酸调节pH至3.3,用水稀释至1 000 mL)(65:35);流速:0.25 mL·min-1;检测波长:270 nm;进样量:10 μL。
离子源:ESI源;电压:4.3 kV;鞘气(N2):25 arb;辅助气(N2):5 arb;碰撞气(Ar):1.5 mTorr;离子传输毛细管温度:350 ℃;采用全扫描一级质谱及全扫描二级质谱同时测定。
核磁共振仪器1H-NMR的工作频率为400 MHz,13C-NMR工作频率为100 MHz,氘代甲醇为溶剂。进行1H-NMR、13C-NMR、HMBC、HSQC、DEPT135和H-H COSY的扫描。
3 样品处理方法 3.1 HPLC-MS/MS分析样品溶液的制备称取苯丙哌林原料药40 mg,置10 mL量瓶中,用50%甲醇溶液溶解并定容至刻度,混匀即得。
3.2 NMR分析样品溶液的制备称取苯丙哌林原料药15 g,置100 mL量瓶中,用甲醇溶解并稀释至刻度,使用制备液相对未知杂质进行分离及纯化,40 ℃旋转蒸发至近干,2 mL水复溶后使用十八烷基键合硅胶为填充剂的固相萃取柱进行脱盐,脱盐后样品40 ℃旋转蒸发至近干,室温条件下减压干燥过夜,使用0.5 mL氘代甲醇复溶。
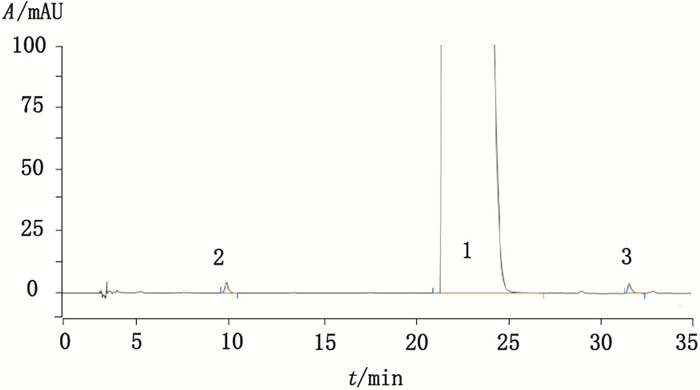
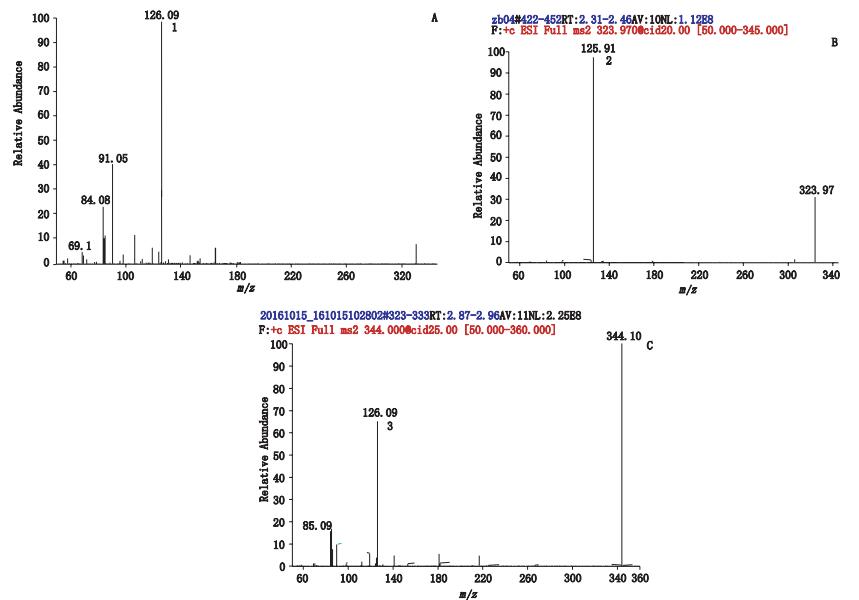
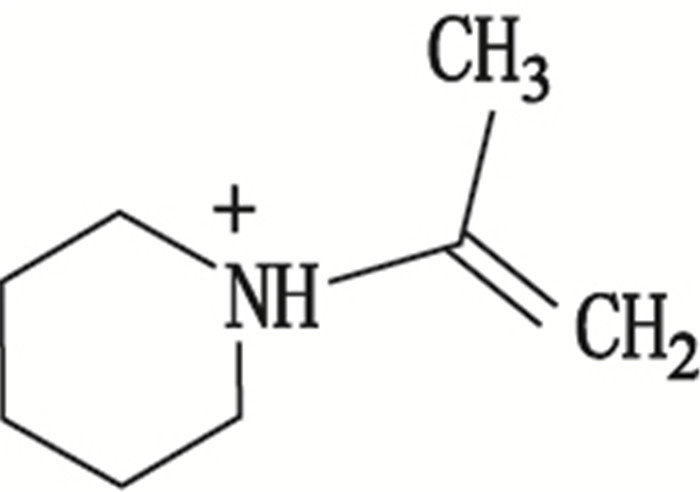
4 结果 4.1 HPLC-MS/MS分析在苯丙哌林的色谱图中,可确定其含有2个明显杂质,见图 2。通过液相质谱联用得全扫描一级质谱图及全扫描二级质谱图见图 3。1、2与3号峰的一级全扫描质谱图均出现[M+H]+,其m/z分别为310、324和344。全扫描二级质谱图中均出现m/z为126的产物离子。由于三者含有相同的产物离子,推测两未知杂质均为苯丙哌林的同系物。相同产物离子碎片结构式图 4。
|
1.苯丙哌林(benproperine)2.杂质A(impurity A)3.杂质B(impurity B) 图 2 苯丙哌林样品的HPLC色谱图 Figure 2 HPLC chromatogram of benproperine sample |
|
1.苯丙哌林(benproperine)2.杂质A(impurity A)3.杂质B(impurity B) 图 3 苯丙哌林(A)、杂质A(B)及杂质B(C)的LC-MS全扫描二级质谱图 Figure 3 ESI-MS/MS spectra of benproperine(A)、impurity A(B) and impurity B(C) |
|
图 4 二级质谱产物离子碎片结构式 Figure 4 Structure of the same product-ion of benproperine and impurities in benproperine |
杂质A(2号色谱峰)一级质谱质核比与苯丙哌林相差14,与苯丙哌林二级质谱相比,其二级质谱图中不存在m/z为91的卓鎓离子,推测杂质A为苯丙哌林苯环区连接两苯环的15位碳由亚甲基变为羰基。
4.1.2 杂质B质谱分析杂质B(3号色谱峰)一级质谱质核比与苯丙哌林相差34,同时杂质B一级质谱图中存在m/z为344与346 2个较强峰,m/z 344的离子强度为100,m/z 346的离子强度为34,满足含1个氯元素化合物的同位素峰3:1的特征,怀疑杂质B苯环存在1个氯取代的情况。由于杂质B二级质谱图存在m/z为91的卓鎓离子,说明苯环区连接两苯环的15位碳亚甲基无变化,推测氯取代在中间的苯环上而非端基苯环上,但氯取代的具体位置无法确定,需进一步进行核磁波谱分析,以确定氯取代的位置。
4.2 NMR分析[9]结合苯丙哌林的核磁谱及文献报道[10],苯丙哌林含有21个碳,其中含有3个季碳及1个手性碳。通过13C谱及DEPT135谱可知,两个杂质分别含有21个碳,均含有4个季碳。其中杂质A含有δC 198.95的季碳,结合质谱结果,确定其为15位羰基碳。杂质B中第4个季碳与11和12位氢相关,与15位氢无相关,确定其为苯环上10位的氢被氯取代。分别对杂质A和杂质B的1H和13C数据作完全的归属。
杂质A的HMBC谱解析如下:δH 0.88(3H,d)与C6、C8相关,归属为H-7;δH 1.29(2H,broad s)与C1~C4相关,归属为H-3;δH 1.52(4H,broad s)与C1~C5相关,归属为H-2和H-4;δH 2.46~2.51(4H,broad d)与C1~C5相关,归属为H-1和H-5;δH 2.79(1H,broad s)与C1和C5相关,归属为H-6;δH 4.00~4.09(2H,m)与C7相关,归属为H-8;δH7.10~7.16(2H,m)与C10、C12和C13相关,归属为H-10和H-12;δH 7.36~7.38(1H,m)与C9、相关,归属为H-11;δH 7.12~7.13(2H,m)与C16、C18和C20相关,归属为H-18和H-20;δH 7.52~7.57(1H,m)与C9、C14相关,归属为H-13;δH 7.59~7.62(1H,m)与C17、C21相关,归属为H-19;δH 7.74~7.76(2H,m)与C19相关,归属为H-17和H-21。
杂质B的HMBC谱解析如下:δH 1.12(3H,d)与C6、C8相关,归属为H-7;δH 1.41~1.45(2H,m)与C1~C4相关,归属为H-3;δH 1.53~1.59(4H,m)与C1~C5相关,归属为H-2和H-4;δH 2.51~2.64(4H,m)与C1~C5相关,归属为H-1和H-5;δH 2.90~2.98(1H,m)与C1、C5、C6、C7和C8相关,归属为H-6;δH 3.90~3.94(1H,dd)和4.03~4.06(1H,dd)与C7和C6相关,归属为H-8;δH 3.94~3.98(2H,m)与C9、C14、C16、C17、C21相关,归属为H-15;δH 6.91~6.94(1H,d)与C9、C10、C14相关,归属为H-12;δH 7.12~7.13(2H,m)与C17、C19和C21相关,归属为H-17和H-21;δH 7.22~7.26(2H,m)与C16、C17、C18、C20和C21相关,归属为H-18和H-20;δH 7.15~7.19(2H,m)与C9、C10和C17、C21相关,归属为H-11和H-19。
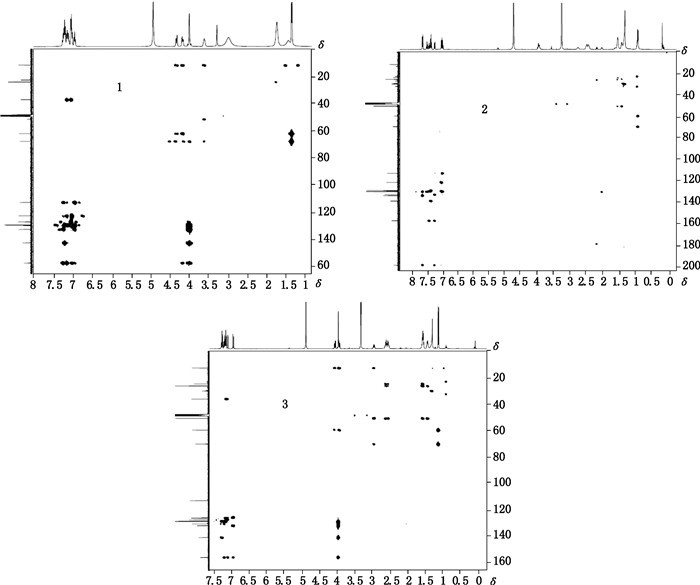
根据以上的分析,可确认杂质A为1-[2-(2-苯甲酰基苯氧基)-1-甲基乙基]哌啶,杂质B为1-[2-(2-苄基-6-氯苯氧基)-1-甲基乙基]哌啶,HMBC相关谱见图 5,1H和13C信号归属见表 1。
|
1.苯丙哌林(benproperine) 2.杂质A(impurity A) 3.杂质B(impurity B) 图 5 苯丙哌林、杂质A及杂质B的HMBC谱图 Figure 5 HMBC spectra of benproperine and impurity A and impurity B |
|
|
表 1 未知杂质的1H-NMR、13C-NMR数据 Table 1 1H-NMR, 13C-NMR data of unknown impurity in benproperine |
原有对苯丙哌林的研究未对其杂质进行结构确证。本文对苯丙哌林未知杂质进行了结构确证,通过1H-NMR、13C-NMR、HMBC、HSQC、DEPT135及H-H COSY核磁共振技术对化合物的结构进行了确认,苯丙哌林及杂质B氢谱中由于6位碳为手性碳,因此8位氢裂分为一对双二重峰;同时15位上的氢受两苯环的影响产生屋脊效应,裂分为中间高、两边低的多重峰。通过实验确定杂质A为1-[2-(2-苯甲酰基苯氧基)-1-甲基乙基]哌啶、杂质B为1-[2-(2-苄基-6-氯苯氧基)-1-甲基乙基]哌啶,并对1H-NMR和13C-NMR数据进行了HMBC全归属。由于苯丙哌林较稳定[6-7],可以初步判断杂质为合成苯丙哌林原料不纯引起,且由于杂质与苯丙哌林结构极为相似,未能在纯化过程除去,从而引入到最终的苯丙哌林中。
| [1] |
Martindale:the Extra Pharmacopoeia 37th Edition[S].2016:1552
|
| [2] |
钱之玉. 药理学[M]. 北京: 中国医药科技出版社, 2009, 478. QIAN ZY. Pharmacology[M]. Beijing: China Medical Science Press, 2009, 478. |
| [3] |
中国药典2015年版. 二部[S]. 2015: 1571 ChP 2015. Vol Ⅱ[S]. 2015: 1571
|
| [4] |
刘克江, 陈怡. HPLC法测定磷酸苯丙哌林颗粒的含量[J]. 天津药学, 2004, 16(4): 10. LIU KJ, CHEN Y. Determination of benproperine phosphate granules by HPLC[J]. Tianjin Pharm, 2004, 16(4): 10. |
| [5] |
欧阳冬华, 朱丹利, 陈雅萍. HPLC法测定磷酸苯丙哌林片的含量[J]. 安徽医药, 2008, 12(2): 135. OUYANG DH, ZHU DL, CHEN YP. Determination of benproperine phosphate tablets by HPLC[J]. Anhui Med Pharm J, 2008, 12(2): 135. |
| [6] |
王蓓, 高慧钦. 磷酸苯丙哌林口服溶液的有关物质研究[J]. 现代中西医结合杂志, 2007, 16(8): 1085. WANG B, GAO HQ. Study of benproperine phosphate related substances by HPLC[J]. Mod J Integr Tradit Chin Western Med, 2007, 16(8): 1085. |
| [7] |
傅强, 贺浪冲, 郭琦, 等. 高效液相色谱法测定磷酸苯丙呱林含量及有关物质[J]. 药物分析杂志, 2006, 26(1): 55. FU Q, HE LC, GUO Q, et al. HPLC determination of benproperine phosphate and its related substances[J]. Chin J Pharm Anal, 2006, 26(1): 55. |
| [8] |
张军武, 赵琦. 磷酸苯丙哌林口服液中有关物质检查方法的改进[J]. 西北药学杂志, 2008, 23(4): 205. ZHAN JW, ZHAO Q. Improvement of detection of related substances in benproperine phosphate oral liquid[J]. Northwest Pharm J, 2008, 23(4): 205. |
| [9] |
姚新生, 陈英杰, 徐绥绪, 等. 超导核磁共振波谱分析[M]. 北京: 中国医药科技出版社, 1991, 151. YAO XS, CHEN YJ, XU SX, et al. NMR Spectrometer with Superconducting Magnet[M]. Beijing: China Medical Science Press, 1991, 151. |
| [10] |
LISE SCHJELDERUP, ARNE JORGEN AASEN. The absolute configuration of benproperinium dihydrogen phosphate, an antitussive drug[J]. Chirality, 1989, 1(1): 86. DOI:10.1002/(ISSN)1520-636X |
| [11] |
LI Y, ZHONG DF, CHEN SW, et al. Identification of some benproperine metabolites in humans and investigation of their antitussive effect[J]. Acta Pharmacol Sin, 2005, 26(12): 1519. DOI:10.1111/aphs.2005.26.issue-12 |
| [12] |
黄海华, 崔洪霞, 钟大放, 等. 利用微生物转化模型研究苯丙哌林的代谢产物[J]. 中国药理学与毒理学杂志, 2001, 15(4): 297. HUANG HH, CUI HX, ZHONG DF, et al. Study on metabolites of benproperine using microbial model of transformation[J]. Chin J Pharmacol Toxicol, 2001, 15(4): 297. |
| [13] |
桂静, 宋林, 王凌. 人血浆中磷酸苯丙哌林的测定及其缓释制剂在人体内的生物等效性研究[J]. 华西药学杂志, 2010, 25(3): 296. GUI J, SONG L, WANG L. Determination of Benproperine phosphate in human plasma and bioavailability study of its preparations in healthy volunteers[J]. West China J Pharm Sci, 2010, 25(3): 296. |
| [14] |
孙煌, 娄志红, 付璀莹, 等. 核磁共振和液相色谱-质谱法对多索茶碱未知杂质的结构分析[J]. 药物分析杂志, 2013, 33(3): 443. SUN H, LOU ZH, FU CY, et al. Structural analysis of an unknown impurity in doxofylline by NMR spectroscopy and liquid chromatography-mass spectrometry[J]. Chin J Pharm Anal, 2013, 33(3): 443. |
| [15] |
董宇, 王晓黎, 曲建国. 应用高效液相色谱-飞行时间质谱及离子阱质谱分析磷酸苯丙哌林中的杂质[J]. 中国药学杂志, 2012, 47(19): 1585. DONG Y, WANG XL, QU JG. Analysis of impurity in benproperine phosphate bulk drug by high performance liquid chromatography-time of flight mass spectrometry and ion trap mass spectrometry[J]. Chin Pharm J, 2012, 47(19): 1585. |
 2017, Vol. 37
2017, Vol. 37 