2. 资阳市食品药品检验所, 资阳 641300
2. Ziyang Institute for Food and Drug Control, Ziyang 641300, China
独一味为唇形科独一味属植物独一味Lamiophlomis rotata(Benth.)Kudo的干燥地上部分,是藏族习用药材,具有活血止血、祛风止痛的功效,用于跌打损伤、外伤出血、风湿痹痛、黄水病,现收载于中国药典2015年版一部中,单方制剂独一味片、独一味胶囊也收载于中国药典2015年版一部中[1]。独一味药材产于西藏、青海、四川西部及云南西北部,生于海拔2.7~4.5 km的高原或高山上强度风化的碎石滩或石质高山草甸、河滩地中[2]。近年来由于需求量剧增,连年过度采收造成可采资源急剧下降,市场上出现以糙苏属植物的根冒充独一味的现象。2015年国家药品评价性抽验中抽得独一味药材23批,经鉴定12批为唇形科糙苏属植物糙苏Phlomis spp.的根。糙苏分布较为广泛,辽宁、内蒙古、河北、山东、山西、陕西、甘肃、四川、湖北、贵州及广东均有分布,其根也有作药用,有清热、止咳祛痰、愈伤生肌之功[3],糙苏的亲缘关系较近,化学成分有一定相似性,但也有较大区别,和独一味不能等同使用[4]。独一味中化学成分的含量测定研究有一些报道,最多同时测定芦丁等7个成分含量[5-11]。糙苏的含量测定研究较少,王争等[12]采用HPLC法测定了糙苏中3种苯乙醇苷成分。尚小飞等和李茂星等比较了独一味与糙苏中环烯醚萜苷类成分[13-14],本课题组前期研究中采用HPLC法比较了独一味和糙苏中4个成分的含量[15]。本文建立HPLC法同时测定独一味及糙苏中胡麻属苷、山栀苷甲酯、绿原酸、8-O-乙酰山栀苷甲酯、连翘酯苷B、木犀草苷和毛蕊花糖苷7个成分的含量,并进行比较研究,为独一味及其制剂的规范使用提供科学依据。
1 仪器、试药及样品 1.1 仪器安捷伦公司1260型液相色谱仪、二极管阵列检测器,沃特世公司Waters HSS T3 C18色谱柱(4.6 mm×250 mm,5 μm;填料:十八烷基硅烷键合硅胶),赛多利斯公司QUINTIX313-1CN型万分之一电子天平、MSE125S型十万分之一电子天平,江苏昆山市超声仪器有限公司KQ-500DV型超声波清洗器,密理博公司Milli-Q去离子水发生器。
1.2 试药对照品绿原酸(批号110753-201314)、山栀苷甲酯(批号111873-201103)、8-O-乙酰山栀苷甲酯(批号111872-201102)、连翘酯苷B(批号111811-201102)、木犀草苷(批号111720-201408)、毛蕊花糖苷(批号111530-201512)由中国食品药品检定研究院提供,胡麻属苷(批号MUST-16021205)由成都曼斯特生物科技有限公司提供,HPLC-DAD(面积归一化法)检测纯度均大于98.0%。甲醇、乙腈、磷酸均为色谱纯,水为Milli-Q纯化水。
1.3 样品药材均来自药材市场和饮片公司抽检样品,11批正品药材(编号1~11)经中国食品药品检定研究院中药民族药检定所郑健研究员鉴定为唇形科独一味属植物独一味Lamiophlomis rotata(Benth.)Kudo的干燥地上部分,12批伪品(编号12~23)鉴定为唇形科糙苏属植物糙苏(Phlomis spp.)的根。
2 方法与结果 2.1 混合对照品溶液取胡麻属苷、山栀苷甲酯、绿原酸、8-O-乙酰山栀苷甲酯、连翘酯苷B、木犀草苷和毛蕊花糖苷的对照品适量,置于50 mL棕色量瓶中,用甲醇溶解并定稀释至刻度,配制成上述7个成分质量浓度分别为202.6、206.4、192.4、191.2、187.4、376.4、189.0 μg·mL-1的混合对照品储备液;取混合对照品储备液1.0 mL,置于10 mL量瓶中,加甲醇定容至刻度,即得上述7个成分分别为20.26、20.64、19.24、19.12、18.74、37.64、18.90 μg·mL-1的混合对照品溶液,即得。
2.2 供试品溶液取样品粉末(过3号筛)约0.6 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇25 mL,密塞,称量,加热回流1 h,放冷,再称量,用70%甲醇补足减失的量,摇匀,滤过,精密量取续滤液2 mL,置10 mL量瓶中,加甲醇至刻度,摇匀,滤过,取续滤液,即得。
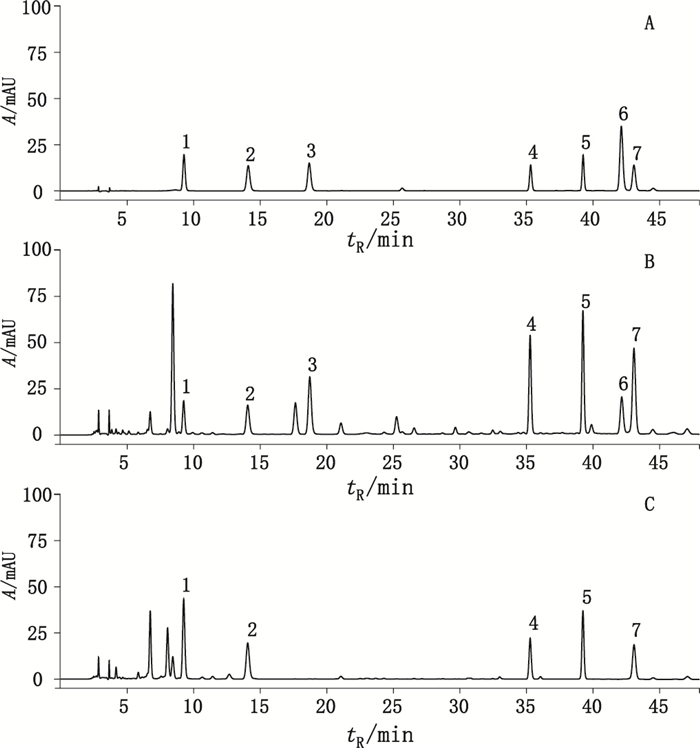
2.3 色谱条件及系统适用性试验采用Waters HSS T3 C18(4.6 mm×250 mm,5 μm)色谱柱,以乙腈(A)-0.1%磷酸水溶液(B)为流动相,梯度洗脱(0~11 min,9%A;11~35 min,9%A→18%A;35~50 min,18%A),流速1.0 mL·min-1,检测波长为235 nm,柱温30 ℃,进样量10 μL。各峰与邻峰的分离度均大于1.5,理论塔板数均在6 000以上。对照品及样品的色谱图见图 1。
|
1.胡麻属苷(sesamoside)2.山栀苷甲酯(shanzhiside methyl ester)3.绿原酸(chlorogenic acid)4. 8-O-乙酰山栀苷甲酯(8-O-acetyl shanzhiside methylester)5.连翘酯苷B(forsythoside B)6.木犀草苷(luteoloside)7.毛蕊花糖苷(acteoside) 图 1 混合对照品(A)、3号独一味(B)及15号糙苏(C)HPLC色谱图 Figure 1 HPLC chromatogram of mixed reference substances(A), Lamiophlomis Herba of sample No. 3(B)and Phlomis Radix of sample No. 15(C) |
依次精密吸取混合对照品储备液0.1、0.2、0.5、1.0、2.0、4.0 mL,分别置于6个10 mL量瓶中,加甲醇定容至刻度,配制成不同质量浓度的混合对照品溶液。取不同质量浓度的混合对照品溶液各10 μL,注入液相色谱仪,记录峰面积。以对照品质量浓度(μg·mL-1)为横坐标,以峰面积为纵坐标,绘制标准曲线,结果见表 1,表明各化合物在相应线性范围内线性关系良好。以对照品溶液逐步稀释法进样检测,以信噪比(S/N)为3:1和10:1为基准测得各化合物的检测限和定量限,结果见表 1。
|
|
表 1 7个被测定成分的回归数据、检测限及定量限 Table 1 Regressive data, limit of detection(LOD)and limit of quantification of 7 investigated components |
精密吸取“2.1”项下混合对照品溶液10 μL,连续进样6次,记录峰面积。结果胡麻属苷、山栀苷甲酯、绿原酸、8-O-乙酰山栀苷甲酯、连翘酯苷B、木犀草苷和毛蕊花糖苷峰面积的RSD分别为0.26%、0.35%、0.28%、0.19%、0.24%、0.16%和0.21%(n=6),表明仪器精密度良好。
2.6 重复性考察取独一味样品(1号)粉末和糙苏样品(15号)粉末各6份,分别按照“2.2”项下方法制备供试品溶液,按“2.3”项下色谱条件进样测定,记录峰面积,计算含量。结果独一味中胡麻属苷、山栀苷甲酯、绿原酸、8-O-乙酰山栀苷甲酯、连翘酯苷B、木犀草苷和毛蕊花糖苷测定结果的RSD(n=6)分别为0.89%、1.1%、1.3%、1.6%、0.78%、0.95%和1.4%,糙苏中胡麻属苷、山栀苷甲酯、8-O-乙酰山栀苷甲酯、连翘酯苷B和毛蕊花糖苷测定结果的RSD(n=6)分别为1.3%、1.2%、0.92%、1.5%和1.6%,表明独一味和糙苏的测定重复性良好。
2.7 溶液稳定性试验取独一味样品(1号)和糙苏样品(15号)的供试品溶液各1份,分别于0、2、4、8、12、24 h进样测定。结果独一味中胡麻属苷、山栀苷甲酯、绿原酸、8-O-乙酰山栀苷甲酯、连翘酯苷B、木犀草苷和毛蕊花糖苷峰面积的RSD(n=6)分别为0.78%、0.85%、1.1%、1.2%、0.65%、0.78%和0.96%,糙苏中胡麻属苷、山栀苷甲酯、8-O-乙酰山栀苷甲酯、连翘酯苷B和毛蕊花糖苷峰面积的RSD(n=6)分别为0.45%、0.72%、1.0%、0.86%和0.78%,结果表明独一味和糙苏的供试品溶液在24 h内稳定。
2.8 加样回收率试验取已知含量的独一味样品(1号)粉末6份,每份约0.3 g,置具塞锥形瓶中,精密加入各对照品溶液(胡麻属苷1.405 mg·mL-1、山栀苷甲酯3.052 mg·mL-1、绿原酸0.372 mg·mL-1、8-O-乙酰山栀苷甲酯1.502 mg·mL-1、连翘酯苷B 0.354 mg·mL-1、木犀草苷2.086 mg·mL-1和毛蕊花糖苷0.312 mg·mL-1)各1 mL,再精密加入70%甲醇18 mL,密塞,余下操作按照“2.2”项下方法制备供试溶液,按“2.3”项下色谱方法测定,记录峰面积,计算回收率,结果胡麻属苷、山栀苷甲酯、绿原酸、8-O-乙酰山栀苷甲酯、连翘酯苷B、木犀草苷和毛蕊花糖苷平均加样回收率(n=6)分别为98.45%、98.65%、96.88%、97.45%、99.23%、98.74%和99.21%,RSD分别为1.6%、1.8%、2.1%、1.8%、1.9%、2.3%和1.6%。同法取糙苏样品(15号)粉末6份,每份约0.3 g,置具塞锥形瓶中,精密加入各对照品溶液(胡麻属苷1.972 mg·mL-1、山栀苷甲酯1.726 mg·mL-1、8-O-乙酰山栀苷甲酯0.622 mg·mL-1、连翘酯苷B 1.692 mg·mL-1和毛蕊花糖苷1.236 mg·mL-1)各1 mL,同上法制备供试溶液,进样测定,记录峰面积,计算回收率,结果胡麻属苷、山栀苷甲酯、8-O-乙酰山栀苷甲酯、连翘酯苷B和毛蕊花糖苷平均加样回收率(n=6)分别为97.68%、98.36%、97.69%、98.12%和97.68%,RSD分别为1.8%、2.3%、2.2%、1.7%和2.4%。
2.9 独一味和糙苏的含量测定每个样品取2份,分别按“2.2”项下方法制备供试品溶液。精密吸取各供试品溶液10 μL,按“2.3”项下色谱条件进行测定,用外标法计算出含量,结果见表 2。
|
|
表 2 独一味和糙苏中7种成分含量测定结果(%) Table 2 Contents of seven components in Lamiophlomis Herba and Phlomis Radix |
本文采用梯度洗脱法分离独一味及其伪品糙苏中的7个主要化学成分,50 min内完成分离,胡麻属苷、山栀苷甲酯、绿原酸、8-O-乙酰山栀苷甲酯、连翘酯苷B、木犀草苷和毛蕊花糖苷分离效果良好,符合含量测定要求。色谱条件依据中国药典2015年版一部独一味含量测定项下条件优化而成,流动相水相中加入0.1%磷酸改善色谱峰的拖尾,峰形对称,分离度较好,效果理想,故最终确定此流动相。通过二极管阵列检测器进行全波长扫描(190~400 nm),结果235 nm时7个化学成分均有较大吸收,且杂质成分干扰少,故选择235 nm作为检测波长。
3.2 含量测定由表 2可见,11批独一味中均含有胡麻属苷、山栀苷甲酯、绿原酸、8-O-乙酰山栀苷甲酯、连翘酯苷B、木犀草苷和毛蕊花糖苷7个化学成分。12批糙苏中均含有胡麻属苷、山栀苷甲酯、8-O-乙酰山栀苷甲酯、连翘酯苷B、毛蕊花糖苷5个化学成分,其中绿原酸和木犀草苷均未检出。12批糙苏中均含有中国药典2015年版一部独一味含量测定项下规定的山栀苷甲酯和8-O-乙酰山栀苷甲酯,并且含量可以达到限量要求,推测是市场上以糙苏冒充独一味销售的主要原因,建议增加绿原酸或木犀草苷作为检测指标,可有效控制独一味及其制剂的质量。
另外,从独一味及糙苏的色谱图(图 1)上看,两者具有一定的相似性,但糙苏的的色谱图中山栀苷甲酯和8-O-乙酰山栀苷甲酯的色谱峰之间几乎没有色谱峰检出,而独一味的山栀苷甲酯和8-O-乙酰山栀苷甲酯的色谱峰之间有数个较大色谱峰检出,除峰3为绿原酸外,其他几个色谱峰尚需进一步研究。
3.3 小结本实验在以中国药典2015年版一部独一味含量测定项下色谱条件为基础,同时测定不同批次独一味中胡麻属苷、山栀苷甲酯、绿原酸、8-O-乙酰山栀苷甲酯、连翘酯苷B、木犀草苷和毛蕊花糖苷7个有效成分的含量,方法简便、快速、准确,具备了定性和定量双重作用,为有效控制独一味及其制剂的质量提供了科学依据。
| [1] |
中国药典2015年版. 一部[S]. 2015: 262, 1268, 1269 ChP 2015.Vol Ⅰ [S].2015:262, 1268, 1269 |
| [2] |
中国科学院中国植物志编辑委员会. 中国植物志[M]. 65卷. 北京: 科学出版社, 1989, 480. Editorial Committee of Flora of China of Chinese Academy of Sciences. Flora of China[M]. Volume 65. Beijing: Science Press, 1989, 480. |
| [3] |
卫生部药品标准蒙药分册[S]. 1998: 57 Drug Specifications Promulgated for Mongolian Medicine by the Minister of Public Health, P R China [S].1998:57 |
| [4] |
李茂星, 李文斌, 贾正平, 等. 独一味和糙苏属关系的研究进展[J]. 中药材, 2008, 31(9): 1451. LI MX, LI WB, JIA ZP, et al. Research progress of relationship of Lamiophlomis and Phlomis[J]. J Chin Med Mater, 2008, 31(9): 1451. |
| [5] |
沈建伟, 王锐娟, 王环, 等. 藏药独一味的研究进展[J]. 安徽农业科学, 2008, 36(5): 1920. SHEN JW, WANG RJ, WANG H, et al. Research progress of traditional Tibetan herb Lamiophlomis rotata[J]. J Anhui Agric Sci, 2008, 36(5): 1920. |
| [6] |
张娟红, 徐丽婷, 王荣, 等. 藏药独一味生药学及化学成分研究进展[J]. 兰州大学学报(医学版), 2015, 41(5): 57. ZHANG JH, XU LT, WANG R, et al. Research advances in the pharmacognostics and chemical constituents of traditional Tibetan herb Lamiophlomis rotata[J]. J Lanzhou Univ(Med Sci), 2015, 41(5): 57. |
| [7] |
潘正, 高运玲, 张涛, 等. HPLC法测定独一味根中环烯醚萜苷和苯乙醇苷[J]. 中草药, 2011, 42(2): 279. PAN Z, GAO YL, ZHANG T, et al. HPLC determination of iridoid glycosides and phenylethanoid glycosides in roots of Lamiophlomis rotata[J]. Chin Tradit Herb Drugs, 2011, 42(2): 279. |
| [8] |
何映霞, 张来, 沈昱翔, 等. 独一味4种药用成分含量的测定[J]. 贵州农业科学, 2013, 41(8): 73. HE YX, ZHANG L, SHEN LX, et al. Simultaneous determination of four medicinal components in Lamiophlomis rotata[J]. Guizhou Agri Sci, 2013, 41(8): 73. |
| [9] |
钟世红, 古锐, 王铃鑫, 等. HPLC法同时测定独一味中的7种成分含量[J]. 中国中药杂志, 2014, 39(22): 4373. ZHONG SH, GU R, WANG LX, et al. Simultaneous determination of seven constituents in Lamiophlomis rotata by HPLC[J]. Chin J Chin Mater Med, 2014, 39(22): 4373. |
| [10] |
樊鹏程, 李茂星, 贾正平, 等. RP-HPLC同时测定不同产地独一味药材中4种环烯醚萜苷[J]. 中草药, 2010, 41(3): 483. FAN PC, LI MX, JIA ZP, et al. Simultaneous determination of 4 iridoid glycosides in Lamiophlomis rotata materials from different habitates with RP-HPLC[J]. Chin Tradit Herb Drugs, 2010, 41(3): 483. |
| [11] |
罗米娜, 赵亮, 刘霞, 等. 藏药独一味中槲皮素、木犀草素和芹菜素的HPLC测定[J]. 药物分析杂志, 2006, 26(12): 1773. LUO MN, ZHAO L, LIU X, et al. HPLC determination of quercetin, luteolin and apigenin in Lamiophlomis rotata(Benth.)Kudo and its capsules[J]. Chin J Pharm Anal, 2006, 26(12): 1773. |
| [12] |
王争, 邓瑞雪, 杨友亮, 等. HPLC法同时测定糙苏中3个苯乙醇苷类化合物的含量[J]. 药物分析杂志, 2011, 31(4): 668. WANG Z, DENG RX, YANG YL, et al. HPLC simultaneous determination of three phenylethanoids in Phlomis umbrosa[J]. Chin J Pharm Anal, 2011, 31(4): 668. |
| [13] |
尚小飞, 李茂星, 樊鹏程, 等. 独一味与糙苏中环烯醚萜苷类成分的比较[J]. 华西药学杂志, 2009, 24(4): 391. SHANG XF, LI MX, FAN PC, et al. Comparison the iridoid glycosides between in Lamiophlomis rotata and Phlomis umbrosa[J]. West China J Pharm Sci, 2009, 24(4): 391. |
| [14] |
李茂星, 张超, 乌兰, 等. 独一味、螃蟹甲、糙苏和萝卜秦艽中5个环烯醚萜苷的含量测定[J]. 中药材, 2011, 34(1): 727. LI MX, ZHANG C, WU L, et al. Content determination of five iridoid glycosides in Lamiophlomis rotata, Phlomis yonghusbandii, Phlomis umbrosa and Phlomis medicinalis[J]. J Chin Med Mater, 2011, 34(1): 727. |
| [15] |
昝珂, 焦兴苹, 过立农, 等. 藏药独一味及其伪品HPLC特征图谱和4种成分含量测定[J]. 中国中药杂志, 2016, 41(12): 2284. ZAN K, JIAO XP, GUO LN, et al. HPLC specific chromatogram of Lamiophlomis Herba and its counterfeit and determination of four effective components[J]. China J Chin Mater Med, 2016, 41(12): 2284. |
 2017, Vol. 37
2017, Vol. 37 
