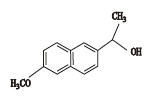
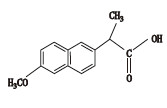
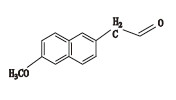
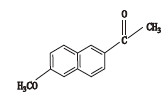
萘普生钠(naproxen,结构式见图 1)为芳基乙酸类非甾体抗炎镇痛药萘普生的钠盐,是萘普生的换代产品,萘普生钠盐可以增加药物的溶解度,便于药物的溶出,有利于机体对药物的吸收利用[1]。文献报道,光线、空气、pH对萘普生钠的稳定性有较大影响[2]。中国药典2015年版采用薄层色谱法测定萘普生钠的有关物质[3]。欧洲药典采用高效液相色谱法对萘普生钠进行有关物质的分析,但流动相中使用了非挥发性的磷酸盐体系,无法与质谱联用进行有关物质结构的分析[4]。笔者在参与针对新版药典用的萘普生钠化学对照品的标化工作中,查阅各国药典及相关文献[4-10],建立了液相色谱-串联质谱(LC-MS/MS)法测定萘普生钠中强制破坏后的降解产物,并对其主要降解产物进行结构鉴定,为该药品的质量标准提高提供科学参考。
|
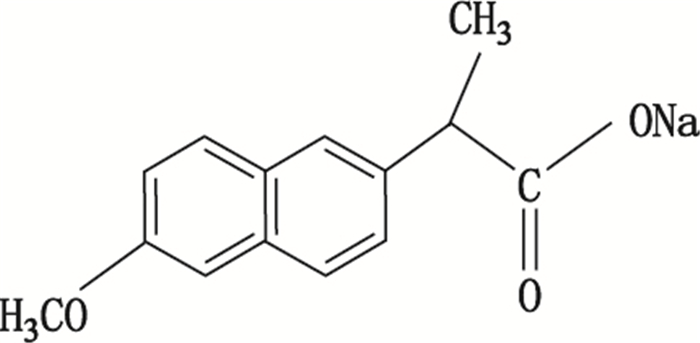
图 1 萘普生钠化学结构 Figure 1 The chemical structure of naproxen sodium |
Waters 2695型高效液相色谱仪,2996二极管阵列检测器,Empower色谱工作站;(包括四元泵,柱温箱,自动进样器,二极管阵列PDA检测器,美国Waters公司);Infinity 1290超高效液相色谱仪/6530A Q-TOF联用质谱仪(包括四元泵、自动进样器、柱温箱、二极管阵列检测器,四级杆飞行时间质谱仪,美国Agilent公司);Mettler Toledo XS-205型电子天平(瑞士梅特勒-托利多公司)。
1.2 试药萘普生钠对照品(批号:100330-200702,中国食品药品检定研究院,含量(按C14H13NaO3计):100.0%,供UV法含量测定用);6-甲氧基-2-萘乙酮(批号:100140-200303,中国食品药品检定研究院,供TLC法萘普生有关物质检查用);乙腈、甲酸均为色谱纯,水为超纯水,其余试剂均为分析纯。
2 方法与结果 2.1 色谱条件色谱柱:CAPCELL PAK C18(填料:十八烷基硅烷键合硅胶,250 mm × 4.6 mm,5 μm);流动相:乙腈-水-甲酸(48:52:0.1);柱温:35 ℃;检测波长:262 nm;流速:1.0 mL·min-1;PDA扫描范围:190~400 nm;进样量:20 μL。
2.2 质谱条件电喷雾离子源ESI,正离子检测模式,喷雾电压:3.5 kV;毛细管温度:350 ℃;干燥气流量:10 L·min-1;干燥气压力:310.3 kPa;MS扫描范围:m/z 50~1 000;MS/MS扫描范围:m/z 50~500;MS/MS分析时的碰撞能量:20 eV。样品从高效液相色谱仪通过T型三通阀以1:1的分流比引入质谱离子源内。
2.3 溶液的配制 2.3.1 供试品溶液精密称取萘普生钠对照品10 mg,置20 mL量瓶中,加流动相溶解并稀释至刻度,摇匀,即得。
2.3.2 对照溶液精密量取供试品溶液1 mL,置100 mL量瓶中,加流动相稀释至刻度,摇匀,即得。
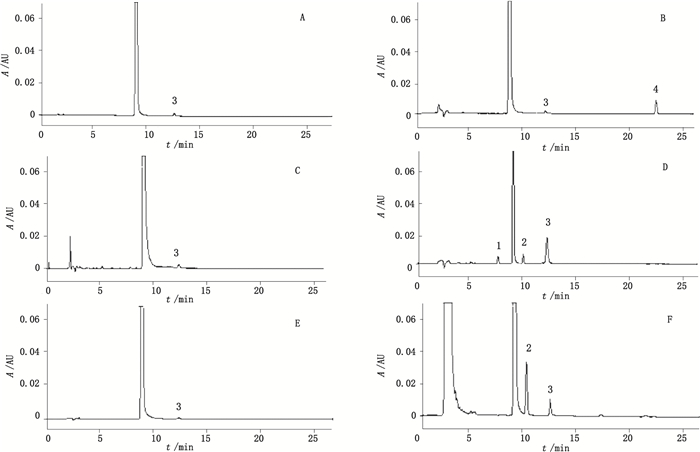
2.4 方法的验证 2.4.1 破坏性试验取萘普生钠对照品约50 mg,置50 mL量瓶中,加流动相溶解并稀释至刻度,摇匀,精密量取续滤液5 mL,分别置10 mL量瓶中,进行破坏性试验:①酸破坏:加1 mol·L-1盐酸溶液2 mL,室温下放置3 h,用1 mol·L-1氢氧化钠溶液调节pH至中性,加流动相稀释至刻度,摇匀;②碱破坏:加1 mol·L-1氢氧化钠溶液2 mL,室温下放置3 h,用1 mol·L-1盐酸溶液调节pH至中性,加流动相稀释至刻度,摇匀;③光破坏:置照度为(4 500±500)lx的灯检箱下照射24 h,加流动相稀释至刻度,摇匀。④高温破坏:沸水浴放置2 h后,放冷至室温,加流动相稀释至刻度,摇匀;⑤氧化破坏:加30%过氧化氢2 mL,室温下放置3 h,加流动相稀释至刻度,摇匀。按“2.1”项下的色谱条件记录色谱图,见图 2。可见,该方法能有效检测出各种破坏产生的降解产物,且各降解产物峰间及降解产物峰与主峰间均能达到基线分离。
|
A.未破坏(untreated)B.酸破坏(destruction with acid)C.碱破坏(destruction with base)D.光照破坏(photo destruction)E.高温破坏(heat destruction)F.氧化破坏(oxidative destruction) 图 2 破坏性试验HPLC色谱图 Figure 2 HPLC chromatograms of samples in destruction tests |
取同一供试品溶液,按“2.1”项下色谱条件测定,连续进样6次,记录各色谱图的峰面积,RSD为0.30%(n = 6)。
2.4.3 检出限精密称取萘普生钠对照品适量,加流动相溶解并定量稀释,按“2.1”项下的色谱条件测定,当信噪比为3:1时,得到检出限为1.1 ng。
2.4.4 稳定性试验取同一供试品溶液,在室温下于0、2、4、8、10、12 h分别进行测定,记录色谱峰面积,结果RSD为0.19%(n = 6),表明室温下供试品溶液在12 h内稳定。
2.4.5 耐用性试液分别对液相色谱方法中典型变动因素:流动相组成比例乙腈-水-甲酸(48:52:0.1,45:55:0.1)、不同品牌的同类型色谱柱[Agilent Eclipse C18柱(150 mm × 4.6 mm,3.5 μm)、Waters Xbridge C18(250 mm × 4.6 mm,5 μm)]、柱温(32、38 ℃)及流速(0.8、1.2 mL·min-1),以同一破坏性试验样品进行检测,各降解产物峰与主峰的分离度均达到要求,表明该方法耐用性良好。
2.5 萘普生钠降解产物测定按“2.3”项下分别制备供试品溶液和对照溶液,按“2.1”项下的色谱条件,取对照溶液20 μL注入液相色谱仪,调节检测灵敏度,使主成分峰高约为满量程的10%~20%;再取供试品溶液20 μL,注入液相色谱仪,记录色谱图至主成分峰保留时间的3倍,平行测定3次,采用主成分自身对照法计算降解产物含量,结果测得对照品中单个最大降解产物含量为0.03%。
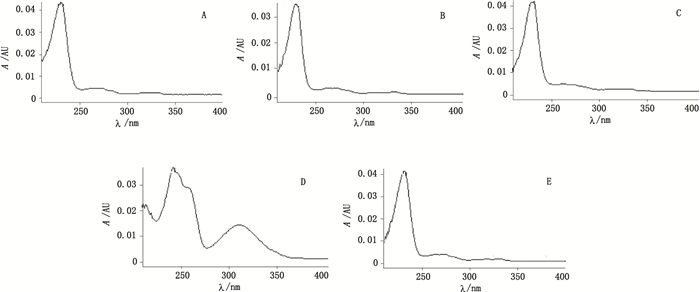
2.6 主要降解产物的确认对供试品溶液破坏后4个主要的降解产物,按“2.1”项下的色谱条件和质谱条件进行分析,得到其LC-PDA(图 3)和LC-MS/MS,检查各峰的纯度,4个峰均被认为是单一物质峰,LC-TOF测得这些降解产物母离子的精密质量(见表 1),经综合解析,确证了其主要的结构。
|
A.萘普生钠(naproxen sodium)B.降解产物1(degradation compound 1)C.降解产物2(degradation compound 2)D.降解产物3(degradation compound 3)E.降解产物4(degradation compound 4) 图 3 萘普生钠及其主要降解产物的LC-PDA图 Figure 3 LC-PDA spectra of naproxen sodium and its major degradation compounds |
|
|
表 1 萘普生钠及其主要降解产物的质谱特征和推测结构 Table 1 Mass spectrometry characteristics and proposed chemical structures of naproxen sodium and its major degradation compounds |
萘普生钠:萘普生钠在该流动相体系中以萘普生的形成存在,萘普生的相对分子质量为230,一级质谱图中测得的m/z 231和m/z 253分别为萘普生的[M+H]+和[M+Na]+峰,进一步对m/z 231进行二级全扫描质谱分析,其二级质谱图及可能裂解途径见图 4。
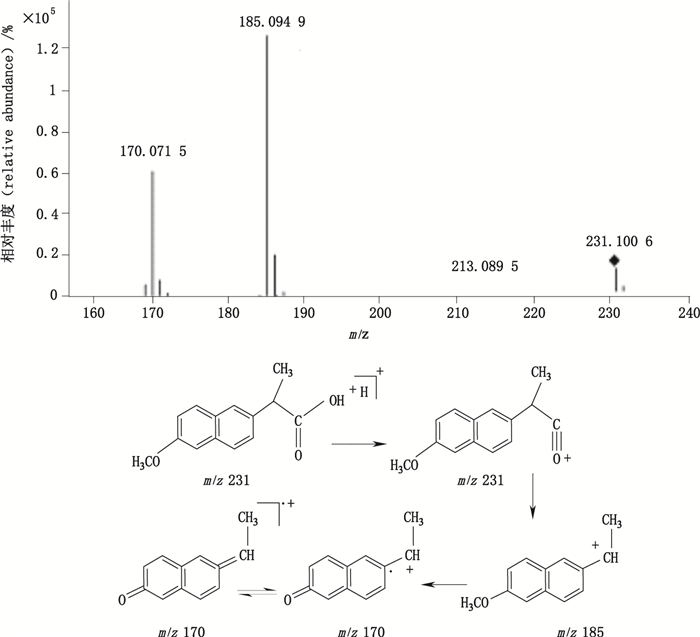
|
图 4 萘普生[M+H]+离子图的二级质谱图及其裂解途径 Figure 4 MS/MS spectrum of naproxen [M+H]+ ion and its fragmentation pathway |
降解产物1:ESI+-MS测得萘普生钠降解产物1的一级质谱图中m/z 203为[M+H]+峰,表明其相对分子质量为202,进一步对m/z 203进行二级全扫描质谱分析,其二级质谱碎片与萘普生钠相似,且其PDA谱也与萘普生钠相似,说明其与萘普生钠具有相似的共轭体系。结合其二级质谱碎片信息及欧洲药典[3],推测降解产物1为萘普生钠的羧基还原产物。其二级质谱主要碎片均可经此结构合理裂解产生(图 5)。
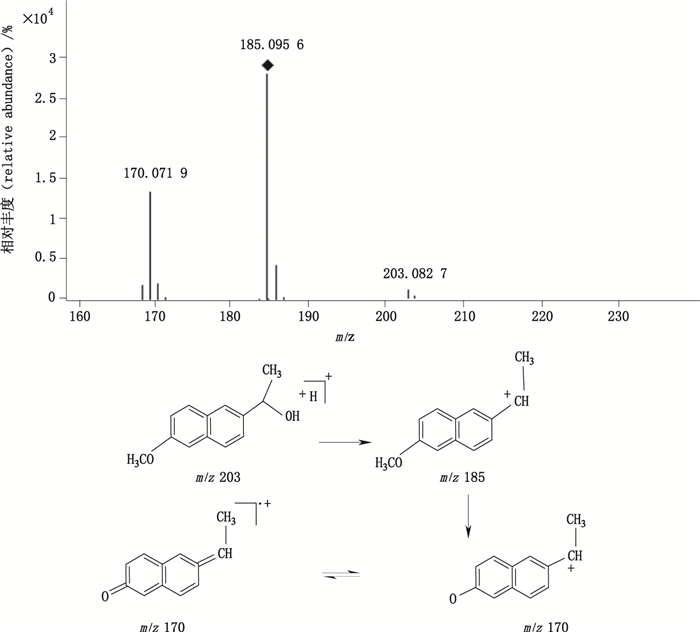
|
图 5 降解产物1[M+H]+离子图的二级质谱图及其裂解途径 Figure 5 MS/MS spectrum of degradation compound 1 [M+H]+ ion and its fragmentation pathway |
降解产物3:对6-甲氧基-2-萘乙酮对照品进行质谱分析,一级质谱分析结果产生了准分子离子峰[M+H]+ m/z 201,在相同的色谱及质谱条件下,萘普生钠降解产物3与6-甲氧基-2-萘乙酮对照品色谱保留时间及PDA光谱图均相同。此外,在相应的一级全扫描质谱及二级全扫描分析中,检测到降解产物3与6-甲氧基-2-萘乙酮相同的准分子离子峰及二级质谱碎片也完全相同,由此证明降解产物3为6-甲氧基-2-萘乙酮,其二级质谱主要碎片及可能裂解过程如图 6所示。
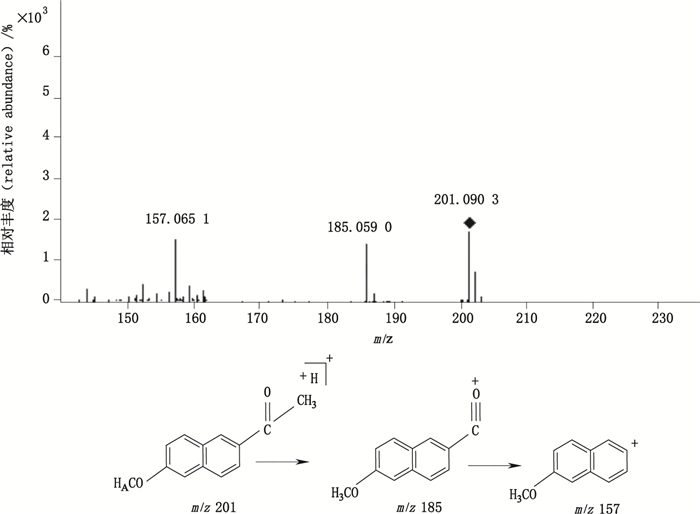
|
图 6 降解产物3[M+H]+离子图的二级质谱图及其裂解途径 Figure 6 MS/MS spectrum of degradation compound 3 [M+H]+ ion and its fragmentation pathway |
降解产物2:ESI+-MS测得降解产物2的一级质谱图中m/z 201为[M+H]+峰,表明其相对分子质量为200,与6-甲氧基-2-萘乙酮相对分子质量相同。同时与6-甲氧基-2-萘乙酮相比,降解产物2的PDA光谱谱缺少242 nm的吸收带,最大吸收波长在230 nm,说明其萘环上的共轭体系减少,K吸收带蓝移[11]。推测降解产物2与6-甲氧基-2-萘乙酮具有相同的母体结构,取代基部分有所不同,二级质谱主要碎片均可经此结构合理裂解产生(图 7)。
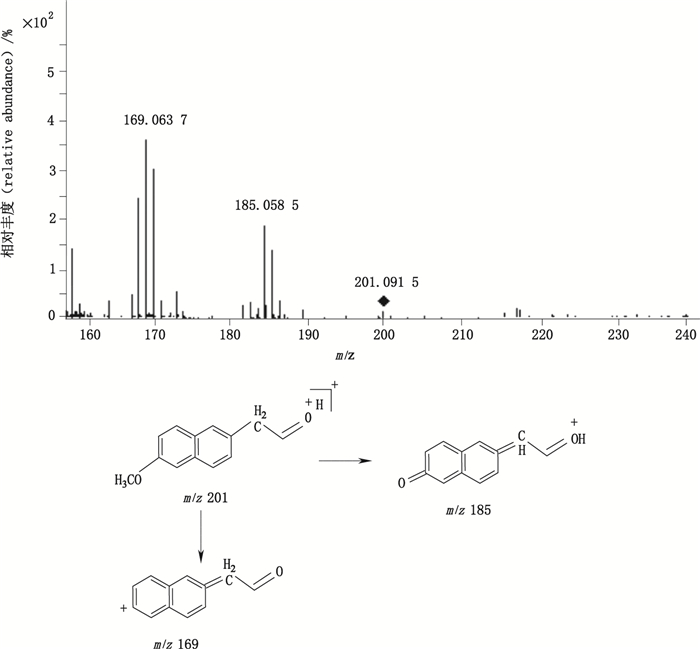
|
图 7 降解产物2[M+H]+离子图的二级质谱图及其裂解途径 Figure 7 MS/MS spectrum of degradation compound 2 [M+H]+ ion and its fragmentation pathway |
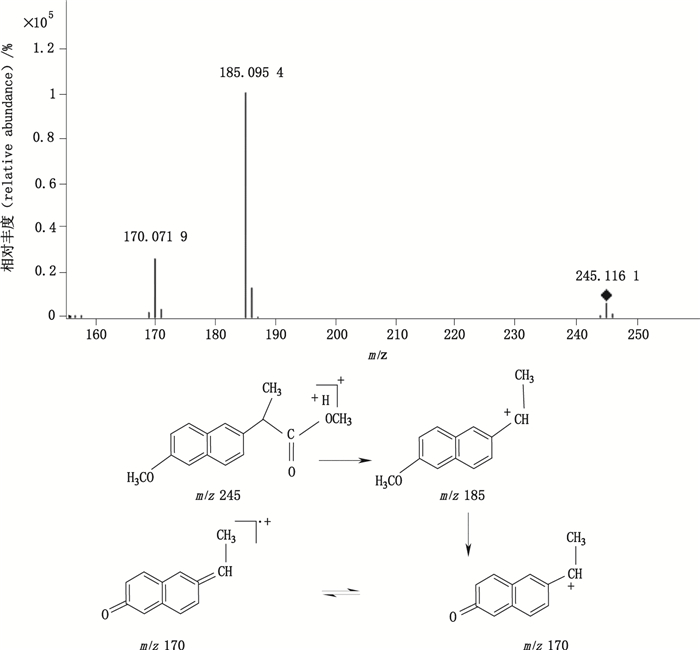
降解产物4:ESI+-MS测得降解产物4的一级质谱图中m/z 245为[M+H]+峰,表明其相对分子质量为244,比萘普生多14,与一个甲基单元对应。降解产物4的LC-PDA光谱图均与萘普生钠相似,且其二级质谱碎片也与萘普生钠相似,结合欧洲药典[4],推测降解产物4与萘普生钠具有相同的母体结构,取代基部分有所不同,见图 8。
|
图 8 降解产物4[M+H]+离子图的二级质谱图及其裂解途径 Figure 8 MS/MS spectrum of degradation compound 4 [M+H]+ ion and its fragmentation pathway |
采用PDA检测器分别对萘普生钠及其主要降解产物进行光谱分析,萘普生钠及其降解产物在262 nm波长处均有较大的响应,且在该波长下测得的杂质个数较多,基线更平直,色谱峰形更好,故最终确定262 nm为检测波长。
3.2 杂质来源分析萘普生钠在高温、强碱、强酸条件下较为稳定,但在光照、氧化条件下降解产物明显增多,尤其是降解产物2、3,故在药品制备或贮存过程中应注意密闭隔氧。根据萘普生的合成工艺[12-15],降解产物3可能为合成过程中不完全反应带入的杂质。参照欧洲药典[4]所规定的可能降解产物结构,结合各降解产物峰的一级及二级质谱信息,初步鉴定出萘普生钠的降解产物1、3、4分别与英国药典的杂质K、L、E相对应,而降解产物2尚未见报道,其准确结构有待于通过制备进行H-NMR确证。
4 结论文献报道大多采用磷酸盐的色谱体系对萘普生或萘普生钠进行质量控制[4, 16],但是,磷酸盐作为非挥发性盐常常会由于结块而将电喷雾质谱的喷针堵死,因而无法利用色谱-质谱联用技术对萘普生钠的降解产物进行定性分析。本文建立了LC-MS/MS法分析萘普生钠强制破坏后的主要降解产物,该方法简便、灵敏、准确,专属性强,为评价萘普生钠的质量提供了依据。
| [1] |
王丽君, 王东凯, 黎玲, 等. HPLC法测定注射用萘普生钠的含量及有关物质[J]. 中国药剂学杂志, 2006, 4(1): 16. WANG LJ, WANG DK, LI L, et al. Determination of naproxen sodium for injection with HPLC[J]. Chin J Pharm, 2006, 4(1): 16. |
| [2] |
王国祥, 宋宏春, 宋士强, 等. 萘普生钠注射液的稳定性研究[J]. 中国药学杂志, 1992, 27(11): 663. WANG GX, SONG HC, SONG SQ, et al. Study on the stability of naproxen sodium injection[J]. Chin Pharm J, 1992, 27(11): 663. |
| [3] |
中国药典2015年版. 二部[S]. 2015:1211 ChP 2015. Vol Ⅱ[S]. 2015:1211 |
| [4] |
EP 8. 0[S]. 2013:2830
|
| [5] |
杨俊玲, 康新立. HPLC法测定萘普生钠片的含量[J]. 中国当代医药, 2011, 18(20): 39. YANG JL, KANG XL. Determination of daidzein naproxen sodium tablets by HPLC[J]. China Mod Med, 2011, 18(20): 39. DOI:10.3969/j.issn.1674-4721.2011.20.018 |
| [6] |
高磊, 石嫱. HPLC法测定萘普生有关物质[J]. 中国药品标准, 2005, 6(6): 17. GAO L, SHI Q. Examination of related substances in naproxen by HPLC[J]. Drug Stand China, 2005, 6(6): 17. |
| [7] |
刘玉春, 许世辉. HPLC法测定萘普生钠注射液的含量[J]. 海峡药学, 2008, 20(11): 60. LIU YC, XU SH. Determination of naproxen sodium injection by HPLC[J]. Strait Pharm J, 2008, 20(11): 60. DOI:10.3969/j.issn.1006-3765.2008.11.032 |
| [8] |
王国祥, 宋宏春, 宋士强, 等. 紫外分光光度法测定萘普生钠含量[J]. 内蒙古医学院学报, 1990, 12(1): 35. WANG GX, SONG HC, SONG SQ, et al. Assay of naproxen sodium by ultraviolet spectrophotometry[J]. Acta Acad Med Nei Mongol, 1990, 12(1): 35. |
| [9] |
陈寅生, 马莉. HPLC法测定复方奈福泮萘普生钠缓释胶囊中两组分的含量[J]. 河南大学学报(医学版), 2011, 30(3): 159. CHEN YS, MA L. Determination of the contents of two components in compound nefopam and naproxen sodium sustained release capsules by HPLC[J]. J Henan Univ(Med Sci), 2011, 30(3): 159. |
| [10] |
沈炳香, 李德刚, 聂松柳. HPLC法同时测定萘普生钠伪麻黄碱缓释片中两组分的含量[J]. 安徽医药, 2007, 11(11): 1002. SHEN BX, LI DG, NIE SL. Simultaneous determination of naproxen sodium and pseudoephedrine hydrochloride sustained-release tablets by HPLC[J]. Anhui Med Pharm J, 2007, 11(11): 1002. DOI:10.3969/j.issn.1009-6469.2007.11.025 |
| [11] |
李发美. 分析化学[M]. 第七版. 北京: 人民卫生出版社, 2008, 1. LI FM. Analytical Chemistry[M]. 7th ed. Beijing: People' s Medical Publishing House, 2008, 1. |
| [12] |
刘丽梅, 张富江, 于海龙. 萘普生合成工艺的研究[J]. 黑龙江医药, 2000, 13(4): 214. LIU LM, ZHANG FJ, YU HL. Study on the new syntheitc process of naproxen[J]. Med J Heilongjiang, 2000, 13(4): 214. |
| [13] |
杨芳. 萘普生及其中间体的合成和工艺改进[D]. 南京: 南京理工大学, 2004 YANG F. The Synthesis of Naproxen and Its Intermediates[D]. Nanjing:Nanjing University of Science and Technology, 2004 |
| [14] |
袁学军, 苏增权, 康敏, 等. 萘普生的不对称合成工艺改进[J]. 中国医药工业杂志, 1999, 30(10): 433. YUAN XJ, SU ZQ, KANG M, et al. The improvement of asymmetrical synthesis of naproxen[J]. Chin J Pharm, 1999, 30(10): 433. |
| [15] |
李民前. 高效低毒新药萘普生钠[J]. 华西药学杂志, 1991, 6(1): 57. LI MQ. Naproxen:a new drug of high activity and low poison[J]. West China J Pharm Sci, 1991, 6(1): 57. |
| [16] |
HADI MA, RAGHAVENDRA RAO NG, SRINIVASA RAO A. Pharmacokinetic parameters determination and in vitro-in vivo correlation of ileocolonic-targeted pH-responsive coated minitablets of naproxen[J]. Sci Pharm, 2015, 83(4): 645. DOI:10.3797/(ISSN)0036-8709 |
 2017, Vol. 37
2017, Vol. 37