2. 广西壮族自治区食品药品检验所, 南宁 530021;
3. 云南省食品药品监督检验研究院, 昆明 650000
2. Guangxi Institute for Food and Drug Control, Nanning 530021, China;
3. Yunnan Institute for Food and Drug Control, Kunming 650000, China
青阳参为萝藦科鹅绒藤属植物青阳参Cynanchum otophyllum Schneid.的干燥根,主产于云南、湖南、广西、贵州、四川和西藏等省区,具有强筋健骨、健脾和胃、祛风解痉的功效,用于腰肌劳损、筋骨疼痛、食欲不振、癫痫、小儿惊风。在云南白族、彝族、纳西族、傈僳族等少数民族中作药材使用。白族药名为“嘟巴优”,纳西族药名为“白药根”、“大白药根”,彝族药名为“期夺齐”。青阳参药材标准收录于《云南省中药材标准》2005年版和《湖南省中药材标准》2009年版中[1-4]。青阳参中主要含有酚类、C21甾体苷类化合物[5-9]。有学者[7]采用HPLC法测定了青阳参中7个C21甾体苷类化合物的含量,但由于该类结构较为相似,含量较低,并且紫外吸收很弱,用其作为指标性成分进行HPLC测定时分离度差,干扰多。在实验过程中,发现青阳参中的另一类化合物——酚类,紫外吸收强,用其作为指标进行HPLC含量测定时分离度好,干扰较小。对羟基苯乙酮具有较好的利胆作用,是中国药典2015年版茵陈提取物指标性成分[11-12];白首乌二苯酮具有神经保护作用,能够透过血脑屏障,具有抗脑缺血损伤的作用,这和其用于治疗癫痫的功效相吻合[13]。本课题组前期建立了HPLC法分别测定了青阳参中的对羟基苯乙酮和白首乌二苯酮的含量[14-15],但应用HPLC法对青阳参中所含的多种酚类成分进行同时测定还未见报道。因此,为控制药材质量,本研究采用HPLC法对不同产地的青阳参药材中的对羟基苯甲酸、香草酸、对羟基苯乙酮、2,5-二羟基苯乙酮、白首乌二苯酮、2,4-二羟基苯乙酮6种酚类成分的含量进行测定,为建立科学、完整的青阳参药材质量标准提供依据。
1 仪器、试药与样品 1.1 仪器1260型液相色谱仪(安捷伦公司),二极管阵列检测器(安捷伦公司),Waters HSS T3 C18(250 mm×4.6 mm,5 μm;填料:十八烷基硅烷键合硅胶;沃特世公司),QUINTIX313-1CN型万分之一电子天平(赛多利斯公司),MSE125S型十万分之一电子天平(赛多利斯公司),KQ-500DV型超声波清洗器(江苏昆山市超声仪器有限公司),Milli-Q去离子水发生器(密理博公司)。
1.2 试药对羟基苯甲酸对照品(批号20140801,纯度98.9%)、2,5-二羟基苯乙酮(批号20151101,纯度99.2%)、2,4-二羟基苯乙酮(批号20150102,纯度99.5%)购于国药集团化学试剂有限公司,香草酸(批号110776-201503,纯度99.8%)、对羟基苯乙酮(批号111897-201001,纯度99.9%)购于中国食品药品检定研究院,白首乌二苯酮(自制,纯度99.6%)。甲酸、甲醇和乙腈为色谱纯,水为超纯水。
1.3 药材药材样品为产地采集,经中国食品药品检定研究院民族药室郑健研究员鉴定为萝藦科鹅绒藤属植物青阳参Cynanchum otophyllum Schneid.的干燥根。
2 方法与结果 2.1 混合对照品溶液的制备取对羟基苯甲酸、香草酸、对羟基苯乙酮、2,5-二羟基苯乙酮、白首乌二苯酮、2,4-二羟基苯乙酮的对照品约10 mg,精密称定,分别置10 mL量瓶中,用甲醇溶解并定容至刻度,即得各单一对照品储备液;精密吸取上述6个对照品储备液依次为1、1、2、1、1、4、1 mL于50 mL量瓶中,用甲醇定容,摇匀,制成每1 mL中分别含对羟基苯甲酸、香草酸、对羟基苯乙酮、2,5-二羟基苯乙酮、白首乌二苯酮、2,4-二羟基苯乙酮对照品约20、20、40、20、80、20 μg·mL-1的混合对照品储备液;取混合对照品储备液1 mL,置10 mL量瓶中,加甲醇配制成上述6个成分分别约2、2、4、2、8、2 μg·mL-1的混合溶液,即得混合对照品溶液。
2.2 供试品溶液的制备取本品粉末(过4号筛)0.2 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,称量,超声(功率300 W,频率40 kHz)处理30 min,放冷,再称量,用甲醇补足减失的量,摇匀,滤过,取续滤液,即得。
2.3 色谱条件色谱柱:Waters HSS T3 C18(250 mm×4.6 mm,5 μm);流动相:乙腈-0.05%甲酸水溶液(20:80);检测波长:260 nm;流速:1 mL·min-1,柱温:30 ℃;进样量:10 μL。
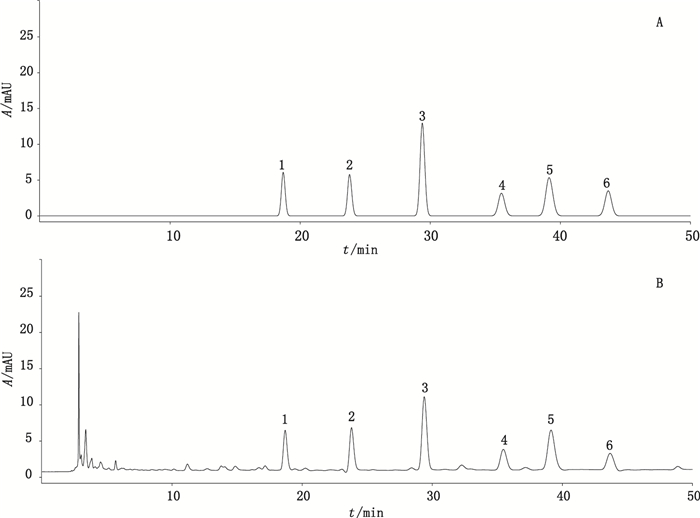
2.4 系统适用性试验考察分别精密吸取混合对照品溶液、供试品溶液各10 μL,按“2.3”项下色谱条件进样测定,记录色谱图,结果见图 1。对羟基苯甲酸、香草酸、对羟基苯乙酮、2,5-二羟基苯乙酮、白首乌二苯酮、2,4-二羟基苯乙酮6个化学成分的保留时间分别为18.65、23.77、29.33、35.41、39.12和43.75 min,本实验条件下所测的6个成分与相邻色谱峰的分离度均大于1.5,与其他组分分离完全,拖尾因子在0.95~1.05之间,理论塔板数大于6 000,色谱系统适用性试验符合含量测定要求。
|
1.对羟基苯甲酸(p-hydroxybenzoic acid)2.香草酸(vanillic acid)3.对羟基苯乙酮(p-hydroxyacetophenone)4.2,5-二羟基苯乙酮(2,5-dihydroxyacetophenone)5.白首乌二苯酮(baishouwubenzophenone)6.2,4-二羟基苯乙酮(2,4-dihydroxyacetophenone) 图 1 混合对照品(A)及青阳参提取物(B)的HPLC色谱图 Figure 1 HPLC chromatograms of mixed reference substances(A)and extract of Radix Cynanchi Otophylli(B) |
精密吸取混合对照品储备液0.1、0.2、0.5、1.0、2.0、5.0 mL,分别置于6个25 mL量瓶中,加甲醇定容至刻度,摇匀,即得系列浓度的混合对照品溶液。分别精密吸取各混合对照品溶液10 μL,注入液相色谱仪,按“2.3”项下色谱条件测定峰面积;以各对照品质量浓度(μg·mL-1)为横坐标,以峰面积为纵坐标,进行线性回归,各被测成分回归方程和线性范围见表 1。结果表明,6个成分在测定范围内线性关系良好。
|
|
表 1 各被测成分的回归方程、相关系数和线性范围 Table 1 Regression equations, correlation coefficients, linear ranges of the investigated |
取混合对照品溶液,以甲醇逐级稀释,进样测定。当信噪比为3时,测得对羟基苯甲酸、香草酸、对羟基苯乙酮、2,5-二羟基苯乙酮、白首乌二苯酮和2,4-二羟基苯乙酮的检测限分别为0.15、0.18、0.23、0.22、0.18和0.28 ng;当信噪比为10时,测得上述6个成分的定量限分别为0.51、0.58、0.62、0.68、0.55和0.71 ng。
2.7 精密度试验精密吸取“2.1”项下混合对照品溶液10 μL,连续进样6次,记录峰面积。结果对羟基苯甲酸、香草酸、对羟基苯乙酮、2,5-二羟基苯乙酮、白首乌二苯酮和2,4-二羟基苯乙酮峰面积的RSD(n=6)分别为0.35%、0.22%、0.30%、0.19%、0.18%、0.21%,表明仪器精密度良好。
2.8 重复性考察取1号样品粉末6份,分别按照“2.2”项下方法制备供试品溶液,按“2.3”项下色谱条件测定,记录峰面积,计算含量。结果样品中对羟基苯甲酸、香草酸、对羟基苯乙酮、2,5-二羟基苯乙酮、白首乌二苯酮和2,4-二羟基苯乙酮的平均含量(n=6)分别为0.102、0.108、0.236、0.106、0.258、0.092 mg·g-1,RSD分别为1.2%、1.6%、1.7%、1.5%、1.4%、0.95%,表明重复性良好。
2.9 溶液稳定性试验取1号样品的同一份供试品溶液,分别于0、2、4、8、12、24 h进样测定。结果对羟基苯甲酸、香草酸、对羟基苯乙酮、2,5-二羟基苯乙酮、白首乌二苯酮和2,4-二羟基苯乙酮峰面积的RSD(n=6)分别为0.55%、0.64%、0.81%、1.0%、0.82%、0.52%,表明供试品溶液在24 h内稳定。
2.10 加样回收率试验取对羟基苯甲酸、香草酸、对羟基苯乙酮、2,5-二羟基苯乙酮、白首乌二苯酮和2,4-二羟基苯乙酮的对照品适量,精密称定,分别以甲醇配制成质量浓度分别为10.25、10.86、23.75、10.96、26.39、9.24 μg·mL-1的对照品溶液。取已知含量的1号样品粉末6份,每份各约0.1 g,精密称定,分别置具塞锥形瓶中,分别精密加入上述6种对照品溶液各1.0 mL,按照“2.2”项下方法平行制备供试溶液,进样分析,计算回收率,结果对羟基苯甲酸、香草酸、对羟基苯乙酮、2,5-二羟基苯乙酮、白首乌二苯酮和2,4-二羟基苯乙酮平均加样回收率(n=6)分别为99.3%、98.2%、99.0%、98.4%、99.2%和98.3%,RSD分别为1.8%、1.5%、1.5%、1.6%、2.3%和1.7%。
2.11 样品含量测定分别取不同产地青阳参药材,按“2.2”项下方法制备供试品溶液,再按“2.3”项下色谱条件进行测定,用外标法计算样品含量。结果见表 2。
|
|
表 2 青阳参中6个成分含量测定结果(mg·g-1) Table 2 Contents of six components of Radix Cynanchi Otophylli |
本文采用等度洗脱色谱法分离青阳参药材中的6个主要酚类成分,50 min内完成分离,对羟基苯甲酸、香草酸、对羟基苯乙酮、2,5-二羟基苯乙酮、白首乌二苯酮、2,4-二羟基苯乙酮分离效果良好,符合含量测定要求。本文通过二极管阵列检测器考察所测物质紫外吸收,结果260 nm时6个酚类成分具有较大吸收,且杂质成分干扰少,故选择260 nm作为检测波长。试验中通过对不同流动相系统甲醇-水、甲醇-甲酸水溶液、乙腈-水、乙腈-甲酸水溶液的分离效果考察,发现乙腈-甲酸水溶液的分离效果较好,进而优选确定乙腈-0.05%甲酸水溶液作为流动相。
3.2 含量测定结果分析根据样品测定结果,对羟基苯甲酸、香草酸、对羟基苯乙酮、2,5-二羟基苯乙酮、白首乌二苯酮、2,4-二羟基苯乙酮6个酚类成分在药材中的含量具有较大差异,白首乌二苯酮的含量最高,对羟基苯甲酸含量最低。另外,不同产地的药材中这6个成分的含量相差较大,其中鲁甸县和宁蒗县的6个酚类成分总含量相对较高,说明不同的采集地对青阳参中酚类成分含量影响较大,但其中是否具有规律尚需进一步研究。
3.3 小结本研究建立的方法可同时测定青阳参药材中6个酚类成分,方法简便,结果准确,重复性好,主成分与各个杂质分离度较好,其专属性较好,为青阳参药材的质量控制提供依据。
| [1] |
中国科学院中国植物志编辑委员会. 中国植物志[M]. 第63卷. , 科学出版社, 1977, 377. Editorial Committee of Chinese Journal of Plant of Chinese Academy of Sciences. Flora of China[M]. Beijing: Science Press, 1977, 377. |
| [2] |
云南省中药材标准[S]. 2005: 61 Yunnan Standards for Chinese Materia Medica [S].2005:61 |
| [3] |
湖南省中药材标准[S]. 2009: 227 Hunan Standard for Chinese Materia Medica [S].2009:227 |
| [4] |
卫生部药品生物制品检定所. 中国民族药志[M]. 北京: 人民卫生出版社, 1984, 312. Institutes for the Control of Pharmaceutical and Biological Products, Ministry of Health, PR China. Records of Chinese Ethnic Medicines[M]. Beijing: People's Medicical Publishing House, 1984, 312. |
| [5] |
黎丽云, 殷志琦, 张庆文, 等. 云南民间药青阳参的研究进展[J]. 海峡药学, 2011, 23(4): 1. LI LY, YIN ZQ, ZHANG QW, et al. Research progress on the Yunnan's folk medicine:Cynanchun otophyllum[J]. Strait Pharm J, 2011, 23(4): 1. |
| [6] |
昝珂, 过立农, 郑健, 等. 民族药材青阳参的化学成分研究[J]. 中国中药杂志, 2016, 41(1): 101. ZAN K, GUO LN, ZHENG J, et al. Chemical constituents of ethnic medicine Cynanchum otophyllum[J]. China J Chin Mater Med, 2016, 41(1): 101. |
| [7] |
殷敏敏, 殷志琦, 张健, 等. 青阳参乙酸乙酯萃取部位的化学成分[J]. 中国药科大学学报, 2013, 44(3): 213. YIN MM, YIN ZQ, ZHANG J, et al. Chemical constituents from ethyl acetate extract of Cynanchum otophyllum[J]. J China Pharm Univ, 2013, 44(3): 213. DOI:10.11665/j.issn.1000-5048.20130305 |
| [8] |
李祥, 张敉, 向诚, 等. 青阳参中C21甾体成分研究[J]. 中国中药杂志, 2014, 39(8): 1450. LI X, ZHANG M, XIANG C, et al. C21 steroids from Cynanchum otophyllum[J]. China J Chin Mater Med, 2014, 39(8): 1450. |
| [9] |
MU QZ, LU JR, ZHOU QL. Two new antiepilepsy compounds-otophyllosides A and B[J]. Sci Sin B, 1986, 29(3): 295. |
| [10] |
杨金铧, 殷敏敏, 张健, 等. HPLC波长切换法测定青阳参中7个C21甾体皂苷的含量[J]. 中国药科大学学报, 2014, 45(2): 200. YANG JH, YIN MM, ZHANG J, et al. Simultaneous determination of seven C21 steroidal saponins in the radix of Cynanchum otophyllum Schneid.by HPLC wavelength switching method[J]. J China Pharm Univ, 2014, 45(2): 200. DOI:10.11665/j.issn.1000-5048.20140212 |
| [11] |
中国药典2015年版. 一部[S].2015:410 ChP 2015.Vol Ⅰ[S].2015:410 |
| [12] |
王静, 张玉萍, 刘影. 不同采收期茵陈中对羟基苯乙酮的含量测定[J]. 现代中药研究与实践, 2011, 25(3): 7. WANG J, ZHANG YP, LIU Y. Content determination of hydroxyacetophenone in Artemisia capillaries from different collection time by HPLC[J]. Chin Med J Res Pract, 2011, 25(3): 7. |
| [13] |
岳荣彩, 天然产物白首乌二苯酮的神经保护作用和两面针碱的免疫调控作用机制研究[D]. 上海: 第二军医大学, 2013 YUE RC.Studies on the Neuroprotective Effects of Cynandione A and Immune-Modulating Effects of Nitidine [D].Shanghai:The Second Military Medical University, 2013 http://cdmd.cnki.com.cn/Article/CDMD-90030-1013232769.htm |
| [14] |
昝珂, 郑健, 过立农, 等. HPLC法测定民族药材青阳参中对羟基苯乙酮的含量[J]. 中国药事, 2015, 29(12): 1310. ZAN K, ZHENG J, GUO LN, et al. Determination of 4-hydroxyace-tophenone in Radix Cynanchi Otophylli by HPLC[J]. Chin Pharm Aff, 2015, 29(12): 1310. |
| [15] |
昝珂, 张欣, 刘杰, 等. HPLC法测定民族药材青阳参中白首乌二苯酮的含量[J]. 中国药事, 2016, 30(5): 472. ZAN K, ZHANG X, LIU J, et al. Determination of baishouwubenzo-phenone in Radix Cynanchi Otophylli by HPLC[J]. Chin Pharm Aff, 2016, 30(5): 472. |
 2017, Vol. 37
2017, Vol. 37 
